Note: Descriptions are shown in the official language in which they were submitted.
2 ~ 2 2
L`invention concerne un proc~de d'isomerisation des n-paraffines en
isoparaffines, ayant notamment pour but d'ameliorer l'indice d'octane d~
certaines coupes petrolières, plus particulièrement d~ celles qui
contiennent des pentanes et des hexanes normaux ainsi que des pentanes
et des hexanes ramifies (coupes C5/C6)~
Les procédés actuels d'isomérisation des hydrocarbures en C5/C6 utilisant
des catalyseurs au platine de typ~ alurnin0 chloree à haute activité op~rent
sans recyclage (en anglais "once through"~, ou avec un recyclage partiei,
après fractionnement, des n-paraffines non converties, ou av~c un
recyclage total après passage sur des systèmes de tamis moléculaires en
phase liquide.
La mise en oeuvre sans recyclage, bien que simple, manqu~ d'efficacité
dans l'accroissement d~ l'indice d'octane. Pour obtenir des indicss
d'octane élevés, on doit effectuer le recyclage des constituants à faible
indice d'octane, après passage soit dans des colonnes de séparation (par
exernple un désisohexaniseur) soit sur des tamis moléculaires, en phas~
liquide ou vapeur.
Un procédé d'isomérisation bien connu, ulilisant des tamis moléculaires
pour la separation en phase vapeur des n-paraffines non converties,
intègre i'étape d'adsorption par tamis moteculaire à l'étape réactionnell~
C'est le procédé dit "Total Isomerization Process" ~ou "TIP") décrit par
exemple dans le brevet US-A-4210771. Il combine la mise en oeuvr~ d'un
réacteur d'isomérisation alimenté par le mélange de la charge, d'un
effluent de désorption et d'hydrogèn0, et la mise en oeuvre d'une section
de séparation par adsorption des n-paraffines sur tamis moléculaire, la
désorption etant effectuée par un strippage à l'hydrogène. I~ans un tel
procéde, le systèm~ r~actionnel ne peut pas consister en une étape à
l'alumine chlorée à haute activité, en raison des risques de contamination
par l'acide chlorhydrique dss tarnis moléculaires intégrés. On utilise alors
un systsme catalytique moins performant, à bas~ de zeotithe ne mettant
pas en oeuvre de chlore. Il en résul~e un produi~ présen~an~ un indice
:
2~ 2
d'octane inf~rieur de l ~ 2 poin~s ~ celui qui aurait ~t~ obtenu avec un
catalyseur à base d'alumine chlorée.
En effet~ il est connu dans l'art que plus la température d'isomérisation est
basse, plus la conversion des n-paraffines en isoparaffines est ~lev~e et,
5 de plus, meilleure est la conversion des isomères en C6 à faihle indice
d'octane ~méthyl-pentanes) en isom~res en C~ ~ plus haut indice d'octana
~diméthylbutanes).
Il est connu également que le catalyseur ~ base d'alumino chlor~e
10 imprégnée de platine permet de mener la reaction d~isomérisation ~ un~
température plus basse que les catalyseurs de type 7éolithe non chlorbe,
plus stables.
Il était donc par~iculièrement int~rsssant d~ concevoir un proc~clé qui
15 puisse combiner un systbme rgactionnel ~ basse température (pour avoir l~
meilleur accroissement de l'indice d'octane "sans recyclagen), avec un
systèrne de recycla~e des consti~uants ~ faible indioe d'octane, non in~égr~
ou résistant au chlore.
20 C)n peut c~nsidérer les schémas classiques utilisan~ des colonnes de
séparation ~désisopentaniseur et désisohexaniseur), du fait que les
colonnes de séparation peuvenl être immunisees oontre la contamination
par le chlore. Mais ces schémas son~ lourds en equipernent et gros
consommateurs cl'énergi~, donc ooûteux ~ mettre en oeuvr~. Un sch~ma à
25 une colonne de séparation (seulement le désisohexaniseur) serait rnoins
coûteux mais ne présenterait pas la faeulté cle convertir tout le pentan~
normal en isopenlane et, de ce ~ait, ne permettrait pas d'obtenir les nivsaux
d'accroissement de l'indlce d'octane des schémas avec recyelage.
30 Pour éviter la contamina~ion par le chlore des tamis moléculaires utilisés
pour la séparation, on peut envisager un système non int~gr~ mettant en
oeuvr~ une é~ape de s~abilisation de l'sfflu~nt d'isomérisation avant d~
I`envoyer à l'étape d'adsorption. Cette approohe a déjà ét~ proposée dans
le procéd~ combine dit "PENEX MOLEX~, dans lequel les hydrocarbures an
- ,
. . . .
, . . ~ -
.
.
2 ~ 2 2
G5/C6 sont isomérisés dans une r~ction ca~alytique à l'alumine chlor~e,
suivie par une adsorption swr lamis moléculairc en phase liquide des
parai~ines normales à par~ir du Sond du stabilisatsur, à la températur~ d~
~ond.
S L'utilisation d'un ~amis moléculaire en adsorp~ion et d~sorption en phase
liquide est plus difficile à réaliser qu'en phase vapeur~ En effet le rapport
des quantités de paratfinQs normales adsorbées aux quantités
d'isoparaf~ines présentes en phase mobile est nettement en ~avewr de la
mise en oeuvre en phase vapeur.
1 0
Un autre obstacle à l'utilisation des syst~mes catalytiques à haute activit~
est leur sensibilité aux contaminants de la charç~e, à savoir ie soufre at
l'eau. La charge liquide et l'appoint d'hydrogène doivent ~tre adoucis,
débarrassés du soufre et déshydratés avant d'être introduits dans le
1 5 systbme réactionnel.
Dans l'état actuel de la technique utilisant des systèmes catalytiques à
base d'alumine chlorée, les charges sont séchées dans des opérations de
prétraitement au moyen de piusieurs tamis moléculaires.
~0
L'objet de l'invention est de proposer un nouveau procédé permettant
d'augmenter le pJus possi~le l'indice d'octane d'une coupe pétrslièro
contenant des paraffines normales tout en lirnitant la dépense éner~étique,
25 La presente invention perrnet no~amment de pallier les inconY~nients des
procédés connus, en combinant le systerne à haute ac~ivite utilisant par
exemple un c~talyseur consistant en une alumine chlorée imprégné~ de
platine avec un système original d'adsorption-désorption sur tamis
moléculaire en phase vapeur (systèmc non intégré). De plus, la désorption
30 des n-para~ines est realisée dans des eonditions avantageuses du point
de vue énergbti~ue en combinan~ un abaissement d0 pression e~ une
opération de strippage utilisant un~ vap~ur riche en méthyl-pentanes ~ui
sont aussi recyclés et convertis.en diméthylbutanes lors du passage
travers ie réac~eur d'isomérisation,
:
2 ~ 2 2
Pour fournir l'eluant ~apeur rich~ en méthyl-pentanes pour le cycl~ ci~
désorption, on incorporc en aval du syslbme une colonne de
désisohexanisation qui fractionn~ l'effluent dc l'étap~ d'adsorption 0n 2
5 coupes: une coup~ distillat n9 contenant que des isomeres ~ tr~s hau1
indice d'octane ayant une forte concentration ~n dirnethyl butanes et une
coupe de f~nd de la colonne ayant une fo~ concentration des m~thyl~
pentane~ d'indice d'octane bien in~érieur à celui du distillat.
10 Par ailleurs, I'utilisation judicieuse de méthyi-perltanes fournis par ia
dbsisohexanisation dans l'étape de désorption permet de supprimer une
étape de purge à la fin de celle-ci~ En effet, la colonne d'adsorbant alors
remplie da rn~thyl-pentanes peut être immédiatement réutilis~e ~n
adsorption, I'effluent de l'adsorption ne contenant pas alors d~ n-paraffinss,
15 même au début de celle-ci~ Cela conduit ~ une simplification impo~ante de
l'unité en permettant notamrnent l'utilisation d'un syst~me ne contenant que
deux lits d'adsorbant, chacun opérant alternativement en adsorption et en
désorption.
20 Selon un autre aspect de-l'invention, on peut utiliser un système de
recompression des vapeurs de tête du désisohexaniseur (pompe à
chaleur) pour fournir tou~e l'énerQie de rebouiilage du désisohexaniseur
par la condensation du reflux et du distillai net de celui-ci.
25 Le procédé de l'invention est décrit ci-apr~s en liaison avec les Figuras 1, 2
et 3, parmi lesquel!es:
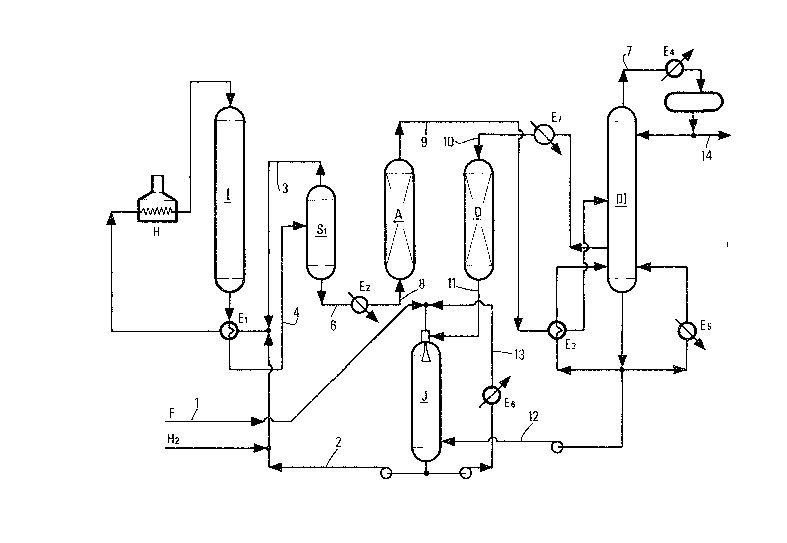
~: - La Figure 1 en représente un schéma de principe;
- La Fi~ur~ 2 représente un schéma p1us détaillé du procéd~ de
30 I'invention, et;
- La Figure 3 représente schérnatiquement une étape da stabilisation.
~ .
`: :
~ .
: ~:
: ................... : , , -
- . .
. , . .- ~
- . . , . .. - .
,
-. . .
..
- - -
~- . .. - : . : .
:: . . , : - - . . .
, - . .
209:L1 22
On decrit plus particuli~remellt l'isom~risation d'un~ charg~ d~ naphta
léger con~enant une proporlion prépond~rante d'hydrocarbur~s en Cs ~t en
C6 ~n un isom~rat à haut indice d'octane.
5 Le procéd~ d~ l'invention comprend principalemsnt : une éSape ~1 )
d'isom~risation dans laquelle on envoie dans un réacteur d'isomérisalion
uno coupe C~/C6 repr~sentant la charge fraîche, m~lang~e au moins avec
un recyclage d'un flux riche en paraffines normales et en m~thyl-pentanes
provenant de l'étape (3) de d~sorption, I'effluent da cett~ ~tap~ étant
10 envoy~ dans un séparateur dans lequel on s~par~ une phase vapeur, qui
est recyclbe ~ I'entr~e du réact0ur, et une phase liquide qui constitue
l~isom~rat brut;
- une étape (2) d'adsorption dans laquelle on envoi~ dans un adsorbeur
15 garni d'un tamis mol~culaire capable de retenir les n-para~fines, en courant
ascendant, un flux vapeur de l'effluent liquide de l'étape d'isomérisation,
après vaporisation, et l'on recueille un isom~rat débarass~ des n-
paraffines;
20 - une étape (3) de désorption, alternant avec l'étape (2), et dans laquelle
on abaise la pression dans l'adsorbeur et on fait passer à travers le tamis
moléculaire un ~lux gazeux rich~ en méthyl-penanes prélevé dans l'étape
da désisoh~xanisation (4)~ I'e~fluent de cette btape de desorption étant
envoyé v~rs l'étape d'isomérisation ~1~; e~
2S
- une étape (4) de désisohéxanisation dans laquell~ on alirnent~ une
colonne de distillation au moyen de l'effluent prevenant d~ l'étap~ (2)
d'adsorption, et l'on obtient un r~sidu liquide, un flux vapeur riohes en
méthylpentanes et un distillat menant au produit ~inal d'isomérisation; l~
30 flux vapeur riche en méthylpentanes ~tant envoy~ comme d~sorbant vers
I'étape ~3) de désorption.
:
~: : Dans l'étape t1), on envoie dans une ~one d'isom~risation 1, par la lign~ 2,
la charge de naphtha l~ger (ligne 1) m~lang~e avec au moins un r~cyclag~
.
.
., ' . .:
.
2 ~ 2 2
d`un flux riche en paraffines normales et en mélhylpentanes prov0nant de
l'etape de désorption (3) (ligne 11) et ~ventuellement un recyclag~ d'uno
partie du r~sidu liquide de l'~tape d~ désisohexanisa~ion (43 ~ligne ~2).
La réaction d'isomérisation est conduite à une t~mpérature d~ 140 à 300C
en présence d'hydrogène sous une pressivn d~ 10 à 40 bars. La cllarge à
traiter est m~langée ~ un appoint d'hydrogène et ~ventuellernent à un
recyclage d'hydrogène arrivant par la ligne 3, puis est chauff~ par ex~mple
à un~ temp~rature de 140 à 3û0C au moyen d'un ~change d~ chal~ur
charge/effluent, dans l'~changeur E1 et d'un chauffag~ finai dans un four H.
La réaction d'iscmérisation est effectuee de préference sur un catalyseur à
haute activité, comme par exemple un catalyseur à base d'alumin~ chlor~e
ct de platin~, ~onctionnant ~ basse temperalure, par exemple entra 130 et
22QC, à haute pression, par exemple de 20 à 35 bars, et avec un faible
rapport molaire hydrogène/hydrocarbures, compris par exemple entre 0,1/1
et 1/1. Des catalyseurs connus utilisables sont constitués par exemple d'un
support en alumine g etlou h de haute pureté renfermant de 2 à 10/~ en
poids de chlore, de 0,1 à 0,35% en poids de platins et éventuellement
d'autres metaux. Ils peuvent être mis en oeuYr0 avec une vitesse spatiale
de 0,5 à 10 h-~- de préférence de 1 à 4 h-1. Le maintien du taux de
chioration du catalyseur nécessite ~énéralem~nt i'appoint en eon~inu d'un
compos~ chlor~ comme le tétrachlorure de carbona injec~ en mélange
avec la charg~ ~ une concentralion d~ 50 à 600 parties par million en
2 5 poids.
Bien entendu on peut é~alement utiliser d'autres calalyseurs connus tels
que ceux constitu~s d'une ~oiith0 de iype mordénite renfermant un ou
plusieurs métaux préférentiellement du groupe \/lll de la classification
périodique des él~ments. Un catalyseur bien connu consiste ~n une
mordénite dc rapport SiO2/Al~O3 compris entre 10 et 40, de préférenc0
entre 15 et 25 et renferrnant de 0,2 ~ 0,4 % ~n poids de platine.
Néanmoins, dans le cadrc du proc~d~ faisant l~objet de l'invention, les
catalyseurs appartenanl ~ cette famillQ sont rnoins intéressants qu~ ceux
.
- - -
-
- ................... .. ~ . - -
. ~ . . - - - . - , .
.
- , .
. . .
.
.
- .
,
base d'alumine chlorée car ils fonctionnen~ à pius haule température (240
à 300C) et conduisent à une conversion moins poussée des paraf~ines
normales en isoparaffines à haut indice d'octane.
5 Dans ces conditions, une partifl des n-paraffines ~st transform~e en
isoparaf~ines et une partie des m~thyl-pentanes est transform~e en
diméthylbutanes; cependant, il rest~ dans l'sffluent sortant du rbacteur
d'isomérisation par la ligne 4 une proportion importante de n-paraffines et
de méthyl-pentanes, qui peut aller jusqu'à environ 50 % en mol~s et qui est
10 de pr~férence comprise entre 2S et 40 % en moles
L'effluent de l'etape d'isomérisation t1), après refroidissement, peu~ passer
dans un séparateur S1 dont ia vapeur est recyclée par la ligne 3 à l'entrée
du réacteur d'isornérisation I et l'e~fluent liquide (isomérat) sortant par la
15 ligne 6 est vaporisé et surchauffé dans l'échangeur E2 avant d'être envoyé
vers l'étape d'adsorption (2~ par la ligne 8.
Dans l'étape (2) d'adsorption, on fait passer le mélange vapeur en courant
ascendant dans l'adsorbeur A, dans lecluel les n-paraffines sont relenues.
20 L'isomérat débarrassé des n-paraffines sort par la ligne 9, peut etre au
moins en partie condensé dans l'échangeur E3puis envoy~ vers la
colonne ds désisohexanisation.
Le lit adsorbant est constitué en général d'un tamis moléculaire à bas~ ds
26 zéolithe capable d'adsorber sélectivement les n-paraffines, et ayant un
diambtre apparent de pores voisin de 5 A = ~5 . 10-8 cm); la zéolithe 5 A
convient parfaitement à cet usage: son diamètre de pores est proche d~
5 A = (5 .lo-~ crr) et sa capacit~ d'adsorption pour les n-paraffines est
irnporlante. On peut cependant employer d'autres adsorbants tels qu~ la
3û chabazit0 ou l'érionite Les conditions opératoires pr~férées sont une
temp~rature de ~00 ~ 400 ~C et un~ pression de 10 à 40 bars. L~ cycl~
d'adsorption durs en général de 2 à 10 minutes. L'effluent recueilli à la
sortie d~ l'adsorbeur A par la ligne 9 ne contient pra~iquernent quf~ des
isoparaffines ~isopentane et isohexane~. Il est condensé, par éch~nga d~
', ' ' ' ' ~
2 2
chaleur, par exemple par échange therrmique avec un des r~bouilleurs ~3
de l'etape (4) d~ désisohexanisation.
Les n-paraffines adsorbees au cours de l'é~ape ~) sont ensui~3 désorbées
5 dans i'étape (3) de désorp~ion repr~sentée sur la Figure 2 par l'adsorb~ur
D, qui n'~st autre que l'absorbeur A saturé en n-paraffines et fonctionnant
~n désorption. L'opéra~ion est réalisée par un abaisserrlent de la pression
jusqu'~ une valeur in~érieure à 5 bars, de pr~férenc~ inférieure ~ 3 bars, ~t
par un strippage au moyen d'un flux gazeux riche en méthyl-pentanes,
t 0 soutir~ à un niveau de la colonne de ~ésisohexanisation convenablo et
amené par la li~ne 10 à traverser l'adsorbeur D en courant d~scendant. Ce
~lux gazeux est en général port~ à une température de 250 à 350 4C dans
l'échangeur E7. La proportion du flux riche en méthyl-pentanss nécessair~
à la désorption correspond avantageusement ~ 0,5 à 2 moles de vapeur
15 rich~ en méthyl-pentanes par mole de n-paraifines ~ désorber. L'opération
dure en général de 2 à 10 minutes: I'effluent de l'etape de désorption (3j
est recyclé vers l'étape d'isomérisation par la ligne 11; il est condens~
directement dans un éjesteur J en contact avec la charge fraîche de naphta
léger arrivant par la ligne 1 et avec un liquide eirculant dans la ligne 13 et
20 refroidi par l'échangeur~6.-
L'adsorbeur D, après désorption, est à nouveau utilisé en adsorption.
L'effluent sortant de l'étape d'adsorption est ensuite envoy~ sous pression
25 d'adsorption vers l'étape (4~ de désisohexanisation.
Dans i'étape (4) on alimente une colonnc de désisohexanisation par laligne 9 au moyen de l~effluent provenant de l~étape (23 ~'adsorption décrito
pr~cédemment, par exemple, ~ wne pression de 1 à 2 bars (pression
3 0 absoluc~.
La colonne de désisohexanisation consiste en ~én~ral en un~ coionn~ de
distillation compo~ant des internes ~e ~rac~ionnement (garnissage struc~ur~
ou plateaux). L'opera~ion ds d~sisohexanisation s~par~ la charge ~n un
- . . . - . . .
: . -. : . . - .: ~ ..
: :
.
.
~ : . . . ..
.. . . , - -, - :
. . , :
.
distillat riche en diméthyl butanes contenant, par exemple, d~ 20 à 40% en
moles de dime~hylbutanes et en un résidu pauvre en dlmé~hylbutanes
contenant par exemple d~ S à 10% en moles de diméthylbutane.
5 Avant d'être introduite dans la colonne de désisohexanisation, la char~e
peut êtra condensée et refroidie, par exemple, à une temp~rature d~ 100 à
120 C, ~ventuellement par échang~ ~hermique avec un das rabouilleurs
de la colonne de désisohexanisation dans l'échangeur E3.
10 La colonne de desisohexanisation opère en général entre une températur~
de fond de 80 à 10ûC et une température de tete de ~0 à 60C,
Le résidu chaud de la colonne de desisohexanisation sortant par la ligne
12 est ensui~e recyclé et envoyé vers le r~acteur d'isomérisatiol- apr~s
15 mélange avec la charge fraîche (ligne 1) et l'etfluen~ de désorption (ligne
11) dans l'éjecteur/mélangeur J. Un soutirage latéral permet de prélever
un courant vapeur riche en msthylpentanes envoyé par ta ligne 10 vers
l'adsorbeur D en cours de désorption.
20 Les vapeurs de tete (distillats) sor~ant par la ligne 7 sont en général
~ondensés par moyen d'un échangeur de chalsur avec l'eau d~
refroidissement dans un condensateur ~4. Le condensat est pa~ie!lemenl
recycl~ en tête du désisohexaniseur (reflux) e~ en partie envoyb p~r
pompaga par la ligne 14 comme produit principal d'isornérisation ou
2 5 isornérisat.
Dans une des versions optionnelies que l~on préfère, les vapeurs de têto
(distillats) sor~ant par la ligne 7 peuvent être eornprimées dans un
compresseur (pornpe ~ chaleur) à une pression suffisante (de 5 à 6 bars~
30 pour qu'eiles se eondensent ~ una température supbrieure de 10 à 25C à
la températur~ requise pour le Je~ouillage du fonrl de colonnc. La
condensation de ces vapeurs peut alors servir ~ lournir l'énergie
nécsssaire au rebouilleur par i~interm~diaire de l'~changeur E5, en ~vitant
un apporl d'~nergie exterieur. La condensation se ~ai~ en ~rande partiG de
-`
.
'
:
2 ~ 2 2
1 o
cette manière, ca ~ui permet d'~conomisef sur les moy~ns d~
refroidissement nécessaires à la condensation tolaie du re~lux et du
distillat.
5 Selon un~ autr~ variante préfér~e du procédé dc I'invention, notamment
lorsque l'on utilise un catalyseur ~ base cl'alumine ehlorés, on intercale
entre l'é~ape d'isomérisation (1) e~ tap~ d'adsorption (2), un~ étap~ de
stabilisation de l'elfluent d0 I'isom~risation. destiné~ esssntiell0mcnt à
éliminer l'acide chlorhydriqu0 provenant du catalyseur en m~ma t~mps qu~
10 I'hydrogène et des hydrooarbures légers de C1 à C~4.
Après refroidissement, par exemple par échange thermique avec la eharge
alimentant ledit réacteur dans l'échangeur E1, I'effluent du r~acteur
d'isomérisation consistant en un mélangs diphasi~ue est envoyé par la
lign~ 4 direc~e~7nent dans une colonne de stabilisation S2 70pérant ~n
~énéral à une pression de 10 à 20 bars, avantageusement à environ 15
bars. Le s~abilisateur S2 est représent7e schématiquement sur la Figur7s 3.
Le stabilisateur élimine en t7~-7te les produils les plus légers ainsi que l'exc~s
20 éventuei d'hydrogene qui sortent par la lign~ 15. Ls distillat est
partiellement condens74 par refroidissernen~ à l'eau dans 17échangeur E7~, le
conden~at ob~enu pouvant être au moins parîiellement recycl~ vers la tet~
du stabilisateur par la lign~ 16. Si on le désire, on peut également recueillir
un LPG comme distillat net, par la ligne 17.
L~acide chlorhydrique ~ventuellsment present ~lors~ue 1~ catalyseur
- diisomérisation est à base d'alurnine chlorée imprégnée d~ piatins) est
su~fisamment volatil pour passer en totalit~ en tête du stabilisateur ~t est
~vacub aYec 1es produits gazeux par la ligne 15. Le produit de ~ond du
3 O stabilisateur, exempt d'acide chlorhydri~ue es1 soulir~ par la lign~ 6 sous la
forme d'un flux vapeur ~ la pression du stabilisatelJr et est envoy~ vers
l'adsorbeur apres un ehauf~age compl~ment~ir~ dans l'~ohangeur E~.
- : -
.
: . . . .
.
. . . .
2 ~ 2
Le rebouilleur du stabilisatellr s~lt ainsi ~ Yaporiser la charge d~
I'adsorbeur A, à una température d'environ 150 a 200 C, permettant
l'alimentation de ce dernier en phas~ vapeur.
S Le procédé d~ l'invention permet d'obtenir, ~ partir de charg~s de naphtas
légers riches en C5/C6 présentant un Indice d'Octane Recherche ~IOR) de
65 à 75, un isom~ra~ présentan~ un IOR do 89 à 92.
L'exemple qui suit, non limitatif, iliustre l'invention.
1 0
EXEMPLE
Le procéd~ faisant l'objet de l'invention est mis en oeuvr~ dans une
installation pilote correspondant au schéma de la Figure 2, modifié selon l~
15 sch~ma de la Figur~ 3. L~ séparateur S1 est donc remplacb par la colonne
de stabilisation S2 et on ne recycle pas d'hy~rogène vers le réacteur
d'isomérisation 1.
La charge F est constituée par un naphta l~ger préalablement désulfur~ et
séché ayant la composition molair~ suivantQ: ~
~. ~
Gonstituant % hAolaire
_ . _ _ __ ~
Isobutan~ (iC4) 0,4
Normaibutana ~nC~) 2,4
lsopentane ~iCs) 21
Normalpentane ~ncs) 29
Cyclopentane (CP) 2,2
2-2 diméthylbutane (22 DMB) 0,5
2-3 dimé~hylbutane (23 DMB) 0,9
2 méthyipentane (2 MP) ~2,7
3 methylpentane (3 MP) t 0
Normal hexane (nC6~ 14
Méthylcyclopentane (M(:;P) 5
Cyclohexan~ ~CH) 0,~
Benzbn~ 1,3
: ~ ___________
:'
: :
:~
.
,
--
2 ~ 2
Sa ten~ur en soulre est de 0,5 ppm en poids, sa teneur en eau de 1 ppm
en poids et son Indice d'Octane Recherche (IOR) de 70,2.
La charg~ liqwida est introduite par la conduita 1 dans un
ejecteur/m~langeur J avec un d~bit dc 77,6 kg/h. Simultan~msnt, on aspire
dans cet éjec~0ur/m~langeur, ~ un d~bit moyen de 44 kglh, un flux de
recyclage isqu de la zone dc d~sorption D par la lign~ 11.
L'~jecteur/mélangeur fonctionn~ sous una pression d~ 2 bars et la chargs
liquide ~ralche et recyclé~, introciuite dedans comme fluida moteur, est
1~ préchauffée à une temp~rature d'envirorl 80C par le contact direot avec la
vapeur issue de la dbsorption. La vapeur est totalement condensé4 e~
refroidie à la même temp~rature. Simultanément, on injecto aussi dans ce
mélangeur, à un d~bit moyen de 25 kgih un flux de recyclaga issu Idu fond
de la colonne de distillation D1 par la ligne 12.
1 5
Le liquide de fond de ce melangeur, repris par une pompe, est envoyé par
la ligne 2 vers le réacteur d'isomérisation I après appoint d'hydrog~ne
préchauffage à une température de 140C sous une pression de 30 bars.
Le réacteur renferm~ 62 litres d'un catalyseur d'isom~risation ~ bas~
d'alumins h renfermant 7% en poids de chlore et 0,23% en poids cle
platine. Pour maintenir l'activit~ du catalyseur on effectu~ l~n appoint en
continu de 42 g/heure cle tétrachlorure de carbone dans la ~harge ce qui
correspond à une teneur de 5û0 ppm en poids. La réaction d'isom~risation
est conduite sous une pression moyenne de 30 bars et ~ un~ t~mpérature
de 140~C (entr~e) ~ 160C (sortie). Dans ces conditions, I'~ffluen~
hydrocarboné du r~acteur d'isomérisation renferme en~iron 8 % en mo1es
de n(~s, ~,5% en moles de n~ et environ ~6% en moles de methyl~
pentanes.
L'effluent complet du r~acteur d'isom~risation est envoy~ directement par
1a ligne 4 dans la colonne de stabilisation S~ (Figure 3) fonctionnant sous
un~ pression de 15,5 bars, avec un~ temp~ratur9 d'cnvirsn 200C au
rebouilleur et une tempbrature de 30C au ballorl d~ reflux. On purg~ en
tête par la li~ne 15 un mblan~e ~azeux renfermant essentiell~ment d~
., , . ~
- ' - .
.
, - ~ , :
l 3
i'hydrogène~ La fraction de fond renfermant moins d~ 0,5 ppm en poids de
HGI sst soutirée en phase vapeur au niveau du rebouilleur par la ligne 6.
~lle est préchauffee ~ une température de 300C, est introduit~ en phase
vapeur au bas de l'adsorbeur A par la li~n~ 8. Celui-ci fonctionne sous un~
prsssion moyenne de 15 bars el ~ une temp~rature rnoyenne ds 300 C
pendant la phase d'adsorption qui dure environ 6 minutes. L'adsorb~ur d~
16 cm de diametr~ int~rieur et 4 m d~ hawteur ren~rme 60 kg d~ ~olith0
5A sous ~orme d'extrudés da 1,6 mm de diam~tre. A la sorti0 d~ l'adsorb~ur
on récupère par la ligne 9, avec un débit moyen ~'environ 123 kg/h, un
isvmérat renfermant moins de 1 % en moles de parafiines nsrmales en Cs
~t C6 et présentant un IOR de 88 ~ 88,5 qwi est envoyé ensuite sous
pression vers le rebouilleur E3 de la colonne de distiilation Dl.
Simultanément le lit d'adsorbant contenu dans l'adsorbeur D, de mêmes
dimensions que celui de l'adsorbeur A et qui a servi dans une phas~
d'adsorption précédente, est en phase de désorption. Celle-ci est réalis~
p~r abaissement de pression de 15 bars ~ 2 bars et injection par le haut du
réacteur, ~ une température de 300 C et avec un débit moyen de 20 kgm,
d'un soutirag0 de vapeur de la co1Onne Dl riche en méthylpentanes (ligne
10~. I a température du lit d'adsorbant est voisine de 300 C duran~ toute la
phase de désorption qui dur~ 6 minutes. L'effiuent de désorption soutir~ au
bas de l'adsorbeur D renferme environ 29% en moles de nCs ~t ~l % en
moles de nCs. Il est recycl~ par la ligne 11 vers l'éjecteur/mélangeur J.
A la fin de chaque période de 6 minutes, les adsorbeurs A et D sont
permutés au moyen d'un jeu ds vannes, cie mani~re ~ fonctiorlner
alternativement en phasa d'adsorption et de d~sorption.
L'effluent de l'adsorbeur A (li~na 9) totalement condens~ dans la
rebouillaur E3 de la colonne de ~istiilation est dé~endu dans une vann~ d~
controle da pression et le mslange détendu est introduit cians la colonn~ d~
disliliation Dl. La colonne remplie d'un garnissa~e struc~urg présentant
une efficacilé ci'environ 40 btages th~oriques fonc~ionna sous une presslon
do 2 ùars avec un taux dc wflux de 4 par rapport au distillat n~t.
1 4
La ~apeur de la t~te de ta colonne est condensb~ avec l'eau d~
refroidissement et le oondensat est recueilli dans lo ballon de r~flux. De c~
ballon de reflux on soutire par la ligne 14, 76 kg/h d~ distillat qui constilu0
5 le produit final.
Le proc~d~ a ~t~ mis en oeuvre en continu pendant 34 jours dans les
conditions décrites préc~dernment en fournissant un isom~rat dont l'lndicc
d'(:~ctane Recherche (IOR) est rest~ compris entre 89.5 et 91.7.
1 0
, . .
:
:
. .
~:
,:
~ ~:
... .. .
~: : . . .. : .
: . : . . -- : . . :. . :
: - . - ,
.
~ .
: ~ . . . , ~ - . . , . : : .