Note: Descriptions are shown in the official language in which they were submitted.
21 93263
WO 96101902 r~.~r~
~ 1
ADFNovrRus COMPORTANT UN GFNE COD~NT POUR UNE NO
SYNT~A~
La présente invention concerne un adénovirus ~L-~ ~,., h r s comportant un gène
codant pour une NO sy-nthase. Elle concerne également des c~n~ c
r1 -~ permettant l'i ' Iocale et efficace de ces virus
'et plus I ~-', leur utilisation pour le traitement de la
resténose.
Les d~ r~- sont des désordres du ~ . des
l;p~ t~ lr~lY)r~- h1r~ du transport, dans le sang et les fluides p' ~ de
10 lipides comme le cholestérol et les iLigly~,fLilles. Elles conduisent à des pathologies
~ p.~ . Iiées le~ ,iivemclll à rLy~lellOleslelulelllie ou rhypertri~;lyl ' ~ '' ~ .
terles que notamment l'ilillélu~,léLui~r,.
L'dll~r~ lf~ a est la cause principale des infarctus du myocarde et est
'' de près de la moitié du taux de mor-alité dans les pays développf~s.
15 I~Ly~ r~q~ r ns ,1~ erle se traduit I ~ l ' par la formation, au niveau de laparoi des grosses artères, de plaques constituées de cholestérol, lipu~.. ' cellules
spumeuses et/ou tissus fibreux. V ~ '' '' t, ces plaques ' ''
sont la ~r~ ~AI r r . r d'une réponse ~ '' ~ e excessive à ume lésion chronique au
niveau de l'~ ~ ' des parois ar-érieLLes. Ce type de plaque ~.;I._.ulll~ i est
très nettement en relief sur la paroi, ce qui lui confère un caractère sténosimt,,--'.1F- des occlusions vasculaires par athérome, thrombose ou embolie qui
- chez les patients les plus atteints.
La technique cl';-a,M~ pl-~l F est la thérapie la plus ~:UI ' mise en
oeuvre pour rétablir la circulation sanguine à travers l'ar-ère ainsi obstruée. Toutefois,
dans environ 4036 des cas, cette technique échoue du fait de resténose, ~;u~u i~_ à
la blessure mécanique de la paroi artérielle. Cette seconde pathologie est liée
à la migration et la ~ 1 rrl~ rl de ceDlules ' lisses
vasculaires (CMLV) qui premment place en rabsence de la protection etlou du
l t~ exercé5 par le5 ceriules r~nrl~-thf~liA1F~: de l'intima.
Un traitement proposé pour contrer cette ~lulil'él~iiull des cerLules CMLV,
~ consiste à les supprimer par ~' ~ ~ de substances chimiques ou protéiques
adéquates. C'est ainsi que des dérivés de psolarènes sont incorporés dans les cerlules
~luli~ ive~ de manière à les sensibiLiser à raction de la lumière [March et al,
Circulation, ~Z 184-191, (1993)]. De même, certaines cytotoxines, constituées d'ume
~EUILLE DE REMPLACEMENT (REGLE 26)
2 1 ~3263
WO 96/01902 r~.l/rl~ C '~
protéine de fusion entre un fragment de toxine de plante ou bactériemne et un facteur
de croissance, ont également été utilisées à ces fins rPickering et al, J. Clin. Invest.,
2L 724-729 (1993); Biro et al, Circ. Res., :ZL 640 645, (1992); Casscerls et al,Proc.Natl.Acad.Sci.USA, 89. 7159-7163, (1992)].
Toutefois, ces traitements ne donnent pas entière satisfaction en raison
notamment de leur faible spécificité, Ieur efficacité moyenne et un délai d'action
important.
La présente invention a l pour objet de proposer une nouveLe
méthode, par thérapie genique, l "" efficace et sélective pour le
traitement de la resténose post 6 ~. .
L'approche retenue dans le cadre de la présente invention, se distingue
totalement de ce qui précède et consiste à interverlir au niveau de l'expression d'un
des facteurs impliqués dans la uluL'u.aLù-l des CMLV. ~ " t, elle vise à
augmenter la teneur d'un facteur jouimt um rôle d'agent bloquant à l'égard de cette
15 t,lulir~ L~.L
Plus l ' t, la présente invention vise à accroitre la ~ en
monoxyde d'azote, NO, au niveau de la paroi vasculaire, soumise à rh.~g:u~ ;., via
1'. . de la NO synthase, enzyme catalysant la synthèse de NO à partir
d'arginine.
On peut admettre que les quantités de NO, produites à l'état ~ i,iolog.~lu~ par
les ceLIules ~ ~' ' " ' , . ' aux ~ nécessaires à l'intégrité,
i.e. au bon r - ' de la paroi vasculaire. La destruction mécanique de
r. '.( ' "~ ' .~, à 1' ,, I ' ~ conduit donc à une baisse de la prcduction
de NO.
L....... t, il est établi que la r~ n p~ q~ des taux de NO
est capable d'interférer avec la l ' ' des CMLV observée lors de la resténose
[McNamara et al., Biochem. Biophys. Res. Com., 193(1), 291-296, (1993)] ont
notamment montré que 1' ' de L-arginine, précurseur de NO, réduit
l'h~ . ' ~ mtimale dans un modèle de sténose p~ l ' chez le lapin.
L'expression de NO synthase, selon la présente invention, ' au
niveau de la paroi: ' q..,' . permet ~ , de rétablir rapidement des
suffisantes en NO, d'améliorer ainsi le l~,.no~l..~_ vasculaire via la
v~~ DRF dépendante et de bénéficier en outre des effets associés
i..~ti comme ume inhibition de la ~luLf~aLuil des CMLV et une réduction de
I'agrégation l' . Par aiLeurs, NO est également impliqué dans les
2 1 q3263
WO 96101902 r~,l/r. ~.. 3
d' ~- V ' (Ziche et al., J t'lin T .~t. 94, 2036-2044 (1994). Cette
activité - g O' , est reflétée in vitro par la capacité de donneurs de NO tels que
le SNP (sodium l ' ) à s~muler la croissance et la migration des cellules
'~ ' " ' (Ziche et al., J.Chin. Invest. 94, 2036-2044 (1994). NO pourrait donc
5 agir comme un facteur autocrine de la néuv ~ important
dans les situations d'ischérnie notamment .l.yu~.,..Ly.~.
La présente invention ~ rapporte l , ~ à un adenovirus
comportant au moins un gène codant, en totalité ou non, pour l'intégralité ou une
10 partie active d'une enzyme catalysant la synthèse de l'oxyde d'azote.
Les avar~ages de la pré~nte invention résident notamment dans la forte
capacité des adénovirus de l'invention à infecter les cerlules ' ~_ lis~s
vasculaires en IJluliffélaLi~l. Ceci permet d'utiliser des quantités ' ~. faibles
de principe actif (&d~.~.~..~ ' '.~, et permet également une action efficace
très rapide sur les sites à traiter. Les adénovirus de l'invention sont également
capables d'exprimer à très hauts niveaux les gènes introduits, ce qui leur confère une
action i' , , tres efficace. En raison de leur caractère episomal, les
adénovirus de l'invention ont une persistance Lmitée dans les cellules I "~ ve:. et
donc un effet transitoire l ' adapté à reffet i' ~ . recherché.
Le monoxyde d'azote est connu pour intervenir au niveau de l'activité
biologique de EDRF (: ' ' ' derived relaxing factor). EDRF joue un role
important au niveau de la régulation notamrnent du flux sanguin en inhibant les
des muscles mous et ragrégation I ' , ' e [Radomski et al., Lancet 2,
1057-1058 (1987)]. Il faut noter que NO est également présent dans le plasma sous la
forme de g , S . ' ' liés à des protéines telles que ralbumine. Les
S-nitroso-protéines ainsi générées, plus stables que NO, sont , ' ' , du moins
t, de l'activité EDRF. Outre leurs propriétés v ' ' les
S-nitroso-protéines sont également de puissants agents ~ ~ r' l '' '
[Simon et al. ~. .~ . ;. .~. l~ . . .- - and Tl ' , L~. 791-799 (1993)]. Dans le cas des
maladies ~.diuv ' eO, une production altérée de EDRF est associée à la
~,' de l' ' '' u~ et de l'hy~.~ JII pulmonaire et s~ A Le
monoxyde d'azote est également reconnu comme ' t, au niveau du système
nerveux, à titre de r~... et comrne participant, au niveau du système
~ _, à ractivité ~ . . des lI~ Plus ~ t, le monoxyde
d'azote a été décrit comme un agent capable d'agim" sur la ~uLît~al;ull des
2~ 93263
wo 96/0~902 r~ c . . ~13
CMLV puisqu'in vitro, diff6rents composés, donneuts de NO, inhibent la mitogénèse
des CMLV en culture [Garg et al., J. Clin.lnvest., ~, 1774-1777, (1989)].
Les enzymes ~ '' de la production en monoxyde d'azote dans
chacun de ces systèmes, désignées ci-après NO synthases sont, ~ , réparties
5 en trois catégories dites isoforme 1, isoforme 11 et isoforme m.
- La NO synthase dite isoforme I, est exprimée de manière continue et dépendante du
calcium, au niveau des cellules du cerveau. Cette NO synthase neuronale est
constitutive. Elle 2 récemment été clonée chez l'homme [Nakane M., Schmidt H.H,
Pollock J.S., ForstmaM U., et Murad F; Lett. ~l~i (2) 175- 180 (1993)1.
L'isoforme Iï est exprimée dans les ll~l ,' ~ murins et induite par le TNF ou
l'IL 1. La 1 ' ~ des NOS de type inductible est pri~rir:llPm.ont leur capacité àproduire de fortes - de NO en réponse à certaines cytokines. Dans le
cadre de la présente invention, on peut l r '' ' envisager leur expression sous
15 contrôle d'un promoteur exogène, viral ou non, ne contenant pas d'élément de
réponse aux cytokines. Le controle de la production en monoxyde d'azote est, dans ce
cas, assuré par un promoteur présent dans l'~e..~,v,.us. Deux NO synthases humaines
inductibles ont notamment été clonées [Geller et al. Proc. Natl. Acad. Sci. USA, ~Q,
3491-3495 (1993) et Charles et al. Proc. Natl. Acad. Sci. USA, 90. 11419-11423
(1993)].
- En ce qui concerne risoforme m, elle est exprimée dans les cellules ~ '~ ' " ' et
est calcium- ~ s~ ~ Cette isoforme dite ~ v~ ou; '.( ~" ' .
est ' exprimée dans la paroi vasculaire et associée à ractivité EDRF. La
NO synthase ~ '~ ' " ' humaine a été clonée Panssens et al. J Bio. Chem. 267.
14519-145~ (1992) et Marsden et al. FEBS Lett. 307. 287-293 (1992)]. De part sespropriétés d'EDRF, le monoxyde d'azote produit par cette NO synthase joue un rôle
essentiel dans la relaxation des CMLV.
Selon la présente invention, tout gène codant pour l'intégralité ou seulement
une partie active d'une NO synthase ou un de ses dérivés et ~I.,f;~ -. " codant
pour l'une de ces trois isoformes de NO synthases peut être incorporé dans un
adenovirus en vue de son expression in vivo. Par dérivé de NO synthase, on entend
désigner tout pvl.~l;..e obtenu par ~.r '' et consenant une activité
WO 96101902 2 1 9 3 2 6 3 P.l~r~
.
biologique. Par ....- I f;- -:; . on doit entendre toute mutation, ~ délétion,
addition ou, ..I;r;, -l:.... de nature génétique et/ou chimique.
La NO synthase, ou son dérivé, produit dans le cadre de la présente invention
peut être une NO synthase humaine ou une NO synthase animale. Il peut en particulier
5 s'agir d'une NO synthase bovine.
La séquence d'ADN codant pour la NO synthase ou un de ses dérivés, utilisée
dans le cadre de la présente invention peut être un ADNc, un ADN génomique
(ADNg), ou une ~ hybride consistant par exemple en un ADNc dans lequel
10 seraient insérés un ou plusieurs introns. Il peut également s'agir de séquences
~,~ 1 ou
De manière ~ v v , on utilise un ADNc ou un ADNg.
Selon un mode préféré de l'invention, il s'agit une séquence d'ADNc codant
pour une NO synthase humaine.
Pour la ~~ ~ 'h ~ 1 ~ des adénovirus selon l'invention, différents sérotypes
peuvent être utilises. Il existe en effet de nombreux sérotypes .I'~d;..vv.l~, dont la
structure et les propriétés varient quelque peu. Parmi ces sérotypes, on préfèrecependant utiliser dans le cadre de la présente invention les adénovirus humains de
type 2 ou 5 (Ad 2 ou Ad 5) ou les adénovirus d'origine animale (voir demande FR 93
05954). Parmi les adénovirus d'origine animale utilisables dans le cadre de la présente
invention on peut citer les adénovirus d'origine canine, bovine, murine, ~exemple:
Mavl, Beard et al., Virology ~ 81, (1990)], ovine, porcine, aviaire ou encore
simienne (exemple: SAV). De préférence, I'~ vv~.s d'origine animale est un
adénovirus canin, plus l un adénovirus CAV2 [souche manhattan ou
A26/61 (ATCC VR-800) par exemple]. De préférence, on utilise dans le cadre de
l'invention des adénovirus d'origine humaine ou canine ou mixte.
Cornme indiqué ci-avant, les adéno~irus selon rinvention sont défectifs,
c'est-à-dire qu'ils sont incapables de se répliquer de façon autonome dans la cellule
cible. t' ' t, le génome des adénovir~s défectifs utilisés dans le cadre de la
présente invention est donc dépourvu au moins des séquences nécessaires à la
réplication dudit virus dans la ceLIule infectée. Ces régions peuvent être sOie eliminées
(en tout ou en partie), soit rendues non-~ " . soit subsdtuées par d'autres
séquences et notamment par le gène suicide. r.. ~ t, r~d~.vvllus defectif
wo 96/01902 2 1 9 3 2 6 3 . ~I/r~ s ~
conserve néanmoins les séquences de son génome qui sont nécessaires h
.. des particules virales.
r ,r, .. ~ t, les adénovirus défectifs de l'invention ~ A ' les
lTR, une séquence perrnettant 1'~ et le gène codant pour une enzyme NO
synthase. Encore plus ~ rf~ t, dans le génome des adénovirus de
l'ulvention, le gène E1 et au moins l'un des gènes E2, E4, LI-L5 sont non
' Le gène viral considéré peut être rendu non fonctionnel par toute
technique connue de l'homme du métier, et notamment par sup~ totale,
"" délétion partielle, ou addition d'une ou plusieurs bases dans le ou les
genes considérés. De terles "~ peuvent être obtenues in vitro (sur de
l'ADN isolé) ou in situ, par exemple, au moyens des techniques du génie génétique,
ou encore par traitement au moyen d'agents mutagènes
Les adénovirus ' défectifs selon l'invention peuvent être
préparés par toute technique connue de rhomme du métier [Levrero et al., Gene, 101,
195, (1991), EP 185 573; Grabam, EMBO J. ~, 2917, (1984)]. En particulier, ils
peuvent être préparés par ' homologue entre un adénovirus et un
plasmide portant entre autre le gène codant pour la NO synthase. La .
homologue se prcduit après co-i C_Liun desdits adénovirus et plasmide dans une
lignée ceDlulaire appropriée. La lignée ceDlulaire utilisée doit de préférence (i) être
r ~ par lesdits éléments, et (u), comporter les séquences capables de
, ' ' Ia partie du génome de rh~:l~luv~u~ défectif, de préférence sous forme
intégrée pour éviter les risques de l~. ' A titre d'exemple de lignée, on peut
Ia lignée de rein ~ humain 293 [Graham et al., J. Gen. Virol.
~, 59, (1977)] qui contient t, intégrée dans son génome, la partie gauche
du génome d'un adénovirus Ad5 (12 %). Des stratégies de, u. ~ de vecteurs
dérivés des adénavirus ont également été décrites dans les demandes n~ Fl~ 93 05954
et FR 93 08596, Ensuite, les adénovirus qui se sont multipliés sont récupérés etpurifiés selon les techniques classiques de biologie I '' ' comme irlustré dans
les exemples.
Av ~ t, dans les adénovirus de l'invention, le gene codant pour
une enzyme NO synthase est placé sous le contrôle d'un promoteur permettant son
expression dans les ceLlules infectées. ll peut s'agir du propre promoteur du gène, d'un
promoteur h. l; . . .1O~ ou d'un promoteur b,~ ' ' , N( t, il peut s'agir de
promoteurs issus de genes eucaryotes ou viraux. Par exemple, il peut s'agir de
WO96~0l90~ 2 1 ~3263 I_llrl ~ ,i3
séquences ~JIUI~UtLiC~.s issues du génome de la ceLule que l'on désire infecter. De
même, il peut s'agir de séquences IJlUnlVt i~ issues du génome d'un virus, y compris
du virus utilisé. A cet égard, on peut citer par exemple les plUlllVt~ ElA, MLP,CMV, LTR-RSV, etc. En outre, ces séquences d'~ oll peuvent être modifiées
5 par addition de séquences d'activation, de régulation, ou permettant Ime expression
tissu-spécifique. Il peut en effet être I ' ' intéressant d'utiliser des signaux
d~J~JII actifs s~' ~, ou ~ t dans les cellules . - ..1~ .
Iisses vasculaires de préférence en division, de manière à ce que le gène ' ' r '' 1
ne soit exprimé et ne produise son effet que lorsque le virus a ~r~ . infecté
10 une cellule musculaire lisse vasculaire.
Dans un mode particulier de réalisation de l'invention, on utili~ un
adénovirus IC ~ ' ' défectif r , ~ un gène codant pour une NO synthase
sous le contrôle d'un promoteur viral, choisi de préférence parmi le LTR-RSV ou le
promoteur précoce du CMV.
La pré~nte invention vi~ l'utilisation des adénovirus ~lon l'invention à des
fins i' I , et plus I " ~ leur application pour le traitement de la
resténose. Cette application peut notamment être étendue aux situations
u .k.~ ; d'ischémie où les propriétés de NO comme relais: ~g ag
peuvent être Llvul.lL~ exploitées. Leur utilisation est également I~IIV' v
20 pour le traitement de ~ liées au système nerveux central.
Un autre objet de la pré~nte invention concerne donc une,
au moins un adénovirus 1. ' défectif selon
l'invention associé le cas échéant à un excipient Wll.. ' '
Les doses d~d~l'vv--~ ' ' cléfectif utilisées peuvent être adaptées
en fonction de différents paramètres, et notamment en fonction du mode
.1' ' utilisé, de la pathologie wncernée ou enwre de la durée du traitement
recherchée. D'une manière générale, les adénovirus ' selon l'invention sont
30 formulés et administrés sous forme de doses wmprises entre 104 et 1014 pfu/ml, et de
préférence 106 à 101~ pfu/mL Le terme pfu (nplaque forming unit") wrrespond au
pouvoir infectieux d'une solution de virus, et est déterminé par infection d'une culture
cellulaire appropriée, puis mesure, g~ ' ' nprès 48 heures, du nombre de plages
de cellules infectées. Les techniques de " du titre pfu d'une solution virale
sont bien J ' ' dans la littérature.
WO96/01902 2 1 93263 P~,~/r~S.'~ ~13
Un autre objet de rinvention concerne toute cellule de ~' infectée par
un ou plusieurs adénovirus ' défectifs tels que décrits ci-dessus. Plus
' ' . t, rinvention concerne toute population de cerlules hurnaines infectée
par ces adénovirus. n peut s'agir en particulier de cellules; ' ' ' ' cellules
' ~ Iisses, ceriules neuronales, cellules tumorales, etc.
Les cellules selon rinvention peuvent être issues de cultures prirnaires. Celles-
ci peuvent être prélevées par toute technique connue de l~omme du métier, puis mises
en culture dans des conditions pennettant leur ~uLr&~Li~ . S'agissant plus
' ' de '-l '' ceux-ci peuvent etre aisément obtenus à partir de
10 biopsies, par ex~nple selon la technique décrite par Ham [Methods CerBiol. 21a
(1980) 255]. Ces oeDiules peuvent être utilisées dh~h.lu..; pour l'infection par les
adénovirus, ou conservées, par exemple par ~.~ng~ n pour r~ ~ de
banques autologues, en vue d'une utilisation ultérieure. Les oellules selon rinvention
peuvent également être des cultures ' ~ obtenues par exemple à partir de
15 banques préétablies.
Les oellules en culture sont ensuite infectées par des adénovirus
' ~ . pour leur conférer la capacité de produire de la NO synthase. L'infection
est réalisée in vitro selon des techniques connues de l~ornme du métier. En particulier,
selon le type de oellules utilisé et le nombre de copies de virus par oerlule désiré,
20 I'homme du métier peut adapter la multiplicité d'infection. Il est bien entendu que ces
étapes doivent être effectuées dans des conditions de stérilité alJIJlv~ lorsque les
oellules sont destinées à une ~' in vivo. Les doses d'~.l'..~,vl.us
' ~ utilisées pour rinfection des oerules peuvent être adaptées par l'homme
du méder selon le but recherc}~é. Les conditions décrites ci-avant pour r
25 in vivo peuvent être appliquées à rinfeclion in vitro.
Un autre objet de rrnvention conoerne un implant ~des cerlules
marnmifère infectées par un ou plusieurs adénovirus ' ~défectifs telles que
décrites ci-dessus, et une matrioe; " ' I~ t, les implants selon
Frnvention CUI~ ' 105 à 101~ oellules. Plus I ~ " t, ils en
CC.~ ' 106 8 108.
Plus I '' t, dans les implants de l'invention, la matrice
" ' ~ ~ comprend un composé gelifiant et ~.. " un support
permettant l'ancrage des oellules.
WO96101902 2 1 9 26~ P~/r~
Pour la préparation des implants selon l'invention, différents types de
gélifiants peuvent être employés. Les gélifiants sont utilisés pour l'inclusion des ceLules
~ dans une matrioe ayant la ~ ': ~ d'un gel, et pour favoriser rancrage des ceLules
sur le support, le cas écl~éant. Différents agents d'adhésion oeLulaire peuvent donc etre
5 utilises comrne gélifiants, tels que notamment le collagène, la gélatine, les
~Iy~. ~gl~, ~, la ~' les lectines, ragarose etc.
Comme indiqué ci-avant, les ~ ~ .c:l: . selon rinvention,
a~ ' un support permettant rancrage des oeLules. Le terme ancrage
désigne toute forme d' biologique et/ou chimique eVou physique er~aiinant
10 radhésion eVou la fixation des oellules sur le support. Par aiLeurs, les oeLules peuvent
soit recouvlir le support utilisé, soit pénétrer à rintérieur de oe support, soit les deux.
On préfère utiliser dans le cadre de rinvention un support solide, non toxique eVou
bio-compatible. En particulier, on peut utiliser des fibres de ~ul~; ~ ' ' ;l~leCPTFE) ou un support d'origine biologique comme par exernple un greffon veineux.Les irnplants selon l'invention peuvent être implantés en différents sites de
r~ ~ - En particulier, l" ,' peut être effec~ee au niveau de la cavité
1 ' ' e, dans le tissu sous-cutané (région sus-pubienne, fosses iliaques ou
inguinales, etc), dans un organe, un muscle, une tumeur, le systeme nerveux central,
ou encore sous une muqueuse. Les implants selon rinvention sont l ' '
20 avantageux en oe sens qu'ils permettent de contrôler la libération du produiti' li , dans rorganisme: CeLe-ci est tout d'abord déterminée par la multiplicitéd'infection et par le nombre de oeDlules implantées. Ensuite, la libération peut etre
contrôlée soit par le retrait de rimplant, oe qui arrête d'~ i le traitement, soit
par l'ulilisation de rystèmes d'~oll régulable, permettant d'induire ou de réprimer
25 r~ , des gènes i'
Par ailleurs, il a été noté que les propriétés ' ~ ~ 'og, de NO sont
étroitement oontcolées par des réactions d'oxydation. En particulier, la ' '
de NO- par l'ion superoxyde aboutit à la formlation d'ion ~u~ ONOO- et par
30 conséquent à la perte de l'activité EDRF. Selon White et al.
[Proc.Natl.Acad.Sci.USA, 2L 10441048, (1994)], oe processus d'oxydation est
impLqué dans le du.. ' l~, de 1' ' u~l~u~;. Deux .. ~
, " ~ sont en fait mis en jeu: la réduction de l'activité guanylate cyclase
des CMLV inhérente à l'ma~,Liv~liu.l de NO et 1'~ ~ de l'oxydation des
35 L~u~u~L.~,, résultant de l'apparition de pc.u~
2 i 93263 --
wo s6Jol902 P_l/r- ~13
.
L'assosiation d'un traitement anti-oxydant à 1' ~ de l'activité NO
synthase peut par conséquent être souhaitable afin de conserver le bénéfice
i- , . Iié à la production locale de NO. Dans cette perspective, I'
conjointe de '' A ~ rd~' dismutase SOD [Wlute et al., Proc.Natl.Acad.SciUSA, 2L
1044-1048, (1994)] permet de garantir l'u.l~ vasculaire de la production
d'ion ~ On peut I ~ envisager de procéder à une ' ~ ~
conjointe d'un adénovirus selon l'invention avec au moins un second adenovirus
comportant un gène codant pour une superoxyde disrnutase ou encore de met~e en
oeuvre un adénovirus selon rinvention comportant outre le gène codant pour une NO
s,vnthase, un gène codant pour une superox,vde disrnutase.
L'adénovitus et la ~ . l' , , selon la présente invention,
constituent dea mo~vens l ' ' avantageux pour le traitement de la resténose
p~t. ~ . .
La présente invention sera plus ~ .'' décrite à raide des exemples
qui suivent, qui doivent être considérés comme illustratifs et non limitatifs.
L~n~ r~-c
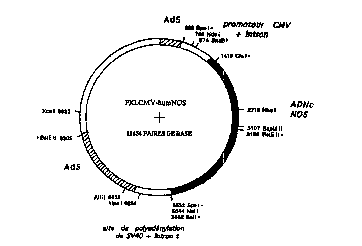
Figure 1: R~ du vecteur pXLCMV-hum NOS
Figure 2: Re~L~.,Ia~ic,n du vecteur pXLRSV-humNOS
Figure 3: T ''' ' de la NOS neuronale humaine sur CMLV; r .
20 par le vecteur pXLRSV-humNOSn.
Figure 4: Validation du vecteur pXLRSV-humNOSn sur CMLV (mise en évidence
de ractivite NOS par mesure de la converaion d'arginine en citmlline).
WO96/01902 2 1 9 32 6 3 ~ rJ u~ [9l3
.
11
r~ ' b- ' ~
Les méthodes l utiTisées en biologie ~ telles que les
extractions ~ ~ d'ADN 1~ qu la ~ , d'ADN ~ en
gradient de chlorure de césium, r;'~ 1 ' ' sur gels d'agarose ou d'~,lyLull; ;k, la
5 r '~ de fragments d'ADN par ~'~ " les extractions de protéines au
phénol ~ au phénol- -' U~ull.~-t la IJl~;~;.4Li~)ll d'ADN en milieu salin par del'éthanol ou de r l l -1, la j r ' dans F~ ' ~ ~ coli, etc ... sont bien
connues de l'homme de métier et sont -~~~- décrites dans la littérature
[Maniatis T. et al., "Molecular Cloning, a Laboratory Manual", Cold Spring Harbor
10 Laboratory-~ Cold Spring Harbor, N.Y., (1982); Ausubel F.M. et al. (eds), ~Current
Protocols in Molecular Biology", John Wiley & Sons, New York, (1987)].
Les plasrnides de ty~e pBR322, pl~C et les phages de la série M13 sont
d'origine ~ (Bethesda Research T ~
Pour les ligatures, les fragments d'ADN peuvent etre séparés selon leur taille
15 par él~i~u~Lu~ en gels d'agarose ou d'..ul~l~.u.l~,, extraits au phénol ou par un
mélange l- 1,'. - uçull~e~ précipités à l'éthanol puis incubés en présence de
rADN ligase du phage T4 (Biolabs) selon les .~ - du '.~
Le ".:rpl; .~,.. des extrémités 5' 1"~ peut être effectué par le
fragment de Rlenow de l'ADN Pol~ ' I d'E. coli (Biolabs) selon les
20 .~lf~ r;.~ du ' La destruction des extrémités 3' pl~ ' ~ est
effectuée en présence de l'ADN Polymérase du phage T4 (13iolabs) utilisée selon les
~ du fabricant. La destruction des extrémités 5' 1 ' ~ est
effectuée par un traitement ménagé par la nucléase Sl.
La _' ' dirigée in vitro par ol;~5~16ui~ , ' ~, peut
25 être effectuée selon la méthode développée par Taylor et aT. [Nucleic Acids Res. 1
8749-8764, (1985)] en utiTisant le kit distribué par Amersham.
L~s ~ ;r;~ e -L.r . de fragments d'ADN par la technique dite de
PCR [~ûl~ catalyzed Chain ~eaction, Saiki R.K. et aT., Science ~Q, 1350-
1354 (1985); Mullis R.B. et FaToona F.A., Meth. Enzym. 1~, 335-350, (1987)] peut30 être effectuée en utilisant un "DNA therrnal c~cler" (Perkin Elmer Cetus) selon les
y~. r;. ~ du fabricant.
La vérification des séquences " ", peut être effectuee par la
méthode développi~e par Sanger et al. [Proc. Natd. Acad Sci. USA, 74 (1977) 5463-
5467] en utilisant le kit distribué par Amersham.
WOg6/01902 21 932G3 ~l/r~S 1513
.
12
F ' 1: C ' . '' du vecteur PXLCMV-humNOS porlant le gène
codant pour la NO synthase sous le controle du L" . précoce du
' . ;. ~ (figure 1)
Cet exemple décrit la ~ uuliu~l d'un vecteur contenant l'ADNc codant
5 pour la NO svnthase ~ 1r humaine, sous le contrôle d'un promoteur constitué
par le promoteur précoce du cytomégalovirus (CMV), ainsi qu'une régiûn de
l'hd~,..uvhusAd5 nécessaire à la L~
Le fragment EcoRI de l'ADNc de la NO svnthase; k ' ' ' humaine,
décrit par Jarssens et al. [J. Biol. Chem. 2Ç:Z, 14519-14522, (1992)] a été recloné
10 dans r''' , II SK + (STRATAGENE), dans l'~ ~ mettant les bases 5' de
l'ADNc du côté du site Not I de pT~ , Un site Sal I est créé par ~ ' de
deux, ' ~ ' ' appariés au niveau du site Not 1.
Le fragment Cla I-Sal I du plasmide résultant contient l'ADNc de la NO
synthase i k ' ' '~ humaine. Ce fragment a été inséré, entre les sites Cla I et Sal I,
dans le plasmide PXL2375 (PCT/FR94/00422) qui comprend les séquences du
promoteur précoce du ~ uus (CMV) et les régions Ad5 permettant la
~ . . r , Le plasmide obtenu a été désigné PXLCMV-humNOS.
E '- 2: ~' ~ du vecteur pXLRSV-humNOSn portant la NO
20 synthare neuronale humaine (type 1) sous le controle du ~,.. LTR-RSV
(figure 2):
Cet exemple décrit la Wll~ll UUliUII d'un vecteur contenant l'ADNc codant pour la NO
synthase neuronale humaine, sous le contrôle d'un promoteur constitué par le LTR du
25 vr;us de sarcome de Rous (LTR-RSV), ainsi qu'une région de l'hu.,nu~llus Ad5
nécessarre à la l~ ' ~ h~-rnr~ g~.o
Le fragment EcoRI de rADNc de la NO synthase neuronale humaine, cloné dans le
vec~Nr pcDNAI (Nakane et al, FELS 316: 175-180, 1993), a été recloné dans le
30 vecteur plC-20H dans l'~ ~ mettant l'extrémité 5' de l'ADNc de la NOS
neuronale du côté du site Cla I (Marsh et al., Gene 32: 431~35, 1984). Le fragment
Cla I-Sal I du plasmide résultant a été inséré entre les sites Cla I et Sal I du plasmide
pXL-RSV-LPL (Ei~ 94 06758) qui comprend les séquences du ptomoteur LTR-RSV
et les régions Ad5 permettart la l~ ' ~ homol(~ P Le plasmide obtenu a été
35 designé pXLRSV-humNOSn.
wo s6/o~so~ 2 1 9 3 2 6 3 r~l/r-- . ,13
13
F. ' 3: Controle de l'activité des vecteurs porhnt le gène codant pour une
NO synthase sur rlodèles de culture ceUulaire in vi~ro
L'activité des vecteurs contenant l'ADNc de NO synthase est controlée sur
des modèles i~l vi~o. Les ceLlules sont j r 'C par les vecteurs contenant les
différentes isoformes de NO synthase (cf. exemple 1,2). La .' de l'activité
NO synthase des cerlules b permet de comparer l'activité des NO synthases
ainsi que l'efficacité des ~,~, utilises (ex.: ~SV-LTR, CMV1
La quantits de N02-/N03-, pr~duits d'oxydation de NO, est determinée dans
le surnageant de culture par la méthode de Ciriess ou si nécessaire par des méthodes
plus sensibles [Misko et al., Analytical F ' y 214, 11-16,
(1993)]. Par ailleurs, ractivité NO svnthase " ' c~ peut etre quantifiée de
manière directe, par mesure de la conversion d'argimne en citrulline [Nakane et al.,
FEBS Letters, ~lk, 1~5-180, (1993)]. L'activité des NO synthases est sensible à
raddition de N- ''yl-L-arginine~ T ~. t, l', ~ ;.". du calcium
est associée à une stimulation de l'activité de la NO sy-nthase neuronale
et;
Différents modèles cellulaires sont dév,sloppés Des clones stables exprimant
les NO synthases sont ~ à partir des lignées cellulaires CHO. Des
transitoires sont aussi effectuées sur d'autres modèles cellulaires tels que
les cellules ' lisses vasculaires de rat et de lapin.
La, u~,hOll pXLRSV-humNOSn (~f ~ , ' 2) a ainsi été validée in
vi~ro sur cvlture primaire de cellules ' ~ lisses de lapin. Brièvement, ainsi
que le montre la figure 3, la présence de la NOS a éte contrôlée par
à l'aide d'anticorps spécifiques de la NOS neuronale (anti-NOS
B220-1, Interchim). En paraUèle, ractivité NO synthase a été mesurée par la méthode
de conversion d'argimne en citrulline (cf supra). Ainsi, l'activité NOS reflétée par la
présence de citrulline tritiée est mise en évidence dans les cellules ' ~ ~ lisses
de lapin; r '~ par le plasmide pXLRSV-humNOSn. Cette activité NOS n'est
pas retrouvée dans les ceUules i ' ' p,ar le plasmide pXLRSV-humNOSn.
Cette activité NOS n'est pas retrouvée dans les cellules I r ~f par un plasmide
témoin exprimant le gène de la b gol~ 1~ de E. Coli sous le contrôle du
promoteur L'rR-RSV (cf. figure 4).
wo96/01902 21 9 3 2 6 3 ~ I/r~ 13
14
Par aiLIeurs, afin de vérifier la 1, " des vecteurs et compléter les
données initiales de Garg et Hassid rJ. Clin. Invest., ~, 1774-1777, (1989)],1'effet de
1'., ~ de la NO synthase est également mesurée sur la ~JluLf~aL;vll des cerluleslisses vasculaires de lapin. Nous avons ~,., ' ~' démontré dans
5 notre modèle ceLlulaire de CMLV de lapin que les donneurs de NO tels que le SNP
ou rh~hv~ ' ~ réduisent la l)luLr~allùn de CMLV de lapin incubées en présence
de ~ optimales de sérum de veau foetal. A forte, l'effet des
donneurs de NO est également associée à une mort ceriulaire qui s'apparente à
rapoptose. Nous avons ainsi mis en évidence une r. c"~ I n.. ~ ' , de
10 I'ADN en oligomères de 180 paires de bases.
4: C ~ d'un a ' . ;. ~ . ~ ' ~ contenant une séquence
codant pour une NO synthrâse
Le plasmide décrit dans l'exemple 1 est linéarisé et .l,l,. f., l~ pour la
~ homologue avec le vecteur adénoviral déficient dans les cellules
15 helper (lignée 293) apportant en trans les fonctions codées par les régions E1 (ElA et
EllB) d'adénovirus.
Plus 1,. ~ l'hd~f.vvllus Ad-CMV-humNOS a été obtenu par
~ homologue in vivo entre l'hd~,..vvlll~5 mutant Ad-dll324
[1'1- ,, ,ya et al., Cerl ~L 543, (1982)] et le plasmide pXL-CMV humNOS,
20 selon le protocole suivant: le plasmide pXL-CMV humNOS linéarise et r~d~.lvvh~la
Ad-dll324, linéarisé par renzyme Clal, ont été co-transfectés dans la lignée 293 en
pr~sence de phosphate de calcium, pour permettre la ' ~ hnn~nlnguP
L'adénovirus ' ~ Ad-RSV-NOSn contenant une séquence codant pour une
NO synthase neuronale humaine a été construit de manière similaire, le plasmide
25 pXLRSV-humNOSn ayant éte linéarisé par l'enzyme Fsp I. Les adénovirus
' ~ ainsi générés ont été _'1--1~ ' par l ~ sur plaque. Après
isolement, rADN de l'~l~ vvh~ ~ 1 - - a été amplifié dans la lignée cerlulaire
293, ce qui conduit à un surnageant de culture contenant l'ad~.~)vll~ défectif
' ~ non purifié ayant un titre d'environ 101~ pfulml.
Les particules virales sont ensuite purifiées par . . ~r ~ '- sur gradient de
chlorure de césium selon les techniques connues (voir notamment Graham et al.,
Virology 52, 456, 1973). Les adénovirus Ad-CMV-humNOS et Ad-RSV-humNOSn
peuvent etre conservés à ~30~C dans 20% de glycérol.
WO 96/01902 2 1 9 3 2 6 3 P~rJ~ c ~ n3
E ' 5: Validation in n/ro de 1'~ Ad-CMV.NOS
contenant une séquence contenant pour une NO synthase
Les cellules ' ~ lisses vasculaires sont I ' ' ' 'infectées par
l'ud~ vil~ [Lee et al., Circulation Research ;73. 797-807, (1993)]. La quantité de
NO générée est alors mesurée ainsi que l'effet de la production de NO sur la
~Lu~ 4aLun ceLlulaire par les techniques décrites dans rexcmple 3. La l~lvlif;.aLv
cerlulaire est determinée par mesure d'il~,v~l~uluLu~l de BrdU dans rADN (Ceri
Fr '~' AssayRPN210,Amersnam).