Note: Descriptions are shown in the official language in which they were submitted.
CA 02324875 2009-01-12
1
PROCEDE ET DISPOSITIF DE PREPARATION DE MATIERES PREMIERES
POUR LA FABRICATION DE VERRE
L'invention concerne un procédé de préparation de certaines des
matières que l'on peut utiliser pour fabriquer du verre ainsi qu'un
dispositif de mise en aeuvre du procédé.
Dans le contexte de la présente invention, on comprend par
" matières premières " tous les matériaux, matières vitrifiables, minerais
naturels ou produits synthétisés, matériaux issus de recyclage du type
calcin etc..., qui peuvent entrer dans la composition venant alirnenter
un four verrier. De même, on comprend par N verre " le verre au sens
large, c'est-à-dire englobant tout matériau à matrice vitreuse,
vitrocéramique ou céramique. Le terme de " fabrication " comprend
l'étape de fusion indispensable des matières premières et
éventuellement toutes les étapes ultérieures/complémentaires visant à
affiner/conditionner le verre en fusion en vue de sa mise en forme
définitive, notanunent sous forme de verre plat (vitrages), de verre creux
(flacons, bouteilles), de verre sous forme de laine minérale (verre ou
roche) utilisée pour ses propriétés d'isolation thermique ou phonique ou
méme éventuellement de verre sous forme de fils dits textile utilisés
dans le renforcement.
L'invention s'intéresse tout particulièrement aux matières
premières nécessaires pour fabriquer les verres ayant une teneur
CA 02324875 2000-10-04
WO 00/46161 PCT/FROO/00239
2
significative en alcalins, notamment en sodium, par exemple les verres
de type silico-sodo-calcique utilisés pour faire du verre plat. La matière
première actuellement la plus fréquemment utilisés pour apporter le
sodium est le carbonate de sodium Na2CO3, choix qui n'est pas dénué
d'inconvénients. En effet, d'une part ce composé n'apporte que le
sodium comme élément constitutif du verre, toute la partie carbonée se
décomposant sous forme de dégagements de C02 lors de la fusion.
D'autre part, il s'agit d'une matière première onéreuse,
comparativement aux autres, car c'est un produit de synthèse, obtenu
par le procédé Solvay à partir de chlorure de sodium et de calcaire,
procédé imposant un certain nombre d'étapes de fabrication et assez
peu économe en énergie.
C'est la raison pour laquelle différentes solutions ont déjà été
proposées pour utiliser comme source de sodium non pas un carbonate
mais un silicate, éventuellement sous forme d'un silicate mixte
d'alcalins (Na) et d'alcalino-terreux (Ca) que l'on prépare préalablement.
L'utilisation de ce type de produit intermédiaire a l'avantage d'apporter
conjointement plusieurs des constituants du verre, et de supprimer la
phase de décarbonatation. Elle permet également d'accélérer la
fusion des matières premières dans leur ensemble, et de favoriser leur
homogénéisation en cours de fusion, comme cela est indiqué, par
exemple, dans les brevets FR-1 211 098 et FR-1 469 109. Cependant,
cette voie pose le problème de la fabrication de ce silicate et ne propose
pas de mode de synthèse pleinement satisfaisant.
L'invention a alors pour but la mfse au point d'un nouveau
procédé de fabrication de ce type de silicate, qui soit notarrnnent apte à
assurer une production industrielle avec une fiabilité, un rendement et
un coût acceptables.
L'invention a tout d'abord pour objet un procédé de fabrication de
composés à base de silicates d'alcalins tels que Na, K et/ou à base
d'alcalino-terreux tels que Mg ou Ca, et/ou à base de terres rares
comme le cérium Ce, éventuellement sous forme de silicates mixtes
CA 02324875 2008-05-30
3
associant au moins deux éléments parmi les alcalins, les alcalino-
terreux et les terres rares, notamment des silicates associant aux
alcalins des alcalino-terreux et/ou des terres rares. Ce procédé consiste
à synthétiser ces composés par conversion de silice et d'halogénure(s),
notamment de chlorure(s), desdits alcalins et/ou desdits alcalino-
terreux et/ou desdites terres rares, du type NaCI, KCl ou CeC14 (et
éventuellement des halogénures, notamment des chlorures d'alcalino-
terreux, dans le cas des silicates en contenant), l'apport thermique
nécessaire à cette conversion étant fourni, au moins pour partie, par un
(des) brùleur(s) immergé(s).
L'invention a également pour objet un procédé de fabrication de
composés à base de silicate d'alcalins, d'alcalino-terreux, de terres rares,
ainsi que de silicates sous formes mixtes associant au moins deux de ces
éléments, par conversion de silice et d'halogénures, de sulfates ainsi que
de nitrates desdits alcalins, desdites terres rares, ainsi que desdits
alcalino-terreux, caractérisé en ce que l'apport thermique nécessaire à la
conversion est fourni, au moins pour partie, par au moins un brûleur
immergé dont les flammes se développent au sein même de la masse des
matières en cours de transformation.
Toujours dans le cadre de l'invention, on peut remplacer tout ou
partie des halogénures comme source d'alcalins/ alcalino-terreux/ terres
rares par des sulfates ou même des nitrates. Il peut ainsi s'agir de
sulfate de sodium Na2SO4. Dans le contexte de l'invention, ces
différents produits de départ (halogénures, nitrates, sulfates) sont donc
à considérer comme équivalents et interchangeables.
On comprend ici sous le terme de " silice " tout composé
contenant majoritairement de la silice (oxyde de silicium) Si02, mème
s'il peut également contenir d'autres éléments, d'autres composés
minoritaires, ce qui est tout particulièrement le cas lorsqu'on utilise des
matériaux naturels du type sable.
CA 02324875 2008-05-30
3a
On comprend ici par " brûleurs immergés ", des brûleurs
configurés de manière à ce que les " flammes " qu'ils génèrent ou les gaz
de combustion issus de ces flammes se développent dans le réacteur où
s'opère la conversion, au sein mème de la masse des matières en cours
de transformation. Généralement, ils se trouvent disposés de façon à
affleurer ou à dépasser légèrement des parois latérales ou de la sole du
réacteur utilisé (on parle ici de flauTUnes, mème s'il ne s'agit pas à
proprement parlé des mèmes " flamrnes " que celles produites par des
brûleurs aériens, pour plus de simplicité).
L'invention a ainsi trouvé une solution technologique
particulièrement judicieuse pour parvenir à exploiter industriellement
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
4
une transformation chimique déjà proposée par Gay-Lussac et Thénard,
à savoir la conversion directe de NaCl en soude, faisant intervenir la
réaction de NaCI avec de la silice à haute température en présence
d'eau selon la réaction suivante :
2 NaCI + SiOz + H20 -+ Na2SiO3 + 2 HCl
le principe consistant à extraire la soude par formation du silicate,
l'équilibre étant déplacé constamment dans le sens de la décomposition
du NaCI parce que les deux phases ne sont pas miscibles.
(dans le cas où l'on utilise du sulfate de sodium plutôt que du chlorure
10. de sodium, la réaction est la suivante :
Na2SO4 + Si02 + H20 + Na2SiO3 + H2S04
Il se forme en fait d'abord du S03, qui se transforme en acide sulfurique
sous l'effet de la température et de l'eau de combustion du brùleur
immergé) .
Cette réaction posait jusqu'ici des problèmes de mise en oeuvre
considérables, liés à des difficultés pour réaliser un mélange intime des
réactifs, et pour assurer leur renouvellement en cours de fabrication,
liés également à des difficultés pour évacuer HCl (ou H2SO4) sans qu'il
réagisse à nouveau sur le silicate formé, pour extraire le silicate et pour
parvenir à apporter l'énergie thermique suffisante.
Utiliser des brùleurs immergés pour apporter cette énergie
thermique résout en même temps la plupart de ces difficultés.
En effet, avoir recours à un chauffage par des brûleurs immergés
avait déjà été proposé pour assurer la fusion de matières vitrifiables
pour faire du verre. On pourra par exemple se reporter aux brevets US-
3 627 504, US-3 260 587 ou US-4 539 034. Mais y avoir recours dans
le contexte précis de l'invention, à savoir la synthèse de silicates à partir
de sels, est extrêmement avantageux :
r- ce mode de combustion génère en effet de l'eau, eau qui, on l'on vu
plus haut, est indispensable à la conversion voulue. Grâce aux
brùleurs immergés, on peut ainsi fabriquer in situ l'eau nécessaire à la
conversion, au moins en partie (même si, dans certains cas, un apport
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
en eau complémentaire peut être nécessaire). On est aussi sûr
d'introduire l'eau au sein même des autres produits de départ, à savoir
la silice et le(s) sel(s) (on désignera par souci de concision sous le terme
de " sels " tous les halogénures de type chlorures d'alcalins, de terres
5 rares, et d'alcal9no-terreux éventuellement, utilisés comme réactifs de
départ), ce qui est bien sûr propice à favoriser la réaction,
b- par ailleurs, la combustion des brûleurs immergés provoque au sein
des matières en cours de réaction de fortes turbulences, de forts
mouvements de convection autour de chacune(s) des " flamme(s) " et/ou
de chacun des jets de gaz provenant de chacun des brûleurs. De fait,
elle va donc assurer, au moins pour partie, un fort brassage entre les
réactifs, brassage nécessaire pour garantir un mélange intime entre les
différents réactifs, tout particulièrement ceux introduits sous forme
solide (pulvérulente) comme la silice et le(s) sel(s),
~- les brûleurs immergés sont aussi particulièrement intéressants sur le
plan strictement thermique, car ils apportent la chaleur directement là
où elle est nécessaire, à savoir dans la masse des produits en cours de
réaction, en minimisant donc toute déperdition d'énergie, et parce qu'ils
sont suffisamment puissants, efficaces pour que les réactifs puissent
atteindre les températures relativement élevées nécessaires à leur
fusion/à leur conversion, à savoir des températures d'au moins 1000 C,
notamment de l'ordre de 1200 C,
'-- ils sont en outre un mode de chauffage particulièrement respectueux
de l'environnement, en réduisant au minimum toute éventuelle
émission de gaz de type NOX notamment.
On peut donc conclure que l'efficacité de ces brûleurs à tous les
niveaux (qualité du mélange, excellent transfert thermique, un des
réactifs généré in situ) fait que la conversion est grandement favorisée,
et cela sans qu'il y ait nécessairement besoin d'atteindre des
températures extrêmement élevées.
Le comburant choisi pour alimenter le(s) brûleur(s) immergé(s)
peut être simplement de l'air. De préférence, on privilégie cependant un
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
6
comburant sous forme d'air enrichi en oxygène, et même sous forme
substantiellement d'oxygène seul. Une forte concentration en oxygène
est avantageuse pour différentes raisons : on diininue ainsi le volume
des fumées de combustion, ce qui est favorable sur le plan énergétique
et évite tout risque de fluidisation excessive des matières en cours de
réaction pouvant provoquer des projections sur les superstructures, la
voûte du réacteur où s'opère la conversion. En outre, les " flammes "
obtenues sont plus courtes, plus émissives, ce qui permet un transfert
plus rapide de leur énergie aux matières en cours de fusion /
conversion.
En ce qui concerne le choix du combustible pour le(s) brûleur(s)
immergé(s), deux voies sont possibles, alternatives ou cumulatives :
r- on peut choisir un combustible liquide du type fioul, ou gazeux du
type gaz naturel (majoritairement du méthane), propane, hydrogène,
b- on peut aussi utiliser un combustible sous forme solide contenant du
carbone, par exemple du charbon ou tout matériau contenant des
polymères hydrocarbonés, éventuellement chlorés.
Les choix faits pour le comburant et le combustible des brûleurs
immergés influent sur la nature des produits obtenus, mis à part les
silicates. Ainsi, quand les brûleurs sont alimentés en oxygène et en gaz
naturel, on a schématiquement les deux réactions suivantes qui se
produisent : (en partant du cas de figure le plus simple où l'on veut
faire du silicate de Na à partir de NaCI, mais on peut le transposer à
tous les autres cas, où il s'agit de faire des silicates de K, de Ce,
contenant Ca ou Mg, etc...) :
(a) 2 NaCI + Si02 + H20 -+ Na2SiO3 + 2 HCl
(b) CH4+202-+ C02 + 2 H20
On peut regrouper ces deux réactions en une seule :
(c) 4 NaC1 + 2 SiO2 + CH4 + 2 02 -+ 2 Na2S1O3 + 4 HCl + CO2
Quand on utilise un combustible de l'hydrogène plutôt que du gaz
naturel, on n'a plus d'émission de C02, la réaction globale s'écrit :
(d) 4 NaCI + 2 SiOz + 2 H2 + 02 -+ 2 Na2SiO3 + 4 HC1
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
7
Quand on utilise un combustible sous forme solide, contenant du
carbone, avec toujours un comburant sous forme d'oxygène, la réaction
suivante s'écrit :
(e) 2 NaCl + 3/2 0 2 + C + Si02 -+ Na2SiO3 + C12 + C02
Cette fois, on ne produit donc plus du HCI, mais du chlore Cla
comme sous-produits de la conversion.
Il est donc clair de ces différentes réactions-bilans que la
conversion envisagée par l'invention génère également des dérivés
halogénés, tout particulièrement des dérivés chlorés valorisables comme
HCl ou C12 que l'on retrouve dans les fumées de combustion. Deux voies
d'utilisation sont possibles :
i-- l'une consiste à les retraiter comme des effluents. On peut ainsi
neutraliser HC1 avec du carbonate de calcium CaCOa, ce qui revient à
fabriquer du CaC12, éventuellement valorisable (pour le déneigement des
routes par exemple),
bu- l'autre voie consiste à considérer la conversion selon l'invention
comme un moyen de fabriquer de manière industrielle HCl ou Cla (ou
H2SO4), produits chimiques de base largement utilisés dans l'industrie
chimique. (On peut notamment substituer le HCl ou le C12 fabriqué
selon l'invention au chlore obtenu par voie électrolytique qui est
nécessaire à la fabrication de polymères chlorés du type PVC,
polychlorure de vinyle). Dans ce cas, il faut alors les extraire des fumées
et établir ainsi une filière de production industrielle de HCl ou de C12,
par exemple en implantant le dispositif de mise en o uvre du procédé
selon l'invention directement dans un site de l'industrie chimique ayant
besoin de ce type de produits chlorés. Valoriser ainsi les dérivés chlorés
formés permet d'abaisser encore le coût des matières premières
porteuses d'alcalins nécessaires à la fabrication du verre.
Un premier débouché pour les silicates fabriqués selon l'invention
concerne l'industrie verrière : ils peuvent se substituer, au moins pour
partie, aux matières premières traditionnelles pourvoyeuses d'alcalins
ou de terres rares, avec tout particulièrement en ce qui concerne le
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
8
sodium, une substitution au moins partielle du CaCO3 par Na2SiO3. On
peut donc employer les silicates de l'invention pour alimenter un four
verrier, et ceci notamment de deux façons différentes :
w- la première façon consiste à traiter les silicates formés pour les
rendre compatibles avec une utilisation en tant que matières premières
vitrifiables pour four verrier : il s'agit donc de les extraire du réacteur et
généralement de les mettre " à froid " en phase solide pulvérulente,
notamment par une étape de granulation selon des techniques connues
de l'industrie verrière. On a donc une déconnexion complète entre le
processus de fabrication du silicate et le processus de fabrication du
verre avec mise en forme appropriée, et stockage/transport éventuel du
silicate formé avant qu'il n'alimente le four verrier,
w- la seconde façon consiste à utiliser le(s) silicate(s) formé(s) selon
l'invention " à chaud ", c'est-à-dire à utiliser un procédé de fabrication
du verre incorporant une étape préalable de fabrication du silicate
venant alimenter, encore en fusion, le four verrier. On peut ainsi
fabriquer le silicate dans un réacteur connecté au four verrier,
constituant un de ses compartiments " amont " par opposition à ses
éventuels compartiments " aval " destinés à l'affinage/le
conditionnement du verre une fois fondu.
Dans ces deux cas de figure, le four verrier peut être de
conception traditionnelle (par exemple four à fusion électrique par
électrodes immergées, four à brüleurs aériens fonctionnant avec des
régénérateurs latéraux, four à boucle, et tout type de four connu dans
l'industrie verrière incluant ainsi les fours à brûleurs immergés), avec
éventuellement une conception et un mode de fonctionnement
légèrement adaptés à un processus de fusion sans carbonate ou avec
moins de carbonate que pour les fusions standards.
Il est à noter que certains silicates autres que le silicate de
sodium sont également très intéressants à fabriquer selon l'invention.
Ainsi, l'invention permet de fabriquer du silicate de potassium à partir
de KCI, ce qui est, économiquement au moins, très avantageux comme
CA 02324875 2000-10-04
WO 00/46161 PCTIFROO/00239
9
matière première porteuse de Si et de K pour fabriquer des verres dits
" à alcalins mixtes ", c'est-à-dire contenant à la fois Na et K. Ces verres
sont notamment utilisés pour faire des écrans tactiles, des verres
d'écran de télévision, des verres pour écran plasma de visualisation
("Plasma Display Panel " en anglais).
De même, l'invention permet de fabriquer de façon plus
économique des verres spéciaux contenant des additifs pour lesquels
les chlorures sont moins chers que les oxydes. C'est le cas des terres
rares comme le cérium : la présence d'oxyde de cérium conférant des
propriétés anti-U.V. aux verres, et les terres rares de ce type rentrent
aussi dans la composition de verres spéciaux à haut module élastique
pour disque dur. L'invention permet ainsi d'avoir une matière première
porteuse de Si et de Ce, le silicate de cérium, à un coùt modéré.
Un autre avantage annexe de l'invention est que la silice
introduite au départ subit lors de la conversion en silicate une certaine
déferrisation car le chlorure de fer est volatil : le verre produit à partir
de ce silicate, en utilisant au moins une certaine quantité de ce silicate
aura donc tendance à être plus clair qu'un verre n'utilisant pas du tout
ce type de silicate. Cela est esthétiquement intéressant, et tend à
augmenter le facteur solaire du verre (dans une application " verre
plat ") .
Un second débouché pour les silicates fabriqués selon l'invention
(à part être utilisés comme matières premières pour four verrier), plus
particulièrement le silicate de soude, concerne l'industrie des
détergents ; le silicate de soude Na2SiOs entrant fréquemment dans la
composition des lessives/détergents.
Un troisième débouché pour les silicates (et éventuellement les
dérivés chlorés) formés selon l'invention concerne la préparation de
silices particulières, désignées communément sous le terme de " silices
précipitées " entrant par exemple dans la composition des bétons. On
peut en effet opérer une attaque acide des silicates formés selon
l'invention, avantageusement par l'acide chlorhydrique HC1 qui a été
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
également formé par la conversion selon l'invention, de manière à faire
précipiter de la silice sous forme de particules ayant une granulométrie
particulière : la dimension des particules visée est généralement
nanométrique (1 à 100 nm par exemple).
5 Le chlorure de sodium également formé lors de la précipitation de
la silice peut avantageusement être recyclé, en servant à nouveau de
matière première pour la fabrication de silicate selon l'invention tout
particulièrement. Il s'agit ici d'un prolongement de l'invention, où,
partant d'une silice particulaire de " grosse " granulométrie (de l'ordre
10 du micron ou plus gros par exemple), on obtient à nouveau de la silice
particulaire mais de dimension de particule bien inférieure, ce contrôle
et cette dimension particulière ouvrant la voie à des utilisations très
variées dans des matériaux utilisés dans l'industrie.
Pour ce troisième débouché plus particulièrement, il est
intéressant de choisir plutôt un sulfate alcalin qu'un chlorure : on
récupère non pas HCl mais H2SO4, qui sert à l'attaque acide du silicate
de soude ainsi formé. C'est ce type d'acide qui est usuellement utilisé
dans l'industrie chimique pour préparer des silices précipitées. Il est
plus avantageux que HC1 dans ce cas particulier, car il évite tout risque
de formation de chlorures résiduels dans la silice précipitée, qui sont
des sources de corrosion potentielles dans certaines applications de
cette dernière.
Un procédé de fabrication de silice précipitée selon l'invention
peut se dérouler ainsi, de façon schématique :
b-- réaction en four équipé de brûleurs immergés (notamment brûleurs
oxy-gas ou oxy-hydrogène), entre un sable de silice de pureté appropriée
et du sulfate de sodium, avec une quantité d'eau à ajouter de façon
contrôlée en complément de celle générée par la combustion, du silicate
de sodium se forme selon la réaction précédemment mentionnée, il est
évacué en continu, le S03 généré se transforme en H2SO4 que l'on
récupère par exemple au niveau de la cheminée équipée en
conséquence,
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
11
b- le silicate de sodium produit avec le module Si02/Na20 adéquat est
ensuite attaqué dans des conditions appropriées (notamment en termes
de pH) par l'acide sulfurique récupéré, la silice est ainsi précipitée, et
traitée ensuite en vue de lui conférer les propriétés voulues selon les
applications envisagées (par exemple en tant que charge pour
caoutchouc pour pneumatiques ...),
b- au cours de cette réaction, il se forme à nouveau du sulfate de
sodium, qui à son tour peut être concentré et recyclé dans le four
équipé de brûleurs immergés comme source de sodium.
On voit que ce procédé peut fonctionner en continu, en boucle
fermée pour ce qui concerne l'acide et la source de sodium. Il se
comporte comme un "tamis à silice" sans autre consommation que celle
du sable et de l'énergie. On peut récupérer aussi la chaleur des fumées
et de condensation de SO3 dans un échangeur approprié pour produire
par exemple la vapeur nécessaire à la concentration des solutions
aqueuses.
Ce type de procédé s'applique de façon tout-à-fait similaire si on
utifise un autre alcalin que le sodium (ou un autre dérivé qu'un sulfate)
ou tout autre élément si tant est que son sulfate est thermiquement
instable et susceptible de conduire au même type de réaction.
Une autre application intéressante du procédé concerne le
traitement (inertage par vitrification tout particulièrement) de déchets
chlorés, tout particulièrement de déchets chlorés et carbonés tels que
des polymères chlorés (PVC, ...) la fusion par brûleurs immergés, selon
l'invention, peut pyrolyser ces déchets, avec comme produits de
combustion ultimes C02. H2O et HCI, HCl (ou même H2SO4) pouvant
être, comme on l'a vu précédemment, neutralisé ou valorisé tel quel. On
peut noter que ces déchets peuvent aussi alors servir de combustible
solide porteur de carbone, ce qui de fait peut permettre de diminuer la
quantité de combustible à injecter au niveau des brûleurs. (Il peut s'agir
d'autres types de déchets comme les sables de fonderie). La pyrolyse de
ces différents déchets est là encore intéressante du point de vue
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
12
économique, car leur coût de traitement par ailleurs nécessaire vient en
déduction du coût de production des silicates selon l'invention. Plutôt
qu'une pyrolyse véritable de déchets, il peut aussi s'agir de vitrification.
Ci-après quelques détails sur l'inertage de ces déchets organo-
chlorés : au sable et au chlorure ou équivalent, on peut donc ajouter
des déchets solides ou liquides du type organo-chlorés. On peut aussi
ajouter différents additifs, comme la chaux, l'alumine (sous forme d'une
argile, matière première peu coûteuse, par exemple), ou d'autres
oxydes. On fait ainsi une véritable vitrification, le vitrifiat obtenu étant à
même d'enrober et de stabiliser les éventuelles charges minérales
contenues dans les déchets en question. Ce vitrifiat peut ensuite être
mis en décharge. L'acide produit peut être récupéré dans une tour
d'absorption ffltrant les fumées et être recyclé. Ce procédé est
économiquement très avantageux : d'une part, le principal fondant
utilisé est apporté par le sel, et une partie au moins de l'énergie
nécessaire à la vitrification est apportée par les déchets eux-mêmes.
D'autre part, il offre la possibilité de recycler l'acide formé, HCI
notamment. On peut bien sûr combiner plusieurs types de déchets
combustibles. Pour cette application, il est préférable de fabriquer un
silicate riche en alcalino-terreux, voire uniquement constitué de silicate
d'alcalino-terreux : puisqu'il s'agit d'inerter des déchets, et non de
fabriquer un verre de haute qualité, il est avantageux d'avoir recours
essentiellement à des silicates d'alcalino-terreux, car la matière
première apportant ces alcalino-terreux est moins coûteuse que celle
apportant des alcalins.
L'invention a également pour objet le dispositif de mise en oeuvre
du procédé selon l'invention, qui comporte de préférence un réacteur
équipé de brûleur(s) immergé(s) et d'au moins un moyen d'introduction
de la silice et/ou des halogénures (ou équivalents du type sulfates ou
nitrates) sous le niveau des matières en fusion, notamment sous la
forme d'une ou plusieurs enfourneuses à vis sans fin. Il en est de
même, de préférence, pour les combustibles solides ou liquides
CA 02324875 2000-10-04
WO 00/46161 PCT/FROO/00239
13
éventuellement utilisés, comme les déchets organo-chlorés
précédemment mentionnés. On peut ainsi introduire directement au
sein de la masse des produits en cours de fusion/réaction au moins
ceux des réactifs de départ susceptibles de se vaporiser avant d'avoir le
temps de réagir : on pense ici tout particulièrement au chlorure de
sodium NaCI, et on garantit un temps de séjour suffisant aux
combustibles liquides ou solides pour achever leur combustion.
De préférence, les parois du réacteur, notamment celles destinées
à être en contact avec les différents réactifs/produits de réaction
impliqués dans la conversion, sont munies de matériaux réfractaires
doublés d'un garnissage de métal. Le métal doit être résistant vis-à-vis
de différentes attaques corrosives, notamment ici de celles provoquées
par HC1. On privilégie donc le titane, un métal de la même famille, ou
un alliage contenant du titane, ou encore du zirconium ou un alliage
contenant du zirconium. Avantageusement, on peut prévoir que tous les
éléments à l'intérieur du réacteur en débouchant dans ce dernier soient
à base de ce type de métal ou protégés superficiellement par un
revêtement de ce métal (les enfourneuses, les brûleurs immergés). Il est
préférable que les parois du réacteur, et notamment aussi toutes les
parties métalliques à l'intérieur de ce dernier soient associés à un
système de refroidissement par circulation de fluide, du type boîte à
eau. Les parois peuvent également être entièrement métalliques, sans
ou avec très peu des réfractaires standards que l'on utilise pour la
construction des fours verriers.
Les parois du réacteur déflnissent par exemple une cavité
sensiblement cubique, parallélépipédique ou cylindrique (base carrée,
rectangulaire ou ronde). Avantageusement, on peut prévoir plusieurs
points d'introduction des réactifs de départ, par exemple répartis de
façon régulière dans les parois latérales du réacteur, sous forme
notamment d'un certain nombre d'enfourneuses. Cette multiplicité des
points d'amenée permet de limiter la quantité de réactifs au niveau de
chacun d'entre eux, et d'avoir un mélange plus homogène dans le
CA 02324875 2008-05-30
14
réacteur.
Le réacteur selon l'invention peut aussi être équipé de différents
moyens de traitement des effluents chlorés, notamment de récupération
ou de neutralisation d'effluents du type C12, HCI, H2S04 et/ou de
moyens de séparation dans les effluents gazeux des particules solides,
notamment à base de chlorures métalliques. Ces moyens sont
avantageusement disposés daris la (les) cheminées évacuant les fumées
hors du réacteur.
Enfin, l'invention a également pour but un procédé d'élaboration
de verre contenant de la silice et des oxydes d'alcalins du type Na20,
K20 et/ou des oxydes d'alcalino-terreux du type MgO ou CaO et/ou des
oxydes de terres rares du type Ce02, par fusion de matières vitrifiables
où l'apport thermique nécessaire à ladite fusion provient au moins pour
partie de brûleurs immergés. Ici, l'invention réside dans le fait que les
matières premières porteuses d'alcalins du type Na, K, ou d'alcalino-
terreux ou de terres rares du type Ce sont au moins pour partie sous
forme d'halogénures, notamment de chlorures, desdits éléments,
comme NaCI, KCI, CeC14 ou des sulfates ou nitrates. C'est ici le second
aspect majeur de l'invention, où, en quelque sorte, tout se passe comme
si on fabriquait le silicate précédemment décrit " in situ ", lors du
procédé même de fusion des matières vitrifiables pour faire du verre.
L'intérét économique à remplacer tout ou partie, notamment, du
carbonate de sodium par du NaCI est clair. On retrouve ici les mêmes
avantages que ceux mentionnés plus haut, concernant la fabrication de
silicate indépendamment de celle du verre, à savoir notainment la
moindre teneur en fer du verre, les valorisations possibles des dérivés
(halogénés) chlorés produits, la pyrolyse ou vitrification de déchets
éventuellement aptes par ailleurs à servir de combustible solide ...
CA 02324875 2008-05-30
19:a
L'invention porte également sur un procédé d'obtention du verre
contenant de la silice et des oxydes d'alcalins du type Na20, K20, des
oxydes d'alcalino-terreux du type CaO, MgO ou des oxydes de terres rares
du type Ce02 par fusion de matières vitrifiables où l'apport thermique
nécessaire à ladite fusion provient au moins pour partie d'au moins un
brûleur immergé dont les flammes se développent au sein même de la
masse des matières en cours de transformation, caractérisé en ce que les
matières vitrifiables porteuses d'alcalins du type Na, K, de terres rares du
type Ce ou d'alcalino-terreux sont au moins pour partie sous forme
d'halogénures, ou de sulfates ou de nitrates desdits éléments.
L'invention sera ci-après détaillée à l'aide d'un mode de réalisation
illustré par la figure suivante :
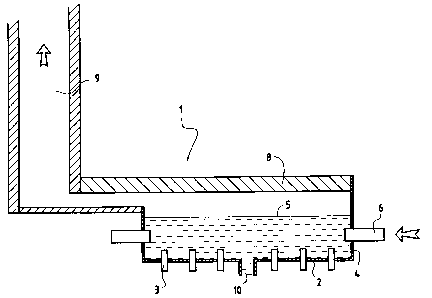
O figure 1 : une installatiori schématique pour fabriquer du
silicate de sodium selon l'invention.
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
Cette figure n'est pas nécessairement à l'échelle et a été
extrêmement simplifiée pour plus de clarté.
Elle représente un réacteur 1 comprenant une sole 2 de forme
rectangulaire percée régulièrement de façon à être équipée de rangées
5 de brûleurs 3 qui la traversent et pénètrent dans le réacteur sur une
hauteur réduite. Les brûleurs sont de préférence recouverts de titane et
refroidis à l'eau. Les parois latérales sont refroidies à l'eau également et
comportent un revétement de réfractaires électrofondus 5 ou sont
entièrement métalliques à base de titane. Le niveau 5 des matières en
10 cours de réaction/fusion est tel que les enfourneuses à vis sans fin 6
introduisent les réactifs au niveau des parois latérales sous ce niveau.
La sole comportant les brûleurs peut avoir une épaisseur de
réfractaires électrofondus plus importante que les parois latérales. Elle
est percée d'un trou de coulée 10 pour extraire le silicate.
15 La voûte 8 peut être une voûte plate suspendue constituée de
matériaux réfractaires du type mullite ou zircone-mullite ou AZS
(alumine- zircone-silice) ou de tout matériau céramique résistant à HCl
et ou NaCI. Elle est conçue de façon à être étanche aux fumées
contenant du HCl : une solution non limitative pour garantir cette
étanchéité consiste à utiliser une structure céramique en nid d'abeille
constituée de pièces hexagonales creuses dans lesquelles on place un
isolant. L'étanchéité est alors réalisée entre les pièces à l'extrados, par
un mastic basse température résistant à HCI. Elle protège ainsi la
structure porteuse métallique. La cheminée 9 est également construite
en matériaux résistants à HCl et NaCI (réfractaires en oxydes, carbure
de silicium, graphite). Elle est munie d'un système de séparation des
particules solides qui sont susceptibles de condenser (chlorures
métalliques) et d'une tour à récupération de HCI, qui ne sont pas
représentés.
Une fois le silicate extrait du réacteur par le trou de coulée 10, il
est acheminé vers un granulateur, non représenté, du type de ceux
utilisé dans l'industrie verrière ou dans l'industrie du silicate de soude
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
16
pour lessive.
Le procédé a pour but de fabriquer un silicate très concentré en
sodium, ce que l'on quantifie de manière connue par un rapport en
mole de NazO par rapport au total (Si02 + Na20) aux environ de 50%, en
introduisant dans le réacteur par les enfourneuses un mélange de sable
(silice) et de NaCl. Ces deux réactifs peuvent être également introduits
séparément, et peuvent avoir été éventuellement préchauffés avant
introduction dans le réacteur.
De préférence, les brûleurs 3 sont alimentés par de l'oxygène et
du gaz naturel ou de l'hydrogène.
La viscosité du mélange en cours de fusion/réaction et la vitesse
de réaction élevée obtenue grâce à la technologie des brûleurs immergés
permettent d'atteindre des tirées spécifiques élevées, pour donner un
ordre de grandeur de par exemple au moins 10 tonnes/jour.
En conclusion, le procédé de l'invention ouvre une nouvelle voie
de fabrication à coût modéré de silicates, tout particulièrement de
silicates de sodium, potassium, cérium (ou encore d'alcalino-terreux). Il
rentre également dans le contexte de la présente invention d'utiliser
mutadis mutandi le même procédé pour fabriquer non plus des silicates
mais des titanates, des zirconates, des aluminates de ces éléments,
(éventuellement mélangés à des silicates).
On substitue ainsi au moins partiellement au silicium un métal,
notamment appartenant aux métaux de transition et plus
particulièrement de la colonne 4b du tableau périodique comme Ti, Zr
ou aux métaux de la colonne 3a du tableau périodique comme Al.
L'avantage d'une telle substitution est que le produit obtenu est soluble
dans l'eau. L'attaque sélection de ces produits en solution aqueuse,
notamment en utilisant l'acide chlorhydrique formé lors de la
conversion, conduit à la précipitation de particules non plus de silice,
comme mentionné plus haut dans le texte, mais de particules d'oxyde
métallique correspondant comme 1102, Zr02, A1203, généralement
présentant des dimensions nanométriques comme lorsqu'on part de
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
17
silice, et qui trouvent de nombreuses applications dans l'industrie. On
peut ainsi les employer en tant que charges dans des polymères, dans
les bétons, les incorporer dans des matériaux céramiques ou
vitrocéramiques. On peut aussi exploiter leurs propriétés
photocatalytiques : sont particulièrement visées les particules de T102
(qui peuvent être incorporées dans des revêtements photocatalytiques à
propriétés anti-salissures pour tout matériau architectural, vitrage,
etc...).
Pour fabriquer selon l'invention ces titanates, zirconates,
aluminates, on transpose directement le procédé décrit plus haut pour
obtenir les silicates, en partant d'halogénures du type NaC1 et des
oxydes métalliques des métaux impliqués (Ti02, Zr02, A1203, ...).
Alternativement, on peut utiliser comme produit de départ de la
conversion porteur du métal directement l'halogénure dudit métal et
non plus son oxyde. Il peut notamment s'agir de chlorure comme TiC14,
ZrC14, A1C13 (on peut également choisir comme produits de départ
porteurs du métal un mélange d'oxyde et de chlorure dudit métal). Dans
ce cas, la matière porteuse d'alcalins peut être le même halogénure du
type NaCl utilisé pour faire du silicate, ce sel pouvant être
éventuellement complété ou remplacé par de la soude quand c'est
l'alcalin sodium qui est impliqué.
Tout comme pour le cas de la " silice précipitée ", ce prolongement
du procédé selon l'invention peut ainsi être vu comme un moyen de
modifîer, notamment d'abaisser la dimension des particules d'un oxyde
métallique, de façon à lui ouvrir d'autres applications dans des
matériaux industriels.
Il est à noter que l'invention permet de recycler différents déchets.
Il peut s'agir, notamment, de nettoyer/traiter du sable pollué,
notamment lors de marées noires : on peut ainsi collecter le sable
souillé comme produit de départ pour la silice. Cela présente deux
avantages majeurs :
~- d'une part, le sable est déjà irnprégné du combustible (le fuel, les
CA 02324875 2000-10-04
WO 00/46161 PCT/FR00/00239
18
composés hydrocarbonés qui le souillent),
à- d'autre part, c'est une méthode simple pour débarrasser les côtes et
les plages de leur sable pollué, quand tout autre moyen pour nettoyer le
sable est trop long ou trop coûteux. La méthode de l'invention permet
donc d'éliminer complètement le fuel. Il est avantageux, pour ce type
d'application, de fabriquer des silicates d'alcalino-terreux ou
majoritairement à base de ces éléments : tout comme pour l'application
à l'inertage des déchets organo-chlorés mentionnée plus haut, il est
économiquement plus intéressant d'utiliser des matières premières
porteuses d'alcalino-terreux que des matières premières porteuses
d'alcalins.