Note: Descriptions are shown in the official language in which they were submitted.
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
1
STRUCTURES COMPOSITES EN ETAT AMORPHE POUR LA PHOTOC.P,TALYSE
La présente invention concerne un nouveau type de
photocatalyseur - structures composites en état amorphe - dont
le fonctionnement est basé sur le phénomène de la séparation
forcée des porteurs de charge libres (électrons, trous)
empêchant leur recombinaison immédiate.
Principes et techniques existants
L'effet photocatalytique est basé sur le phénomène
de l'excitation d'un semi-conducteur par des rayonnements
lumineux (UV ou Visible). L'excitation photonique conduit à la
création de paires électron - trou positif résultant du
passage d'électrons de la bande de valence du semi-conducteur à
sa bande de conduction. Grâce à l'existence des zones interdites
jouant les rôles de barrières énergétiques contre la
recombinaison des porteurs de charge libres, ces dernières
accèdent à la surface du corps solide, s'attaquent aux complexes
d'adsorption et donc favorisent leur transformation en produits
finaux.
Actuellement, seuls les semi-conducteurs (corps
solides cristallins) sous la forme de micro- et nanoparticules
sont considérés comme des photocatalyseurs prometteurs. Leurs
cristallinités garantissent, d'un côté, une séparation
efficace des porteurs de charge (e-, h+) et évitent leur
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
2
recombinaison immédiate. De l'autre côté, les tailles de
ces particules cristallines sont dimensionnées, de
préférence, en dizaines ou centaines de nanomètres, afin
d'assurer pour une partie importante des porteurs libres
l'accessibilité aux surfaces de contact. Ces dimensions
sont compatibles avec les distances parcourues par des
porteurs de charges dans un corps cristallin pendant leurs
durées de vie moyennes, comme mentionné dans la référence
[1] de la bibliographie.
Dans ce qui suit, les chiffres entre crochets
correspondent à des références bibliographiques à la fin de
la présente description.
La figure 1 présente 3 principaux types de
matériaux actifs reconnus pour manifester des capacités
photocatalytiques importantes. Ces matériaux comportent des
composants photocatalytiques généralement dans l'état
cristallin.
Le photocatalyseur industriel le plus répandu est
le produit commercialisé par Degussa - Deutsche
Gesellschaft, Allemagne (nom commercial : Degussa P25,
produit cristallin en dioxyde de titane contenant - 80% de
la phase d'anatase et - 20% de la phase de rutile) [2].
Actuellement l'élaboration de nanoparticules
cristallines du dioxyde de titane s'effectue, dans la plus
part de cas, par les techniques basées sur l'application du
plasma ou par la méthode Sol-gel. Les techniques de plasma
[cf. 3, par exemple] utilisent des précurseurs de titane,
organiques ou inorganiques, en état gazeux qui s'ionisent à
des températures élevées. En présence de l'oxygène, les ions
Ti4+gaZ se transforment en oxyde de titane Ti02 aggloméré en
nanoparticules. La méthode Sol-gel est basée sur l'hydrolyse
des sols d'alcoxydes de métaux dont les produits finaux sont des
oxydes métalliques. Les nanoparticules de Ti02 peuvent être
élaborées, respectivement, par l'hydrolyse des alcoxydes de
titane dans les conditions contrôlées [4].
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
3
Les méthodes plus sophistiqués, comme Layer-by-Layer
Self-Assembly (LBL-SA) [5] ou Ultrasonic Spray Pyrolysis (USP)
[6], sont également appliquées, à l'échelle de laboratoire,
pour la fabrication de cristaux nanométriques.
Les techniques décrites en [5,6] permettent également
d'obtenir des particules cristallines optimisées en taille (10 =
100 nm. de diamètre). Ces dimensions sont considérées comme les
plus appropriées pour l'application photocatalytique.
Cependant, les produits issus des procédés des
références [3-6] représentent toujours des matières
préfabriquées qui ont besoin ensuite d'une fixation solide
sur des parois de support afin d'être appliquées en tant
qu'éléments d'unités photocatalytiques. Le seul mécanisme
permettant de fixer une particule cristalline existante
( préfabriquée ) sur un support externe est son adhésion
physique. L'adhésion physique, par contre, ne permet pas
d'aboutir à la création de composites à des stabilités
suffisantes. Mécaniquement très fragiles, ces systèmes se
dégradent rapidement lors d'utilisation.
Afin d'éviter ces difficultés liés aux manipulations
avec les nanoparticules cristallines préfabriquées, il est
raisonnable d'envisager leur remplacement par des produits
composites dont la phase active peut être chimiquement greffée
in situ sur un support.
La littérature scientifique actuelle présente un
certain nombre de techniques sophistiquées et coûteuses pour
l'élaboration de produits composites à propriétés
photocatalytiques (exemples : Arc Ion Plating (AIP) [7], Dip-
coating [8], Photo-Inducted Sol-gel [9], Plasma Associed
Metallo-Organic CVD [10, 11], Sputtering [12, 13], Photo-
assisted pulsed laser deposition [14], etc.).
Actuellement, ces méthodes ne dépassent pas l'échelle
de laboratoire. Par contre, leurs applications permettent
d'élaborer des structures composites contenant des
nanoparticules cristallines de Ti02 greffées sur différents
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
4
supports poreux (Si02, y-A1203, charbon actif, etc. ). En général,
ces produits manifestent une activité photocatalytique
comparable à celle de Degussa P25.
Les techniques [7-12, 14] et autres techniques
modernes sont appelées à l'élaboration des photocatalyseurs
composites dont les phases actives sont présentées par des
nanostructures cristallines. Dans les cas où les composants
actifs se forment initialement en tant que structures
désordonnées, ils subissent des traitements complémentaires,
tels que l'irradiation ou la calcination, afin d'être
transformés en état cristallin, comme décrit dans [11].
Sauf quelques références rares (par exemple [13, 15,
16]), des matériaux non cristallins ne sont pas considérés comme
les produits photocatalytiques à cause de leurs structures
désordonnées favorisant une recombinaison immédiate des porteurs
de charge. En effet, l'absence dans les structures désordonnées
de barrières énergétiques internes (zones interdites) jouant
contre la recombinaison immédiate des porteurs de charges est
considérée comme un obstacle fatal empêchant des produits
amorphes de concurrencer les produits cristallins.
L'invention
L'invention concerne une composition et un principe de
fonctionnement d'un photocatalyseur composite dont la phase
active est constituée d'agrégats sphériques nano- et
micrométriques de dioxyde de titane en état amorphe,
chimiquement liés avec la surface d'un support manifestant des
fortes propriétés d'acide ou de base de Lewis et jouant donc
pour la phase active le rôle d'une source d'un champ électrique
extérieur réalisant la séparation forcée des porteurs de charge
libres par la neutralisation (piégeage) des charges d'un premier
type (négatives ou positives) à la faveur d'un autre.
Plus précisément, l'invention résulte de l'hypothèse
qu'il est possible de faire fonctionner les structures amorphes
en tant que photocatalyseurs hétérogènes en séparant les
porteurs de charge par une force extérieure. Le rôle de cette
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
force extérieure peut être joué par la force d'interaction entre
des charges électriques opposées. Par exemple, les porteurs de
premier type, négatif ou positif, peuvent être sélectivement
neutralisés in situ par un support manifestant les propriétés
5 électriques particulières - propriétés d'accepteur ou celles de
donneur. Dans cette situation favorable les porteurs de deuxième
type sont protégés contre la recombinaison immédiate.
Ainsi l'invention se rapporte à des structures
composites en état amorphe dont le fonctionnement est basé sur
le phénomène de la séparation forcée des porteurs de charge
libres (électrons, trous) empêchant leur recombinaison
immédiate.
Les supports accepteurs dont les acidités de Lewis
sont importantes, tels que la silice, l'alumine, le phosphate
d'aluminium, ou l'oxyde de zirconium seuls ou en combinaison
sont utilisés comme des pièges à électrons, tandis que les
supports métalliques manifestant des propriétés de base de Lewis
forte sont utilisés comme des piéges à trous.
Ainsi, l'invention concerne, de façon générale, un
système composite comprenant un composant photocatalytique en
état amorphe et un support actif destiné à neutraliser les
porteurs de charges libres d'un premier type, électrons ou
"trous" positifs, afin de protéger les porteurs de charge du
deuxième type contre la recombinaison.
Dans une réalisation, le support actif est un support
accepteur à forte acidité de Lewis.
En variante, le support actif est un support donneur.
Selon une réalisation, l'élément photocatalytique
(composant actif) est constitué de nano et micro-particules
désordonnées (amorphes) de dioxyde de titane chimiquement liées
au support afin d'assurer un transfert efficace des porteurs à
neutraliser vers la masse du support accepteur ou donneur.
L'invention concerne ainsi, dans une réalisation,
l'utilisation du dioxyde de titane en tant que composant actif
des systèmes photocatalytiques. Elle substitue les structures
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
6
cristallines actuellement utilisées dans la pratique, par des
produits composites constitués en nanoagrégats amorphes de Ti02
chimiquement fixés sur les surfaces des supports solides
disposant des capacités importantes d'acceptation ou de donation
d'électrons (supports accepteurs/donneurs).
L'activité photocatalytique de Ti02 amorphe est due à
la séparation artificielle des porteurs de charge (e-, h+) dans
le champ électrique extérieur fourni par le support
accepteur/donneur. Cette séparation forcée préserve les porteurs
de charge contre la recombinaison immédiate et permet aux
porteurs d'un type choisi de garder les états libres lors de
leurs déplacements vers les surfaces actives. Les porteurs de
deuxième type sont neutralisés in situ par l'action du support.
Pour les moyens de l'invention, on décrit un
exemple qui concerne l'élaboration des produits composites
de type Nano-agrégats amorphes de Ti02 - Support d'oxyde
aux capacités d'accepteur prononcées .
Les surfaces d'oxydes amorphes disposent de plusieurs
groupes fonctionnels. Dans les conditions ambiantes et jusqu'à
250-300 C elles sont enrichies en sites actifs de Brôensted
(acides et basiques). Cette population active permet de greffer
chimiquement sur les surfaces d'oxydes des modificateurs de
types différents.
L'élaboration des structures composites de Ti02,
cristallines et amorphe, sur des supports minéraux peut être
effectuée par la plupart des méthodes citées ci-dessus. Du point
de vue technologique, ces composites peuvent être élaborés
notamment par les méthodes Sol-Gel, Sputtering, Plasma
Assistance CVD, ML-ALE-CVD qui signifie Molecular Layering ou,
selon la terminologie alternative, Atomic Layer Epitaxy [17,
18]. Cette dernière, grâce à sa simplicité relative, paraît être
mieux adaptée pour l'élaboration des produits proposés, surtout
de type nano-, microagrégats amorphes de Ti02 - Support
accepteur , tant dans les conditions de laboratoires que dans
les conditions industrielles.
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
7
Selon le procédé ML-ALE-CVD, un support solide dont la
surface est préalablement fonctionnalisée afin d'être enrichie
en sites actifs de Brôensted, est traité in situ par un
précurseur volatil minéral (par exemple, un produit oxy-halogéné
ou halogéné - MeLOMHalN, MeLHalN) ou organométallique (par
exemple, un alcoxyde - MeL-ORN), puis hydrolysé, se transforme
en matériau composite agrégats nanométriques d'oxyde -
support (réactions (1) et (2), exemple avec le précurseur
halogéné)
MeI,H.alN + x(H - 0) - Support ~ N xHal-MeL Ox -
Support + X H-Hal t (1)
N xHal-MeL Ox - Support + (N-X) H2Ovapeur N-x (H -
0) -MeL Ox - Support + (N-X) H-Hal (2)
Une série des produits composites de type Nano-
agrégats amorphes de Ti02 - Support accepteur peut être
élaborée à l'aide de la méthode ML-ALE-CVD comportant des
paramètres opératoires particuliers.
La protection de charges libres contre la
recombinaison in situ par leur séparation forcée peut être
effectuée également par les supports actifs donneurs dont le
rôle consiste en un enrichissement des agrégats
photocatalytiques en électrons. Dans ce cas, les supports
d'oxydes à hautes acidités de Lewis (accepteurs d'électrons)
peuvent être remplacés par des supports poreux contenants des
agrégats de métaux élémentaires dispersés sur leurs surfaces.
Ces supports donneurs fournissent des électrons complémentaires
aux composants photocatalytiques en immobilisant donc les
charges positives (trous électroniques). L'élaboration des
produits composites de type nano- microagrégat amorphes de
Ti02 - Support donneur peut être effectuée par une des
techniques conçues à la création de dépôts d'oxydes sur les
surfaces métalliques, par exemple la technique Sol-Gel.
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
8
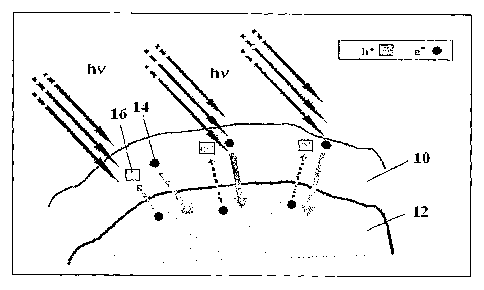
La figure 2 représente un système selon l'invention
qui comprend un composant 10 actif en état amorphe, et un
support 12 accepteur à forte acidité de Lewis ou un support
donneur. Dans le cas d'un support accepteur les électrons e- 14
vont vers le support 12. Dans le cas d'un support donneur les
électrons de ce support vont (flèches en traits interrompus)
vers les trous h+ 16 du composant 10.
Exemple détaillé de réalisation
Les produits composites selon l'invention contiennent
des agrégats nanométriques amorphes de Ti02 greffés sur des
supports de silice (Si02) et d'alumines activées (y-A1203), ainsi
que sur des supports complexes (Si02 * Fe3+, Si02 * Cr207 2-, Si02 *
Cr042 , y A1203 * Fe3+, y-A1203 * Cr207 2 , y A1203* Cr042 ). Les ajouts
de Fe3+ ou Cr6+ dans les supports purs ont été choisis afin de
mieux démontrer le mécanisme de fonctionnement des composites
nano-, microagrégats amorphes de Ti02 - Support accepteur .
Toutefois ces ajouts ne sont pas indispensables pour
l'amélioration des propriétés photocatalytiques des produits
composites selon l'invention.
Les oxydes choisis - Si02r y-A1203 - en tant que
supports actifs sont des acides de Lewis forts (accepteurs
d'électrons). Ils sont capables d'immobiliser les charges
négatives (électrons) [19, 20] en laissant libres les
charges positives (trous électroniques) dans les structures
surfaciques excitées par des rayonnements lumineux. Les trous
électroniques sont considérés comme des oxydants très puissants
favorisant la dégradation efficace des produits pré-adsorbés sur
la surface [21].
Afin de tester l'activité photocatalytique des
échantillons élaborés, deux réactions de l'oxydation totale de
composés organiques volatiles ont été choisies : l'incinération
photocatalytique de vapeur de trichloroéthane (C2H3C13) et celle
de vapeur de toluène (C7H8)
C2H3C13 + 202 2CO2 + 3H01 (3)
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
9
C7H8 + 902 7CO2 + 4H20 (4)
Un des produits de l'oxydation totale de
trichloroéthane est l'acide chlorhydrique, HCl (réaction (3)).
Sa solubilité importante dans l'eau (700 volumes HCl par 1
volume d' eau dans les conditions standard) permet de suivre les
performances photocatalytiques de trichloroéthane C2H3C13 par des
mesures de l'évolution du pH dans un récipient agité en aval de
l'installation de test. La deuxième technique utilisée pour le
suivi des performances photocatalytiques de C2H3C13 et de C7H8 a
été la technique chromatographique (chromatographe Hewlett-
Packard 5890 séries II, avec un détecteur HP 5972 (FID)).
Les tests photocatalytiques ont été réalisés à l'aide
d'une installation de laboratoire. Les paramètres opératoires
sont présentés dans le tableau 1. Tous les échantillons
composites testés contenaient sur leurs surfaces entre 6 et 7%
en masse de Ti02 en état amorphe (produit N 3-5 et 7-9 dans le
tableau 2 ci-après ou cristallin produit N 2 dans le tableau 2).
Tableau 1 : Condition opératoires
Paramètre Valeur
Concentration initiale de trichloroéthane et de Co= 35 - 40 ppm
toluène dans la phase gazeuse
Humidité relative de gaz à traiter cp = 40 %
Débit de gaz à traiter G 400 ml/min
Temps de séjour de mélanges gazeux dans la zone 4ti ;~e12 s
réactionnelle
Dimensions du réacteur de test (réacteur tubulaire) L = 13 cm, D = 3,5 cm
Masse de photocatalyseur dans la zone réactionnelle n1~,,t = 1,1 g
Caractéristiques de la source d'irradiation Lampe UV black light ,
365 nm, 6W
En comparant les échantillons photocatalytiques sur
les supports purs de silices et d'alumines activées, on
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
constate une activité importante pour les premiers et une
activité assez faible pour les derniers (tableau 2,
échantillons 3 et 7).
Cette différence en activité photocatalytique peut
5 être expliquée par des particularités des systèmes
dynamiques Ti02-SiO2 et Ti02-yAl2O3 . En effet, les
capacités de silices en tant que supports accepteurs
dépassent largement celle d'alumines, grâce à la présence
sur les surfaces de silices des sites acides de Lewis très
10 puissants [19].
Les activités des échantillons à base de Degussa P25,
tant pur que sur support accepteur, restent supérieures à
celles du composite Ti02 amorphe - alumine pure
(échantillons 1, 2 et 7 dans le tableau 2), tandis que le
composite Ti02 amorphe - silice pur (échantillon 3)
dépasse largement les produits à base de Degussa P25.
Tableau 2. Activité photocatalytique des produits dans
la réaction de l'oxydation totale de trichloroéthane C2H3C13
No. Echantillon Type de support : Activité,
pur (Pr), pmo1/g,at=h
imprégné (Im) .10~-3
1 Degussa P25 pur (6.2g) Carton (fixation par 15
adhésion)
2 Si02 + Degussa P25 Pr-Si02 (fixation par 50
adhésion)
3 S-1T-CVDm-070504 Pr-Si02 610
4 SF-1T-CVDm-230404 Im Fe +-SiOz (avec 220
1,5% Fe203)
5 SC-1T-CVDm-300404 Im Cr-SiOz (avec 400
1, 5% Cr203)
6 Si02 - 0
7 A-1T-CVDm-290304 Pr-yAlz03 2
8 AF-IT-CVDm-200404 Im Fe3+-yAlz03 (avec 20
1,5% Fe203)
9 AC-IT-CVDm-300404 Im Cr6+-yAlz03 (avec 400
1, 5% Cr203)
10 y-A1203 - 0
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
11
Pour tenter d'améliorer les performances
photocatalytiques des produits composites, on a élaboré une
série d'échantillons sur supports d'oxydes dopés en pièges à
électrons (composés à base des métaux de transition) . Cette
démarche a eu pour but la création de supports accepteurs à des
capacités élevées. En tant que composés de dopage, on a utilisé
les oxydes de fer (Fe203) dont les sites actifs sont présentés
par les cations Fe2+ et Fe3+. Les complexes anioniques de chrome
(chromates et bichromates - Cr042-, Cr207 2-) ont été aussi
appliqués.
L'élaboration des supports dopés a été effectuée par
l'imprégnation des supports initiaux (Si02, y-A1203) en solutions
de sels métalliques, suivie par leur conditionnement et
traitement thermique (conditionnement - 24 h, température
ambiante ; séchage - 8 h, température 110 C ; calcination - 4
h, température 550 C).
Les données présentées dans le tableau 2 mettent en
évidence une amélioration importante de l'activité
photocatalytique des échantillons [yA1203 - Fe3+] * Ti02 et
[yA1203 - Cr6+] * Ti02 (échantillons 8, 9) par rapport à
l'échantillon yA1203 * Ti02 (échantillon 7). Ce phénomène peut
être expliqué par la présence sur les surfaces des alumines
dopées (yA1203 * MeXOY) des sites accepteurs plus forts que les
sites initiaux (A13+) [20]. Par rapport à des alumines pures, ces
supports complexes doivent donc être considérés comme les agents
accepteurs plus efficaces en séparation forcée de charges
électriques.
Au contraire, les capacités d'acceptation d'électrons
pour les supports [Si02 - Fe3+] et [Si02 - Cr6+] ont été supposées
moindres par rapport à celles de la silice pure : les activités
photocatalytiques des échantillons 4 et 5 restent moins
importantes que l'activité de l'échantillon 3 (tableau 2). Cette
circonstance est due, très probablement, à une puissance
exceptionnelle des sites Si4+ en tant qu'acides de Lewis [19].
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
12
Il est à noter que les influences des supports
d'origine (Si02 et y-A1203) sur l'efficacité de la séparation de
charges diminuent rapidement lors de leur enrichissement en
composés de dopage. Par exemple, les échantillons 5 et 9
(tableau 2) manifestent les même activités photocatalytiques,
bien que l'échantillon 5 est élaboré sur un support de Si02 et
l'échantillon 9 sur un support de y-A1203 .
Les meilleurs résultats sont obtenus en utilisant le
support accepteur en silice pure (échantillon 3 dans le tableau
2). Ce fait démontre qu'il n'est pas nécessaire de fournir des
ajouts accepteurs (pièges à électrons) dans les produits
composites de type nano-, microagrégats amorphes de Ti02 -
Support accepteur dont les supports sont constitués de
silices.
La figure 3 représente l'évolution temporelle de la
concentration de toluène en aval de l'unité photocatalytique.
Les courbes 22-24 comportant des triangles, des carrés et des
losanges non remplis correspondent respectivement aux courbes du
Degussa P25 sans éclairage, du composite Silice - Ti02 sans
éclairage et du composite Alumine - Ti02 sans éclairage.
Tandis que les courbes 25-27 comportant des triangles, des
carrés et des losanges remplis correspondent respectivement aux
courbes du Degussa P25 avec éclairage, du composite Silice -
Ti02 avec éclairage et du composite Alumine - Ti02 avec
éclairage.
Le tableau 3 ci-après représente l'activité
photocatalytique des produits dans la réaction de l'oxydation
totale de toluène C7H8 :
No. Echantillon Capacité d'adsorption Activité Contenu de
sans éclairage, photocatalytique Ti02 dans
ug/mg,~at uglmgt!o2*h l'échantillon
composite, mg
1 Si02 - Ti02 1.40 4.10 62
2 yAlz03 - Ti02 0.90 1.80 59
3 Degussa P25 0.01 0.35 60
4 Carton - Ti02 0 0 53
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
13
Les comportements des échantillons vis-à-vis du
traitement photocatalytique de l'air chargé en vapeur de toluène
représentés à travers ce tableau 3 et cette figure 3 peuvent
être discutés en termes de capacité d'adsorption des composites
poreux et en termes de propriétés électroniques des supports
actifs.
Les meilleures capacités photocatalytiques sont
toujours manifestées par les composites nano-, microagrégats
amorphes de Ti02 - Support accepteur à base de silice
(échantillon 1 dans le tableau 3 et courbe représentées par des
carrés pleins sur la figure 3). Au contraire, l'échantillon
composite à base de carton (N 4 dans le tableau 3) ne possède
aucune activité car son support ne dispose pas des capacités
d'acceptation d'électrons et ne peut donc pas activer des
agrégats de Ti02 amorphes situés sur sa surface.
Dans le cas du toluène C7H8 dont les facilités
d'adsorption sur les surfaces solides sont largement supérieures
par rapport à celles du trichloroéthane C2H3C13r l'échantillon à
base d'alumine activée ayant la surface spécifique à l'entour de
260-270 m2/g possède une activité photocatalytique supérieure à
celle du Degussa P25 qui possède une surface spécifique moindre
de 50m2/g.
Dans le cas du toluène et dans celui du
trichloroéthane, les activités photocatalytiques sont donc
renversées (cf tableaux 2 et 3). Ce phénomène peut être expliqué
par le fait que des supports poreux ayant des hautes capacités
d'adsorption, comme les silices et les alumines activées,
peuvent contribuer à la performance photocatalytique des
produits pré-adsorbés en transformant, avec une vitesse
importante, leurs complexes d'adsorption en produits finaux.
Cette hypothèse est vérifiée par les analyses comparatives des
résultats de test présentés dans les colonnes Capacité
d'adsorption sans éclairage et Activité photocatalytique
du tableau 3, ainsi que par la comparaison des allures des
courbes obtenues avec et sans éclairage de la figure 3.
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
14
Par ailleurs, la figure 4 montre des courbes qui
représentent l'état de cristallinité d'échantillons par la
technique XRD (X-Ray Diffraction). Ces courbes ont été obtenues
lors d'analyses réalisées par M. Pierre Gaudon de l'école des
Mines d'Alès.
Cette figure 4 met en évidence que les structures
composites selon l'invention sont amorphes. En effet, les
courbes 30 et 31 des produits selon l'invention à base d'alumine
et de silice possèdent des valeurs d'état de cristallinité très
inférieures à celles du Degussa P25 représentées par 29.
La figure 5 montre des images de structure surfacique
de supports et de produits composites selon l'invention. Ces
images ont été obtenues à l'aide d'un MEB (Microscope
Electronique à Balayage) par Paul Jouffrey de l'école des Mines
de Saint-Etienne.
Plus précisément, la figure 5a montre une surface d'un
support 32 en alumine. Et la figure 5b montre des agrégats 33-35
de Ti02 sur le support 32 en alumine.
Par ailleurs, la figure 5c montre une surface d'un
support 36 en Silice. Et la figure 5d montre des agrégats 37-39
de Ti02 sur le support 36 en Silice.
Ces agrégats sont sphériques et possèdent un diamètre
moyen compris entre 500 et 2000nm.
Avantages de nouveaux produits actifs (activité
photocatalytique, procédé de fabrication, application) :
L'activité photocatalytique des composites amorphes
Ti02 - Support accepteur (donneur) poreux dépasse
largement celle de Degussa P25 (photocatalyseur commercial, cf.
le tableau 2, échantillons 1 et 2).
Par rapport à des structures cristallines
préfabriquées, les composites Nano- microagrégats
amorphes de Ti02 - Support poreux sont également
avantageux du point de vue technologique (facilités de leur
fabrication en tant qu'élément actif prêt à être utilisé et
la fixation fiable sur les surfaces des supports).
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
Leur application éventuelle peut donc être très
favorable pour l'élaboration d'éléments photocatalytiques
(sections de réacteurs, panneaux actifs, etc.) dans les
conditions industrielles.
5 On notera que les composites photocatalytiques
amorphes Ti02 - Support donneur peuvent être difficilement
réalisés dans le cas où les supports existent sous la forme de
pièces usinées (tubes, plaques, panneaux, etc.). Cet
inconvénient est causé par le caractère non poreux des métaux.
10 Variantes et Extensions de 1'invention
Une recherche a été réalisée afin de montrer les
capacités stérilisatrices des produits composites selon
l'invention.
Les figures 6 montre d'ailleurs un dispositif
15 expérimental pour les tests des capacités de stérilisation. La
bactérie Escherichia coli génétiquement modifiée (source - INRA,
France) a été choisie comme l'espèce bactérienne de test.
Dans une première étape représentée sur la figure 6a,
des échantillons de composites photocatalytiques 43 et des
supports non modifiés 44 sont imprégnés d'un brouillard
bactérien 45 pendant 3 minutes.
Ce brouillard 45 est obtenu à partir d'air sec 47 et
d'une solution bactérienne 46 positionnée à une extrémité 48.1
d'un tube 48. Cet air sec 47 soufflé à l'extrémité 48.1 traverse
la solution 46 de manière à former le brouillard bactérien 45.
Le brouillard 45 circule alors dans le tube 48 et imprègne les
échantillons 43 et 44 qui se trouvent à une extrémité 48.2 du
tube 48 opposée à 48.1.
Dans une deuxième étape représentée à la figure 6b, un
échantillon de composites photocatalytiques 43.1 est exposé à
l'irradiation UV-A (longueur d'onde de 365nm) sous une lampe à
UV 49. Et un échantillon 43.1 de composite selon l'invention est
exposé à la lumière solaire.Par ailleurs, un support non modifié
44.1 est exposé à la lumière solaire. Toutes ces expositions
durent 20 minutes.
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
16
Dans une troisième étape représentée à la figure 6c,
les échantillons 43.1, 43.2 et 44.1 ou leur surface ont été
transférés dans deux boîtes de Petrie 50 contenant un gel
nutritif 51. Ces boites sont conservées dans l'obscurité pendant
20 heures à 35 C afin de favoriser le développement des colonies
bactériennes. Une partie 52 de chaque boite 50 ne comporte aucun
échantillon et sert de référence pour l'expérience.
La figure 7 représente le développement de colonies
bactériennes dans des boîtes de Pétri, après conservation, pour
les différents échantillons précités. Ces tests ont été réalisés
en coopération avec Christine Blachère-Lopez, de l'Ecole des
mines d' Alès .
Dans les secteurs 4 et 12 ne comportant que du gel
nutritif et servant de secteur de référence, aucune colonie
bactérienne ne s'est développée.
Dans les secteurs 1 et 9 des boites contenant des
échantillons 44.1 de silice pure (support non modifié) exposés à
la lumière solaire, respectivement 21 et 6 colonies bactériennes
référencées 53 se sont développées en 20 heures d'incubation.
Dans les secteurs 3 et 11 contenant des échantillons
43.2 de composite selon l'invention exposés à la lumière
solaire, seulement une colonie de bactérie 53 s'est développée.
Dans les secteurs 2 et 10 contenant les échantillons
43.1 de composite selon l'invention exposés à l'irradiation UV-
A, aucune colonie bactérienne ne s'est développée.
Autrement dit, 27 colonies (21+6) se sont développées
sur les surfaces des échantillons 44.1 non stérilisateurs contre
une seule sur les surfaces des échantillons 43.1 et 43.2 du
produit selon l'invention.
Ces données montrent que les structures composites
amorphes de Ti02 selon l'invention manifestent une capacité
importante de stérilisation tant sous l'irradiation artificielle
(UV black light , ~~ = 365 nm) que sous la lumière solaire.
Ces produits actifs peuvent donc être conçus pour
l'abattement photocatalytique de composés organiques volatils
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
17
d'une gamme très large, à condition que leurs concentrations
initiales ne dépassent pas certaines limites (par exemple, pour
la phase gazeuse - 3=5 ppm ; ce cas correspond au
conditionnement de gaz dans des espaces confinés).
Mais ces produits peuvent également être conçus en
tant que produits actifs pour la protection collective et
individuelle contre la contamination biologique.
Un autre domaine d'application pour les
photocatalyseurs composite amorphe selon l'invention peut être
le traitement d'effluents liquides. Une recherche préliminaire a
été menée pour démontrer l'intérêt d'application des produits
proposés pour la purification photocatalytique de l'eau
contaminée par des composés organiques en solution.
Ainsi, la figure 8 montre des représentations
graphiques d'une dégradation photocatalytique de l'acétone et
l'éthanol dans une phase liquide à l'aide des composites actifs
à base de Ti02 amorphe sous la lumière solaire.
Une courbe 55 comportant des triangles représente le
rendement de dégradation de l'acétone, tandis qu'une courbe 56
comportant des carrés représente le rendement de dégradation de
l'éthanol.
Pour obtenir ces courbes 55 et 56, deux échantillons
liquides de 25mL en volume contenant 25mg/L d'acétone et
d'éthanol dans l'eau ont été mis en contact avec deux
échantillons composites S-1T-070504 (échantillon N 3 dans le
tableau 2) dont les masses étaient de 1,1g. Deux échantillons
liquides identiques ont été mis au contact avec deux
échantillons de 1,1g de silice pure. Quatre boîtes de Pétri ont
été utilisées en tant que récipients.
Les mélanges ont été exposés à la lumière solaire,
dans des conditions statiques, pendant 2 jours.
Les pertes en acétone et en éthanol lors de leur
dégradation photocatalytique, tenant compte des pertes dues à
l'évaporation ont été contrôlées par la méthode
chromatographique.
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
18
Les rendements de dégradation des produits organiques
en solution ont été calculés comme les différences entre leurs
concentrations restant dans les récipients contenant la silice
pure (Csio2) et leurs concentrations dans les récipients avec les
composites photocatalytiques (Cphoto) , par rapport aux valeurs de
Ceio2 =
Les premiers prélèvements ont été effectués dans une
pièce obscure, avant l'exposition directe des échantillons au
soleil. Ainsi les points à 10h00 et à 11h00 du premier jour
d'essai présentent un rendement négligeable.
Ensuite, les récipients couverts par des plaques de
verre ont été sortis de la pièce obscure sur une terrasse
ensoleillée. Sur les courbes de rendement 55 et 56, deux pics 57
et 58 correspondent à l'heure d'ensoleillement maximum (14h-
16h). En deux jours d'essai, les solutions d'acétone et
d'éthanol dans les récipients contenant les échantillons
photocatalytiques ont été complètement dégradées.
Les variantes et extensions de l'invention peuvent
donc être envisagées, au moins dans le domaine du traitement de
l'eau notamment pour sa purification et sa stérilisation; ainsi
que dans le domaine de protection collective et individuelle
contre la contamination biologique avec par exemple la
réalisation de dispositifs de conditionnement de l'air dans les
établissements hospitaliers, la réalisation de vêtements et
d'outils auto-stérilisateurs...
Ces matériaux photocatalytiques selon l'invention
peuvent être mis en oeuvre sur des supports divers (céramique
poreuse, verre, carton-papier, textile, etc.).
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
19
BIBLIOGRAPHIE
[1] John Wiley & Sons, (1997), Heterogeneous
Photocatalysis, Hardcover;
[2] www.degussa.com;
[3] I. Nakamura, N. Negishi, S. Kutsuna, T. Ihara, S.
Sugihara, K. Takeuchi, (2000), Role of oxygen vacancy in the
plasma-treated Ti02 photocatalyst with visible light activity
for NO removal, Journal of Molecular Catalysis A: Chemical, 161,
205-212;
[4] Robert D., Piscopo A., Heintz 0., Weber J.V.,
(1999), Photocatalytic detoxification with Ti02 supported on
glass-fibre by using artificial and natural light, Catalysis
Today, 54, 291-296;
[5] Tae-Hyun Kim, Sohn B.H., (2002), Photocatalytic
thin fimls containing Ti02 nanoparticules by the layer-by-layer
self-assembling method, Applied Surface Science, 201, 109-114;
[6] V. Jokanovi, A. M. Spasi, D. Uskokovi, (2004),
Designing of nanostructured hollow Ti02 spheres obtained by
ultrasonic spray pyrolysis, Journal of Colloid and Interface
Science, 278, 342-352;
[7] T. Matsumea, T. Hanabusab, Y. Ikeuchi, (2002), The
structure of TiN films deposited by arc ion plating, Vacuum, 66,
435-439;
[8] Ying Ma, Jian-bin Qiu, Ya-an Cao, Zi-shen Guan,
Jian-nian Yao, (2001) Photocatalytic activity of Ti02 fims grown
on different substrates, Chemosphere, 44, 1087-1092;
[9] N. Kaliwoh, J.-Y.Zhang, I.W. Boyd, (2002),
Surfaces Coating technologies, 125, 424;
[10] Lecheng L., Hiu Ping Chu, Xijun Hu, Po-Lock Yue,
(1999), Preparation of heterogeneous photocatalyst
(Ti02/Alumina) by metallo-organic chemical vapour deposition,
Ind. Eng. Res., 38, 3381-3385;
CA 02591030 2007-06-15
WO 2006/064168 PCT/FR2005/051101
[11] M. Karches, M. Morstein, P.R. Von Rohr et al.,
(2002), Plasma-CVD Coated Glass Beds as Photocatalyst for Water
Decontamination, Catalysis Today, 72, 267-279;
[12] M.D. Stamate, (2000), Dielectric properties of
5 Ti02 thin films deposited by a DC magnetron sputtering system,
Thin Solid Films, 372, 246-249;
[13] E. Ogino, K. Mori, Y. Kijima et al., (2001),
Multilayer Structure and Process for Producing the Same, EP-
1068899;
10 [14] J.Y. Zhang, I.W. Boyd, (2002), Structural and
electrical properties of tantalum oxide films grown by photo-
assisted pulsed laser deposition, Applied Surface Science, 80,
40-44;
[15] H. Yumoto, S. Matsudo, K. Akashi, (2002),
15 Photocatalytic decomposition of NOx on Ti02 films prepared by
arc ion plating, Vacuum, 65, 509-514;
[16] S. Masami, (2000), Air Cleaner, Patent of Japan
2000334268 ;
[17] A.A. Malygin, M.O. Bashkin, A.B. Emelyanov et
20 al., (1993), 5th European Congress on application of surface and
interface analysis (Catania - Sicily, Italy), 313;
[18] T. Suntala, (1989), Mater. Sci. Rep., 4, 261 ;
[19] H. Noller, J.M. Parera, (1981), Active sites in
catalysis. An approach based on coordination chemistry, J. Res.
Inst.Catal. Hokkaido Univ., 29, N 2, 95-112;
[20] A. Evstratov, (2001), Incinération économique de
composés organiques volatiles (COV) à l'aide des catalyseurs
d'oxydes aux propriétés superficielles optimisées, Récents
Progrès en Génie des Procédés, 15, 309-317 ;
[21] K. Rajeshwar, (1996), Photochemical strategies
for abating environmental pollution, Chemistry and Industry,
454-458;