Note: Descriptions are shown in the official language in which they were submitted.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
1
VERRES BIOACTIFS DOPES EN STRONTIUM.
L'invention a pour objet de nouveaux verres bioactifs comprenant du, ou
dopés en strontium, un procédé pour leur préparation et leur utilisation dans
des procédés
de réparation ou de reconstruction des os.
Les os sont constitués d'un réseau de fibres de collagène et de cristaux de
phosphate de calcium hydratés et carbonatés. Des cellules appelées ostéocytes,
qui
comprennent les ostéoblastes et les ostéoclastes, sont insérées dans ce
réseau. Elles sont
alimentées par de très petits vaisseaux sanguins.
Lorsqu'un os est endommagé, les ostéoclastes éliminent les fragments
abîmés et les ostéoblastes reconstruisent le réseau de collagène et favorisent
la production
d'enzymes qui vont permettre le dépôt d'apatite cristalline hydroxylée
carbonatée, jusqu'à
la réparation du défaut osseux.
Ce procédé naturel étant lent, il est habituel d'aider la réparation de l'os à
l'aide de ciments osseux ou de prothèses plus ou moins importantes en fonction
des
dimensions de la zone endommagée. Une greffe osseuse est parfois nécessaire
lorsque la
reconstruction de l'os ne se fait pas ou est trop lente.
Dans tous les cas de réparation d'un défaut osseux, il est important,
parallèlement à la mise en place d'une structure de remplacement, de favoriser
la
reconstruction du tissu osseux, qui va progressivement coloniser ou prendre la
place du
substitut osseux.
Dans le cas de certaines pathologies, et notamment l'ostéoporose, il est
important de contrer la dégradation du tissu osseux en stimulant le travail
des ostéoblastes.
Pour toutes ces applications, des verres bioactifs ont été développés
depuis de nombreuses années. Les verres bioactifs réagissent chimiquement avec
les
fluides biologiques, le produit de la réaction est une hydroxyapatite qui
favorise la
formation de la matrice osseuse et la croissance osseuse.
Les premières céramiques bioactives ont été développées par L.L. Hench
(L.L. Hench et al., J. Biomed. Mater. Res. 1971, 2, 117-141 ; L.L. Hench et
al., J. Biomed.
Mater. Res. 1973, 7, 25-42).
Les premiers verres bioactifs ont été préparés à partir de Si02 de P205 et
de CaO et Na20. Les oxydes de silicium et de phosphore sont des formateurs de
réseau qui
participent à la cohésion du réseau vitreux. Les alcalins et alcalino terreux
comme le
sodium et le calcium ne présentent pas cette capacité et viennent modifier le
réseau vitreux
en y introduisant des ruptures de chaines qui sont à l'origine de la faible
température de
fusion de ces verres associée à un désordre structural accru. Leur présence a
pour
conséquence une plus grande réactivité des verres bioactifs dans un
environnement aqueux.
Cette réactivité permet la formation d'hydroxyapatite en milieu physiologique
et favorise
donc la reconstruction osseuse.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
2
Le bioverre qui a été le plus étudié est un verre sodo-silico-phospho-
calcique dit Bioglass ou Bioverre de Hench. Sa composition de base est 55%
Si02 - 20%
CaO - 20% NaZO - 5% P205. Les propriétés bioactives remarquables de ce
matériau ne
sont plus à démontrer. Le Bioglass reste à l'heure actuelle un des matériau
bioactifs
(induisant une réponse spécifique des cellules) les plus intéressants.
De nombreux développements ont été fait dans le domaine des verres
bioactifs depuis leur découverte (M. Vallet-Regi et al., Eur. J. Inorg. Chem.
2003, 1029-
1042), tels que l'incorporation de différents atomes ou l'incorporation de
principes actifs.
Les compositions des verres bioactifs ont été optimisées de façon à favoriser
la
prolifération des ostéoblastes et la formation de tissus osseux (WO 02/04606).
L'incorporation d'argent a été proposée notamment pour conférer des propriétés
antibactériennes aux verres bioactifs (WO 00/76486).
Toutefois, l'incorporation d'un nouvel élément dans un verre bioactif ne
va pas sans présenter des difficultés : en effet, tout atome introduit dans
une composition
de verre bioactif a une influence sur le comportement de ce verre et sur ses
propriétés, en
particulier sur la façon dont ce verre relargue les éléments dont il est
composé. Et le verre
bioactif doit à la fois bien se dissoudre pour permettre la formation
d'hydroxyapatite, mais
la vitesse de dissolution doit être contrôlée pour permettre une colonisation
progressive de
l'hydroxyapatite et un relargage prolongé d'éventuels actifs.
Enfin, les conditions de production de verres bioactifs doivent être
adaptées à chaque nouvelle composition.
Les propriétés de bioactivité des verres et leur vitesse de dissolution sont
influencées par leur composition et leur texture. La composition de base d'un
verre bioactif
est de la forme Si02-CaO-P205 ou Si02-Na2O-CaO-P205. Cependant, le rôle de
certains
éléments traces durant les différentes étapes dans le processus de
dissolution, de relargage
d'ions et les réactions physico-chimiques conduisant à la bioactivité a été
très peu étudié.
Le strontium est naturellement présent dans les tissus osseux et il peut
être incorporé dans les apatites lors des phases de croissance des précipités
(formation
d'apatites déficientes en calcium). Par ailleurs, la littérature décrit cet
élément comme
pouvant jouer un rôle sur les réactions cellulaires. Le strontium améliore les
propriétés
mécaniques de l'os et il a une influence sur la solubilité des apatites. Il
est aussi impliqué
dans l'ostéoporose puisqu'il améliore les propriétés mécaniques des
hydroxyapatites. Il
permet, in vivo d'avoir un meilleur lien avec les tissus environnants. Bien
qu'améliorant
l'adhésion cellulaire, il diminue légèrement la croissance des ostéoblastes en
culture et
augmente la production de lactate deshydrogénase. Le strontium permet aussi
d'immobiliser les cellules et l'adhérence des cellules pourrait être meilleure
quand le
biomatériau est dopé en Sr (E. Canalis et al., Bone 1996, 18, 517-523 ; G.
Boivin et al., J.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
3
Bone Miner. Res. 1996, 11, 1302-1311 ; P. Marie et M. Hott, Metabolism 1986,
35, 547-
551 ; P. Marie, Current Opinion in Pharmacology 2005, 5, 633-636).
Un objet de l'invention a été la mise au point d'un nouveau matériau
bioactif qui présente des propriétés améliorées par rapport aux matériaux de
1'art antérieur.
Le matériau de l'invention est une composition de verre bioactif
comprenant du strontium. Selon une première variante de l'invention, ce verre
bioactif est
issu d'un procédé sol-gel. Cette composition se caractérise par la présence
des éléments ci-
dessous dans les proportions indiquées :
Si02: de40à75%
CaO : de 15 à 30%
SrO : de 0,1 à 10%
PZO5 : de 0 à 10%
Na20 : de 0 à 20%
MgO: de0à10%
ZnO: de0à10%
CaF2 : de 0 à 5%
B203: de 0 à 10%
AgZ0 : de 0 à 10%
A1203: de0à3%
MnO : de 0 à 10%
Autres : de 0 à 10%
Les pourcentages sont des pourcentages en masse par rapport à la masse
totale de la composition.
Avantageusement, la somme des masses des éléments Si02, CaO, SrO,
P205 représente 98 à 100%, encore mieux 99 à 100 %, et préférentiellement 99,9
à 100 %
de la masse totale de la composition du matériau de l'invention.
De façon avantageuse le matériau de l'invention est constitué de :
Si02: de 45 à 75%
CaO : de 15 à 30%
SrO: de2à8%
PZO5 : de 0 à 10%
Autres éléments : de 0 à 1%, préférentiellement de 0 à 0,5%,
en masse par rapport à la masse totale de la composition.
Les matériaux de l'invention peuvent être issus d'un procédé sol-gel et
être sous forme d'une poudre libre ou d'une poudre compactée, sous forme de
fibres ou
encore sous forme d'un revêtement sur un support ou d'un monolithe ou d'un
verre fritté.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
4
Selon une variante de l'invention, les matériaux peuvent être issus d'un
procédé de fusion à haute température suivie d'une trempe. Dans ce cas ils
sont définis par
la composition suivante :
Si02: de 45 à 55%
Na20 : de 10 à 25%
CaO : de 10 à 25%
SrO : de 0,1 % à 10%
P205: de 0 à 10%
MgO: de0à10%
ZnO: de0à10%
CaF2 : de 0 à 5%
B203: de 0 à 10 %
Ag20: de0à10%
A1203: de0à3%
MnO : de 0 à 10%
Autres : de 0 à 10%.
Les pourcentages sont des pourcentages en masse par rapport à la masse
totale du matériau.
Avantageusement, la somme des masses des éléments Si02, Na20, CaO,
SrO, P205 représente 98 à 100%, encore mieux 99 à 100 %, et préférentiellement
99,9 à
100 % de la masse totale de la composition du matériau de l'invention.
De façon avantageuse, selon cette variante, le matériau de l'invention est
constitué de
Si02: de 45 à 55%
NaZO : de 15 à 25%
CaO : de 15 à 25%
SrO: de2à8%
P205: de 0 à 10%
Autres éléments : de 0 à 1%, préférentiellement de 0 à 0,5%,
en masse par rapport à la masse totale de la composition.
Les matériaux de l'invention peuvent être issus d'un procédé de fusion et
être sous forme de monolithe ou de verre fritté.
L'expression verre bioactif désigne un matériau du type verre
inorganique dont l'oxyde de silicium est le composant majoritaire et qui est
capable de se
lier à des tissus vivants lorsqu'il est placé dans un fluide physiologique.
Les verres bioactifs sont bien connus de l'homme du métier et sont
décrits notamment dans An introduction to Bioceramics , L. Hench et J.
Wilson, World
Scientific Edition, New Jersey (1993).
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
Les matériaux de l'invention sont biocompatibles ce qui signifie que
lorsqu'ils sont mis en contact avec un organisme vivant, et notamment avec un
organisme
humain ou animal, ils n'induisent pas de réaction des systèmes de protection
de
l'organisme tels que le système immunitaire notamment. Le terme biocompatible
implique
5 également que lorsque le matériau est implanté chez un patient, il ne
produit pas d'effets
cytotoxiques ou de réactions systémiques.
Les matériaux de l'invention sont à la fois biocompatibles et bioactifs.
Par rapport aux matériaux de l'art antérieur, ils possèdent l'avantage de
renforcer les
propriétés mécaniques de l'os et de favoriser la liaison entre
l'hydroxyapatite et les tissus
environnants. Les biomatériaux de l'invention ont donc des propriétés qui les
rendent
supérieurs aux biomatériaux de l'art antérieur dans la réparation des défauts
osseux et dans
la prévention et/ou le traitement des déficiences osseuses de toutes origines.
Les matériaux de l'invention peuvent être préparés par un procédé sol-
gel, qui présente de nombreux avantages : températures de production plus
faibles par
rapport aux autres procédés, matériaux plus homogènes, contrôle aisé de la
composition
finale et contrôle de la porosité et de la surface spécifique du matériau. La
bioactivité étant
conditionnée par la structure du matériau en plus de sa composition chimique,
on a
constaté que les matériaux issus d'un procédé sol-gel étaient particulièrement
intéressants
dans la mesure où il est facile par ce procédé de contrôler leur vitesse de
dissolution ainsi
que la vitesse de relargage du strontium.
Les matériaux de l'invention peuvent être préparés par un procédé qui
comporte les étapes de mélange en solution des alcoxydes métalliques,
hydrolyse,
formation du gel et chauffage de façon à produire une matrice poreuse ou un
verre dense.
Le procédé sol-gel est mis en oeuvre avec une composition de matière
telle que celle décrite ci-dessus à 3 composants ou plus, dont au moins Si02,
CaO, SrO, et
éventuellement P205 et/ou d'autres oxydes.
Dans une première étape les précurseurs des composants, le solvant (eau
et éventuellement un alcool tel que l'éthanol) sont mélangés en présence d'un
catalyseur,
acide ou basique.
De façon plus détaillée un tétraalcoxysilane tel que le tétraéthoxysilane
est utilisé comme précurseur de Si02, un trialkylphosphate tel que le triéthyl
phosphate est
employé comme précurseur de P205, le nitrate de calcium tétrahydraté ou un
autre sel de
calcium (chlorure, acétate, fluorure, oxalate,...) est employé comme
précurseur de CaO et
le nitrate de strontium ou un autre sel de strontium (chlorure, acétate,
fluorure, oxalate,...)
comme précurseur de SrO.
Les réactions d'hydrolyse et de condensation sont catalysées par le même
catalyseur, comme par exemple HCI. La structure du gel qui se forme est
conditionnée
notamment par la valeur du pH de la solution dans laquelle se font ces
réactions. Au seuil
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
6
de percolation le réseau tridimensionnel formé s'étend à travers tout le
milieu réactionnel
et l'on obtient un gel.
Vieillissement : cette étape implique de maintenir le gel immergé dans le
solvant pendant plusieurs heures à plusieurs jours. Pendant le vieillissement
les
polycondensations se poursuivent jusqu'à ce que toutes les espèces réactives
aient réagi.
Cette étape, dite de synérese, contribue à diminuer la porosité et à renforcer
le gel. La
durée et la température du vieillissement permettent de contrôler la porosité
du gel.
Pendant l'étape du séchage, le liquide présent dans les pores en est
expulsé. Des contraintes capillaires se développent et provoquent le
craquement du gel, à
moins d'opérer dans des conditions qui réduisent les tensions solide-liquide
interfaciales,
comme par exemple par addition de tensioactifs.
La stabilisation et la densification peuvent être obtenus par des moyens
thermiques ou chimiques, dans des conditions qui permettent d'éliminer les
groupes silanol
de surface.
De préférence on opère par chauffage de façon à dégrader les autres
éléments présents dans le gel tels que les nitrates. De préférence le
chauffage se fait à une
température supérieure ou égale à 600 C.
Le produit final est alors obtenu sous forme d'une poudre. La taille des
pores est comprise entre 1 nm et 50 m. De préférence, on obtient une poudre
avec des
pores de 2 à 50 nm de diamètre.
Les utilisations qui peuvent être faites des matériaux de l'invention sont
les suivantes : comblement de défauts osseux, recouvrement d'implants
métalliques,
stimulation de la croissance osseuse dans les cas de dégénérescence osseuse.
Ces applications peuvent être mises en oeuvre de différentes façons
Les matériaux de l'invention peuvent être introduits localement par
chirurgie ou par injection : dans une zone où un défaut osseux a été constaté,
par exemple
par radiographie. Il est possible de combler un défaut osseux par l'insertion
d'un matériau
de l'invention sous forme de poudre libre ou de poudre compactée.
La poudre obtenue par le procédé peut être utilisée en l'état, par exemple
en chirurgie osseuse ou maxillodentaire, en comblement de défauts osseux. Elle
peut être
injectée sous forme d'une composition thérapeutique dans les zones où une
stimulation de
la croissance osseuse est attendue. Cette poudre peut être compactée sous
forme de
pastilles à l'aide d'une presse, de façon à former un objet tridimensionnel
qui est utilisé en
chirurgie.
Selon une variante de l'invention, des fibres de verre bioactif peuvent
être préparées en passant par un procédé sol-gel, en mettant en oruvre les
étapes suivantes :
le sol est extrudé à travers une filière. Les fibres obtenues sont mises à
vieillir, séchées et
stabilisées thermiquement. Les fibres peuvent ensuite être tissées ou
agglomérées à l'aide
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
7
d'un liant, comme par exemple une solution de carboxyméthylcellulose. Un
réseau de
fibres agglomérées peut ensuite être utilisé pour produire un verre fritté par
chauffage dans
un four à des températures produisant la dégradation du liant.
Les fibres de bioverre de l'invention peuvent être utilisées en l'état,
comme fil de suture ou sous forme de tissu, en chirurgie. Elles peuvent être
employées
dans des compositions incluant d'autres matériaux.
Les matériaux de l'invention peuvent être utilisés seuls ou en
combinaison avec d'autres moyens favorisant la réparation et/ou la
régénération du tissu
osseux. Des compositions thérapeutiques, notamment des compositions destinées
à
l'injection ou à une administration par chirurgie, et comprenant au moins un
matériau de
l'invention, constituent un autre objet de l'invention. Ces compositions
peuvent
comprendre tout support pharmaceutiquement acceptable pour l'utilisation qui
est faite de
la composition : notamment support d'injection.
Outre les verres bioactifs de l'invention, on peut prévoir que des
formulations à injecter ou à mettre en place par chirurgie comprennent
également un ou
plusieurs composés choisis parmi les antibiotiques, les antiviraux, les agents
cicatrisants,
les anti-inflammatoires, les immunosuppresseurs, les facteurs de croissance,
les
anticoagulants, les agents vascularisants, les analgésiques, un plasmide...,
Les matériaux de l'invention peuvent aussi être déposés sur un élément
métallique ou céramique tel qu'une vis, une plaque, un tube, une valve qui est
implanté
dans l'organisme comme prothèse.
Les matériaux de l'invention peuvent être associés à une matrice, telle
qu'une matrice osseuse destinée à être greffée. L'association des matériaux de
l'invention
au greffon, notamment lorsque celui-ci est allogène, favorise son
incorporation dans
l'organisme.
Des prothèses recouvertes d'un matériau de l'invention peuvent être
fabriquées de façon connue en trempant une prothèse classique, en métal ou en
céramique,
ou un greffon osseux débarrassé de son réseau cellulaire, ou un polymère
biocompatible,
dans une solution sol-gel ou par projection par plasma de la composition sur
la prothèse,
puis en poursuivant par un chauffage à une température supérieure à 600 C qui
provoque
la formation du verre bioactif.
Une prothèse, métallique ou en céramique ou en polymère, ou une
matrice osseuse, recouvertes partiellement ou sur la totalité de leur surface
par un matériau
de l'invention constituent un autre objet de l'invention.
Les matériaux de l'invention peuvent également être préparés par voie
sol gel sous forme de monolithes de forme contrôlée. Selon cette variante, le
procédé
comporte un contrôle de l'étape de séchage et de densification de façon à
éviter les fissures
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
8
dans le gel. Le sol est mis à gélifier à 60 C dans un récipient en PTFE dont
la forme
définit la forme finale du monolithe.
De tels monolithes sont employés en chirurgie, par exemple pour
combler un défaut osseux.
Les matériaux de l'invention peuvent également être introduits par
chirurgie ou par injection dans une localisation connue pour sa fragilité
osseuse comme le
col du fémur chez les individus souffrant d'ostéoporose.
Les matériaux de l'invention peuvent également être introduits autour des
articulations pour favoriser la réparation et/ou la régénération du cartilage
lorsque celui-ci
est endommagé.
Les matériaux et les compositions de l'invention peuvent être utilisés
pour la réparation d'un cartilage, soit à la suite d'une blessure ayant
entraîné une
dégradation du cartilage, soit dans le cadre d'un traitement de
l'ostéoarthrose. Les maladies
inflammatoires des articulations d'une façon générale peuvent constituer des
situations où
l'utilisation d'un matériau selon l'invention peut être bénéfique.
Les matériaux de l'invention peuvent également être préparés par un
procédé de fusion en mélangeant les oxydes métalliques et les autres
composants, en les
portant à la fusion puis en les refroidissant. La température de fusion est
déterminée en
grande partie par le choix des composants du verre. Elle se situe entre 900 et
1500 C
environ. Les matériaux obtenus dans ce cas sont monolithiques et non poreux.
Selon cette variante, on peut également préparer un verre fritté, de façon
connue à partir de la composition de verre fondu qui est frittée de façon à
produire un
matériau particulaire.
Dans le cas des matériaux obtenus sous forme de monolithes (fusion ou
sol-gel), ces matériaux peuvent être utilisés en chirurgie, par insertion dans
un site à traiter,
soit qu'un défaut osseux nécessite d'être comblé soit qu'un relargage
d'apatite strontiée y
soit utile pour renforcer la structure osseuse existante.
Un autre objet de l'invention consiste en des solutions obtenues à partir
des verres bioactifs, par dissolution des verres bioactifs dans un milieu
aqueux. Ces
solutions peuvent être produites en plaçant le verre bioactif de l'invention
dans une
solution aqueuse puis en laissant le verre se dissoudre et en filtrant le
milieu. La solution
filtrée est récupérée. Elle favorise la croissance des ostéoblastes. Elle peut
être utilisée dans
une composition, notamment une composition injectable, pour administration
dans une
zone localisée de l'organisme où il est souhaitable de stimuler la croissance
des
ostéoblastes. Elle peut aussi être utilisée en laboratoire pour cultiver des
cellules. Elle peut
être utilisée pour préparer un médicament de toute forme telle que solide,
semi-solide,
liquide, comme par exemple sous forme de comprimés, de pastilles, de poudre,
de solution
liquide, de suspension, de suppositoires.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
9
Les matériaux, compositions et prothèses de l'invention sont
particulièrement utiles pour réparer les défauts osseux et/ou cartilagineux et
les carences
associés aux pathologies et aux blessures dans les cas suivants : formation de
tissus osseux
dans une fracture, réparation de défauts osseux tels que ceux dus à l'ablation
d'une tumeur
ou d'un kyste, le traitement d'anomalies dentaires ou du squelette,
reconstruction dentaire
et périodontique, notamment remplacement de l'os alvéolaire, dans les
pathologies
périodontiques qui entraînent une perte osseuse, ou pour remplir une cavité
entre la dent et
la gencive ou pour remplacer provisoirement une dent extraite, dans les cas
d'ostéoporose.
On choisit une forme adaptée à l'usage qui doit en être fait et le plus
souvent une forme permettant l'injection ou l'insertion par voie chirurgicale
sur le site où
une déficience osseuse doit être traitée.
Un autre objet de l'invention consiste en l'utilisation d'un matériau tel
que décrit ci-dessus pour la fabrication d'une prothèse ou d'un médicament
destiné à
prévenir ou traiter l'une ou l'autre des pathologies qui ont été décrites ci-
dessus.
Les biomatériaux élaborés sont des verres bioactifs nanostructurés. Les
études physico-chimiques réalisées lors des interactions biocéramiques/milieu
biologique
mettent en évidence des propriétés de bioactivité permettant in fine la
formation d'une
couche phosphocalcique à la surface des matériaux. Cette couche permet dans le
cas des
matériaux bioactifs un lien intime avec les tissus osseux. De plus, le
contrôle de la texture
(porosité) et de la composition en éléments majeurs et traces (Sr) permettent
de moduler
les propriétés de dissolution et de bioactivité de ces matériaux. Ainsi, les
verres élaborés
relarguent du strontium dans des concentrations physiologiques. Ce relargage
contrôlé
d'un élément trace (présent dans l'os) peut induire une réponse spécifique des
cellules.
Différentes compositions de matériaux conformes à la présente invention
ont été produites et l'on a étudié leur comportement en solution. On a
constaté qu'à
l'interface entre la composition et le milieu dans lequel elle est immergée il
se forme une
hydroxyapatite dont la vitesse de formation peut être contrôlée. On a aussi
constaté le
relargage de strontium sous forme ionique dans le milieu et son incorporation
dans la
couche phosphocalcique produite in situ.
Le strontium, comme le calcium, est un modificateur de réseau dans les
compositions de l'invention. Tous deux ont des rayons ioniques proches. Et on
a
néanmoins constaté que la présence de strontium jouait un rôle dans la vitesse
de relargage
des constituants de la composition alors que le calcium a peu d'influence sur
ce paramètre.
On a notamment constaté que l'augmentation de la quantité de strontium
dans la composition entraînait une diminution de la vitesse de relargage du
strontium, de
calcium, phosphore, du silicium.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
Ainsi, non seulement les compositions de l'invention permettent de
relarguer du strontium dans leur environnement lorsqu'elles sont placées dans
un liquide
physiologique, mais elles permettent aussi de le faire de façon contrôlée.
En résumé, les compositions de l'invention permettent :
5 - le relargage dans des concentrations physiologiques du strontium
directement sur le site d'implantation,
- l'amélioration de la minéralisation osseuse,
- le contrôle de la dissolution et du relargage des matériaux,
- la possibilité d'implanter et d'injecter le matériau sur le site choisi,
10 - la formation d'une couche phosphocalcique à la périphérie des
matériaux en milieu biologique.
PARTIE EXPERIMENTALE
I - Protocole de synthèse
Les verres bioactifs ont été élaborés sous forme de poudres. Le Tableau
I-1 décrit les précurseurs chimiques fournis par Sigma-Aldrich (USA).
Formule Masse molaire Pureté
(g.mol"1) (%)
Tétraéthoxysilane CgHZOO4Si 208,33 99,999
(TEOS)
Triéthylphosphate C6H1504P 182,16 99,8
(TEP)
Nitrate de calcium Ca(N03)2-4H20 236,15 99,99
tétrahydraté
Nitrate de Sr(N03)2 211,63 99
strontium
Tableau I-1 : caractéristiques des précurseurs chimiques.
Pour effectuer la réaction d'hydrolyse du TEOS, nous avons utilisé un
cosolvant (éthanol EtOH). Nous avons employé comme catalyseur de l'acide
chlorhydrique HCI.
Concernant le protocole de synthèse, l'eau distillée nécessaire à
l'hydrolyse est tout d'abord mélangée à l'acide chlorhydrique HCl (2N) et à
l'éthanol
EtOH (99%), qui permet outre d'obtenir une solution homogène après
introduction du
TEOS, de bien dissoudre les cristaux de Ca(N03)2-4H20. Les proportions d'eau,
d'éthanol
et d'acide chlorhydrique sont détaillées dans le tableau I-2.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
11
H20/(TEOS + TEP) R molaire = 12
H20/HCl R volumique = 6
H20/EtOH R volumique = 1
Tableau I-2 : proportions d'eau, d'éthanol et d'acide chlorhydrique.
Ces réactifs sont mélangés dans un ballon sous agitation magnétique
pendant 15 minutes. Le TEOS est alors ajouté au mélange et, après 30 minutes,
le TEP y
est versé ainsi qu'un volume égal d'éthanol. Au bout de 20 minutes, les
cristaux de
Ca(N03)2-4H20 sont introduits. Le mélange est alors agité pendant 60 minutes
supplémentaires.
Puis la solution est placée dans un verre de montre et séchée dans une
étuve à 60 C pour gélification. Cette opération dure 4 heures, et le sol en
ressort totalement
gélifié. L'étuve est ensuite portée à 125 C pendant 24 heures. Le gel est à
cet instant
complètement fragmenté et est broyé finement au mortier pour la dernière étape
de la
synthèse : la calcination à 700 C pendant 24 heures, qui outre la
densification va permettre
d'évaporer intégralement les résidus d'alcool et de nitrate piégés dans les
pores. Le produit
final est obtenu sous forme d'une fine poudre blanche.
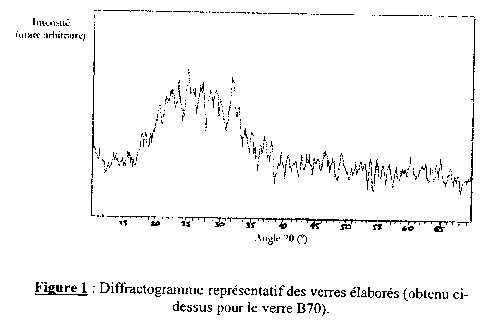
La figure 1 représente le diffractogramme sur un verre, caractérisé par la
méthode d'analyse cristalline de diffraction des rayons X. Les
diffractogrammes obtenus
pour les autres verres sont semblables à celui-ci. L'absence de pics de
diffraction indique
que les verres élaborés sont bien amorphes.
II- Caractéristiques des verres élaborés
II-1- Composition
L'étude de la composition des verres élaborés a été réalisée par
spectrométrie d'émission atomique (ICP-AES). Les résultats de l'analyse par
spectrométrie
d'émission atomique sont détaillés dans les tableaux II-1 et II-2. Les verres
élaborés ont
des concentrations en oxydes conformes aux valeurs escomptées.
B75 B72,5 B70 B67,5
Si02 Théorique 75 72,5 70 67,50
Si02 Expérimentale 72,20 71,49 68,25 63,75
P205 Théorique - 2,5 5 7,5
P205 Expérimentale - 2,48 4,85 6,95
CaO Théorique 25 25 25 25
CaO Expérimentale 24,50 24,36 25,76 24,13
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
12
Tableau II-1 : concentrations en oxydes mesurées en ICP-AES pour les
verres binaires et ternaires (% massique).
B75-Srl B75-Sr5 B67,5-Srl B67,5-Sr5
Si02 Théorique 75 75 67,5 67,5
Si02 Expérimentale 74,22 74,08 67,16 64,93
P205 Théorique - - 7,5 7,5
P205 Expérimentale - - 7,04 7,62
CaO Théorique 24 20 24 20
CaO Expérimentale 23,60 19,03 23,31 20,25
SrO Théorique 1 5 1 5
SrO Expérimentale 0,83 3,83 0,81 4,27
Tableau II-2: concentrations en oxydes mesurées en ICP-AES pour les
verres dopés en strontium (% massique).
II-2- Texture
Les surfaces spécifiques des verres sont été mesurées par adsorption de
gaz sur un appareil Autosorb Quantachrome fonctionnant à 77.4 K par la méthode
BET.
L'adsorbat utilisé est de l'azote de haute pureté (99.999%) avec une section
efficace
d'adsorption de la molécule d'azote de 0.162 nmz pour le calcul de la surface
spécifique.
Avant mesure les échantillons sont dégazés sous vide (p< 1 Pa) à 120 C pendant
12 h. Les
surfaces spécifiques sont calculées à partir des masses des échantillons
dégazés.
Un minimum de 5 points ont été utilisés pour la mesure des quantités de
gaz adsorbées dans un domaine de pression partielle p/po comprise entre 0.05
et 0.3 (avec
Po : pression de vapeur saturante).
Les surfaces spécifiques sont comprises entre 50 et 150 mZ/g. La taille
moyenne des pores est comprise entre 1 nm et 101 nm.
III - Étude in vitro de la bioactivité
Il est clairement établi que la faculté d'un biomatériau à se lier aux tissus
vivants est subordonnée à sa capacité à former une couche apatitique au
contact de fluides
biologiques imitant le plasma sanguin. Les essais in vitro sont donc un outil
puissant pour
évaluer la bioactivité d'un matériau.
Le milieu biologique dans lequel les verres bioactifs ont été immergés est
du DMEM (Dulbecco's Modified Eagle Medium). La composition du DMEM est
similaire
à celle du plasma sanguin chez l'homme (Tableau III-1). Le pH du DMEM à 37 C
vaut
7,43, une valeur analogue à celle du plasma.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
13
Na+ K+ Mg2+ Ca2+ Cl- CO32- PO43- SO42-
142,0 5,0 1,5 2,5 147,8 4,2 1,0 0,5
Tableau III-1: concentrations ioniques du plasma sanguin chez l'homme
(mrriol.L-l).
III-1- Protocole expérimental
Les échantillons de verres bioactifs ont été étudiés sous forme de poudre
et sous forme de pastilles : disques de 13 mm de diamètre et 2 mm de hauteur,
obtenues en
compactant 90 mg de poudre au moyen d'une presse. Les verres bioactifs sont
susceptibles
d'être utilisés dans des applications cliniques sous ces deux formes il est
donc intéressant
d'étudier ces deux types d'échantillons. La bioactivité s'y opère à des
échelles différentes
de temps et de dimensions.
III-1.1- Les échantillons sous forme de pastilles
Les échantillons de pastilles ont été immergés dans 45 mL de DMEM
durant les délais suivants : 1 heure, 6 heures, 1 jour, 2 jours, 5 jours, 10
jours.
Après immersion, les pastilles sont récupérées puis séchées sous
atmosphère ambiante, tandis qu'une partie du DMEM est prélevée afin d'être
dosée en
ICP-AES. Les échantillons de pastilles destinés à être caractérisés par la
microsonde
ionique sont inclus dans de la résine. Des sections transverses du matériau
sont ensuite
réalisées à l'aide d'un microtome Leica RM 2145. Les coupes, de 30 m
d'épaisseur, sont
effectuées perpendiculairement à la surface du disque. Finalement, les coupes
sont placées
sur des supports en Mylar percés en leur centre d'un trou de 3 mm de diamètre.
C'est la
zone de l'échantillon placée au-dessus du trou qui est sondée par le
microfaisceau d'ions.
111-1.2- Les échantillons sous forme de poudre
N'étant pas massifs comme les échantillons de pastilles et ayant en outre
une structure poreuse, les échantillons de grains de poudre réagissent plus
vite que les
échantillons de pastille. Notre étude sur les poudres s'est focalisée sur la
caractérisation de
4 verres bioactifs : les verres B75, B67,5, B75-Sr5 et B67,S-Sr5. Pour chaque
verre, 10 mg
de poudre ont été immergés dans du DMEM suivant un rapport [surface
spécifique]/[volume de DMEM] fixé à 500 cm , ceci afin d'évaluer l'impact sur
la
bioactivité de la composition du verre et non de sa surface de contact avec le
milieu
biologique. Les temps d'immersion dans le DMEM sont les suivants : 1 heure, 6
heures, 1
jour, 2 jours, 3 jours, 4 jours.
III-2- Caractérisation des réactions physico-chimiques lors des
interactions verre bioactif/milieu biolo ig gue
Afin de mieux comprendre les réactions physico-chimiques conduisant à
la formation de différentes couches en périphérie des bioverres, il est
primordial d'analyser
localement la distribution des éléments à l'interface matériaux/fluides
biologiques. Ces
analyses nécessitent l'utilisation de méthodologies ayant une bonne
sensibilité et une
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
14
excellente résolution spatiale. Dans ce cadre, nous avons réalisé des
cartographies
chimiques de l'interface à l'échelle micrométrique par la méthode PIXE
(Particles lnduced
X-ray Emission). Cette méthode est basée sur la fluorescence X induite par
faisceau d'ions
(généralement des protons). Elle permet de réaliser des cartographies
multiéléments
simultanées et des mesures de concentrations sur les éléments majeurs, mineurs
et traces
(ppm) avec une résolution spatiale de l'ordre du micron.
111-2.1- Imagerie chimique multiélémentaire à la périphérie des pastilles
de verre dopées au strontium après immersion dans le milieu biologique
Les cartographies multiélémentaires ont été enregistrées lors de l'analyse
par microfaisceau d'ions des pastilles de verre binaires et ternaires dopées
au strontium.
Des cartographies multiélémentaires ont été obtenues pour chacun des verres
avant
interaction et après 1 heure, 6 heures, 1 jour, 2 jours, 5 jours et 10 jours
d'interaction avec
le milieu biologique. La discussion est faite en effectuant une comparaison
avec l'étude des
pastilles de verre binaires et ternaires non dopées.
Grâce aux images chimiques obtenues, il a été possible de réaliser le
suivi de la distribution en silicium, calcium, phosphore, strontium et
magnésium à
l'interface verre bioactif/milieu biologique en fonction du temps
d'interaction entre le
matériau et le liquide. Les mesures de concentrations dans les verres
réalisées en PIXE
fournissent alors des informations locales sur la réactivité du matériau afin
de disposer
d'informations sur la réactivité globale des échantillons, l'évolution des
concentrations
dans le milieu biologique a été suivie par des mesures en ICP-AES. La
confrontation de
ces résultats est donc nécessaire et donnera des informations complémentaires
sur la
réactivité des matériaux. Concernant l'analyse PIXE, les échantillons de
pastille ont été
sondés au moyen d'un faisceau de protons de diamètre 2 m et d'intensité 500
pA. Les
cartographies ont été accomplies par le balayage de zones carrées de côté
compris entre 40
m et 400 m suivant les régions d'intérêt.
Les cartographies des verres de composition Si02-CaO-SrO révèlent que
l'ajout de strontium dans la composition du verre diminue la dissolution du
matériau
comparativement à un verre Si02-CaO. Cet effet est visible sur les
cartographies du
calcium.
Concernant la distribution du strontium, cet élément est réparti
uniformément jusqu'à 1 heure d'interaction. Une partie du strontium semble
ensuite être
relarguée de la périphérie du matériau et le strontium est détecté dans des
proportions plus
importantes dans les régions intérieures des pastilles.
Le dopage en strontium s'avère également avoir une incidence sur le
développement de la couche phosphocalcique. Ainsi, alors que la présence de
phosphore
était détectée à la périphérie du verre B75 dès 1 heure d'interaction, cet
élément n'est
décelé qu'après 6 heures d'interaction pour les verres B75-Srl et B75-Sr5. De
même, les
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
traces de magnésium ne sont décelées qu'au bout de 6 heures pour les verres
Si02-CaO-
SrO contre 1 heure pour le verre Si02-CaO. Par la suite, la couche Ca-P-Mg
croît de
manière similaire au verre binaire. Après 10 jours d'interaction, on observe
trois régions
dans ces pastilles de verre. Les régions les plus intérieures de la pastille
sont constituées du
5 réseau vitreux originel. La couche périphérique est une région étendue riche
en calcium et
en phosphore, dans laquelle sont présentes des traces de magnésium et de
strontium. Enfin,
entre ces deux régions, on constate la présence d'une zone intermédiaire
localement
enrichie en calcium.
Les cartographies multiélémentaires concernant les verres de
10 composition Si02-CaO-P205-SrO attestent également d'un ralentissement de la
dissolution
du matériau en comparaison du verre non dopé B67,5. L'ajout de strontium se
traduit ainsi
par le ralentissement du relargage du calcium. La capacité de ces matériaux à
former une
couche Ca-P-Mg-Sr est néanmoins avérée après quelques jours d'interaction.
111-2.2- Mesures locales des concentrations élémentaires lors des
15 interactions pastilles de verre/milieu biologique
Suivant la répartition des espèces chimiques, les cartographies
multiélémentaires ont été sectorisées en différentes régions d'intérêt. Chaque
fois que la
région périphérique riche en calcium et en phosphore a été repérée, des
masques de
mesures ont été définis, permettant d'y calculer les concentrations
élémentaires. Suivant la
région d'intérêt, des masques de 5 à 20 m de côté ont été définis,
l'épaisseur de la couche
Ca-P augmentant avec le temps d'immersion. En appliquant cette méthodologie,
l'évolution des concentrations des espèces Ca, P, Si, Sr et Mg à la périphérie
et au centre
des verres a pu être suivie. Pour un temps d'interaction et un verre donnés,
les valeurs de
concentration portées sur les graphes sont la moyenne des concentrations
relevées dans
plusieurs régions d'intérêt.
Evolution des concentrations à la périphérie des pastilles de verre
Les figures 2, 3, 4 et 5 montrent l'évolution des concentrations
élémentaires à la périphérie des verres Si02-CaO-SrO. Les concentrations
mesurées à la
périphérie du verre B75 (Si02-CaO) y sont également portées afin d'opérer une
comparaison. La figure 2 représentant l'évolution des concentrations en
calcium, indique
que les verres B75-Srl et B75-Sr5 adoptent un comportement résolument
différent du
verre B75. Pour les verres Si02-CaO-SrO la concentration en calcium commence
par
augmenter lors des premières heures d'interaction avec le liquide
physiologique.
L'augmentation relative de la concentration en calcium est due à ce que dans
le même
temps la concentration en silicium diminue fortement (figure 4). Ceci tend à
indiquer que
chez les verres dopés en strontium, le relargage du calcium n'avance pas aussi
rapidement
que la décomposition du réseau de silicium : le relargage du calcium est
ralenti et semble
affecter une quantité plus limitée de cations de la matrice. Ce n'est qu'au-
delà de 6 heures
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
16
d'interaction que la concentration en calcium chute jusqu'à un minimum atteint
après 1
jour d'interaction pour le verre B75-Srl et après 2 jours pour le verre B75-
Sr5. Le minima
atteint est plus élevé que celui du verre B75 : l'ampleur de la dissolution
est donc moindre
chez les matériaux dopés en strontium.
Après l'étape de relargage, la quantité de calcium présente en périphérie
des verres croît, mais cette augmentation est moins rapide pour les verres
Si02-CaO-SrO
que pour le verre Si02-CaO. Après 10 jours d'immersion, la proportion de
calcium
contenue dans la couche Ca-P périphérique des verres dopés en strontium est
proche de
30% massiques, ce qui est inférieur à la quantité de calcium détecté dans la
couche Ca-P
périphérique du verre B75 (44% massique). Mais il faut tenir compte du fait
que les
matrices des verres B75-Srl et B75-Sr5 contiennent initialement moins de
calcium.
La figure 4 montre que la décroissance de la concentration en silicium à
la périphérie des matériaux est d'autant plus lente que la proportion en
strontium dans la
matrice vitreuse originelle est élevée. Après 10 jours d'interaction, la
couche périphérique
du verre B75-Srl est encore composée de 6% de silicium, celle du verre B75-Sr5
de 9% de
silicium.
Concernant le phosphore (figure 3) la tendance observée semble
commune aux trois verres B75, B75-Srl et B75-Sr5 ; à savoir, une augmentation
rapide de
la concentration de cet élément en périphérie des pastilles. Un extremum est
finalement
atteint après 10 jours d'interaction. La teneur en phosphore de la périphérie
des verres B75,
B75-Srl et B75-Sr5 est alors voisine de 12%.
Des traces de magnésium sont détectées dans la couche qui se développe
à la surface des verres Si02-CaO-SrO (figure 5). La proportion de magnésium
augmente à
mesure que le temps d'immersion se prolonge et donc que la couche périphérique
s'étend à
la surface des verres. La quantité de magnésium incorporée à la périphérie des
pastilles
s'avère être plus importante pour les verres Si02-CaO-SrO que pour le verre
binaire Si02-
CaO.
Les figures 6, 7, 8 et 9 montrent l'évolution des concentrations
élémentaires à la périphérie des verres Si02-CaO-P205-SrO. Sur la figure 6, on
peut
observer que l'évolution des concentrations en calcium à la périphérie des
verres B67,5-
Srl et B67,5-Sr5 augmente de manière analogue à celle du verre B67,5 ;
cependant
l'évolution est plus lente et le calcium est présent en quantité moins
importante pour les
verres dopés en strontium. Sur la figure 8, on remarque que la cinétique de
décroissance de
la concentration en silicium est moins rapide pour les verres contenant du
strontium que
pour le verre ternaire B67,5. Après 10 jours d'interaction, de plus fortes
concentrations de
silicium subsistent à la périphérie des verres Si02-CaO-P205-SrO. Ces
observations sont le
signe que chez les verres dopés en strontium, la décomposition du réseau
vitreux est opérée
sur une profondeur moindre.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
17
La quantité de phosphore décelée dans la région périphérique des
pastilles augmente rapidement avec le temps d'immersion (figure 7).
L'évolution des
concentrations est commune aux trois verres et la couche périphérique est à
terme
constituée de 11 à 15% de phosphore. Concernant le magnésium, cet élément est
au bout
de 10 jours présent à hauteur du pourcent à la périphérie des pastilles. On
note sur la figure
9 qu'une plus grande quantité de magnésium est incorporée chez les verres
composés de
strontium B67,5-Srl et B67,5-Sr5 comparativement au verre B67,5.
La figure 10 représente l'évolution des concentrations en strontium à la
périphérie des pastilles de verre Si02-CaO-SrO et SiO2-CaO-PZO5-SrO. Sous
l'effet des
échanges ioniques et des réactions physico-chimiques ayant lieu en surface,
d'importantes
fluctuations dans la concentration du strontium sont observées, Il est
néanmoins possible
de dégager pour la couche périphérique une tendance générale à un léger
appauvrissement
de la quantité de strontium. Après 10 jours d'interaction, la périphérie des
matériaux est
d'autant plus riche en strontium que la proportion de cet élément était
importante dans la
matrice vitreuse originelle, et les concentrations mesurées sont inférieures
aux valeurs
avant interaction.
Evolution des concentrations dans la région intérieure des pastilles de
verre
Les mesures des concentrations élémentaires dans les régions intérieures
des pastilles de verre, non directement exposées aux fluides biologiques, ont
été faites pour
les éléments Si, Ca, P, Sr et Mg. Comme remarqué précédemment, les phénomènes
de
diffusion et de migration des ions vers la périphérie du matériau entraînent
des fluctuations
dans la composition de la matrice vitreuse. Les principales variations sont
observées pour
les concentrations en silicium, calcium et strontium lors des 2 premiers jours
d'interaction
avec le milieu biologique. L'évolution de la concentration en phosphore
démontre
également une légère tendance à la hausse. Après 10 jours d'interaction, on
observe que les
concentrations des différents éléments constitutifs retournent à une valeur
proche de celle
qui était leur dans la matrice vitreuse originelle. Les régions intérieures
des pastilles de
verres dopés en strontium ont subi moins de modifications que les verres non
dopés.
L'amplitude et la cinétique de dissolution étant moindre chez les verres
dopés, la couche
Ca-P-Mg développée en périphérie ne semble pas s'étendre jusqu'aux régions les
plus
intérieures des pastilles de verre.
Evolution des rapports atomiques à l'interface pastilles de verre/milieu
biologique
On a étudié l'évolution des rapports atomiques Ca/P, Ca/Mg et Ca/Sr à
l'interface verre/milieu biologique.
Lors des premières heures d'interaction, le rapport atomique Ca/P est
plus élevé pour les verres Si02-CaO-SrO que pour le verre Si02-CaO. Cela tient
au fait que
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
18
le calcium, relargué en quantité moins importante pour les verres Si02-CaO-SrO
est donc
présent en plus fortes proportions à la surface de ces matériaux. Au-delà de 6
heures
d'interaction, la dissolution et le relargage du calcium s'accélèrent pour les
verres B75-Srl
et B75-Sr5 ceci, ajouté à l'incorporation rapide de phosphore issu du milieu,
résulte en la
chute brutale du rapport Ca/P observée à 1 jour d'interaction. Puis, à mesure
que le temps
d'immersion dans le fluide biologique augmente, le rapport Ca/P tend vers une
valeur
limite proche de 1,7, qui est celle de l'hydroxyapatite stoechiométrique.
Ainsi, après 10
jours d'immersion, on constate que la valeur du rapport Ca/P finalement
atteinte est égale à
1,8 pour les verres B75-Srl et B75-Sr5, ce qui est plus proche de la valeur
nominale de
l'apatite stoechiométrique si l'on compare au résultat de 2,1 obtenu pour le
verre B75.
Concernant les verres Si02-CaO-P205-SrO : les rapports Ca/P mesurés à
l'interface sont
constamment inférieurs à ceux du verre Si02-CaO-P205. Ceci est du d'une part à
la plus
faible croissance de la concentration en calcium, et d'autre part à la plus
faible proportion
de calcium initialement présente dans ces matériaux respectivement 24% et 20%
pour les
verres B67,5-Srl et B67,5-Sr5, contre 25% pour B67,5. Après 10 jours
d'interaction, la
remarque émise pour les verres Si02-CaO-SrO est également valable pour les
verres Si02-
CaO-P205-SrO à savoir que le rapport Ca/P pour les verres dopés en strontium
est plus
proche de celui de l'hydroxyapatite stoechiométrique comparativement aux
verres non
dopés. Au bout de 10 jours d'immersion, ce rapport Ca/P vaut 1,6 pour le verre
B67,5-Srl
et 1,7 pour le verré B67,5-Sr5, contre 1,9 pour le verre B67,5.
Evolution de la composition du milieu biologique lors des interactions
avec les pastilles de verre
L'évolution de la concentration en calcium présente dans le DMEM
(figures 11 et 12) présente de faibles variations lors des premières heures
d'interaction. La
quantité de calcium relarguée dans le milieu lors de la phase de
désalcalinisation de la
surface est plus faible pour les verres dopés en strontium que pour les verres
B75 et B67,5.
Ensuite, à mesure que le temps d'immersion s'allonge, on constate pour tous
les verres
dopés une diminution progressive de la concentration en calcium dans le milieu
biologique. Le verre binaire B75 relargue d'importantes quantités de calcium
si bien que
cet élément était présent en plus forte concentration après 10 jours
d'interaction qu'avant
interaction ; cette observation n'est pas constatée pour les verres B75-Srl et
B75-Sr5 Les
verres dopés en strontium s'avèrent incorporer de plus grandes quantités de
calcium
comparées à celles relarguées. Ainsi, après 10 jours d'interaction, la
concentration en
calcium dans le milieu biologique n'est plus que de 62 ppm pour les verres B75-
Srl et
B75-Sr5 alors qu'elle était de 94 ppm pour le verre B75. Pour les verres B67,5-
Srl et
B67,5-Sr5, elle est respectivement égale à 5 et 49 ppm, alors qu'elle valait
67 ppm pour le
verre B67,5.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
19
Les figures 13 et 14 représentent l'évolution de la concentration en
phosphore présente dans le milieu biologique. Pour tous les verres, on
constate une
importante diminution de la concentration de cet élément au fil du temps. Les
décroissances observées pour chacun des échantillons sont analogues. On note
toutefois
qu'après 5 jours d'interaction la consommation de phosphore semble ralentie
chez les
verres dopés en strontium. Ce pourrait être le signe que le système verre-
milieu biologique
parvient à un équilibre.
Concernant le silicium, les figures 15 et 16 montrent une tendance
commune à tous les verres. A mesure que les réactions de dissolution
décomposent le
réseau vitreux sur des profondeurs de plus en plus larges, des concentrations
de silicium de
plus en plus élevées sont décelées dans le milieu biologique. Au bout de 10
jours
d'interaction, les quantités de silicium relarguées dans le milieu biologique
sont plus
faibles pour les verres dopés en strontium. Ceci est un autre indice de la
moindre amplitude
de dissolution chez les verres dopés.
D'autre part, les figures 17 et 18 montrent que les verres dopés en
strontium incorporent plus de magnésium que les autres verres. La
concentration de cet
élément décroît lentement avec le temps d'immersion et au bout de 10 jours, la
diminution
en magnésium est de 2 ppm pour les verres B75-Srl et B75-Sr5, 3 ppm pour le
verre B675-
Srl et 5 ppm pour le verre B67,5-Sr5.
Enfin, les mesures de la concentration en strontium présente dans le
milieu biologique complètent cette étude (figure 19). Initialement égale à
zéro, la quantité
de strontium dans le liquide physiologique s'élève à quelques ppm après le
relargage de cet
élément hors de la surface des verres. On remarque que les verres B75-Sr5 et
B67,5-Sr5
relarguent 5 fois plus de strontium que les verres B75-Srl et B67,5-Srl, ce
qui concorde
avec les teneurs respectives en strontium de ces matériaux.
111-2.4- Mesures locales des concentrations élémentaires lors des
interactions grains de verre/milieu biolo giQue
Evolution des concentrations à la périphérie des grains de verre
L'analyse locale de la périphérie des grains révèle que les phénomènes
observés pour les poudres sont la reproduction de ceux observés pour les
pastilles, à des
échelles de temps et de dimensions réduites toutefois. Les concentrations
élémentaires
affichent des tendances analogues à celles observées précédemment.
Ces observations s'appliquent également à l'évolution de la
concentration en phosphore. Comme pour les pastilles, la concentration de cet
élément
augmente rapidement à la périphérie des grains. Après 4 jours d'interaction,
le phosphore y
est contenu à hauteur de 9-10% pour les verres dopés en strontium, et à
hauteur de 16%
pour le verre ternaire. Pour le verre B75, la quantité de phosphore croît
promptement
jusqu'à 6 heures d'interaction. Au-delà, la concentration en phosphore
s'affaisse jusqu'à
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
des valeurs quasi nulles. La couche phosphocalcique formée en bordure des
grains de verre
B75 apparaît donc instable et est rapidement dissoute sous l'action des
fluides biologiques.
On constate que la concentration en silicium en bordure des grains de
verre B75 décroît lors des premiers temps d'interaction, correspondant à la
brisure du
5 réseau vitreux sur la périphérie du matériau. Cependant, au-delà de 6 heures
d'interaction,
la couche phosphocalcique concentrique est dissoute et conséquemment les
grains ne sont
plus constitués que d'un noyau vitreux riche en silicium. Pour les verres
B67,5, B75-Sr5 et
B67,5-Sr5 le phénomène observé est différent : le réseau de silicium est
progressivement
décomposé sur les régions périphériques des grains, et par suite la
concentration de cet
10 élément diminue. On note que la décroissance est plus lente pour les verres
dopés en
strontium comparativement aux verres non dopés ; c'était aussi le cas pour les
échantillons
sous forme de pastille.
IV- Evaluation préliminaire du comportement des cellules
ostéoblastigues cultivées au contact du bioverre dopé en strontium (B75Sr5)
15 IV-I- Etude in vitro - Méthode de culture
Les bioverres dopés en strontium B75Sr5 sont étudiés sous forme de
granules. Préalablement à leur utilisation, les bioverres sont pesés et
stérilisés à 180 C
pendant 2 heures. Une préincubation des granules dans le milieu de culture
(voir
composition ci-dessous) est ensuite effectuée pendant 48 heures sous
agitation. Suite à
20 cette préincubation, les granules de bioverres sont immédiatement mis au
contact des
cellules.
Des cellules ostéoblastiques sont isolées par digestion enzymatique à
partir de calvaria de foetus de rats âgés de 21 jours. Les calvaria sont
disséquées en
conditions stériles et les fragments sont incubés en présence de collagénase
(Life
technologies(W) pendant 2 heures à 37 C. Les cellules dissociées des fragments
osseux sont
alors ensemencées dans des boîtes de culture (5m1) à une densité de 2.105
cellules/ml.
Lorsque la culture atteint le stade de subconfluence (environ 80% de la
surface colonisée),
les granules de bioverres sont ajoutés aux tapis cellulaires (20 mg/boîte de
culture). Le
milieu de culture est composé de DMEM (lnvitrogen ), d'acide ascorbique (50
g/mL),
de 10 mM de (3-glycérophosphate (Sigma ), de 50 UI/mL de Pénicilline-
Streptomycine
(Gibco ) et de 10% de sérum de veau foetal (SVF) (Hyclone ). Les cellules sont
cultivées pendant 14 jours, dans un incubateur à 37 C dans une atmosphère
humide à 5%
de C02
IV-2- Etude de l'interface grain de verre B75Sr5/cellules osseuses par
Microscopie photonique à contraste de phase.
Les observations par microscopie photonique à contraste de phase
permettent de suivre l'évolution, la maturation ainsi que la formation de
nodules osseux
autour et au contact du bioverre.
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
21
Durant les premiers jours de culture, les cellules prolifèrent (figure 20) et
atteignent le stade de confluence entre le 3e et le 4e jour de culture (figure
20),
immobilisant les granules dans le tapis cellulaire. Dans les jours suivants,
les cellules
continuent de proliférer et s'organisent en multicouches à la périphérie des
granules. Cette
organisation tridimensionnelle est visible dès le début de la deuxième semaine
de culture
sous forme de zones réfringentes (figure 20). A la fin de la deuxième semaine
de culture,
ces zones réfringentes sont très abondantes autour des granules et commencent
à se
propager sur l'ensemble du tapis cellulaire et dès le 13e jour, nous observons
l'apparition
des premiers nodules osseux minéralisés (figure 20).
Ces résultats démontrent qu'en présence de granules de bioverres dopés
en strontium, les cellules de calvaria de rats prolifèrent et se différencient
en ostéoblastes
actifs qui forment des nodules osseux minéralisés.
IV-3- Localisation c oenzymatique de la phosphatase alcaline
Les cellules sont cultivées pendant 14 jours au contact des granules de
bioverre. Ces cellules sont ensuite fixées dans une solution de fixation
(mélange de citrate
et d'acétone) à température ambiante pendant 30 secondes. Les échantillons
cellulaires
sont ensuite rincés et incubés dans une solution colorant les cellules
synthétisant la
phosphatase alcaline (solution de fast blue salt RR et naphtol phosphate,
Sigma ) à
température ambiante pendant 30 minutes à l'abri de la lumière. Après la
réaction
cytoenzymatique, les échantillons sont rincés puis examinés par microscopie
photonique à
contraste de phase.
Au 14e jour de culture un marquage positif de la phosphatase alcaline,
marqueur de la différenciation ostéoblastique, est observé au niveau de
cellules situées
autour et au contact des granules de bioverres (figure 21). Ces résultats
indiquent que la
présence de bioverres de type B75Sr5 permet une différenciation des cellules
de calvaria
de rats.
IV-5- Etude en microscopie optique et microscopie électronique à
transmission
Les cellules sont traitées pour la microscopie électronique à transmission
après 14 jours de culture au contact des granules de bioverres. Les cellules
sont fixées dans
une solution de Karnovsky (4% paraformaldehyde et 1% glutaraldehyde) puis les
échantillons sont déshydratés par des bains d'éthanol croissants. Le tapis
cellulaire avec les
granules immobilisés sont ensuite inclus dans de l'Epon-Araldite, et des
coupes semi-fines
(figure 22) puis ultra-fines (figure 23) sont réalisées avec un couteau en
diamant,
perpendiculairement au tapis cellulaire. Les coupes ultra-fines sont
collectées sur des
grilles de cuivre puis colorées avec de l'acétate d'uranyle et du citrate de
plomb. Les
sections sont ensuite examinées avec un microscope électronique à transmission
(Philips
CM-12).
CA 02694834 2010-01-08
WO 2009/027594 PCT/FR2008/000985
22
Nous observons sur les coupes semi-fines une organisation
tridimensionnelle en multicouches des cellules autour des granules (figure
22).
Les observations en microscopie électronique à transmission révèlent la
présence de nombreuses cellules au contact des granules (figure 23). Ces
cellules ont des
organites intracytoplasmiques développés, indiquant une forte activité
cellulaire. Elles sont
entourées d'une dense matrice extracellulaire riche en fibres de collagène.
Nous pouvons
également observer dans la matrice de multiples foyers de minéralisation.
Enfin, un contact
intime est observé entre la matrice, les cellules et la périphérie des
granules.
La présence des bioverres n'altère pas les capacités de synthèses
matricielles, puisque les cellules présentent tous les signes d'activité de
synthèse
(réticulum endoplasmique, mitochondries, noyau volumineux ....). Nous
observons
également la présence d'une matrice extracellulaire composée de nombreuses
fibres de
collagène.
Conclusion sur l'étude biologique
L'ensemble de ces résultats démontre le caractère non cytotoxique des
granules de bioverres dopés en strontium sur les cellules primaires issues de
calvaria de rat.
En effet, après 14 jours de culture au contact des bioverres, aucun signe de
souffrance
cellulaire n'est relevé et les cellules cultivées au contact de ces granules
prolifèrent,
s'organisent en structure tridimensionnelle et sont capables de synthétiser
une matrice
extracellulaire. De plus, l'activité phosphatase alcaline de ces cellules et
l'apparition de
nodules osseux minéralisés après 2 semaines de cultures indiquent que la
présence des
granules de bioverres ne nuit pas à la différenciation ostéoblastique des
cellules étudiées.