Note: Descriptions are shown in the official language in which they were submitted.
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
1
DETERMINATION PAR ANALYSE EN COMPOSANTES INDEPENDANTES
DE L'EFFICACITE D'UN TRAITEMENT
L'invention a pour domaine technique les systèmes de
classement statistique, et plus particulièrement les systèmes de
classement statistique d'images hyper-spectrales.
Lors de phases d'essais cliniques, l'évolution des maladies de
peau est quantifiée par des dermatologues sur toute une période de
traitement. Dans une première phase, le degré d'atteinte par la maladie
est mesuré sur chaque patient d'un groupe. La mesure est réalisée
cliniquement par un dermatologue. Dans une seconde phase, un
traitement statistique des mesures permet de quantifier l'efficacité du
traitement.
En pratique, on utilise un protocole opératoire reposant sur
l'étude au cours du temps des symptômes liés à une maladie cutanée
exprimés dans un groupe de Ne patients. Chaque patient reçoit un
traitement sur une première zone de peau atteinte et un véhicule sur
une seconde zone de peau atteinte. La première zone de peau et la
deuxième zone de peau sont choisies de façon à présenter une
superficie et une atteinte par la maladie similaires. Dans le cas d'une
maladie touchant la face, une joue reçoit le traitement tandis que
l'autre joue reçoit le véhicule, sous condition que les deux joues
présentent la même atteinte par une maladie cutanée.
Un dermatologue estime ainsi le degré d'atteinte d'un patient
par la maladie, zone par zone, patient par patient. De ce fait, la
quantification de l'efficacité du traitement peut être empirique et
soumise à une certaine part de subjectivité.
Afin d'améliorer l'observation et la quantification du degré
d'atteinte par une maladie tout en augmentant la reproductibilité de
ces étapes, on peut utiliser l'imagerie hyper-spectrale. On rappelle que
l'imagerie hyper-spectrale consiste à acquérir plusieurs images sous
des longueurs d'onde différentes.
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
2
En effet, les matériaux et éléments chimiques réagissent plus
ou moins différemment lors de l'exposition à un rayonnement d'une
longueur d'onde donnée. En balayant la gamme des rayonnements, il
est possible de différencier des matériaux intervenant dans la
composition d'un objet de part leur différence d'interaction. Ce
principe peut être généralisé à un paysage, ou à une partie d'un objet.
L'ensemble des images issues de la photographie d'une même
scène à des longueurs d'onde différentes est appelé image hyper-
spectrale ou cube hyper-spectral.
Une image hyper-spectrale est donc constituée d'un ensemble
d'images dont chaque pixel est caractéristique de l'intensité de
l'interaction de la scène observée à une longueur d'onde particulière.
En connaissant les profils d'interaction des matériaux avec différents
rayonnements, il est possible de déterminer les matériaux présents. Le
terme matériau doit être compris dans un sens large, visant aussi bien
les matières solides, liquides et gazeuses, et aussi bien les éléments
chimiques purs que les assemblages complexes en molécules ou
macromolécules.
L'acquisition d'images hyper-spectrales peut être réalisée selon
plusieurs méthodes.
La méthode d'acquisition d'images hyper-spectrales dite de
scan spectral consiste à utiliser un capteur de type CCD, pour réaliser
des images spatiales, et à appliquer des filtres différents devant le
capteur afin de sélectionner une longueur d'onde pour chaque image.
Différentes technologies de filtres permettent de répondre aux besoins
de tels imageurs. On peut, par exemple, citer les filtres à cristaux
liquides qui isolent une longueur d'onde par stimulation électrique des
cristaux, ou les filtres acousto-optique qui sélectionnent une longueur
d'onde en déformant un prisme grâce à une différence de potentiel
électrique (effet de piézo-électricité). Ces deux filtres présentent
l'avantage de ne pas avoir de parties mobiles qui sont souvent source
de fragilité en optique.
La méthode d'acquisition d'images hyper-spectrales dite de
scan spatial vise à acquérir ou imager simultanément toutes les
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
3
longueurs d'ondes du spectre sur un capteur de type CCD. Pour
réaliser la décomposition du spectre, un prisme est placé devant le
capteur. Ensuite, pour constituer le cube hyper-spectral complet, on
réalise un balayage spatial ligne par ligne.
La méthode d'acquisition d'images hyper-spectrales dite de
scan temporel consiste à réaliser une mesure d'interférence, puis de
reconstituer le spectre en faisant une transformée de Fourrier rapide
(acronyme anglais : FFT) sur la mesure d'interférence. L'interférence
est réalisée grâce à un système de type Michelson, qui fait interférer
un rayon avec lui-même décalé temporellement.
La dernière méthode d'acquisition d'images hyper-spectrales
vise à combiner le scan spectral et le scan spatial. Ainsi, le capteur
CCD est partitionné sous forme de blocs. Chaque bloc traite donc la
même région de l'espace mais avec des longueurs d'ondes différentes.
Puis, un balayage spectral et spatial permet de constituer une image
hyper-spectrale complète.
Appliquée aux études dermatologiques, l'imagerie hyper-
spectrale permet l'acquisition d'images comprenant une information
liée à la longueur d'onde. L'intensité de chaque pixel en fonction de la
longueur d'onde est enregistrée. L'application de méthodes de
classification à ces images permet de distinguer les zones saines et des
zones atteintes. On peut citer les travaux de P. Comon, "Independent
component analysis: a new concept?," Signal Processing, Elsevier, vol.
36, pp. 287-314, 1994 concernant une méthode d'analyse en
composante indépendantes permettant la classification de signaux.
La classification d'images hyper-spectrales relève d'un
domaine particulièrement actif. Plusieurs algorithmes existent pour
traiter et classer les images hyper-spectrales obtenues sur la peau.
I.L. Weatherall et B.D. Coombs, "Skin color measurements in
terms of CIELAB color space value," Journal of Investigative
Dermatology, vol. 99, pp. 468-473, 1992 enseignent le traitement
d'images couleurs par la décomposition CIEL*a*b.
G. N. Stamatas et al., "Non-invasive measurements of skin
pigmentation in situ." Pigment cell res, vol. 17, pp. 618-626, 2004
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
4
enseignent que la composante L* ou l'index ITA calculé avec les
composantes L* et b* permet de décrire la pigmentation.
G. N. Stamatas et al., "In vivo measurement of skin erythema
and pigmentation: new means of implementation of diffuse reflectance
spectroscopy with a commercial instrument," British Journal of
Dermatology, vol. 159, pp. 683-690, 2008 décrivent la séparation des
contributions de la mélanine et de l'hémoglobine dans une image
hyper-spectrale sur la base de l'étude empirique de leurs absorptions
respectives.
S. Prigent et al., "Spectral analysis and unsupervised SVM
classification for skin hyper-pigmentation classification," IEEE
Workshop on Hyperspectral Image and Signal Processing : Evolution
in Remote Sensing (Whispers), Reykjavik, Islande, Juin 2010 et S.
Prigent et al., "Multi-spectral image analysis for skin pigmentation
classification," Proc. IEEE International Conference on Image
Processing (ICIP), Hong-Kong, Chine, Septembre 2010 décrivent des
méthodes de classification de zones saines et de zones malades à partir
d'images hyper-spectrales.
En procédant à l'acquisition d'autres images hyper-spectrales à
différents instants, il est possible d'ajouter une information
temporelle. Il devient alors possible d'observer l'évolution d'une
maladie dermatologique au cours du temps. Enfin, en procédant à
l'analyse statistique des résultats d'un panel d'individus, il est
possible de déterminer l'efficacité d'un traitement sur la maladie
observée et ceci plus particulièrement, dans les désordres
pigmentaires, l'acné, la rosacée, ou le psoriasis. Cette détermination
peut être étendue aux images hyper-spectrales de phanères, notamment
de phanères atteints de mycoses comme par exemple l'onychomycose.
Par phanères, on entend les ongles et les cheveux. Parmi les phanères,
on s'intéresse plus particulièrement aux ongles.
Un effet notable n'est reconnu à l'heure actuelle qu'à l'issue
d'une étude statistique sur un large panel de patients. Afin de traiter
les données issues des différentes images à différents instants pour les
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
différents patients, il est nécessaire de disposer d'un système de
traitement des images performant.
Un but de l'invention est de générer des images présentant un
contraste maximum entre des images d'une zone atteinte par une
5 maladie et des images d'une zone épargnée par la maladie.
Un autre but de l'invention est de déterminer un indice
numérique reflétant l'efficacité du traitement d'une maladie.
Un autre but de l'invention est un système de traitement
d'images apte à déterminer un indice numérique reflétant l'efficacité
du traitement d'une maladie.
Un objet de l'invention est un procédé de détermination d'une
valeur de quantification de la déviation de la valeur moyenne d'une
distribution de l'écart de sévérité entre un instant initial et un instant
postérieur à l'instant initial, la sévérité dépendant du contraste entre
des zones recevant un traitement et des zones recevant un véhicule. Le
procédé comprend des étapes au cours desquelles :
on acquiert, pour au moins un patient, à un instant initial et à
au moins un instant postérieur à l'instant initial, au moins une image
hyper-spectrale comprenant au moins une zone choisie parmi une zone
malade recevant le traitement, une zone saine recevant le traitement,
une zone malade recevant le véhicule et une zone saine recevant le
véhicule,
on détermine une décomposition en composantes indépendantes
des images hyper-spectrales,
on détermine, pour chaque image, parmi les composantes
indépendantes, une composante représentative maximisant l'écart entre
zone saine et zone pathologique,
on mémorise, pour chaque image, la combinaison linéaire des
bandes spectrales correspondant à la composante représentative,
on détermine la moyenne sur toutes les images, des valeurs
absolues des combinaisons linéaires des bandes spectrales
correspondant chacune à la composante représentative d'une image,
on détermine, pour chaque image, une composante
représentative corrigée en fonction de la moyenne des composantes
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
6
représentatives, on détermine une valeur de l'écart de sévérité en
fonction des composantes représentatives corrigées des images hyper-
spectrales acquises, pour chaque patient et pour chaque instant de
mesure, et
on détermine une valeur de quantification de la déviation de la
valeur moyenne entre une distribution de l'écart de sévérité à l'instant
initial et une distribution de l'écart de sévérité à un instant postérieur
à l'instant initial en fonction de la valeur de l'écart de sévérité pour
chaque patient à l'instant initial et à l'instant postérieur.
L'invention présente l'avantage de fournir un indice numérique
unique pour caractériser l'efficacité du traitement entre deux instants
de mesure de façon automatique et à partir des seules images hyper-
spectrales d'un ensemble de patients, les images hyper-spectrales étant
classées entre images d'une zone saine et images d'une zone
pathologique.
On peut déterminer une valeur de l'écart de sévérité pour un
instant de mesure,
en déterminant, pour chacune des images acquises, une
moyenne d'intensité égale à la valeur moyenne des pixels pour la
composante représentative corrigée,
en déterminant une valeur de la sévérité de la maladie pour un
patient à un instant de mesure, calculée pour les images relatives aux
zones ayant reçues le traitement concernant le patient et l'instant de
mesure considéré,
en déterminant une valeur de la sévérité de la maladie pour le
patient considéré à l'instant de mesure considéré, calculée pour les
images relatives aux zones ayant reçues le véhicule, concernant le
patient considéré et l'instant de mesure considéré, et
en déterminant une valeur de l'écart de sévérité de la maladie
entre les zones ayant reçues le traitement et les zones ayant reçues le
véhicule pour un patient à un instant de mesure.
On peut déterminer la valeur de la sévérité de la maladie pour
un patient à un instant de mesure, calculée pour les images relatives
aux zones ayant reçues le traitement, concernant le patient considéré et
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
7
l'instant de mesure considéré, en réalisant la différence simple de la
valeur moyenne d'intensité pour l'image de la zone saine ayant reçu le
traitement et de la moyenne d'intensité pour l'image de la zone malade
ayant reçu le traitement, et
on peut déterminer la valeur de la sévérité de la maladie pour
le patient considéré à l'instant de mesure considéré, calculée pour les
images relatives aux zones ayant reçues le véhicule, concernant le
patient considéré et l'instant de mesure considéré, en réalisant la
différence simple de la moyenne d'intensité pour l'image de la zone
saine ayant reçu le véhicule et de la moyenne d'intensité pour l'image
de la zone malade ayant reçu le véhicule.
On peut déterminer la valeur de la sévérité de la maladie pour
le patient considéré à l'instant de mesure considéré, calculée pour les
images relatives aux zones ayant reçues le traitement, concernant le
patient considéré et l'instant de mesure considéré, en réalisant la
différence relative de la moyenne d'intensité pour l'image de la zone
saine ayant reçu le traitement et de la moyenne d'intensité pour
l'image de la zone malade ayant reçu le traitement, et
on peut déterminer la valeur de la sévérité de la maladie pour
le patient considéré à l'instant de mesure considéré, calculée pour les
images relatives aux zones ayant reçues le véhicule, concernant le
patient considéré et l'instant de mesure considéré, en réalisant la
différence relative de la moyenne d'intensité pour l'image de la zone
saine ayant reçu le véhicule et de la moyenne d'intensité pour l'image
de la zone malade ayant reçu le véhicule.
On peut déterminer la valeur de la sévérité de la maladie pour
le patient considéré à l'instant de mesure considéré, calculée pour les
images relatives aux zones ayant reçues le traitement, concernant le
patient considéré et l'instant de mesure considéré, comme étant égale à
la moyenne d'intensité pour l'image de la zone malade ayant reçu le
traitement, et
on peut déterminer la valeur de la sévérité de la maladie pour
le patient considéré à l'instant de mesure considéré, calculée pour les
images relatives aux zones ayant reçues le véhicule, concernant le
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
8
patient considéré et l'instant de mesure considéré, comme étant égale à
la moyenne d'intensité pour l'image de la zone malade ayant reçu le
véhicule.
On peut déterminer une valeur de l'écart de sévérité de la
maladie entre les zones ayant reçues le traitement et les zones ayant
reçues le véhicule pour le patient considéré à l'instant de mesure
considéré en réalisant la différence simple de la sévérité de la maladie
pour le patient considéré à l'instant de mesure considéré, calculée pour
les images relatives aux zones ayant reçues le traitement et la valeur
de la sévérité de la maladie pour le patient considéré à l'instant de
mesure considéré, calculée pour les images relatives aux zones ayant
reçues le véhicule.
On peut déterminer une valeur de l'écart de sévérité de la
maladie entre les zones ayant reçues le traitement et les zones ayant
reçues le véhicule pour le patient considéré à l'instant de mesure
considéré en réalisant la différence relative de la sévérité de la
maladie pour le patient considéré à l'instant de mesure considéré,
calculée pour les images relatives aux zones ayant reçues le traitement
et la valeur de la sévérité de la maladie pour le patient considéré à
l'instant de mesure considéré, calculée pour les images relatives aux
zones ayant reçues le véhicule.
Le véhicule peut être un placebo.
Le véhicule peut être un autre traitement.
Un autre objet de l'invention est un système de traitement
d'image pour la détermination de la sévérité d'une maladie comprenant
un dispositif d'acquisition d'images hyper-spectrales connecté à un
moyen de traitement, le moyen de traitement étant connecté à un
moyen de stockage de données et à un dispositif d'interaction homme
machine, le moyen de traitement étant apte à appliquer le procédé
défini ci-dessus.
Un autre objet de l'invention est l'application du procédé
décrit ci-dessus à la détermination de l'efficacité d'un traitement
dermatologique.
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
9
D'autres buts, caractéristiques et avantages apparaîtront à la
lecture de la description suivante donnée uniquement en tant
qu'exemple non limitatif et faite en référence aux figures annexées sur
lesquelles :
- la figure 1 illustre le procédé de détermination selon
l'invention, et
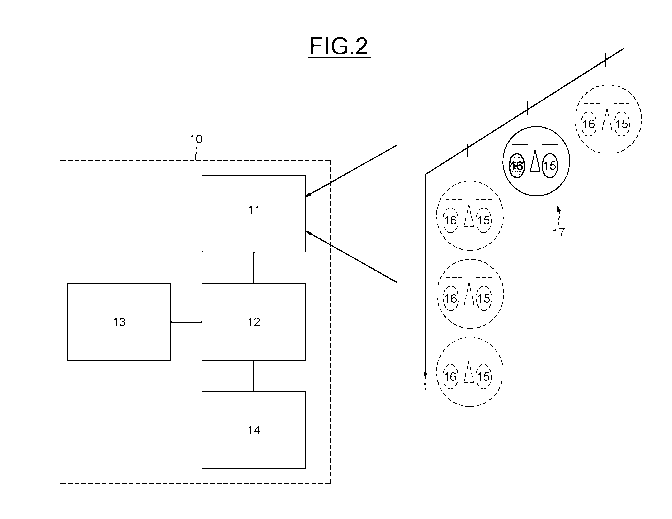
- la figure 2 illustre le système de traitement d'image associé.
Le procédé de détermination débute par l'acquisition 1 d'au
moins une image hyper-spectrale comprenant une zone parmi une zone
malade recevant le traitement, une zone saine recevant le traitement,
une zone malade recevant le véhicule et une zone saine recevant le
véhicule. Ces images hyper-spectrales sont acquises à chaque instant
de mesure et pour chaque patient. Dans la suite de la description, on
considérera que l'on a procédé à l'acquisition de quatre images
comprenant chacune une zone d'intérêt.
Toutefois, il est possible d'avoir au moins deux zones d'intérêt
réparties sur une image. L'image peut alors être scindée en autant de
sous-images que de zones d'intérêt présentes sur l'image initiale. Dans
ce cas, on prendra soin d'obtenir des sous-images de même nombre de
pixels. On prendra également soin de redimensionner les images
hyper-spectrales n'ayant pas bénéficié d'un découpage en sous-images
à une taille d'image présentant le même nombre de pixels que les sous-
images.
L'homme du métier sera ainsi capable d'adapter le procédé
décrit ci-après au cas où au moins une image comprend plusieurs zones
d'intérêt en insérant une étape de création d'une sous-image par zone
d'intérêt et de redimensionnement des images ne subissant pas de
découpage. Dans tous les cas, quatre images hyper-spectrales
correspondant chacune à une zone d'intérêt sont fournies au procédé.
Par véhicule, on entend une composition comprenant les mêmes
excipients que ceux correspondant au traitement mais ne comprenant
pas les principes actifs agissant sur les causes de la maladie, Le
véhicule peut également être un placebo ou une solution de contrôle.
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
Le véhicule peut être un autre traitement c'est-à-dire une
composition comprenant des principes actifs et des excipients
différents de la composition du premier traitement.
Bien que le procédé décrit soit fondé sur l'application d'un
5 traitement et d'un véhicule, il est possible d'appliquer le procédé afin
de comparer une zone recevant un premier traitement à une zone
recevant un deuxième traitement.
Les quatre images hyper-spectrales sont traitées par un procédé
d'analyse en composantes indépendantes ( Independant Component
10 Analysis en langue anglaise, identifié par l'acronyme ICA ).
Chaque image est transformée par le procédé ICA en une image de
même taille et comprenant autant de composantes indépendantes que
l'image d'origine comprenait de longueurs d'onde. Chacune des
composantes indépendantes est issue d'une combinaison linéaire des
longueurs d'ondes de l'image d'origine.
On détermine, pour chaque image, parmi les composantes
indépendantes, une composante représentative maximisant l'écart entre
zone saine et zone pathologique.
On mémorise, pour chaque image, la combinaison linéaire des
bandes spectrales correspondant à la composante représentative. Par
combinaison linéaire, on entend les coefficients de pondération de
chaque bande spectrale. Il peut exister des variations de coefficients
d'un patient à un autre. Afin d'obtenir une référence, on réalise la
moyenne des valeurs absolues des coefficients de pondérations entrant
dans la combinaison linéaire de la composante représentative de
chaque patient. On pourrait également réaliser la moyenne des valeurs
absolues en écartant préalablement les valeurs aberrantes ou extrêmes.
On obtient ainsi des coefficients moyens.
On détermine, pour chaque image, une composante
représentative corrigée en fonction de la moyenne des composantes
représentatives, c'est-a-dire en fonction des coefficients moyens.
L'extension spatiale de la maladie n'est pas prise en compte.
Ainsi, le procédé de détermination comprend une étape 2 de
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
11
détermination d'une valeur moyenne des pixels de la composante
représentative corrigée M, pour chaque image.
A l'issue de cette étape, on obtient donc quatre valeurs
moyennes ( mnv, mpv, mnA, et iimpA) correspondant chacune à une
des images reçues lors de l'étape précédente. Ces valeurs sont
déterminées à chaque instant de mesure et pour chaque patient.
La moyenne d'intensité sur une composante représentative
corrigée M d'une zone malade recevant le traitement est notée iimpA.
La moyenne d'intensité sur une composante représentative
corrigée M d'une zone saine recevant le traitement est notée mhA.
La moyenne d'intensité sur une composante représentative
corrigée M d'une zone malade recevant le véhicule est notée mpv.
La moyenne d'intensité sur une composante représentative
corrigée M d'une zone saine recevant le véhicule est notée mhv.
Une moyenne d'intensité notée m peut être déterminée par
l'équation suivante :
1
!am= (Moy(I))mI(m;1\4)¨
1É (Eq. 1)
irt-1 Np
Avec (Moy(I))m= l'intensité moyenne relative à la composante
représentative corrigée M
Nb : le nombre total de bandes
Np : le nombre total de pixels par bande de l'image
I(m,M) : l'intensité du pixel m de la composante représentative
corrigée M.
Le procédé de détermination détermine ensuite une valeur
unique pour quantifier la maladie d'un patient à partir des quatre
moyennes d'intensité déterminées à l'étape précédente. La valeur
unique obtenue est la sévérité D. . Pour obtenir la sévérité Dte , on
réalise une première normalisation appliquée entre la zone malade et la
zone saine, au cours d'une étape 3 du procédé suivie d'une deuxième
normalisation au cours d'une autre étape 4 du procédé.
La première normalisation peut être réalisée par une simple
différence.
dte ¨ [lut ¨11mp (Eq. 2)
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
12
Alternativement, la première normalisation peut être réalisée
par une différence relative.
e 1-1 mh [IMp
d, (Eq. 3)
1tMh
avec
dte : la sévérité de la maladie pour le patient e à l'instant t de
mesure
IMh : la moyenne d'intensité pour une zone saine,
Mp : la moyenne d'intensité pour une zone malade.
Selon une autre alternative, la première normalisation peut
correspondre à la mesure moyenne pour la zone malade
=!..tmp (Eq. 4)
Les mesures IMhet 1..imp étant homogènes, l'équation de
normalisation 2 est préférée. Ces valeurs sont déterminées à chaque
instant de mesure et pour chaque patient.
A l'issue de cette étape, on obtient une sévérité de zones ayant
reçues le traitement clA si les valeurs lamh et iamp sont remplacées par
les valeurs laivinA et i.impA relatives aux moyennes d'intensité pour des
zones traitées. De même, on obtient une sévérité de zones ayant reçues
le véhicule dte'v si les valeurs lamh et iamp sont remplacées par les
valeurs lamhV et iampv relatives aux moyennes d'intensité pour des
zones ayant reçues le véhicule.
Le procédé de détermination applique l'équation 2 en
remplaçant les valeurs lamh et !ami, par les valeurs laivinA et i.impA afin
d'obtenir la sévérité dte'A.
dte'A Ote)A (144h Mp A = 1-1AMh 1-1A4p (Eq. 5)
Par analogie, on obtient la sévérité dte'v en remplaçant les
valeurs lamh et iamp de l'équation 5 par les valeurs lamhV et iampv.
Alternativement, le procédé de détermination applique
l'équation 3 en remplaçant les valeurs lamh et !ami, par les valeurs mhA
30A
et iamp afin d'obtenir la sévérité de A .
(A A
1-1 mn ¨ 1-1 mp 1- ¨
dte'A = Ote )A = ____________________ 1 mn Mp A (Eq. 6)
1t 1-1 mn
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
13
Par analogie, on obtient la sévérité dte'v en remplaçant les
valeurs iamhA et i.impA de l'équation 6 par les valeurs II mh-V et iampv.
Alternativement, le procédé de détermination applique
l'équation 4 en remplaçant les valeurs II m h et !ami, par les valeurs mhA
et i.impA afin d'obtenir la sévérité dte'A.
dte'A (dte)A ¨1.tAmp (Eq. 7)
Par analogie, on obtient la sévérité dte'v en remplaçant la valeur
i.impA de l'équation 7 par la valeur iampv. Avec
1.tmv, : la moyenne d'intensité pour une zone saine ayant reçu le
véhicule,
1.tmvp : la moyenne d'intensité pour une zone malade ayant reçu
le véhicule,
A
[Imh : la moyenne d'intensité pour une zone saine ayant reçu le
traitement,
15= LIA la moyenne d'intensité pour une zone malade ayant reçu
mp =
le traitement.
Pour les raisons évoquées en regard des équations Eq. 2, Eq. 3
et Eq. 4 la normalisation préférée ici est celle relative à l'équation Eq.
5.
Pour obtenir la sévérité Dte à partir des deux sévérités dte'A et
dte'v, une deuxième normalisation est appliquée entre la zone recevant
le traitement et la zone recevant le véhicule.
La deuxième normalisation permet de déterminer la sévérité Dte
du patient e à l'instant de mesure t issue de la comparaison du
traitement et du véhicule. A partir des sévérités dte'A de zones ayant
reçues le traitement et des sévérités dte'v de zones ayant reçues le
véhicule, on peut déterminer une sévérité Dte pour le patient e à
l'instant de mesure t.
D te d te,A d te,V (Eq. 8)
Alternativement, on peut déterminer une sévérité Dte pour le
patient e à l'instant de mesure t d'après l'équation suivante :
d te,A d teS
Dte ________________________________________________________ (Eq. 9)
d te,V
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
14
avec
dte'A : la sévérité de la maladie pour le patient e à l'instant t de
mesure, calculée pour les images relatives aux zones ayant reçues le
traitement,
dte'v : la sévérité de la maladie pour le patient e à l'instant t de
mesure, calculée pour les images relatives aux zones ayant reçues le
véhicule.
Le procédé de détermination applique l'équation 8 afin de
déterminer la sévérité Dte pour le patient e à l'instant de mesure t.
Alternativement, l'équation 9 est appliquée pour déterminer la sévérité
Dte pour le patient e à l'instant de mesure t.
Pour les raisons évoquées en regard des équations Eq. 2, Eq. 3,
et Eq. 4 la normalisation préférée ici est celle relative à l'équation Eq.
8. Ces valeurs sont déterminées à chaque instant de mesure et pour
chaque patient.
A ce stade, la répartition des sévérités Dte entre les différents
patients n'est pas encore prise en compte. Afin d'en tenir compte, une
analyse statistique est nécessaire. Pour cela, les inventeurs ont
appliqué de façon ingénieuse une méthode de t-test aux données
caractérisant l'écart entre la zone malade traitée et la zone malade
recevant le véhicule. En d'autres termes, le t-test est appliqué à
l'indice de sévérité D.
Le t-test est notamment décrit dans l'ouvrage de A. M. Mood,
F. A. Graybill, et D. C. Boes, Introduction to the theory of
statistics , McGraw-Hill, 1974. Cet ouvrage divulgue une méthode de
caractérisation de la déviation de la valeur moyenne entre deux
distributions. La méthode est appelée test de Student ( Student test
en langue anglaise), ou t-test.
(t)¨(t0)
É't (t)= (Eq. 12)
1
324 (5240)
,\Ne Ne
Avec Z" (t) la quantification de la déviation de la valeur
moyenne entre deux distributions, ¨X(t) la valeur moyenne de X, a(t)
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
l'écart type de X, Ne le nombre de patients dans le groupe, t l'instant
de mesure et to l'instant de la mesure de référence. L'hypothèse nulle
est que la valeur moyenne de la distribution n'évolue pas entre le
temps to et le temps t. L'hypothèse nulle est rejetée si la quantification
5 de la
déviation Z" (t) entre le temps to et le temps t a une probabilité
(obtenue suivant la loi de Student) inferieure à la valeur p=0,05.
Par ailleurs, plus basse est la valeur de la quantification de la
déviation, plus grande est l'écart entre les valeurs moyennes des deux
distributions entre l'instant t et l'instant to.
10 Ce
test est donc appliqué aux sévérités Dte obtenues à l'issue de
l'optimisation de l'écart entre zone saine et zone malade, X (t) étant
alors la valeur moyenne sur l'ensemble des patients considérés des
sévérités D te à l'instant t, et at(t) étant alors l'écart type de la
distribution des sévérités Dte à l'instant t.
15 La
valeur moyenne des sévérités Dte peut être calculée de
plusieurs façons connues de l'homme du métier, comme par exemple
une moyenne simple, une moyenne relative, une moyenne statistique.
De plus, il est possible de retirer les valeurs extrêmes, ou les valeurs
aberrantes. Dans ces deux derniers cas, l'écart type de la distribution
des sévérités Dte est calculé en écartant les mêmes valeurs retirées de
l'ensemble des valeurs considérées pour réaliser la moyenne.
Alternativement, on considère un t-test apparié défini de la
façon décrite ci-après. Une fois la valeur optimiséeX.^ déterminée, la
valeur de la sévérité Dte correspondant à la valeur optimiséeX.^ est à
nouveau déterminée pour chaque instant de mesure et pour chaque
patient, et utilisée pour les étapes ultérieures du procédé.
A ce stade, la répartition des sévérités Dte entre les différents
patients n'est pas encore prise en compte. Afin d'en tenir compte, une
analyse statistique est nécessaire. Pour cela, les inventeurs ont
appliqué de façon ingénieuse une méthode de t-test apparié aux
données caractérisant l'écart entre la zone malade traitée et la zone
malade recevant le véhicule. En d'autres termes, le t-test apparié est
appliqué à l'indice de sévérité D.
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
16
La méthode est appelée test de Student apparié ( Paired
Student test en langue anglaise), ou t-test apparié.
(t)
zt,t, (t) _ (Eq. 13)
=N/1\
Avec Ztlt) la quantification de la déviation de la valeur
moyenne entre la distribution X et une distribution normale
standardisée N(0,1), X(t) la valeur moyenne de X, a(t) l'écart type de
X, Ne le nombre de patients dans le groupe, t l'instant de mesure et to
l'instant de la mesure de référence. L'hypothèse nulle est que la valeur
moyenne de la distribution n'évolue pas entre le temps to et le temps t.
L'hypothèse nulle est rejetée si la quantification de la déviation Z" (t)
entre le temps to et le temps t a une probabilité (obtenue suivant la loi
de Student) inferieure à la valeur p=0,05.
Par ailleurs, plus basse est la valeur de la quantification de la
déviation, plus grande est l'écart entre X et N(0,1).
Ce test est donc appliqué aux sévérités Dte obtenues à l'issue de
l'optimisation de l'écart entre zone saine et zone malade, X(t) étant
alors la valeur moyenne sur l'ensemble des patients considérés de la
différence Dte ¨D entrel'instant t et l'instant to, et a(t) étant alors
l'écart type de la distribution de la différence Dte ¨Dteoentre l'instant t
et l'instant to.
La valeur de la différence Dte ¨D entrel'instant t et l'instant to
peut être calculée de plusieurs façons connues de l'homme du métier,
comme par exemple une moyenne simple, une moyenne relative, une
moyenne statistique. De plus, il est possible de retirer les valeurs
extrêmes, ou les valeurs aberrantes. Dans ces deux derniers cas, l'écart
type de la distribution des sévérités Dte ¨Dte, est calculé en écartant les
mêmes valeurs retirées de l'ensemble des valeurs considérées pour
réaliser la moyenne.
Le procédé de détermination comprend ainsi une étape 5 de
détermination d'une valeur Z" (t) de la quantification de la déviation
de la valeur moyenne de la distribution des sévérité Dte entre le temps
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
17
to et le temps t. Cette valeur de quantification sera d'une part
comparée à l'hypothèse nulle pour déterminer la présence d'un effet,
puis comparée à des valeurs Z" (t) d'autres traitements pour en
comparer les effets, ou comparée à des Z" (t) à d'autres instants afin
de déterminer l'évolution dans le temps.
Si l'écart entre une valeur de la statistique de Student associée
à zt,to(t) et la valeur 0,05 de l'hypothèse nulle est important, cela
signifie que la zone traitée évolue de plus en plus distinctement de la
zone non traitée. Le traitement est alors considéré comme efficace. La
statistique de Student est obtenue par lecture de la table de la loi de
Student. Pour une valeur de Z en abscisse, correspond une probabilité
en ordonnée.
La valeur Z permet de caractériser l'efficacité du traitement
sur la durée totale de traitement. La valeur Z permet également de
comparer l'efficacité d'un traitement à l'efficacité d'un autre
traitement de même durée.
Le système de traitement d'images hyper-spectrales 10
comprend un dispositif d'acquisition d'images hyper-spectrales 11
connecté à un moyen de traitement 12, lui-même connecté à un moyen
de stockage de données 13 et à un dispositif d'interaction homme
machine 14.
Le dispositif d'acquisition est apte à réaliser des images hyper-
spectrales de zones (15,16) d'un patient 17. Les zones dont l'image est
acquise sont une zone saine 15 et une zone malade 16. Les images sont
également prises sur des fractions de ces zones ayant reçues un
traitement ou un véhicule. L'acquisition est répétée pour plusieurs
sujets et à des instants de mesure différents. Les données obtenues
sont transmises au moyen de traitement 12 qui les traite en temps réel
ou les redirige vers le moyen de stockage de données 13 pour un
traitement différé.
Le moyen de traitement 12 applique les étapes du procédé de
détermination d'une valeur de quantification de la déviation de la
valeur moyenne d'une distribution de l'écart de sévérité entre un
instant initial et un instant postérieur à l'instant initial, la sévérité
CA 02824911 2013-07-15
WO 2012/098227 PCT/EP2012/050864
18
dépendant du contraste entre des zones recevant un traitement et des
zones recevant un véhicule.
Les résultats du traitement sont affichées par l'intermédiaire du
dispositif d'interaction homme machine 14. Le résultat peut être
affiché sur un écran, transmis à un autre système pour être l'objet d'un
autre traitement, ou transmis par un moyen de communication
électronique distant à ou plusieurs utilisateurs.