Note: Descriptions are shown in the official language in which they were submitted.
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
1
Aminoalcools gras et procédé de préparation de ceux-ci
Domaine de l'invention
L'invention concerne des aminoalcools gras et le procédé de préparation de
ceux-ci, de préférence d'aminoalcool gras de mono-, di- ou triglycérides. En
particulier,
l'invention se rapporte à un procédé de préparation d'aminoalcool gras à
partir d'esters
gras comprenant au moins deux doubles liaisons carbone-carbone.
Arrière plan technologique de l'invention
Les amines aliphatiques sont couramment employées pour la synthèse de
produits ou d'intermédiaires utilisés dans l'industrie pharmaceutique ou
agrochimique.
Ce type d'amines est également utilisé en tant que précurseurs pour la
production de
polymère tel que des polyuréthanes.
La réaction d'hydroaminométhylation a été rapportée par Reppe (Liebigs Ann.
Chem. 1953, 582, 133-161) en utilisant un catalyseur de cobalt. Cette réaction
consiste
en une réaction tandem et one-pot d'hydroformylation/amination d'une oléfine
dans
laquelle l'aldéhyde issu de l'hydroformylation de l'oléfine, réagit avec une
amine
primaire ou secondaire pour former respectivement une amine secondaire ou
tertiaire.
On connaît par US 3,513,200 l'hydroaminométhylation d'une oléfine en
présence d'un catalyseur de rhodium/PPh3 pour la synthèse d'amines tertiaires.
On
connaît également par DE 10321421, US 7,220,884 ou Behr et al. (Tetrahedron
Letters
51 (2010) 2438-2441) des réactions d'hydroaminométhylation. Afin d'améliorer
les
performances de la réaction, l'utilisation de co-catalyseurs, notamment à base
de
rhodium et d'iridium permet une formation rapide d'amine. Le rhodium
intervient dans
la réaction d'hydroformylation, l'iridium dans la réduction catalytique de
l'énamine ou
de l'imine intermédiaire. Les réactions d'hydroaminométhylation sont également
connues pour l'obtention directe de polymère. Müller et al. ont montré que
l'utilisation
de substrat ou d'amine polyfonctionnelles permet d'obtenir par
hydroaminométhylation
des dendrimères de polyamine (Müller et al., Org. Biomol. Chem., 2006, 4, 826-
835).
Wang et al. ont montré l'efficacité de réactions d'hydroaminométhylation sur
des oléfines grasses en présence de différentes amines (Wang et al. Applied
Catalysis
A: General 272 (2004) 151-155). Les réactions étaient effectuées en émulsion
et
nécessitait l'utilisation de tensioactifs comme le CTAB impliquant des étapes
supplémentaires pour la récupération du substrat et du catalyseur. Behr et al.
ont
utilisé les ester méthyliques d'acide oléique dans des réactions
hydroaminométhylation
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
2
où l'amine utilisée est par exemple la proline (Eur. J. Lipid Sci. Technol.
2014, 116,
477-485; Eur. J. Lipid Sci. Technol. 102 (2000) 467-471). Ce type de réaction
ne
forme exclusivement que des amines à partir d'oléfines grasses monoinsaturées.
L'hydroaminométhylation de l'alcool oléique est également connu de Behr et
al.,
Chemie lngenieur Technik, 2007, 79, 5, 621-636.
Résumé de l'invention
La présente invention permet la préparation de composés aminoalcool, c'est-à-
dire comprenant au moins un groupement fonctionnel alcool et au moins un
groupement fonctionnel amine à partir de composés polyinsaturés. Le procédé
est
particulièrement intéressant pour la préparation sélective de composés
aminoalcool à
partir d'esters polyinsaturés, de préférence d'esters gras polyinsaturés. Le
procédé
selon la présente invention couple en une seule étape une réaction
d'hydroaminométhylation d'une première double liaison carbone-carbone et une
réaction d'hydrohydroxyméthylation c'est-à-dire une réaction d'hydrogénation
d'aldéhydes formés in-situ par hydroformylation d'une seconde double liaison
carbone-
carbone.
Selon un premier aspect de la présente invention, des composés aminoalcool
sont fournis. Lesdits composés sont de formule R5-[C(R1)(R2)].-R6 (la) dans
laquelle
u est un nombre entier compris entre 1 et 10;
R1, R2, R5, R6 représentent indépendamment pour chacune des unités
[C(R1)(R2)]. et indépendamment les uns des autres H, -OR', -0C(0)R15, alkyle
en
Cl-030 substitué ou non par un ou plusieurs groupes OR', aryle en 06-012
substitué
ou non par un ou plusieurs groupes -OR', cycloalkyle en 03-010 substitué ou
non
par un ou plusieurs groupes -OR', un groupe de formule (II), ou R6 ou R5 et R1
de
l'une quelconque des unités [C(R1)(R2)]., ou R1 de l'une quelconque des unités
[C(R1)(R2)]. et R2 de l'une quelconque des unités [C(R1)(R2)]. forment
ensemble
avec les atomes de carbone sur lequel ils sont attachés un hétérocycle à 5 ou
6
chaînons,
le groupe de formule (II)
0
0 A n
(11)
comportant au moins 4 atomes de carbone, et au plus 80 atomes
de carbone et dans laquelle
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
3
n est un nombre entier compris entre 1 et 15, avantageusement entre 1 et 10,
de
préférence entre 1 et 6, en particulier entre 1 et 5 ;
A est indépendamment pour chacune des unités [A]n un groupe de formule -[(X)a-
Y-
(X)b]- dans lequel Y est C(R)=C(R'), C(R)(CH2NR3R4)-CH(R'), C(R)(CH2OH)-CH(R')
ou C(R)(R') ;
X représente indépendamment pour chacune des unités (X)a et (X)b et
indépendamment pour chacune des unités [A]n un alkyle en Ci-Cio, aryle en 06-
018,
cycloalkyle en 03-010, hétérocycle de cinq à sept chainons, hétéroaryle de
cinq à
sept chainons, ou un groupe de formule -[(C(R")(R¨))n-(Z)-(C(R")(R¨))d]- dans
lequel Z est aryle en 06-018, cycloalkyle en 03-010, hétérocycle de cinq à
sept
chainons ou hétéroaryle de cinq à sept chaînons ;
R, R', R" et R" représentent indépendamment les uns des autres, indépendamment
pour chacune des unités (C(R")(R")) et indépendamment pour chacune des unités
Y: H, alkyle en Ci-Cio, aryle en 06-012 ou cycloalkyle en 03-010;
R3, R4 représentent indépendamment l'un de l'autre H, alkyle en Ci-Cio, aryle
en 06-
012, benzyle, cycloalkyle en 03-010, ou R3 et R4 forment ensemble avec l'atome
d'azote auquel ils sont attachés un hétérocycle à cinq ou six chaînons;
a, b, c, d étant des nombres entiers compris entre 0 et 20, avantageusement
entre 0
et 15, de préférence entre 0 et 10, la somme de a+b ou c+d étant inférieure à
20 ;
R15 représente H, alkyle en 01-030 substitué ou non par un ou plusieurs
groupes OH
ou par un ou plusieurs groupes de formule (Il) tel que défini ci-dessus, ou
hétérocycle à cinq ou six chaînons substitué ou non par un ou plusieurs
groupes -
OH ou par un ou plusieurs groupes de formule (Il) tel que défini ci-dessus ;
le composé de formule (la) comprenant au moins un groupe de formule (Il) dans
lequel
Y est CR(CH2NR3R4)-CHR' dans au moins une des unités [A]n et au moins un
groupe
de formule (Il) dans laquelle Y est CR(CH2OH)-CHR dans au moins une des unités
[A]n .
Selon un second aspect de la présente invention, un procédé de préparation
d'aminoalcool à partir de composés polyinsaturés est fourni. En particulier,
la présente
invention fournit un procédé de préparation d'aminoalcool à partir d'un
composé B
comprenant au moins deux doubles liaisons carbone-carbone, ledit procédé
comprenant une étape a) de mise en présence sous agitation, d'au moins un
précatalyseur, d'une amine de formule HNR3R4 dans laquelle R3 et R4
représentent
indépendamment l'un de l'autre H, alkyle en Ci-Cio, aryle en 06-012,
cycloalkyle en 03-
Cio ou R3 et R4 forment ensemble avec l'atome d'azote auquel ils sont attachés
un
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
4
hétérocycle à cinq ou six chaînons; et dudit composé B, sous une atmosphère
d'hydrogène et de monoxyde de carbone. Ledit précatalyseur est un complexe de
métaux de transition choisi parmi les colonnes 8 à 10 du tableau périodique.
La présente invention permet de manière surprenante la préparation sélective
de composés aminoalcool gras à partir d'un composé polyinsaturé. En
particulier, la
présente invention permet la préparation sélective de composés esters gras,
tels que
des triglycérides, comprenant un groupement fonctionnel de type amine et deux
groupements fonctionnels de type alcool ou la préparation sélective de
composés
esters gras, tels que des triglycérides, comprenant deux groupements
fonctionnels de
type amine et un groupement fonctionnel de type alcool.
Brève description des figures
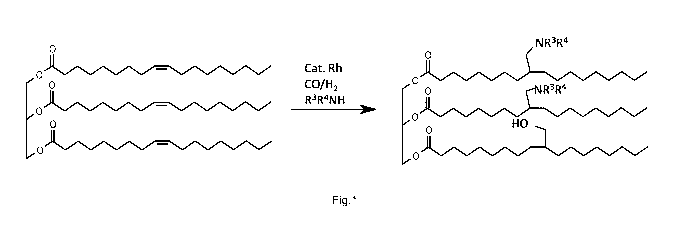
La fig. 1 représente un schéma de la synthèse de composés aminoalcool selon
un mode de réalisation particulier de l'invention.
La fig. 2 représente un spectre RMN d'un composé aminoalcool selon la
présente invention
Description détaillée de la présente invention
Le terme substitué tel qu'utilisé dans la présente invention signifie que
un
ou plusieurs atomes d'hydrogène du groupement auquel le terme substitué
fait
référence est remplacé par un des substituants nommés à condition que la
valence
normale de l'atome sur lequel la substitution est considérée n'est pas
dépassée et que
la substitution résulte en un composé chimique stable, c'est-à-dire un composé
suffisamment robuste pour être isolé d'un mélange réactionnel.
Le terme alkyl se réfère à des chaînes hydrocarbonées linéaires ou
branchées contenant le nombre spécifié d'atomes de carbone. Par exemple,
alkyle en
Cl-06 signifie un groupe alkyle linéaire ou branché contenant au moins 1, et
au plus, 6
atomes de carbone. Le terme aryle se réfère à un cycle hydrocarboné
aromatique
contenant le nombre spécifié d'atomes de carbone substitué ou non par un
alkyle Cl-
010 non substitué, halogène, NO2, ON, SO3H, un groupement carbonyle,
carboxyle,
OH, alkoxy en Cl-010. Par exemple, aryle peut être un phényle, naphtyle,
anthracyle ou
phénanthryle. Le terme cycloalkyle se réfère à un cycle hydrocarboné non
aromatique monocyclique ou polycyclique condensé comportant le nombre spécifié
d'atomes de carbone. Par exemple, cycloalkyle comprend le cyclopropyle,
cyclobutyle,
cyclopentyle, cyclohexyle, cycloheptyle ou cyclooctyle. Le terme hétéroaryle
se
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
réfère à un cycle hydrocarboné aromatique monocyclique ou polycyclique
condensé
comportant le nombre de chaînons spécifié, dans lequel au moins un des atomes
de
carbone est remplacé par un atome de phosphore, de soufre, d'azote ou
d'oxygène.
Par exemple, hétéroaryle inclut sans y être limité le furane, le thiophène, le
pyrrole,
5 l'imidazole, le pyrazole, le triazole, le tétrazole, le thiazole,
l'oxazole, la pyridine, le
pyridazine, la pyrazine, l'indole et l'indazole. Le terme hétérocycle se
réfère à un
cycle hydrocarboné non aromatique monocyclique ou polycyclique condensé
comportant le nombre de chaînons spécifié, dans lequel au moins un des atomes
de
carbone est remplacé par un atome de phosphore, de soufre, d'azote ou
d'oxygène.
Par exemple, hétérocycle inclut sans y être limité le tétrahydrofurane, le
dihydropyrane,
le tétrahydropyrane, le pyrane, la pipéridine, le pyrrolidine et le dioxane.
Composé aminoalcool
Selon un premier aspect de la présente invention, des composés aminoalcool
sont fournis. Lesdits composés sont de formule R5-[C(R1)(R2)]õ-R6 (la) dans
laquelle
u est un nombre entier compris entre 1 et 10 ;
R1, R2, R5, R6 représentent indépendamment pour chacune des unités
[C(R1)(R2)]. et indépendamment les uns des autres H, -OR', -0C(0)R15, alkyle
en
Cl-030 substitué ou non par un ou plusieurs groupes OR', aryle en 06-012
substitué
ou non par un ou plusieurs groupes -OR', cycloalkyle en 03-010 substitué ou
non
par un ou plusieurs groupes -OR', un groupe de formule (Il), ou R6 ou R5 et R1
de
l'une quelconque des unités [C(R1)(R2)]., ou R1 de l'une quelconque des unités
[C(R1)(R2)], et R2 de l'une quelconque des unités [C(R1)(R2)]. forment
ensemble
avec les atomes de carbone sur lequel ils sont attachés un hétérocycle à 5 ou
6
chaînons,
le groupe de formule (Il)
0
0 A n
(11)
comportant au moins 4 atomes de carbone, et au plus 80 atomes
de carbone et dans laquelle
n est un nombre entier compris entre 1 et 15, avantageusement entre 1 et 10,
de
préférence entre 1 et 5;
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
6
A est indépendamment pour chacune des unités [A]n un groupe de formule -[(X)a-
Y-
(X)b]- dans lequel Y est C(R)=C(R'), C(R)(CH2NR3R4)-CH(R'), C(R)(CH2OH)-CH(R')
ou C(R)(R') ;
X représente indépendamment pour chacune des unités (X)a et (X)b et
indépendamment pour chacune des unités [A]n un alkyle en Ci-Cio, aryle en 06-
018,
cycloalkyle en 03-010, hétérocycle de cinq à sept chainons, hétéroaryle de
cinq à
sept chainons, ou un groupe de formule -[(C(R")(R¨))c-(Z)-(C(R")(R¨))d]- dans
lequel Z est aryle en 06-018, cycloalkyle en 03-010, hétérocycle de cinq à
sept
chainons ou hétéroaryle de cinq à sept chaînons ;
R, R', R" et R" représentent indépendamment les uns des autres, indépendamment
pour chacune des unités (C(R")(R")) et indépendamment pour chacune des unités
Y: H, alkyle en Ci-Cio, aryle en 06-012 ou cycloalkyle en 03-010;
R3, R4 représentent indépendamment l'un de l'autre H, alkyle en Ci-Cio, aryle
en 06-
012, benzyle, cycloalkyle en 03-010 ou R3 et R4 forment ensemble avec l'atome
d'azote auquel ils sont attachés un hétérocycle à cinq ou six chaînons;
a, b, c, d étant des nombres entiers compris entre 0 et 20, avantageusement
entre 0
et 15, de préférence entre 0 et 10, la somme de a+b ou c+d étant inférieure à
20 ;
R15 représente H, alkyle en 01-030 substitué ou non par un ou plusieurs
groupes OH
ou par un ou plusieurs groupes de formule (Il) tel que défini ci-dessus, ou
hétérocycle à cinq ou six chaînons substitué ou non par un ou plusieurs
groupes -
OH ou par un ou plusieurs groupes de formule (Il) tel que défini ci-dessus ;
le composé de formule (la) comprenant au moins un groupe de formule (Il) dans
lequel
Y est CR(CH2NR3R4)-CHR' dans au moins une des unités [A]n et au moins un
groupe
de formule (Il) dans laquelle Y est CR(CH2OH)-CHR dans au moins une des unités
[A]n. Ainsi, un même groupe de formule (Il) peut comporter une unité [A] dans
laquelle
Y est CR(CH2NR3R4)-CHR' et une autre unité [A] dans laquelle Y est CR(CH2OH)-
CHR. Alternativement, le composé peut comprendre un groupe Y étant
CR(CH2NR3R4)-CHR' dans une unité [A] d'un premier groupe de formule (Il) et un
groupe Y étant CR(CH2OH)-CHR dans une unité [A] d'un second groupe de formule
(II).
Avantageusement, le groupe de formule (Il) comporte au moins 4 atomes de
carbone, de préférence au moins 8 atomes de carbone, en particulier au moins
10
atomes de carbone, plus particulièrement au moins 12 atomes de carbone, et au
plus
80 atomes de carbone, de préférence au plus 60 atomes de carbone, en
particulier au
plus 50 atomes de carbone, plus particulièrement au plus 40 atomes de carbone.
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
7
Selon un mode de réalisation particulier, le composé selon la présente
invention
peut être de formule (la) dans lequel au moins deux des substituants R1, R2,
R5 ou R6
représentent indépendamment les uns des autres un groupe de formule (Il)
0
- H
0 _ A n
(ID
comportant au moins 4 atomes de carbone, et au plus 80 atomes
de carbone et dans laquelle
n est un nombre entier compris entre 1 et 15, avantageusement entre 1 et 10,
de
préférence entre 1 et 5;
A est choisi indépendamment pour chacune des unités [A]n parmi les groupes de
formule (11a), (11b), (11c) ou (11d)
¨[(CH2)q-CH=CH-(CH2)t]- (11a),
¨[(CH2)v-CH(CH2NR3R4)-CH2-(CH2)]- (11b),
¨[(CH2)y-CH(CH2OH)-CH2-(CH2)z1- (11c),
-[(CH2)x]- (11d),
q, t, y, w, y et z étant des nombres entiers compris entre 0 et 20,
avantageusement
entre 0 et 15, de préférence entre 0 et 10, la somme de q+t, v+w ou y+z étant
inférieure à 20 ;
x est un nombre entier entre 10 et 30;
le composé de formule (la) comprenant au moins un groupe de formule (Il) dans
lequel
au moins une des unités [A]n est de formule (11b) et au moins un groupe de
formule (Il)
dans lequel au moins une des unités [A]n est de formule (11c).
Selon un mode de réalisation préféré, le composé selon la présente invention
peut être de formule (111a) :
R9
R7
R1 _________ [ 1u R8
R6 R1 R5
(111a)
dans laquelle
u est un nombre entier compris entre 1 et 7, avantageusement entre 1 et 6, de
préférence entre 1 et 5, en particulier entre 1 et 4,
R1, R7, R8, R9,
K R5
et R6 représentent indépendamment les uns des autres et,
pour R1 indépendamment pour chacune des unités [CHR1]., un groupement de
formule (Il), H, -0R15, alkyle en Ci-Cio substitué ou non par un ou plusieurs
groupes
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
8
-OR', aryle en 06-012 substitué ou non par un ou plusieurs groupes -OR',
cycloalkyle en 03-010 substitué ou non par un ou plusieurs groupes -OR',
R15 représente H ou alkyle en Ci-Cio substitué ou non par un ou plusieurs
groupes -
OH, par un ou plusieurs groupes de formule (11) ou par un groupe de formule
(IV)
R2Lo
R22( R2
R21
(Iv) dans laquelle
R20, R21, R22, rç 1-,23
représentent indépendamment les uns des autres H, -OH, alkyle
R24 en Ci-Cio substitué ou non par un ou plusieurs groupes ¨OR' ; rç
représente H,
alkyle en Ci-Cio substitué ou non par un ou plusieurs groupes -OH, ou un ou
plusieurs groupes de formule (11);
le groupe de formule (11) étant représenté ci-dessus dans lequel n est un
nombre entier
compris entre 1 et 15, avantageusement entre 1 et 10, de préférence entre 1 et
5; A
est choisi indépendamment pour chacune des unités [A] parmi les groupes de
formule
(11a), (11b), (11c) ou (11d)
¨[(0H2)q-CH=CH-(0H2)t]- (11a),
¨[(CH2)v-CH(CH2NR3R4)-CH2-(CH2),1- (I lb),
¨[(0H2)y-CH(CH2OH)-0H2-(0H2)z1- (11c),
-[(CH2)x]- (11d),
R3, R4 représentent indépendamment l'un de l'autre H, alkyle en Ci-Cio, aryle
en 06-
012, benzyle, cycloalkyle en 03-010 ou R3 et R4 forment avec l'atome d'azote
auquel ils
sont attachés un hétérocycle à cinq ou six chaînons ; q, t, y, w, y et z étant
des
nombres entiers compris entre 0 et 20, avantageusement entre 0 et 15, de
préférence
entre 0 et 10, la somme de q+t, v+w ou y+z étant inférieure à 20 ; x est un
nombre
entier entre 10 et 30 ; le composé de formule (111a) comprenant au moins un
groupe de
formule (11) dans lequel au moins une des unités [A]n est de formule (11b) et
au moins
un groupe de formule (11) dans lequel au moins une des unités [A]n est de
formule (11c)
tel que défini ci-dessus.
De préférence, dans ce mode de réalisation préféré, au moins deux des
substituants R1, R5, R6 représentent indépendamment l'un de l'autre un groupe
de
formule (11) dans laquelle n est 1 et A est un groupe de formule (11b) ou
(11c).
Selon un autre mode de réalisation préféré, le composé selon la présente
invention peut être de formule (111b) :
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
9
,
,R5
R`
\____¨......,
R'i
'R6
(111b)
dans laquelle
R1, R2, R5 et R6 représentent indépendamment l'un de l'autre un groupe de
formule (11),
-OR', alkyle en Ci-Cio substitué ou non par un ou plusieurs groupes -OR',
R15 représente H, alkyle en Ci-Cio substitué ou non par un ou plusieurs
groupes -OH,
ou un ou plusieurs groupes de formule (11) ou un groupe de formule (IV) ;
le groupe de formule (11) étant représenté ci-dessus dans lequel n est un
nombre entier
compris entre 1 et 15, avantageusement entre 1 et 10, de préférence entre 1 et
5; A
est choisi indépendamment pour chacune des unités [A] parmi les groupes de
formule
(11a), (11b), (11c) ou (11d)
¨[(CH2)q-CH=CH-(CH2)t]- (11a),
¨[(CH2)v-CH(CH2NR3R4)-CH2-(CH2)]- (I lb),
¨[(CH2)y-CH(CH2OH)-CH2-(CH2)z1- (11c),
-[(CH2)x]- (11d),
R3, R4 représentent indépendamment l'un de l'autre H, alkyle en Ci-Cio, aryle
en 06-
012, benzyle, cycloalkyle en 03-010 ou R3 et R4 forment avec l'atome d'azote
auquel ils
sont attachés un hétérocycle à cinq ou six chaînons ; q, t, y, w, y et z étant
des
nombres entiers compris entre 0 et 20, avantageusement entre 0 et 15, de
préférence
entre 0 et 10, la somme de q+t, v+w ou y+z étant inférieure à 20 ; x est un
nombre
entier entre 10 et 30 ;
le composé de formule (111b) comprenant au moins un groupe de formule (11)
dans
lequel au moins une des unités [A]n est de formule (11b) et au moins un groupe
de
formule (11) dans lequel au moins une des unités [A]n est de formule (11c) tel
que défini
ci-dessus.
De préférence, dans ce mode de réalisation, R5 représente un groupe de
formule (11) dans laquelle n est 1 et A est de formule (11b) et R6 représente
un groupe
de formule (11) dans laquelle n est 1 et A est de formule (11a).
Selon un autre mode de réalisation préféré, le composé selon la présente
invention peut être de formule (111c) :
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
R5
0- __________ ---
Y-0
R6
(111c)
dans laquelle
R5 représente un groupe de formule (Il) dans laquelle
n est un nombre entier compris entre 1 et 15, avantageusement entre 1 et 10,
de préférence entre 1 et 5 ; A est un groupe de formule
5 ¨RCH2)v-CH(CH2NR3R4)-CH2-(CH2)]- (11b),
R3, R4 représentent indépendamment l'un de l'autre H, alkyle en Ci-Cio, aryle
en 06-012, benzyle, cycloalkyle en 03-010 ou R3 et R4 forment avec l'atome
d'azote auquel ils sont attachés un hétérocycle à cinq ou six chaînons ; y et
w
étant des nombres entiers compris entre 0 et 20, avantageusement entre 0 et
10 15, de préférence entre 0 et 10, la somme de v+w étant inférieure à 20
; et
R6 représente un groupe de formule (Il) dans laquelle
n est un nombre entier compris entre 1 et 15, avantageusement entre 1 et 10,
de préférence entre 1 et 5 ; A est un groupe de formule
¨[(0H2)y-CH(CH2OH)-0H2-(0H2)z1- (11c),
y et z étant des nombres entiers compris entre 0 et 20, avantageusement
entre 0 et 15, de préférence entre 0 et 10, la somme de v+w étant inférieure à
20.
Selon un mode de réalisation particulier, le composé selon la présente
invention
est de formule (111a) dans laquelle
u est un nombre entier compris entre 1 et 5, de préférence entre 1 et 4;
R7, R8, R9, r< ¨19
représentent un hydrogène,
R1, R5 et R6 représentent indépendamment les uns des autres, et pour R1
indépendamment pour chacune des unités [CHR1]., un groupe de formule (Il) dans
laquelle A est choisi indépendamment pour chacune des unités [A]n- parmi les
groupes de formule (11a), (11b) ou (11c),
le composé de formule (111a) comprenant au moins un groupe de formule (Il)
dans
lequel au moins une des unités [A]n est de formule (11b) et au moins un groupe
de
formule (Il) dans lequel au moins une des unités [A]n est de formule (11c).
Le composé selon la présente invention peut être de formule (111a) dans
laquelle
u est un nombre entier compris entre 1 et 5, de préférence entre 1 et 4;
R7, R8, R9, r< ¨19
représentent un hydrogène,
CA 02970218 2017-06-08
WO 2016/128390
PCT/EP2016/052712
11
R1, R5 et R6 représentent indépendamment les uns des autres, et pour R1
indépendamment pour chacune des unités [CHR1, un groupe de formule (Il) dans
laquelle n est 1, et A est choisi indépendamment pour chacune des unités [A]i-
parmi les groupes de formule (11a), (11b) ou (11c) ; le composé (111a)
comprenant au
moins un groupe de formule (Il) dans lequel A est (11b) et au moins un groupe
de
formule (Il) dans lequel A est (11c).
Le composé selon la présente invention peut être de formule (111a) dans
laquelle
R7, R8, R9, rç ¨19
représentent un hydrogène,
u est 1,
R1, R5 et R6 représentent indépendamment les uns des autres un groupe de
formule (Il) dans laquelle A est choisi indépendamment pour chacune des unités
[A]n- parmi les groupes de formule (11b) ou (11c),
R3, R4, y, w, y et z étant tels que définis ci-dessus;
n est un nombre entier compris entre 1 et 5 ;
chacun des substituants R1, R5 et R6 comprenant au moins 12 atomes de carbone
et au plus 25 atomes de carbone,
le composé de formule (111a) comprenant au moins un groupe de formule (Il)
dans
lequel au moins une des unités [A]n est de formule (11b) et au moins un groupe
de
formule (Il) dans lequel au moins une des unités [A]n est de formule (11c).
Le composé de formule (111a) peut comprendre plus de groupes de formule (Il)
dans lequel au moins une des unités [A]n est de formule (11b) que de groupes
de
formule (Il) dans lequel au moins une des unités [A]n est de formule (11c).
Alternativement, le composé de formule (111a) peut comprendre moins de groupes
de
formule (Il) dans lequel au moins une des unités [A]n est de formule (11b) que
de
groupes de formule (Il) dans lequel au moins une des unités [A]n est de
formule (11c).
Plus particulièrement, le composé selon la présente invention peut être de
formule (111a) dans laquelle
R7, R8, R9, rç ¨19
représentent un hydrogène, u est 1,
R1, R5 et R6 représentent indépendamment l'un de l'autre un groupe de formule
(Il)
dans laquelle n est 1, A est un groupe de formule (11b) ou (11c)
¨[(CH2)v-CH(CH2NR3R4)-CH2-(CH2)]- (11b), ou
¨[(CH2)y-CH(CH2OH)-CH2-(CH2)z]- (11c);
R3, R4 représentent indépendamment l'un de l'autre H, alkyle en Ci-Cio, aryle
en
06-012, benzyle, cycloalkyle en 03-010 ou R3 et R4 forment ensemble avec
l'atome d'azote auquel ils sont attachés un hétérocycle à cinq ou six
chaînons;
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
12
y, y, w et z sont indépendamment l'un de l'autre un nombre entier compris
entre
4 et 9,
v+w ou y+z étant un nombre entier compris entre 11 et 15,
le composé de formule (111a) comprenant au moins un groupe de formule (Il)
dans
lequel A est de formule (11b) et au moins un groupe de formule (Il) dans
lequel A est de
formule (11c), de préférence le composé de formule (111a) comprenant un groupe
de
formule (Il) dans lequel A est de formule (11b) et deux groupes de formule
(Il) dans
lequel A est de formule (11c) ou deux groupes de formule (Il) dans lequel A
est de
formule (11b) et un groupe de formule (Il) dans lequel A est de formule (11c).
Procédé de préparation
Selon un second aspect de la présente invention, un procédé de préparation
d'aminoalcool est fourni. Le procédé permet en une seule étape
l'hydroaminométhylation d'une première double liaison carbone-carbone et
l'hydrohydroxyméthylation d'une seconde double liaison carbone-carbone, i.e.
l'hydrogénation d'aldéhydes formés in-situ par hydroformylation de ladite
seconde
double liaison carbone-carbone. Ainsi, l'hydrogénation d'aldéhydes formés in-
situ
permet la formation d'alcool. En particulier, la présente invention fournit un
procédé de
préparation d'aminoalcool à partir d'un composé B comprenant au moins deux
doubles
liaisons carbone-carbone, ledit procédé comprenant une étape a) de mise en
présence
sous agitation dans un réacteur, d'au moins un précatalyseur, d'une amine de
formule
HNR3R4 dans laquelle R3 et R4 représentent indépendamment l'un de l'autre H,
alkyle
en Ci-Cio, aryle en 06-012, cycloalkyle en 03-010 ou R3 et R4 forment ensemble
avec
l'atome d'azote auquel ils sont attachés un hétérocycle à cinq ou six
chaînons; et dudit
composé B, sous une atmosphère d'hydrogène et de monoxyde de carbone. Ledit
procédé permet la préparation d'un composé dans lequel un atome de carbone
d'au
moins une des doubles liaisons carbone-carbone du composé B a été substitué
par un
groupement ¨CH2NR3R4, l'autre atome de carbone de cette même double liaison
carbone-carbone étant substitué par un hydrogène ; et dans lequel un atome de
carbone d'au moins une autre des doubles liaisons carbone-carbone du composé B
a
été substitué par un groupement ¨CH2OH, l'autre atome de carbone de cette même
double liaison carbone étant substitué par un hydrogène. Les doubles liaisons
carbone-carbone contenues dans le composé B peuvent être de configuration cis
ou
trans. Le terme double liaison carbone-carbone englobe les deux
configurations.
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
13
La figure 1 illustre le procédé selon un mode de réalisation particulier de la
présente invention faisant intervenir une réaction d'hydroaminométhylation et
d'hydrohydroxyméthylation. Le composé B est représenté par la trioléine
comprenant
trois doubles liaisons carbone-carbone. Le procédé selon la présente invention
permet
ainsi la préparation d'un composé aminoalcool dans lequel deux des trois
doubles
liaisons carbone-carbone sont hydroaminométhylées tandis que la troisième
double
liaison carbone-carbone est hydrohydroxyméthylée.
Le présent procédé est donc effectué sous pression d'une atmosphère
d'hydrogène et de monoxyde de carbone. La pression peut être comprise entre 10
bars
et 200 bars, avantageusement entre 20 bars et 150 bars, de préférence entre 50
bars
et 100 bars. La pression se rapporte à la somme des pressions partielles de
monoxyde
de carbone et d'hydrogène. Le rapport molaire entre le monoxyde de carbone et
l'hydrogène est compris entre 1 : 10 et 10: 1, avantageusement le rapport
molaire
entre le monoxyde de carbone et l'hydrogène est compris entre 1 : 5 et 5: 1,
de
préférence le rapport molaire est compris entre 1 : 3 et 3: 1, en particulier
le rapport
molaire entre le monoxyde de carbone et l'hydrogène est compris entre 1 : 2 et
2 : 1.
Plus particulièrement, le rapport molaire entre le monoxyde de carbone et
l'hydrogène
est de 1 : 2.
Avantageusement, ledit composé B peut être de formule (V') Ra-[C(Rd)(Re)]-Rf
dans lequel
u est un nombre entier compris entre 1 et 10
Ra, Rd, Re, Rf représentent indépendamment les uns des autres, et
indépendamment
pour chacune des unités [C(Rd)(Re)], H, -OR, -0-C(0)-RJ, alkyle en Cl-030
substitué
ou non par un ou plusieurs groupes ¨OR, aryle en 06-012 substitué ou non par
un ou
plusieurs groupes ¨OR, cycloalkyle en 03-010 substitué ou non par un ou
plusieurs
groupes ¨OR, un groupe de formule (V), ou Re ou Rf et Rd de l'une quelconque
des
unités [C(Rd)(Re)], ou Rd de l'une quelconque des unités [C(Rd)(Re)] et Re de
l'une
quelconque des unités [C(Rd)(Re)] forment ensemble avec les atomes de carbone
sur
lequel ils sont attachés un hétérocycle à 5 ou 6 chaînons,
le groupe de formule (V) comportant au moins 3 atomes de carbone et au plus 79
atomes de carbone, et étant de formule ¨0-C(0)-[A]n-H (V) dans lequel A est -
(X)a-
C(R)=C(R')-(X)b-
n est un nombre entier compris entre 1 et 10, de préférence entre 1 et 6 ;
X représente indépendamment pour chacune des unités (X)a et (X)b et
indépendamment pour chacune des unités [A]n un alkyle en Cl-010, aryle en 06-
018,
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
14
cycloalkyle en 03-010, hétérocycle de cinq à sept chainons, hétéroaryle de
cinq à sept
chainons, ou un groupe de formule [(C(R")(R¨))c-(Z)-(C(R")(R'"))d] dans lequel
Z est
aryle en 06-018, cycloalkyle en 03-010, hétérocycle de cinq à sept chainons ou
hétéroaryle de cinq à sept chainons;
a, b, c et d étant des nombres entiers compris entre 0 et 20, avantageusement
entre 0
et 15, de préférence entre 0 et 10, la somme de a+b étant inférieure à 20 ;
R, R', R" et R" représentent indépendamment les uns des autres, indépendamment
pour chacune des unités (C(R')(R")) et indépendamment pour chacune des unités
Y:
H, alkyle en Ci-Cio, aryle en 06-012 ou cycloalkyle en 03-010;
RJ représente H, alkyle en 01-030 substitué ou non par un ou plusieurs groupes
OH,
alkyle en 01-030 substitué ou non par un ou plusieurs groupes de formule (V)
tel que
défini ci-dessus, un hétérocycle à cinq ou six chaînons substitué ou non par
un ou
plusieurs groupes OH, ou un hétérocycle à cinq ou six chaînons substitué ou
non par
un ou plusieurs groupes de formule (V) tel que défini ci-dessus ;
le composé B de formule (V') comprenant au moins deux groupes de formule (V)
ou un
groupe de formule (V) dans lequel n est au moins 2, pour préparer un composé
selon
la présente invention de formule (la).
De préférence, le groupe de formule (V) est de formule (Va) comportant au
moins 3 atomes de carbone et au plus 79 atomes de carbone,
-0-C(0)-[-(CH2)p-C=C-(CH2)s-k-H (Va)
dans laquelle
r est un nombre entier compris entre 1 et 15, avantageusement entre 1 et 10,
de
préférence entre 1 et 6, en particulier entre 1 et 5 ;
p et s étant des nombres entiers compris entre 0 et 20, avantageusement entre
0
et 15, de préférence entre 0 et 10, la somme de p+s étant inférieure à 20 et
supérieure à 1;
le composé B de formule (V') comprenant au moins deux groupes de formule (Va)
ou un groupe de formule (Va) dans lequel r est au moins 2.
Les doubles liaisons carbone-carbone contenues dans le groupe de formule (Va)
peuvent être de configuration cis ou trans.
En particulier, ledit composé B est de formule (Via), (Vlb) ou (Mc) :
Rb Rf
Ra [ Rg
Rc Rd Rb
(Via)
dans laquelle
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
u est un nombre entier compris entre 1 et 7, avantageusement entre 1 et 6, de
préférence entre 1 et 5, en particulier entre 1 et 4,
Rd, Rb, Rc, Rg, Ra
et Rf représentent indépendamment les uns des autres et,
pour Rd indépendamment pour chacune des unités [CHRd]., un groupement de
5
formule (Va) tel que défini ci-dessus, H, -OR, alkyle en Ci-Cio substitué ou
non par
un ou plusieurs groupes ¨OR, aryle en 06-012 substitué ou non par un ou
plusieurs
groupes ¨OR, cycloalkyle en 03-010 substitué ou non par un ou plusieurs
groupes ¨
OR,
R représente H, alkyle en Ci-Cio substitué ou non par un ou plusieurs groupes -
OH,
10 par un
ou plusieurs groupes de formule (Va) tel que défini ci-dessus ou par un
groupe de formule (IV)
R2Lo
R21
(IV) dans laquelle
R20, R21, R22, rc 1-+23
représentent indépendamment les uns des autres H, -OH, alkyle
1-+24
en Ci-Cio substitué ou non par un ou plusieurs groupes ¨OR' ; rc représente H,
15 alkyle
en Ci-Cio substitué ou non par un ou plusieurs groupes ¨OH ou par un ou
plusieurs groupes de formule (Va) tel que défini ci-dessus ;
ou
d
RaRf
(Vlb)
dans laquelle
Ra, Rf, Rd et Re représentent indépendamment les uns des autres un groupe de
formule (Va) tel que défini ci-dessus, -OR, alkyle en Ci-Cio substitué ou non
par
un ou plusieurs groupes ¨OR,
R représente H, alkyle en Ci-Cio substitué ou non par un ou plusieurs groupes
¨
OH, par un ou plusieurs groupes de formule (Va) tel que défini ci-dessus ou
par un
groupe de formule (IV) ;
ou
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
16
Rf
0¨ ____________ --
Y-0
Ra
(VIc) dans laquelle
Ra et Rf représentent indépendamment l'un de l'autre un groupe de formule (Va)
tel
que défini ci-dessus ;
le composé de formule (Via), (Vlb) ou (\Ac) comprenant au moins deux groupes
de
formule (Va) tel que défini ci-dessus ou un groupe de formule (Va) tel que
défini ci-
dessus dans lequel r est au moins 2. Ainsi, des composés de formule (111a),
(111b) ou
(111c) selon la présente invention peuvent être préparés.
Plus particulièrement, ledit composé B est de formule (Via)
Rb Rf
Ra [ 1 lu Rg
Rc Rd Rb
(Vla)
dans laquelle
Rb, Rc, Rg, Rb représentent un hydrogène,
u est un nombre entier compris entre 1 et 5, avantageusement entre 1 et 4, de
préférence u est 1 ;
Ra, Rd et Rf représentent indépendamment les uns des autres, et pour Rd
indépendamment pour chacune des unités [CHRI, un groupe de formule (Va) tel
que défini ci-dessus.
De manière privilégiée, ledit composé B est de formule (Via) dans laquelle Rb,
Rc, Rg, Rb représentent un hydrogène, u est 1, Rd, Ra et Rf représentent
indépendamment les uns des autres un groupe de formule (Va) tel que défini ci-
dessus
dans laquelle r est 1, p et s sont compris indépendamment l'un de l'autre
entre 4 et 9,
p+s étant compris entre 10 et 14.
Selon un mode de réalisation préféré, l'étape a) du présent procédé est
réalisée
à une température comprise entre 25 C et 150 C, avantageusement entre 35 C et
120 C, de préférence entre 50 C et 120 C.
De préférence, l'étape a) est réalisée à une température comprise entre 25 C
et
65 C, avantageusement entre 25 C et 55 C. Dans cette gamme de température,
l'hydroformylation de la double liaison carbone-carbone, puis la réduction en
alcool du
groupement carbonyle (réaction d'hydrohydroxyméthylation) est favorisée.
Ainsi, la
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
17
préparation d'un composé de formule (111a) dans laquelle le nombre d'unité A
de
formule (11c) est supérieur au nombre d'unité A de formule (11b) peut être
favorisée.
Alternativement, l'étape a) est réalisée à une température comprise entre 65 C
et 150 C, avantageusement entre 70 C et 120 C. Dans cette gamme de
température,
l'hydroaminométhylation de la double liaison carbone-carbone est favorisée.
Ainsi, la
préparation d'un composé de formule (111a) dans laquelle le nombre d'unité A
de
formule (11b) est supérieur au nombre d'unité A de formule (11c) peut être
favorisée.
Selon un mode de réalisation préféré, la proportion d'amine mise en oeuvre à
l'étape a) du présent procédé est supérieure à 0,8 équivalent par rapport à la
quantité
de composé B mis en oeuvre à l'étape a), avantageusement, la proportion est
comprise
entre 0,8 et 2 équivalents, de préférence entre 0,8 et 1,5 équivalents. Dans
ce mode
de réalisation, la préparation, à partir d'un composé B de formule (V'), d'un
composé
de formule (la) comprenant moins d'unité A dans laquelle Y est CR(CH2NR3R4)-
CHR'
que d'unité A dans laquelle Y est CR(CH2OH)-CHR est favorisée. En particulier,
la
préparation, à partir d'un composé B de formule (Via) avec u = 1, d'un composé
de
formule (111a) dans lequel u est 1 et comprenant une unité A de formule (11b)
et deux
unités A de formule (11c) est favorisée.
Selon un mode de réalisation alternatif, la proportion d'amine mise en oeuvre
à
l'étape a) du présent procédé est inférieure à 0,8 équivalent par rapport à la
quantité
de composé B mis en oeuvre à l'étape a), avantageusement, la proportion est
comprise
entre 0,1 et 0,8 équivalents, de préférence entre 0,2 et 0,7 équivalents. Dans
ce mode
de réalisation, la préparation d'un composé de formule (la) selon la présente
invention
comprenant plus d'unité A dans laquelle Y est CR(CH2NR3R4)-CHR' que d'unité A
dans
laquelle Y est CR(CH2OH)-CHR est favorisée. En particulier, la préparation, à
partir
d'un composé B de formule (Via) avec u = 1, d'un composé de formule (111a)
dans
lequel u est 1 et comprenant deux unités A de formule (11b) et une unité A de
formule
(11c) est favorisée.
Selon un mode de réalisation préféré, le précatalyseur est un complexe
comprenant un métal de transition choisi parmi les colonnes 8 à 10 du tableau
périodique, avantageusement le métal de transition est choisi parmi la colonne
9 du
tableau périodique, de préférence, le précatalyseur est un complexe comprenant
un
métal de transition choisi parmi le rhodium ou le cobalt. Le précatalyseur
peut
comprendre un ou plusieurs ligands. Au moins un desdits un ou plusieurs
ligands est
choisi parmi CO, acetylacetonate, cyclooctadiene, norbornène, acétate.
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
18
Lesdits un ou plusieurs ligands peuvent également comprendre au moins un
ligand phosphoré monodentate ou bidentate comprenant au moins un substituant
aryle
en 06-018 substitué en position ortho par rapport à l'atome de phosphore ou
comprenant au moins un substituant aryloxy en 06-018. Avantageusement, ledit
ligand
phosphoré peut être de formule P(Ar)3 ou (Ar)2-P-L-P(Ar)2 dont laquelle Ar est
un
groupement aryle en 06-018 substitué u moins en position ortho par rapport à
l'atome
de phosphore par un groupement sélectionné parmi le groupe consistant en Cl-Cs
alkyle, phényle, benzyle, 03-06 cycloalkyle, halogène, alcoxyle en 01-06,
aryloxy en
06; et L est un bras espaceur sélectionné parmi le groupe consistant en alkyle
en 01-
Cs, aryle en 06-012, cycloalkyle en 03-010. L'expression substitué en
position ortho
par rapport à l'atome de phosphore signifie que, dans le cycle aryle, au
moins une
des deux positions ortho par rapport à l'atome de carbone lié à l'atome de
phosphore
est substituée par l'un de groupements mentionnés. De préférence, ledit ligand
phosphoré peut être de formule P(Ar)3 dans laquelle Ar est un groupement aryle
en 06-
018 substitué en position ortho par rapport à l'atome de phosphore par un
groupement
sélectionné parmi le groupe consistant en méthyle, éthyle, méthoxy, phényle,
benzyle,
-F, cyclohexyle.
Alternativement, ledit ligand phosphoré peut être de formule P(0-Ar)3 ou (Ar-
0)2-P-L-P(0-Ar)2 dans laquelle Ar est un groupement aryle en 06-018 substitué
ou non
par groupement sélectionné parmi le groupe consistant en Cl-Cs alkyle, 03-06
alkyle,
halogène, alcoxyle en 01-06, aryloxy en 06; et L est un bras espaceur
sélectionné
parmi le groupe consistant en alkyle en 01-06, aryle en 06-012, cycloalkyle en
03-010.
De préférence, ledit ligand phosphoré peut être de formule P(0-Ar)3 dans
laquelle Ar
est un aryle en Cs substitué ou non un groupement méthyle, éthyle, méthoxy,
phényle,
benzyle, cyclohexyle.
En particulier, ledit ligand phosphoré peut être P(OPh)3, P(06F5)3, P(o-
Melph)3,
P(o-OMePh)3.
Alternativement, lesdits un ou plusieurs ligands comprennent également au
moins un ligand phosphoré monodentate ou bidentate hydrosoluble comprenant au
moins un groupement fonctionnel S03-X+, NR3+A-, 002-X+, X représentant Li, Na
ou
K ; et A représentant Cl, Br ou I. Avantageusement, ledit ligand phosphoré
peut être de
formule P(Ar)3 ou (Ar)2-P-L-P(Ar)2 dans laquelle L est un bras espaceur
sélectionné
parmi le groupe consistant en alkyle en Cl-Cs, aryle en 06-012, cycloalkyle en
03-010;
et Ar est un aryle en 06-018 substitué par au moins un groupement fonctionnel
S03-X+,
NR3+A-, CO2-X+, X représentant Li, Na ou K, et A représentant Cl, Br ou I ; et
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
19
optionnellement substitué par un groupement sélectionné parmi le groupe
consistant
en Cl-Cs alkyle, phényle, benzyle, 03-06 cycloalkyle, halogène, alcoxyle en 01-
06,
aryloxy en Cs.
Selon un mode de réalisation particulier, l'étape a) met également en présence
une cyclodextrine ¨a, ¨13, ¨y méthylée présentant un degré de substitution
moyen
compris entre 0,5 et 2,0 ou une cyclodextrine ¨a, ¨13, ¨y hydroxylée
présentant un
degré de substitution moyen compris entre 0,5 et 0,9. Ladite cyclodextrine ¨a,
¨13, ¨y
méthylée peut présenter un degré de substitution moyen compris entre 1,6 et
2,0, ou
compris entre 0,9 et 1,6 ou compris entre 0,5 et 0,9. Lorsqu'une cyclodextrine
et un
ligand phosphoré hydrosoluble tel que mentionnée ci-dessus sont utilisés à
l'étape a),
de l'eau est également ajouté à cette même étape a) pour créer un milieu
biphasique
comprenant une phase organique et une phase aqueuse. Avant la mise en oeuvre
de
la réaction, la phase organique est notamment constituée du composé B selon la
présente invention et de l'amine. Dans ce mode de réalisation, le composé B
est de
formule (Via) selon la présente invention et l'amine est de formule HNR3R4
dans
laquelle R3 et R4 représentent indépendamment l'un de l'autre alkyle en 04-
010, aryle
en 06-012, cycloalkyle en 03-010, de préférence R3 et R4 représentent
indépendamment
l'un de l'autre alkyle en 04-010. Lorsque le procédé est réalisé en présence
d'une
cyclodextrine, le précatalyseur comprenant au moins un ligand phosphoré
monodentate ou bidentate hydrosoluble telle que défini ci-dessus. En outre, le
procédé
est alors réalisé dans des conditions opératoires permettant l'établissement
d'une
émulsion lors de l'agitation et une décantation des produits de la réaction
après arrêt
de l'agitation, de préférence la décantation d'au moins une partie du composé
selon la
présente invention. Avantageusement, la proportion de cyclodextrine est
comprise
entre 15 et 40% en poids sur base du poids total d'eau, de cyclodextrine et de
composé B de formule (V') ou (Via) ou (Vlb) ou (\Ac) mis en présence à l'étape
a).
Alternativement, selon un mode de réalisation particulier, lorsque le
précatalyseur comprend un ligand phosphoré hydrosoluble, l'étape a) peut
également
mettre en présence un co-solvant de formule RPOH dans laquelle RP représente
un
alkyle en Cl-010, un aryle en 06-012 ou un cycloalkyle en 03-010;
avantageusement RP
représente un alkyle en 01-04, de préférence le co-solvant est l'isopropanol.
Le co-
solvant peut remplacer la cyclodextrine. Optionnellement un tensioactif neutre
comprenant un groupe polaire hydroxylé peut également être ajouté.
Le procédé selon la présente invention peut également comprendre une étape
de recyclage lorsque le procédé est effectué en milieu biphasique. L'étape de
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
recyclage comprend le dégazage du réacteur dans lequel le procédé selon la
présente
invention est effectué, le prélèvement de la phase organique sous atmosphère
contrôlée, et l'ajout dans le réacteur dudit composé B et de l'amine et
optionnellement
d'un ou plusieurs ligands tels que décrits ci-dessus. Lors de cette étape de
recyclage,
5 la température reste constante, c'est-à-dire reste à la température à
laquelle la réaction
d'hydroaminométhylation et d'hydrohydroxyméthylation ont été effectuées.
Exemples
10 Détermination de la sélectivité en amine ou en alcool
La caractérisation des produits de réaction avant purification a été réalisée
en
résonance magnétique nucléaire (RMN) dans le chloroforme deutéré (CDCI3). Les
analyses RMN sont effectuées sur un appareil BRUKER 300 MHz. Les sélectivités
en
aldéhydes, amines, alcools et C=C hydrogénées supportées par les produits
issus de
15 la réaction sont déterminées par intégration des signaux RMN 1H. Une
caractérisation
des produits de réaction a également été effectuée en spectrométrie de masse
par
ionisation laser assisté par matrice (MALDI). La spectrométrie de masse est
effectuée
à partir d'un échantillon préparé dans une matrice d'acide 2-
5,dihydroxybenzoïque
(DHB).
20 La structure des produits de réaction a été confirmée par trans-
estérification de
ceux-ci puis analyse des produits de trans-estérification par RMN 1H. La trans-
estérification a été réalisée en présence de méthanol afin d'obtenir les
esters
méthyliques correspondant pouvant être séparés par chromatographie liquide sur
silice
avec par exemple un gradient heptane/acétate d'éthyle.
Exemple 1
Dans un réacteur, 1 mL de trioléine (1 mmol), 5 mL de toluène, 3,9 mg de
Rh(C0)2(acac) (0,015 mmol), 530 pL de dibutylamine (3,3 mmol) sont ajoutés. La
réaction est effectuée sous une pression de 80 bars de monoxyde de carbone et
d'hydrogène (rapport molaire 1:1) pendant 18 heures.
Le tableau 1 ci-dessous reporte les résultats obtenus à différentes
températures. Les produits obtenus comprennent en moyenne deux fonctions amine
et
une fonction alcool lorsque la température de réaction est de 80 C ou 100 C
(exemple
la et lb). La figure 2 représente un spectre RMN 1H du produit obtenu et la
formule
de celui-ci. Le pic noté 1 sur le spectre RMN de la figure 2 correspond à
l'atome
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
21
d'hydrogène porté par l'atome de carbone noté 1 du motif glycérol. Le pic noté
2 sur le
spectre RMN de la figure 2 correspond aux atomes d'hydrogène porté par les
atomes
de carbone noté 2 du motif glycérol. Le pic noté 3 sur le spectre RMN de la
figure 2
correspond aux atomes d'hydrogène porté par l'atome de carbone noté 3. Le pic
noté 4
sur le spectre RMN de la figure 2 correspond aux atomes d'hydrogène porté par
les
atomes de carbone noté 4. La sélectivité de la réaction est orientée vers la
formation
préférentielle de fonction alcool lorsque la température est de 50 C (exemple
1c).
Tableau 1 ¨ Performances catalytiques en fonction de la température
Ex. T ( C) Conversiona Sélec.b Sélec.b Sélecb Sélec.b
Rapport
(%) Aldéhyde Alcool Amine Hydrogén alcool /
ation aminec
la 80 100 0 28 68 4 0,41
lb 100 100 0 20 79 1 0,25
lc 50 76 0 55 44 1 1,25
a (nombre de moles de C=C du triglycéride converties divisé par le nombre
total de moles de
C=C du triglycéride) x 100. b (nombre de mole d'une fonction donnée divisé par
le nombre de
mole de C=C converties) x 100. c proportion de fonctions alcool par rapport
aux fonctions amine
dans le triglycéride aminohydroxylé.
L'exemple 1 démontre que la température permet de privilégier facilement soit
une
réaction d'hydroaminométhylation soit une réaction d'hydrohydroxyméthylation.
Exemple 2
L'exemple 1 a été reproduit pour une température de 80 C en faisant varier
l'amine et la concentration de celle-ci. Le tableau 2 reprend les résultats
obtenus.
Tableau 2 ¨ Performances catalytiques en fonction de la nature et la
concentration de
l'amine
Ex Amine Conversiona Sélec.b Sélec.b Sélecb Sélec.b Rapport
(%) Aldéhyde Alcool Amine Hydrog alcool/
=
énation aminec
2a H N(Et)2d 100 0 27 65 8 0,41
2b H2N(Hex)e 100 0 33 60 7 0,55
2c H N(Et)2f 100 0 51 46 3 1,1
2d H N(Et)2g 100 0 79 19 2 4,16
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
22
a (nombre de moles de C=C du triglycéride converties divisé par le nombre
total de moles de
C=C du triglycéride) x 100. b (nombre de mole d'une fonction donnée divisé par
le nombre de
mole de C=C converties) x 100. c proportion de fonctions alcool par rapport
aux fonctions amine
dans le triglycéride aminohydroxylé. d diéthylamine (3,3 mmol) ; e hexylamine
(3,3 mmol) ; f
diéthylamine (2 mmol) ; g diéthylamine (1 mmol) ;
Les résultats repris dans le tableau 2 montrent une influence de la
concentration de l'amine sur la sélectivité du produit final. Ainsi, en défaut
d'amine
dans le milieu réactionnel, la formation de groupement alcool par une réaction
d'hydrohydroxyméthylation est favorisée. Dans des conditions stoechiométriques
entre
l'amine et la trioléine, la formation d'un composé comprenant plus de
fonctions amine
que de fonctions alcool est favorisée.
Exemple 3
Dans un réacteur, 1 mL de trioléine (1 mmol), 5 mL de toluène, 3,9 mg de
Rh(C0)2(acac) (0,015 mmol), 530 pL de dibutylamine (3,3 mmol) sont mélangés.
Une
phosphine est également ajoutée au milieu réactionnel dans des proportions de
l'ordre
de un équivalent ou 5 équivalents par rapport au précatalyseur. La réaction
est
effectuée sous une pression de 80 bars de monoxyde de carbone et d'hydrogène
(rapport molaire 1:1) pendant 18 heures à une température de 80 C. L'exemple
3d met
en oeuvre une phosphine hydrosoluble et dans ce cas le toluène est substitué
par un
mélange constitué de 5 mL d'eau et 2 mL d'isopropanol. L'exemple 3e met en
oeuvre
une phosphine hydrosoluble ainsi qu'une cyclodextrine modifiée. Le tableau 3
ci-
dessous montre les résultats obtenus.
Tableau 3 - Performances catalytiques en fonction de la nature et la
concentration de
la phosphine
Sélec. Sélec Sélec.b Rapport
Conversiona Sélec.b
Ex. Phosphine
(%) Aldéhyde Hydrog alcool/
Alcool Amine énation aminec
3a o(Me)3TPP 100 0 27 74 1 0,36
3b o(Me)3TPP 100 0 31 68 1 0,46
3c o(OMe)3TPP 100 0 22 77 1 0,29
3d o(Me)3TPPTS 63 9 57
29 5 1,96
TPPTS + 3,62
3e 88 1 76 21 2
CRYSMEB
CA 02970218 2017-06-08
WO 2016/128390
PCT/EP2016/052712
23
a (nombre de moles de C=C du triglycéride converties divisé par le nombre
total de moles de
C=C du triglycéride) x 100. b (nombre de mole d'une fonction donnée divisé par
le nombre de
mole de C=C converties) x 100. c proportion de fonctions alcool par rapport
aux fonctions amine
dans le triglycéride aminohydroxylé. 3a ¨ o(Me)3TPP : Tri(ortho-tolyle)
phosphine 0.015 mmol;
3b - o(Me)3TPP : Tri(ortho-tolyle) phosphine 0.075 mmol; 3c - o(OMe)3TPP :
Tri(ortho-
methoxyphenyl) phosphine 0.015 mmol; 3d ¨ P(2-(Me)-4-(SO3Na)-Ph)30.075 mmol;
3e ¨ P(3-
SO3Na-Ph)3 (sel trisodique de la tripénylphosphine tri sulfonée en position
meta) 0.075 mmol +
2,3 g de Crysmeb (cyclodextrine partiellement méthylée sur les hydroxyles 2
avec une degré
de substitution moyen par unité glucopyranose de 0,8)
De très bons résultats sont obtenus lorsqu'une phosphine est ajoutée comme
ligand du précatalyseur. La réaction d'hydroaminométhylation est favorisée en
milieu
homogène et en présence d'une phosphine ortho-encombrée (Exemples 3a-3c). La
conversion et la sélectivité de la réaction sont maintenues même en présence
d'un
excès de phosphine par rapport au précatalyseur (exemple 3b). L'exemple 3d
mettant
en oeuvre une phosphine hydrosoluble dans un milieu biphasique tend à
favoriser la
formation d'un produit comprenant plus de fonctions alcool que de fonctions
amine.
Ceci est d'autant plus favorisé lorsque qu'une cyclodextrine méthylée
présentant un
degré de substitution de 0,8 est ajouté (exemple 3e).
Exemple 4
Dans un réacteur, 1 mL de trioléine (1 mmol), 5 mL de toluène, 3,9 mg de
Rh(C0)2(acac) (0,015 mmol), 530 pL de dibutylamine (3,3 mmol) sont ajoutés. La
réaction est effectuée sous une pression de 80 bars de monoxyde de carbone et
d'hydrogène pendant 6 heures.
Les expériences ci-dessous exemplifient l'utilisation de différents rapports
molaires du gaz de synthèse CO/H2 utilisé dans cette réaction. La variation de
ce
rapport est faite par introduction dans l'autoclave de pressions partielles
des différents
gaz CO et H2 de façon successive. Le mélange de gaz possède donc une
stoechiométrie égale au rapport des différentes pressions partielles.
Tableau 4. Influence du rapport CO/H2 sur la réaction de synthèse d'amino
alcool.[a]
Ex. Pression Pression Rapport Conv. Selec Selec Selec. Selec.
partielle partielle CO/H2 (`)/0) Aldéhyde Alcool Amine Hydrogé-
CO H2 (%) (%) (%)
nation
(bars) (bars) (%)
4a 40 40 1 95 0 25 72 3
4b 26 54 0.5 94 0 44 55 1
[al Conditions : 1mL de trioléine (1 mmol, 3 mmol de doubles liaisons) ;
toluène : 5 ml;
Rh(C0)2(acac) : 3.9 mg, (0.015 mmol) ; amine : NH(Bu)2 : 530 pL (3.3 mmol), 80
C, pression
totale : 80 bars, 6 h.
CA 02970218 2017-06-08
WO 2016/128390 PCT/EP2016/052712
24
Ces résultats montrent que le rapport molaire CO/H2 peut orienter la réaction
vers la formation préférentielle de fonctions alcool ou de fonctions amine. En
effet,
l'augmentation de la pression partielle de H2 dans le milieu augmente la
proportion en
alcool au détriment de la formation d'amine tertiaire.
Le procédé selon la présente invention permet donc la préparation sélective
des composés aminoalcool gras tels que décrit dans la présente demande.
Les termes et descriptions utilisés ici sont proposés à titre d'illustration
seulement et ne constituent pas des limitations. L'homme du métier reconnaîtra
que de
nombreuses variations sont possibles dans l'esprit et la portée de l'invention
telle que
décrite dans les revendications qui suivent et leurs équivalents ; dans celles-
ci, tous les
termes doivent être compris dans leur acception la plus large à moins que cela
ne soit
indiqué autrement.