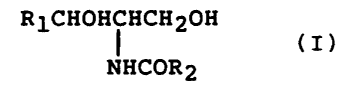Note: Descriptions are shown in the official language in which they were submitted.
CA 02061692 2002-09-11
La présente invention a pour objet de nouveaux céramides, leur
procédé de préparation ainsi que leur utilisation, notamment pour les
traitements et les soins de la peau et des cheveux en cosmétique ou en
dermopharmacie.
s L'exposition de la peau au froid, au soleil, aux atmosphères à faible
humidité relative, les traitements répétés avec des compositions de lavage ou
encore le contact avec des solvants organiques, sont des facteurs qui
entraînent, â des degrés divers, un dessëchement apparent. La peau apparaît
plus sèche, moins souple et le relief cutané plus prononcé. Par ailleurs, les
io cheveux, qui sont soumis trop fréquemment à certains traïternents
capillaires, perdent leur aspect brillant et peuvent devenir rèches et
cassants.
La Demanderesse a donc recherché des composés qui permettent de
prévenir ou de corriger ces phénomènes se traduisant par un dessèchement
apparent et qui redonnent â la peau sa souplesse et aux cheveux leur
i5 brillance et leur douceur.
Pour résoudre ce problème, on a déjà proposé d'utiliser des
céramides. On sait en effet que ces composés sont les éléments constitutifs
prépondérants des lipides intercornéocytaires du stratum cornéum et
participent au maintien de l'intégrité de la barrïère cutanée. Ils
représentent,
2o selon DOWNING ("The Journal of Investigative Dermatology", Vol. 88,
N°
3, p. 2s-6s, 1987), environ 40% de la totalité de ces lipides.
Les céramides utilisés en cosmétique sont des extraits naturels issus
notamment de la peau de porc, du cerveau de boeuf, de l'oeuf, des cellules
du sang, des plantes etc.. (demandes de brevet ,japonais Nos. 61/260008 et
CA 02061692 2002-09-11
62/120308). De tels céramides ont également été proposés pour la protection
des cheveux {brevet européen No. 278 S0>).
II s'agit donc toujours de mélanges de teneur plus ou moins
importante en céramides et dont la composition est difficile à contrôler.
s De plus, ces mélanges sont ~;ujets à la contamination bactérienne. Leur
conservation est très diff cile à maîtriser. Lorsqu'ils sont d'origine
animale, il y a en plus un risque de contarninatïon par l'agent responsable
de la BSE (encéphalopathie bovine spongiforme).
Pour résoudre ces problèmes, la I~)emandere sse s'est donc tournée
io vers les céramides de s~mthèse.
C'est ainsï que la Demanderesse a découvert de nouveaux
composés dont la constitution peut être représentée par la formule
survante:
R1CHOH;HCH20H (I)
NHCOR2
i5 dans laquelle:
R, désigne un radical alcoyle ou alcényle en C, ~-C21, et
préférablement un radical en C~5 dérivé de sphinginosine ou de
dihydrosphinginosine.
R2 désigne un radical hydrocarboné en C.'ll-C~<~, linéaire et portant
ao une ou plusieurs insaturations éthyléniques et notamment une ou deux, ou
un mélange de composés de formule (;l) et de formule (la):
RzCHOHCHCH20H
(la)
NHCOR2
dans laquelle:
- 2 -
CA 02061692 2002-09-11
R, est tel que défini précédemment et R2 est un radical hydrocarboné
linéaire saturé en C"-C',<~, la proportion de composés. de formule (Ia) dans
le
mélange n'excédant pas 35%.
s Ces composés étant sous forme de mélange racémique des
diastéréoisomères érythro et thréo dans les proportions étythroahréo de
85:15 à 60:40.
Les composés de formule (I) selon 1 'invention, qui sont des cires
de bas point de fusion, présentent donc un
- 2a -
zo~~~~~
intérét tout particulier pour les traitements et les soins de
la peau et des cheveux en cosmétique ou en dermopharmacie en
permettant de prévenir ou de corriger certains effets du
dessëchement apparent.
Ces camposés présentent par ailleurs une faible
agressivité vis-â-vis de la peau ou des muqueuses oculaires
et une bonne tolérance vis-â-vis des membranes cellulaires
comme celles des êrythrocytes.
Les nouveaux composés de formule (I) ci-dessus
présentent des propriétés émollientes et adoucissantes. I1
sont facilement solubilisés dans, les phases grasses des
préparations cosmétiques ou dermopharmaceutiques.
Lss poils traités par ces composés présentent un
aspect brillant et une moïns grande sensibilité â l'eau, due
â l'apport de matiëre lipidique uniformément répartie sur les
écailles du poila Les propriétés mécaniques et de nervosité
sont également améliorées.
Ces composés forment, en association avec d'autres
lipides, des vésicules.
La présente invention a ainsi pour objet les
nouveaux céramides de formule (I) définis ci-dessus, sous
forme de mélange racémique des diastëréoisomères ërythro et
thrêo dans les proportions de 85:15 â 60:40.
Les céramides de formule (I) ci-dessus résultent de
l'acylation de la fonction amine d'une sphingosine ou d'une
dihydrosphingosine par un acide activé de formule RzCOA où R2
a la signification indiquée ci-dessus et A peut prendre
notamment les significations suivantes:
CA 02061692 2002-09-11
-C1,-OCOC2H5,-O Q NOZ,-O-N ,
0
o
H- ~=N , -OC;H3, -OC2H5,
0
-N , -N etc . .
'.r. N N
Dans la présente demande, on entendra par sphingosine ou
dihydrosphingosine les composés D, L:, c'est-à-dire les mélanges
racémiques des diastéréoisomères érythro et thréo.
s Un autre objet de la présente invention est donc constitué par le
procédé de préparation des composés de formule (I) qui peut être
représenté par le schéma suivant:
R1CHOHCHCH20H--~1 R~CHOH¿HCH20H
NH2 NH~R2
0
(II) CI)
R, et R2 ayant les signïfications indïquées ci-dessus.
1o Les composés de formule (I) sont obtenus conformément à
l'invention par acylation des composés de formule (II) soit avec un
chlorure d'acide, soit par un anhydride, soit par un ester de
paranitrophénol, soit par un ester de succinimide., soit par un ester de
dicyclohexylcarbodümide, soit par un ester d'alkyle en C~-C~, soit par un
i5 azolide et notamment un imidazolide ou un pyrazolide.
- 4 -
CA 02061692 2002-09-11
De préférence, on utilise à titre d'ester d'alkyle en C1-C6 un ester de
méthyle ou d'éthyle.
Les réactions d'acylation avec un ester d'alkyle en C1-C6 se font à
l'état anhydre. Elles sont notamment clécrïtes par E. F. JORDAN dans
JAOCS p. 600-605 ( 1961 ).
Les autres réactions sont effectuées dans des solvants tels que le
tétrahydrofuranne, la pyridine, le diméthylformamide, le dichlorométhane
etc...
L'acylation par un ester de succinimide et de
dicyclohexylcarbodümide est décrite notamment par LAPIDOT dans J.
Lipid Res. 8, 142-145 ( 1967).
L'acylation par un ester de paranitrophénol est décrite notamment
par BODANSI~Y dans Nature N° 4459, p. 685 (1955).
L'acylation par un anhydride mixte est décrite par J. L. TORRES
dans Tetrahedron Vol. 43, N° l 7, p. 4031-:3 ( 1 x)87).
Les acylations avec les azolides sont décrites par H. A. STAAB dans
Angew, Chem. Internat. Edit. Vol. l, N° 7. p. 357-367 (1962).
Les réactions d'acylation sont décrites en général par J. MARCH
dans Advanced Organic Chemïstry-Third Edition - JOHN WII,EY &
SONS-INC p. 370-377 ( 1985).
Pour la préparation du composé do formule (I) de l'invention, on
peut également utiliser le chlorhydrate du composé de formule (II).
Les composés de formule (II) SOIR des composés connus. Leur
synthèse a été décrite en particulier par D. SHAPIRO dans "Chemistry of
Sphingolipids", HERMANN, Paris ( 1969).
_ 5 _
CA 02061692 2002-09-11
Quand Rl désigne un radical alcényle, les composés de formule (II)
sont des sphïngosines dont la synthése est décrite ~ la page 21 de
"Chemistry of Sphingolipîds".
-Sa-
Z~~~~
Quand Rl désigne un radical alcoyle, les composés
de formule (II) sont des dihydrosphingosines. Elles peuvent
être préparées en particulier à partir de 2-acétamido-3-oxo-
alcanoa-te de méthyle ou d'êthyle, comme dêcrit dans
'°Chemistry or Sphingolipids", page 32.
Les procédés de synthése des sphingosines ou
dihydro-sphingosines décrits ci-dessus conduisent à des
mélanges racêmiques des dias~téréoisomères êrythro et thréo
dans les proportions érythro-thréo de 85:15 à 60:40.
Les composés selon l'invention peuvent recevoir des
applications dïverses, notamment en tant que constituants
cireux dans des compositions cosmétiques et dermopharma-
ceutiques. Ces composês possèdent en plus 1a propriêté de
former des vésicules en association avec d'autres lipides,
lorsqu'ils sont dispersés dans l'eau.
La présente invention a donc pour objet
l'utilisation des composés lipidiques de formule (I) en tant
que constituants cireux dans des émulsions, des. dispersions
ou dans des lotïons. Elle a également pour objet l'utili--
20 cation de ces composés, associés à d'autres lipides, pour la
formation de sphérules lipidiques.
La prêsente invention a également poux objet des
compositions à usage cosmétique ou dermopharmaceutique
contenant un composé de formule (I).
ün autre objet de l'invention est constitué par un
procêdé de traitement cosmêtique de la peau, des cheveux ou
des poils consistant à appliquer sur ces derniers une
quantité suffisante d'une telle composition contenant un
composé de formule (I).
30 Les compositions à usage cosmétique ou
dermopharmaceutïque, conformes à l'invention, sont essentiel-
- 6 -
lement caractérisées par le fait qu°elles contiennent dans un
milieu cosmétiquement ou pharmaceutiquement acceptable au
moins un composé de formule (I).
Les compositions selon l'invention peuvent se '
présenter sous forme d'émulsions (lait ou crème), de lotions
hydroalcooliques, huileuses ou oléoalcooliques, de gels, de
dispersions ou de bâtonnets solides, de sprays ou de mousses
aérosol.
Les composës de formule (T) représentent de
prêférence 0,05 â 20~, et en.particulier 0,1 à 10~ du poids
total de la composition.
Les compositions sont par exemple des lotions, des
laits ou des crèmes émollients, des laits ou des crëmes pour
les soins de la peau ou des cheveux, dés crêmes, des lotions
ou des laits démaquillants, des bases de fond de teint, des
lotions,, des laits ou des crèmes antisolaires, des lotions,
des laits ou des crèmes de bronzage artificiel, des crèmes ou
des mousses de rasage, des logions après rasage, des
shampooings ou des mascaras.
Ces compositions peuvent également se présenter
sous la forme de bâtons pour les lèvres destinés soit â les
colorer, soit à éviter les gerçures, ou de produits de
maquillage pour les yeux ou de fards et fonds de teint pour
1e visage.
Lorsque les compositions selon l'invention se
présentent sous forme d°émulsions du type eau-dans-huile ou
huile-dans-l'eau, la phase grasse est essentiellement
constituée d'un mélange de composé de formule (I) avec au
moins une huile, et éventuellement un autre corps gras. La
phase grasse des émulsions peut constituer 5 à 60 ô du poids
total de l'émulsion. La phase aqueuse de ces émulsions
Z~~~~~
constitue de préférence 30 à 85~ du poids total de
l'émulsion. La proportion de l'agent émulsionnant est
comprise de préférence entre 1 et 2.0ô, et en particulier
entre 2 et 12~ du poids total de l'émulsion.
Lorsque les compositions selon l'invention se
prêsentent sous forme de lotions huileuses, olëoalcooliques
ou hydroalcooliques, elles peuvent constituer, par exemple,
des lotions antisolaires contenant un filtre absorbant les
rayons UV, des lotions adoucissantes pour la peau; les
lotions huileuses peuvent en outre constituer des huiles
moussantes contenant un tensio-actif oléosoluble, des huiles
pour 1e bain, etc.
Parmi ies principaux adjuvants pouvant être
prêsents dans les compositions selon l'invention, on peut
citer les corps gras tels que les huiles ou les cires
minérales, animales ou végétales, les acides gras, les esters
d'acides gras tels que les triglycérides d'acides gras ayant
de 6 à 18 atomes de carbone, les alcools gras; les
émulsionnants comme les alcools gras oxyéthylënés ou les
alcoylëthers de polyglycérol; les solvants tels que les
monoalcools ou polyalcools inférieurs contenant de 1 à 6
atomes de carbone nu encore l'eau.
Les mono- ou polyalcools plus particulièrement
prëfêrês sont choisis parmi l'éthanol, l'isopropanol, le
propylëneglycol, le glycérol et le sorbitol.
A titre de corps gras, parmi les huiles minérales,
on peut citer l'huile de vaseline; parmi les huiles animales,
les huiles de baleine, de phoque, de menhaden, de foie de
flétan, de morue, de thon, de tortue, de pied de boeuf, de
pied de cheval, de pied de mouton, de.vison, de loutre, de
marmotte, etc.; parmi les huiles végétales, les huiles
_ g _
2~~~.~~~
d'amande, de germe de blé, d'olive, de germe de maïs, de
jojoba, de sésame, de tournesol, de palme, de no~.x, de
karité, de shoréa, de macadamia, de pépins de cassis et
similaires.
Parmi les esters d'acides gras, on peut utiliser
des esters d'acides en C12 à C22 saturés ou insaturés et
d'alcools inférieurs comme l'isopropanol ou le glycêrol ou
d'alcools gras en Cg à C22, linéaires ou ramifiés, saturês ou
insaturés ou encore d'alcanediols°1,2 en Clp-C22.
On peut également citer comme corps gras, la
vase7.ine, 1a paraffine, la lanoline, la lanoline hydrogénée,
le suif, la lanoline acétylée, les huiles de silicone.
Parmi les cires, on peut citer 1a cire de Sipol, la
cire de lanoline, la cire d°abeille, la cire de Candelila, la
cire rnicrocristalline, la cire de Carnauba, le spermaceti, le
beurre de cacao, le beurre de karité, les cires de silicone,
les huiles hydrogénêes concrêtes à 25°C, les sucroglycérides,
les oléates, myristates, linoléates et stéarates de Ca, Mg et
Al.
Parmi les alcools gras, on peut citer les alcools
laurique, cétylique, myristique, stéarique, palmitique,
olêique et les alcools de GüERBET comme le 2-octyldodêcanol,
le 2°dêcyltêtradêcanol ou le 2-hexyldécanol.
A titre d'émulsionnants, parmi les alcools gras
polyoxyéthylénés, on peut citer les alcools laurique,
cétyl:ique, stéarylique et oléique comportant de 2 à 20 moles
d'oxyde d'éthylène et parmi les alcoyléthers de polyglycérol,
les alcools en C12°Clg comportant de 2 à 10 moles de
glycérol.
Il peut aussi être utile d'utiliser des
épaississants tels que les dérivés de cellulose, .Les dérivés
- 0
d'acide polyacrylique, les gommes de guar ou de caroube ou 1a
gomme de xanthane.
La composition selon l'inve.ntion peut également
contenir des adjuvants habituellement utilisês en cosmétique
ou en dermopharmacie et notamment des produits hydratants,
des adoucissants, des produits pour le traitement
d'affections cutanées, des filtres solaires, des germicides,
des colorants, des conservateurs, des parfums et des
propu7.seurs .
Lorsque les compositions selon l'invention sont des
dispersions, il peut s'agir de dispersions de composés de
formule (T) dans l'eau en présence de tensio-actif ou encore
de dispersions aqueuses de sphérules lipidiques, constituêes
de couches moléculaires organisées enfermant. une phase
aqueuse encapsulée, ces couches étant constituées d'au moins
un composé de formule (I), associé â au moins un autre
composé lipidïque.
an peut citer, â cet effet, comme composés
lipidiques, les alcools et diols â longue chaîne, les stérols
tels que le cholestérol, les phosphalipides, les cholestéryl
sulfate et phosphate, les amines â longue chaîne et leurs
dérivés d'ammonium quaternaire, les dihydroxyalkylamines, les
amines grasses polyoxyëthylënêes, les esters d'aminoalcools â
longue chaîne, leurs sels et dérivés d'ammonium quaternaire,
les esters phosphoriques d'alcools gras tels que 1e
dicétylphosphate acide ou son sel de sodium, les
alkylsulfates tels que le cétylsulfate de sodium, les acides
gras sous forme de sels ou encore les lipides du type de ceux
décrits dans les brevets français Nos 2.315.991, 1.477.048 et
~0 2.091.516 ou dans la demande de brevet international N° WO
83/01 571.
- 10 -
2~~.~~>
On peut par exemple u-til~.ser comme autres lipides,
des lipides comportant une chaîne lipophile longue contenant
12 à 30 atomes de carbone, saturée ou insaturée, ramifiée ou
linéaire, par exemple une chaîne olëique, lanolique,
tétradécylique, hexadécylique, isostéarylique, laurique ou
alcoylphénylique. Le groupement hydrophile de ces lipides
peut âtre un groupement ionique ou non-ionique. A titre de
groupements non-ioniques, on peut citer des groupements
dérivés de polyéthylèneglycol. On peut aussi utiliser
avantageusement comme lipides formant la phase lamellaire,
des éthers de polyglycérol tels que ceux décrits dans les
brevets français Nos 1.477.048, 2.091.516, 2.465.780 et
2.482.128.
A titre de groupement ionique, on peut avanta-
geusement utiliser un groupement dérivé d'un composé
amphotëre, anionique ou cationique.
D' autres lipides décrits clans la demande de brevet
internatïonal N° W0 83/01 571 comme pouvant être utilisés
pour la formation de vésicules sont les glycolipides comme le
lactosylcêramide, le galactocérébroside, les gangliosides et
1e trihexosylcéramide, ainsi que les phospholipides tels que
le phosphatidylglycérol et le phosphatidylinositol.
La présente invention a donc également pour objet
une dispersion de sphérules lipidiques constituées de couches
moléculaires organisées de cornposê(s) de fo-rmule (I) et de
lipide défini ci-dessus renfermant une phase aqueuse à
encapsuler.
La phase continue de 1a dispersion qui entoure les
sphérules est une phase aqueuse.
Les sphérules en dispersion ont un diamëtre compris
de préférence entre 0,05 ~m et 5 gym.
- 11 _
La phase aqueuse encapsulée dans les sphérules peut
être de l'eau ou une solution aqueuse de substance active et
est dans' ce cas de préférence isoosmotique par rapport à la
phase continue de la dispersion.
Les sphërules peuvent étre obtenues en particulier
suivant le procédé décrit dans le brevet français N 2.315.991
de la Demanderesse, selon lequel on prépare une dispersion de
sphérules constituées de couches moléculaires organisées
renfermant une phase aqueuse à encapsuler, en mettant en
contact, d'une part au moins un composé lipidique de formule.
(I) associé à au moins un lipide défïni ci-dessus, et d°autre
part la phase aqueuse à encapsuler dans les sphêrules, en
agitant pour assurer le mélange et obtenir une phase
lamellaire, en ajoutant ensuite un liquide de dispersion en
quantïté supérieure à la quantité de phase lamellaire obtenue
et en secouant énergiquement pendant une durée allant de 15
minutes â 3 heures environ.
Le rapport pondéral entre la phase aqueuse à
encapsuler et le composé de formule (I) associé aux lipides
formant la phase lamellaire, est de préférence comprîs entre
0,1 et 20.
Le rapport pondéral de la phase aqueuse de
dispersion que l'on ajoute ~. la phase lamellaire que l'on
disperse, est de préférence compris entre 2 et 100, la phase
de dispersion et la phase aqueuse â encapsuler étant de
préférence isoosmotiques.
L' agitation est réalisée au moyen d' un agitateur à
secousses. Le procédé est de préférence mis en oeuvre â une
température comprise entre 30° et 120°C.
Un autre procédé de préparation peut consister à
utiliser le procédé dénommé REV (reverse-phase evaporation
- 12 -
~~~1~~
vesicle) ou évaporation en phase inverse décrit dans Proc.
Natl. Acad. Sci. USA., Vol. 75, N° 9, pages 4194-4198 (1978),
par SZOKA et PAPAHADJOPOULOS.
On peut également mettre en oeuvre le procédé qui
comprend. 1a succession d'étapes consistant à dissoudre au
moins un lipide dans au moïns un solvant organique non
miscible à l'eau; ajouter la phase organique ainsi obtenue à
une phase aqueuse; former une dispersion des deux phases sous
forte agitation, la taille des vésicules pouvant être réglée
en faisant varier la vitesse d'agitation au cours de ce
mélange des phases; conduire l'évaporation du (ou des)
solvants) sous forte agitation; et, le cas échéant,
concentrer 1a dispersion.
Les substances actives peuvent être des substances
ayant un intérêt pharmaceutique, alimentaire ou des
substances ayant une activité cosmétique. Lorsqu'elles sont
hydrosolubles, elles sont dans la phase aqueuse encapsulée â
l'intérieur des vésicules.
Les substances hydrosolubles ayant une activité
cosmétique et/ou pharmaceutique peuvent être des produits
destinés aux soins ou aux traitements de la peau et du cheveu
tels que par exemple des humectants comme la glycérine, le
sorbitol, le pentaêrythritol, l'acide pyrrolidone carboxy
lique et ses sels; des agewts de brunissage artificiel tels
que la di.hydroxyacêtone, l'êrythrulose, le glycêraldéhyde,
les y-dialdéhydes tels que l'aldéhyde tartrique, ces composés
étant éventuellement associés â des colorants; des filtres
solaires hydrosolubles; des antiperspirants, des déodorants,
des astringents, des produits rafraîchissants, toniques,
cicatrisants, )cératolytiques, dépilatoires, des eaux
parfumées; des extraits de tissus végétaux, tels que les
- 13 -
polysaccharides: des colorants hydrosolubles; des agents
antipelliculaires: des agents antiséborrhéiques, des oxydants
tels que des agents de décoloration comme l'eau oxygénée, des
réducteurs tels que l'acide thioglycolique et ses sels.
On peut citer êgalement les vitamines, les
hormones, les enzymes telles que la superoxyde dismutase, les
vaccins, les anti-inflammatoires tels que l'hydrocortisone,
les antibiotiques, les bactéricides, les agents cytotoxiques
ou anti-tumoraux.
Lorsque les substances act9_ves sont liposolubles,
elles se trouvent incorporées dans les feuillets des
vésicules. Elles peuvent être choisies dans le groupe formé
par les filtres solaires liposolubles, les substances
destinées à améliorer l'êtat des peaux rêches ou séniles, les
tocophérols, les vitamines E, E' ou A et leurs esters, l'acide
rétinoïque, les antioxydants, les acides gras essentiels,
l'acide glycyrrhêtinique, les l~cératolytiques et les
caroténoïdes.
On peut également ajouter à la phase aqueuse des
dispersions de sphérules selon 1°invention une phase liquide
L non miscible à l'eau. En particulïer, la composition selon
l'invention peut contenir de 2 à 70~ en poids de phase
liquide L, non miscible â l'eau, par rapport au poids total
de 1a composition, la proportion pondérale relative de(s)
lipides) constitutifs) de vésicules par rapport à la phase
liquide dispersée L étant comprise de préférence entre 0,02/1
et 10/1,
Le(s) constituants) de la phase liquide L
dispersée dans la phase aqueuse D, peut (peuvent) être
choisis) dans le groupe formé par les huiles, telles que les
esters d'acides gras et de polyols, et les esters d'acides
_ 14
gras et d'alcools ramifiés de formule R3-COOR~, formule dans
laquel~.e R3 représente le reste d'un acide gras supérieur
comportant de 7 à 19 atomes de carbone et Rg représente une
chaîne hydrocarbonée ramifiée contenant de 3 à 20 atomes de
carbone; les hydrocarbures, tels que l'hexadécane, l'huile de
paraffine, le perhydrosqualène; les hydrocarbures halogénés,
tels que le perfluorodécahydronaphtalène; la perfluoro-
tributylamine; les polysiloxanes; les esters d'acides
organiques, les éthers et polyéthers. La phase liquide L peut
.renfermer au moins un parfum et/ou au moins une substance
active liposoluble. De telles substances liposolubles peuvent
être constituées par les filtres solaires liposolubles, les
substances destinées à améliorer l'état des peaux séches ou
séniles, les tocophérols, les vitamines E ou F, la vitamine A
et ses esters, l'acide rétir~oïque, les antioxydants, les
acides gras essentiels, l'acide glycyrrhétinique, les agents
lcératolytiques et les carotênoïdes.
On peut également ajouter aux dispersions de
sphérules selon l'invention divers adjuvants tels que des
opacifiants, des gélifiants, des arômes, des parfums ou des
colorants.
Les dispersions de sphérules lipidiques selon
l'invention présentent l'intérêt de véhiculer des substances
actives qui se trouvent ainsi masquées et protégées vis-à-vis
des différents agents d'altération: oxydants et plus
généralement composés réactifs vis-à-vis des substances
actives encapsulêes. La pénêtration et la fixation des
substances actives peuvent être modulées par la variation de
la taille des sphérules et de leur charge électrique.
L'action de ces substances actives peut également être ainsi
différée (effet retard). Enfin, il est possible d'obtenir
- 15 -
ZQ~~
grâce à l'utilisation des lipides de formules (I) selon
l'ïnvention, et de substances actives combinées, une action
bénéfique spécifique de la substance active utilisée et en
même temps assouplissante, particulièrement intéressante dans
le cas du traitement de la peau.
La présente invention a donc également pour objet
l'utilisation en cosmétique d'une dispersion aqueuse de
sphérules constituée de couches moléculaires organisées de
composés lipidiques de formule (I) associés à d'autres
lipides renfermant une phase aqueuse à encapsuler, en
particulier pour le traitement de la peau.
L'invention vise également l'utilisation d'une
telle dispersion de sphérules lipidiques en dermopharmacie au
dans l'industrie alimentaire.
La présente invention sera mieux illustrée par les
exemples non limitatifs suivants.
EXEM'PLF 1
Préparation du 2-oléovlamino-1 3-octadécanediol
lère étape
Préparation d'un composé de formule (II) avec:
R1 = C15H31%
chlorhydrate du 2-amino-1~3-octadécanediol (mélange êrythro-
thréo
Le 2-acétamido-3-oxo octadécanoate de méthyle (100
g, soit 0,27 M) est mis en suspension dans 1 litre d'éthanol
absolu. La température du milieu réactionnel est amenée en
dessous de 0°C. A cette température, on ajoute en trois fois
30,7 g (0,8 M) de borohydrure de sodium et on maintient
l'agitation à cette température pendant 3 heures. Le milieu
réactionnel est alors porté â reflux du solvant pendant 3
heures. Après refroidissement â la température ordinaire, on
- 16 -
ajoute 140 cm3 d'aride chlorhydrique concentré et on porte à
nouveau le milieu réactionnel à reflux pendant 3 heures. Ce
milieu est filtré encore chaud sur un verre fritté. Le
filtrat est concentré à sec sous pression réduite.
Le solide obtenu est recristallisé dans 300 cm3 de
mélange de solvant heptane: acétate d'êthyle - 90:10. On
isole 88 g d'un solide blanc dont l'indice d'acide mesuré
dans l'éthanol par une solution de soude N/1.0 est de 2,99
meq/g.
Le spectre RMN13C de ce solide est conforme à la
structure attendue:
CH3-CH2-CH2-(CH2)10-CH2CH2-!H-iH-CH20H
OH NH2,HC1
T1 s'agit bien du chlorhydrate de dihydro-
sphingosine sous forme de mélange racêmique D,L érythro-
thréo.
2ême êtape
Préparation du composé de formule (I L dans laauelle
--ÇOR2 = oléoyle
Matiëres Premiêres
- Chlorhydrate de dihydrosphingosine préparé
dans la premiére étape 100 g
- Chlorure d'oléoyle (1) 84,7 g
- Triéthylamine 60 g
- Tétrahydrofurane 400 ml
- Isoprôpanol 150 m1
- Résine AMBERLT'PE IRN 150 (marque de commerce) 160 g
- Acétate d'éthyle 600 ml
(1) Commercialisê par BASF avec un titre en chlorure d'acide
de 98%. La rêpartition des principales chaînes est la
suivante:
17 -
C14 . 4,5ô C18 1~ 65%
C16 . 8,5ô C18 '2= 4.8%
C18 . 3,4% Clg -3: 0,5%
Mode opératoire
Dans un réacteur sous azote, on introduit 400 ml de
~tétrahydrafurane et 100 g de chlorhydrate de dihydro-
sphingosine (0,296 mole) que l'on disperse par chauffage à
45°C; on ajoute alors 31 g de triéthylamine (0,307 mole), ce
qui provoque un trouble du milieu réactionnel et une
augmentation de la température à 48°C; le pH "apparent" est
alors de 8,3 t 0,1. On laisse revenir à 30°C 1 1°C.
Par une ampoule â introduction, on commence alors à
introduire le chlorure d'olêoyle jusqu'à amener le pH
'°apparent" jusqu' à 6, 7 et on le maintient à cette valeur en
ajoutant simultanément en 1 heure, 1e reste du chlorure
d'oléoyle et 29 g de triéthylamine (0,287 mole); au caurs de
ces additions, la température s'élève à 33°C et est maintenue
à cette valeur. On poursuit alors la réaction pendant deux
heuxes et demie supplémentaires.
A l'issue de la réaction, 1e mëlange réactionnel
est lavé trois fois par 200 ml d'eau â 50-60°C, débarrassé du
tétrahydrofurane par distillation sous pression réduite, et
repris par 200 ml d'isopropanol à 50°C. La solution trouble
ob~tenLre est agitée pendant une heure en présence de 180 g de
résine AMBERLITE IRN 150 (marque de commerce) puis filtrée
sur verre fritté N° 4 préchauffé; après lavage de la résine
par 50 ml d'isapropanol â 60°C, la solution limpide jaune est
versëe lentement dans 600 ml d'acétate d'éthyle sous vive
agitation. he précipité obtenu est laissé au repos 15 heures
à +4°C puis essoré sur verre fritté N° 3. On obtient aprês
- 18 _
spchage sous pression réduite à 40-45°C, 64 g de produit
blanc, soït un rendement de 40%.
ANALYSES
- F = 76°C
- Spectre IR conforme
- Spectre RMN 1H conforme
- Analyse élémentaire
Cg Hô N$
Calculé 76,40 12,65 2,48 8,48
prouvé 76,55 12,65 2,49 8,63
Rapport érythro : thréo = 75:25
EXEMPLE 2
Prë aration du 2-olëo lamino-1 3-octadécanediol
Dans un ballon, sous atmosphère inerte, on solu-
bilise 3 ml de chloroformiate d°éthy7.e (31 mmoles) dans 5 ml
de tétrahydrofurane; cette salution étant refroidie à -15°C,
on additionne goutte à goutte 11,3 g d'oléate de triéthyl-
amine (29,5 mmoles) préalablement solubilisés dans 10 ml de
tétrahydrofurane.
Après 2 heures d'agitation à température ambiante,
le milieu réactionnel est versé lentement, sous atmosphère
inerte, dans 8,9 g de (D, L) 2-amino-1,3-octadêcanediol
préparé à la lère étape de l'exemple 1 (29,5 mmoles) solubi-
lisés dans 40 ml de tëtrahydrofuranne, à 30°C.
Après 1 heure d'agitation, à 30°C, sous atmosphêre
inerte, (chromatographie sur couche mince de gel de silice,
éluant chlorure de méthylëne/méthanol/ammoniaque 15/3,5/0,6),
le milieu réactionnel est lavé à l'eau, puis évaporê à sec,
sous vide. Le produit brut obtenu est chromatographié sur
34 colonne de silice (êluant . acétate d'éthyle/heptane 5/3) et
- 19 -
aprês évaporation du solvant d'élution, sous vide, on obtient
12,5 g de cristaux blancs (rendement 75%).
Les spectres RMN13C et IR sont conformes â la
structure attendue.
Analyse centésimale : C36H71N03
C% H% N% 0%
Calculé 76,40 12,65 2,48 8,48
Trouvé 76,47 12,75 2,60 8,72
Rapport êrythro : thréo ~ 84:16
EXEMPLE 3
Prëparation - --du 2-linoléoylamino-1,3-octadécanediol
Selon le méme mode opératoire que celui décrit à
l'exemple 2 et en utilisant 11,3 g de linoléate de
trîéthylamine (29,5 mmoles), on obtîent 11,6 g de cristaux
blancs (rendement 70%).
Les spectres RMN13C et IR sont confirmes à la
structure attendue.
Analyse centésimale: C36H69N03
C% H% N% 0%
Calculé 76,67 12,33 2,48 8,51
Trouvé 76,74 12,38 2,49 8,64
Rapport érythro : thréo = 74:26
2~~~.r~~~
E~E~~~E ~
Préparation du 2-linoléoylamino-1.3-octadécanediol
Selon le même mode opératoire que celui décrit à
l'exemple 2 e-t en utilisant 11,3 g de linoléate de
triéthylamine *(29,5 mmoles), an obtient 11,6 g de cristaux
blancs (rendement 49ô).
Le spectre RMN13C est conforme à la structure
at~tendue~.
Le spectre de masse est en accord avec la structure
attendue.
Rapport érythro : thréo = 66:34
* A partir d'une vitamine F du commerce dont la
composition est la suivante:
C14 . 0,1~
C16 . 6,5ô
Clg =1 : 15,5ô
Clg =2 : 72,4â
C1$ =3 . 3,4ô
E7iE~iPhEB DE lE'~â~MTJL~1TTQP1
EXE1~IPLE 1
Dispersion vêsiculaire
La préparation est réalisée à L'aide des parties
suivantes:
Partie A
. Céramide de l'exemple 1: 0,90 g
. Cholestérylsulfate de sodium: 0,60 g
Partie B
. Eau: 1,50 g
Partie C
. Tampons phosphate 0,1 M, pH = 6,93: 27,10 g
- 21 -
Eta~e 1
Les constituants de la partie A sont introduits
dans un ballon de l00 m1 puis dissous dans un mélange
contenant 5 ml de chloroforme et 20 ml de méthanol. Le
solvant est ensuite ëvaporë à 40°C sous pression réduite
(pression finale: envïron 5x102 Pa), â l'aide d'un évapora-
teur rotatif.
Eta~e 2
Le film lipïdique formé â l'issue de l'étape 1 est
prélevé et placé dans un flacon de 15 ml. On ajoute aux
lipides la partie B. Le mélange obtenu subit le cycle
suivant: homogénéisation à l'aide d'une spatule-chauffage en
étuve à 75°C pendant une durée da 15 minutes; retour à
température ambiante par refroidissement spontané â l'air. Le
cycle est reproduit en chauffant une fois 15 minutes puis une
autre fois en chauffant 5 minutes.
Eta~e 3
A la phase lamellaire issue de l'étape 2, on ajoute
la partie C. Le mélange ainsi obtenu est agité par secouage
pendant 1 heure à 70°C.
On obtient ainsi une dispersion blanche de
vésicules. La fraction volumique des vésicules est égale à
18~ et leur taux d'encapsulation est égal â 2,6 ul de milieu
aqueux par mg de mélange lipidique.
EXENdPLE 2
D~ersion vésiculaire
La préparation est réalisée â l'aide des parties
suviantes:
Pattie A
. Composé non-ionique de formule générale
C16H330-~-C3H5-(OH)-0-ln-H : 0,56 g
- 22 -
où -C3H5(OH)-O est représenté par les Structures suivantes
prises en mélange ou séparêment:
-CH2-CHO- -CH-CH20-
CH20H CH20H
et n est une valeur statistique moyenne égale à 3;
. Cholestérol: 0,71 g
. Dihexadécylphosphate de sodium: 0,08 g
. Céramide de l'exemple l: 0,15 g
Partie B
. Solution contenant 0,02$ d'azoture de sodium
dans l'eau: 28,50 g
Étape 1
Les const i-tuants de la partie A sont introduits
dans un ballon de 100 ml puis dissous dans un mélange
contenant 10 ml de dichlorométhane et 4 ml de méthanol.
Le solvant est ensuite êvaporë à 41°C sous pression
réduite, par paliers successifs depuis la pression ambiante
jusqu'â environ 5x102 Pa, à l'aide d'un évaporateur rotatif.
Étape 2 '
Au film lipidique formé â l'issue de l'étape 1, on
ajoute la partie B. Le mélange ainsi obtenu est agité par
secouage pendant 2 heures à 70°C.
On obtient ainsi une dispersion blanche de
vésicules.
La fraction volumique des vésicules est égale à 35~
et leur taux d'encapsulation est égal à 9,4 ~1 de milieu
aqueux par mg de mélange lipidique.
Étape 3
La dispersion obtenue à l'issue de l'étape 2 est
portée â la température de 3U°C, et traitëe pendant 2 minutes
à l'aide d'un homogénéisateur â ultrasons vendu sous la
23 -
marque de commerce SONI~'IER B 3.0 par la Société BRANSON
SONIC POWER C0, équipê d'une microsonde.
Conditions de réglage:
- cycle de travail: 50~
- rêglage de puissance: position 5
On obtient ainsi une dispersion blanchâtre de
vêsicules.
La fraction volumique des vêsicules est égale à 19~
et leur taux d'encapsulation est égal à 2,9 ~Sl de milieu
aqueux par mg de mélange lipidique.
La taille moyenne des vésicules mesurée aprês 1
jour de conservation à température ambiante est égale à
(18214) nm; après une semaine: (17913) nm; après 1 mois:
(17714) nm.
E%EMPLE 3
Soin gour la peau: Crme H/E (~ en poids)
- Starate de glycrol 2
- Monostarate de sorbitan 20 moles d'oxyde
d'thylne 1
- Alcool ctylique 0,5
- Acide starique 1.4
- Trithanolamine 0,7
- Acide polyacrylique rticul commercialis
sous la marque de commerce CARBOPOL 940 0,4
- Fraction liquide de graisse de karit 12
- Perhydrosqualne de synthse 12
- Antioxydants 0,05
- Cramide suivant l'exemple 1 ou 2 0,2
- Parfum 0~5
- Eau + conservateurs qsp 10U
- 24 -
EXEMPLE 4
Soin pour la beau: Crème E/H (é en poids)
- Monoisostéarate de sorbitan 5
- Cire microcristalline 1
- Huile de vaseline 10
- Huile de germes de maïs 4
- Esters d'acides gras en Cg-Clg et d'alcools
gras en ClZ-Clg 1
- Octyldodcanol 4,9
- Cramide suivant l'exemple 1 ou 2 0,35
- Gel de montmorillonite modifie et d'huile
neutre ('triglycrides d'acides caprylique et
caprique) 5
- Propylne glycol 3
- Antioxydants 0,1
- Eau + conservateurs qsp 100
EXEMPLE 5
Soin four la peau: lait corporel (~ en poids)
Starate de glycrol 2
-- Monostarate de sorbitan 20 moles d'oxyde
d'thylne 1
- Acide starique 1,4
- Trithanolamine 0,7
- Acide polyacrylique rticul commercialis
sous la marque de commerce CARBOPOL 940 0,2
- Huile d'amandes douces 3
- Huile de vaseline 8
- Antioxydants 0,05
- Cramide suivant l'exemple 1 ou 2 0,3
- Eau + conservateurs qsp 100
- 2.5
CA 02061692 2002-09-11
EXEMPLE 6
Rouge lvres (% en poids)
- Huile de ssame 25
- Lanoline 20
- Cire de Carnauba 20
- Cramide suivant l'exemple 1 ou 2 5
- Pigments 10
- Huile de VASELINE (marque de commerce) 100
EXEMPLE 7
Roue lvres (% en poids)
- Huile de jojoba 20
- Lanoline 25
- Cire microcristalline 20
- Cramide suivant l'exemple 1 ou 2 5
- Pigments 10
- Triglycrides d'acides caprique/caprylique
vendus sous la marque de commerce
MIGLYOL 812 qsp 100
EXEMPLE 8
Dispersion vsiculaire
Dans un ballon rond de 100 ml, on dissout dans10 ml d'un
mlange solvant (chloroforme-mthanol dans le
rapport 2/1), les
produits suivants:
- Cramide de l'exemple 1 120 mg
- Cholestrol 75 mg
- Acide palmitique 75 mg
- Cholestrylsulfate de sodium 30 mg
On vapore le sc>l~lant l'aide d'un vaporateur
rotatif et on
limine les dernires traces de solvant par passagela pompe
palettes pendant 1 heure.
- 26 -
N
On met au contact l' association de lipides obtenue
avec 10 g d'eau déminéralisée dans laquelle on a dissout 17,7
mg dihydrogénophosphate de potassium et 75,5 mg de monohydro-
génophosphate disodique.
On homogénéise le mélange à l' aide d' une secoueuse
pendant 2 heures â la température de 90°C, puis on revient
progressivement à la température ambiante.
On obtient ainsi une dispersion de vésicules
lipidiques dont la taille moyenne est de 0,2 micron.
~X~Mï'LE 9
Shampooing
On prépare un shampooing limpide de composition
suivante:
- Céramide de l'exemple 1 0,5 g
- Chlorure de sodium 5 g
- Laurylsulfate de triéthanolamine à 40~ MA
(matière active) 20 g MA
- Triéthanolamine qs pFI 7
- Eau qsp 100 g
E7~EMPL~ 10
Lotion pour cheveux
On prépare une lotion non rincée de composition
suivante:
Céramide de l'exemple 1 0,4 g
- Décaméthylcyclopentasiloxane vendu sous
la marque de commerce SILB20NE 70045 V 5
par la Société RHONE POULENC 20 g
- Octaméthylcyclotëtrasiloxane vendu sous
la marque de commerce SILBTONE 70045 V 2
par la Société RHONE POULENC 20 g
- 27 -
-- Hexamthyldisiloxane vendu sous la marque
de commerce HUThE AK 0,65 par la Socit WACKER 19,6 g
- Alcool thylique 100 g
EXE~RPLE 1i
Soin gour cheveux
On prpare un soin non rinc pour cheveux abms de
composition suivante:
- Dcamthylcyclopentasiloxane 12,5 g
- Octamthylcyclottrasiloxane 12.,5 g
- Cramide de l'exemple 1 0,1 g
- Mlange d'un polydimthylsiloxane (13~)
hydroxyl en bout de chane et de cyclo-
mthycone (87~) vendu sous la marque de
commerce Q2 - 1401 par la Socit DOW CORNING S5 g
- Henzoate d'alcools gras en C12-C15 vendu sous
la marque de commerce FINSOLV TN 4,95 g
- Alcool thylique 100 g
Cette composton facilite le coiffage, apporte de
la brillance et du maintien ~ la coiffure.
EX .F'~iPIsE ~.2
Mousse restructurante
- Cramde de l'exemple 1 1 g
- Monolaurate de sorbitan oxythyln
20 moles d'oxyde d'thylne vendu sous la
marque de commerce TWEEDI 20 par la Socit ICI 5 g
- Conservateurs
- Eau qsp 100 g
- pH = 5,8
- 28 -
Conditionnement en bombe pressurisée
- Actif 92 g
- Propulseur hydrocarbon vendu sous la marque
de commerce AEROGAZ 3,2N par la Socit ELF
Aquitaine
8 g
Applique en non rinc sur des cheveux dcolors
aprs un'shampooing, la composition amliore le dmlage des
cheveux mouills et apporte un toucher lisse uniForme.
et
EXE'PtiPLE 1.3
Aprs sham~ooinq
- Mlange d'alcool ctylstarylique et d'alcool
ctylstarylique oxythyln 33 moles
doxyde d'thylne vendu sous la marque de
commerce SINNOWAX AO par la Socit HENKEL 2 g
- Alcool ctylique 1 g
- Alcool starylique 1 g
- Hydroxythylcellulose vendue sous :La marque
de commerce NATROSOL 250 HR par la Socit
HERCULES 1 g
- Cramide de l'exemple 1 0,5 g
- Conservateurs
Eau qsp 100 g
- PH . 6
Appliquée sur cheveux décolorés après un
shampooing, la composition apporte un toucher du cheveu plus
durci et plus uniforme.
EiCET~iPâ.~E 14
Mascara
- Stêarate de triéthanolamine 15 g
- Paraffine 5 g
- Cire d'abeilles 4 g
- 29 -
- Cire de Carnauba 4 g
- Céramide de l'exemple 1 0,5 g
- Gomme arabique 0,8 g
- Oxyde de fer noix 5 g
- Parahydroxybenzoate de propyle 0,08 g
- Parahydroxybenzoate de méthyle 0,24 g
- Eau qsp 100 g
MODE DPERATOIItE
1 - On fait fondre les cires (80°C) et on y
incorpore le pigment.
. - On fait chauffer la phase aqueuse contenawt la
gomme et les conservateurs.
3. - On amêne les deux phases â 75°C et on ajoute
le céramide dans la phase cireuse.
4. - On mélange ces deux phases afin de réaliser
l'émulsion.
- 30