Note: Descriptions are shown in the official language in which they were submitted.
W094/2~26 ~1 6 2 S 8 5 PCT~K94tO0571
PKOCEDE D'ENTI~IN~NT D'UN MUSCLE
SQUELEl'rIQUE POUB UN COEUB BIOMEC~NIQUE ET
COEUB BIOMECANIQUE UTILISAN~ UN TEL MUSCLE.
La présente invention concerne un procédé
d'entraînement dynamique d'un muscle squelettique pour
un coeur biomécanique ainsi qu'un coeur biomécanique
utilisant un tel muscle.
Il a déjà été envisagé de réaliser un coeur
biomécanique se présentant sous la forme d'une pompe
circulatoire susceptible d'être complètement implantée
dans la cage thoracique d'un patient, en particulier
dans les cas d'insuffisance cardiaque terminale. Cette
pompe est actionnée par un muscle squelettique, par
exemple le muscle grand dorsal, soumis à une
lS électrostimulation de telle façon que toute l'énergie
pulsatoire de la pompe provienne du métaboliæme du
muscle qui en constitue en quelque sorte le moteur. Un
tel coeur biomécanique, utilisant un muscle
squelettique en tant que moteur, offre l'avantage qu'il
n'entraîne pas une réaction de rejet de l'organisme du
fait que le muscle est prélevé sur le patient dans
lequel le coeur biomécanique est implanté.
Pour pouvoir utiliser, en tant que moteur d'un
tel coeur biomécanique, un muscle non fatigable, à
fibres dites de type I, il a déjà été prévu de
soumettre préalablement le muscle à un entraînement
W094/2~26 ~ PCT~94/00571
2~6Z585
dynamique, ainsi qu'il est décrit dans les
publications:
N.W.Guldner et al.; "Development and training
of skeletal muscle ventricle with low preload";
J.Card.Surg.,l991;vol.6, Nl.
N.W.Guldner et al.;"Dynamic training of
skeletal muscle ventricles - a method to create high
performance for muscle powered cardiac assist."; Fourth
Vienne International Workshop on Functional
Electrostimulation; Baden/Vienne, 24-27 septembre 1992;
ISBN 3-900928-0~-9 1992.
Ce type d'entraînement dynamique consiste à
enrouler le muscle autour d'un appareil d'entraînement
comportant un élément déformable élastiquement à
chambre interne remplie de liquide et terminée à ses
extrémités par des vessies gonflables, un tel appareil
étant décrit dans le document WO-A-9205813. Pour
assurer l'entraînement du muscle, on le relie à un
myostimulateur produisant des impulsions électriques
périodiques de stimulation et lorsque le muscle est
ainsi excité par une impulsion électrique, il se
contracte, ce qui provoque une rétraction de la chambre
centrale et une expulsion du liquide vers les vessies
latérales qui se gonflent. Lorsque le muscle n'est plus
excité, entre deux impulsions électriques successives
et qu'il se relâche, les vessies se dégonflent et le
W094/2~26 ~16 2 ~ ~ ~ PCT/FR94/00571
liquide retourne dans la chambre centrale qui augmente
de volume, et le cycle peut alors recommencer.
La présente invention concerne des
perfectionnements apportés à ce procédé d'entraînement
d'un muscle permettant d'obtenir un accroissement
notable de la masse musculaire et de la puissance
développée.
A cet effet ce procédé d'entraînement dynamique
d'un muscle squelettique destiné à être utilisé dans
un coeur biomécanique, dans lequel on enroule le muscle
squelettique autour d'un appareil d'entraînement
déformable susceptible de pouvoir se contracter, en
opposant une résistance à la contraction, et reprendre
ensuite sa forme initiale et on stimule le muscle
lS squelettique, au moyen d'impulsions électriques
périodiques de manière à provoquer sa contraction et
celle de l'appareil d'entraînement déformable et leur
relaxation subséquente, est caractérisé en ce qu'au
cours d'une première étape on stimule le muscle
squelettique au moyen d'impulsions électriques ayant
une fréquence allant en croissant en fonction du temps
et au cours d'une seconde étape on augmente
progressivement la résistance de l'appareil
d'entraînement déformable à la contraction, les
première et seconde étapes se chevauchant
éventuellement guelque peu.
~1~2~8~
.
On connaît également par le brevet US-A-5 007 927
un dispositif d'assistance cardiaque qui est actionné par
un muscle squelettique soumis à un stimulus fourni par un
générateur d'impulsions programmé.
On sait que, dans la pratique, un tel dispositif
n'est que très peu efficace dans la mesure où le muscle
squelettique utilisé est incapable de fournir une puissance
suffisante-à son actionnement.
La présente invention se propose de remédier à cet
10 inconvénient en utilisant en tant que muscle moteur un
muscle entraîné suivant le procédé d'entrainement objet de
la demande, et ayant ainsi subi des transformations
"mécaniques" lui conférant la puissance nécessaire au bon
actionnement du coeur biomécanique.
L'invention a ainsi également pour objet un coeur
biomécanique utilisant en tant que moteur un muscle
- squelettique ayant été soumis à un tel entrainement
dynamique.
On décrira ci-après, à titre d'exemples non
20 limitatifs, diverses formes d'exécution de la présente
invention en référence aux dessins annexés sur lesquels:
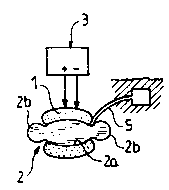
- la figure 1 est un schéma illustrant le procédé,
suivant l'invention, pour l'entrainement dynamique d'un
muscle squelettique destiné à être utilisé dans un coeur
25 biomécanique.
- la figure 2 est un diagramme illustrant la
variation, en fonction du temps, de la fréquence des
impulsions de stimulation électrique et de la charge
FEUILLE ~fiO~lflEE
` 4~ 2 5 8 5J
mécanique .résistante appliquée au muscle pendant son
- entraînement.
- la figure 3 est un diagramme illustrant la plage
de variation de la caractéristique pression/volume pour
5 chacune des vessies gonflables de l'appareil
d'entraînement.
- la figure 4 est une vue en élévation,
- partiellement en coupe axiale, d'un ventricule biomécanique
suivant l'invention, à circulation axiale du flux sanguin.
- la figure 5 est une vue en coupe
transversale, à plus g=a de échelle,
FEUILLE~
21~2~85
W094/2~26 ~ PCT~94/00571
ligne V-V de la figure 4, la moitié supérieure de la
figure représentant le ventricule biomécanique à l'état
relâché tandis que la moitié inférieure représente le
ventricule à l'état contracté.
- la figure 6 est un schéma d'une application
d'un ventricule biomécanique suivant l'invention, à
circulation axiale, pour une assistance cardiaque.
- la igure 7 est une vue en coupe schématique
d'une variante d'exécution d'un ventricule biomécanique
à circulation transversale du flux sanguin.
- la figure 8 est une vue en perspective
schématique illustrant les différentes phases de
l'entraînement d'un muscle logé dans une enveloppe
tubulaire.
- la figure 9 est une vue en coupe transversale
du muscle et de son enveloppe enroulés autour de
l'appareil d'entraînement dynamique.
- la figure lO est une vue en perspective d'un
muscle moteur des figures 8 et 9 enroulé autour d'une
cage à ressorts constituant un dispositif
péricardiaque.
- la figure ll est un schéma illustrant un
muscle enroulé autour de l'appareil d'entraînement
dynami~ue avec interposition d'une enveloppe
intermédiaire.
W09412~26 ~ l 6 2 5 8 5 PCT/FR94100571
- la figure 12 est une vue en coupe axiale
schématique du muscle moteur et de son enveloppe
intermédiaire obtenus après la période d'entraînement.
- la figure 13 est un schéma d'une variante
d'exécution d'un dispositif péricardia~ue comportant un
système de transmission hydraulique entre la pompe et
le coeur humain.
- la figure 14 est une vue en coupe schématique
d'une variante d'exécution du récepteur associé au
coeur humain.
Sur la figure 1 est représenté schématiquement
le procédé d'entraînement dynamique d'un muscle
squelettique 1, par exemple le muscle grand dorsal,
destiné à être utilisé dans un coeur biomécanique
suivant l'invention. Ce muscle 1 est enroulé autour
d'un appareil d'entraînement dynamique 2 et plus
particulièrement autour d'une chambre centrale 2a
remplie de liquide et prolongée, à 8es deux extrémités,
par des vessies gonflables 2b. Le matériau constituant
la chambre interne 2a ne devrait pas etre élastique
alors que le matériau formant les vessies gonflables 2b
l'est. Pour l'entraînement du muscle 1 on procède tout
d'abord à une électrostimulation de ce muscle en le
reliant à un myostimulateur 3 qui est en fait un
générateur d'impulsions électriques périodiques.
Lorsque le muscle est excité par l'une de ces
impulsions, il se contracte, ce qui entraîne une
W094l2~26 216 2 i 8 ~ PCT~94/00571
réduction du volume de la chambre centrale 2a et une
expulsion du liquide à partir de cette chambre vers les
vessies latérales élastiques 2b qui se gonflent, si
bien que l'appareil d'entraînement 2 oppose une
résistance à la contraction du muscle l. Après la
disparition de l'impulsion d'eYcitation électrique, le
muscle l se relâche et les vessies élastiques 2b se
dégonflent en chassant le liquide qui revient dans la
chambre centrale 2a. Cette chambre centrale 2a gonfle
alors à son tour, pour reprendre au moins sa forme
initiale, en exerçant une force de rappel positive sur
le muscle l, force dirigée vers l'extérieur et orientée
en sens inverse de celle exercée par le muscle pendant
sa contraction. Dans le procédé suivant l'invention on
utili8e, d'une part, une variation incrémentielle de la
fréquence des impulsions électriques du générateur 3
et, d'autre part, une variation incrémentielle de la
charge mécanique résistante qui s'oppose à la
contraction du muscle l. A cet effet le volume interne
de l'appareil d'entraînement 2 est relié à un cathéter
S communiquant avec une chambre implantable sous la
peau et permettant d'augmenter progressivement la
quantité de liquide se trouvant dans la chambre
centrale 2a et les vessies gonflables 2b. Pendant une
première étape de l'entraînement du muscle l, indiqué
par I sur la figure 2, on applique à ce muscle des
impulsions de stimulation électriques dont la fréquence
~1625~S
W094/2~26 PCT~94/00571
f augmente progressivement dans le temps. On commence
par exemple par une pulsation lente, de l'ordre d'une
impulsion par minute (correspondant à une fréquence
d'environ 0,017Hz au stimulateur) et on augmente
ensuite cette fréquence progressivement, pendant une
période de temps de l'ordre de 6 à l0 semaines, jusqu'à
un rythme cardiaque normal de l'ordre de 60 à 80
pulsations par minute (fréquence de l à 1,33~z au
stimulateur). Cette augmentation de la fréquence f en
fonction du temps t est illustrée par la courbe A de la
figure 2. Par ailleurs la première étape de stimulation
électrique I est suivie d'une seconde étape II au cours
de laquelle on fait croître progressivement la
résistance r opposée par l'appareil d'entraînement 2 à
la contraction musculaire, ainsi qu'il est représenté
par la courbe B. Cet accroissement de la charge
résistante est obtenu par une introduction progressive
de liquide dans l'appareil 2, au moyen du dispositif 5.
La combinaison de la première étape de
stimulation électrique à fréquence croissante et de la
seconde étape à croissance progressive de la résistance
à la contraction musculaire permet d'obtenir une
augmentation notable de la masse musculaire et de la
puissance du muscle. Ainsi à la suite d'expériences
effectuées sur le muscle grand dorsal du veau, on a pu
atteindre une puissance de lO watts, alors que chez
W094l2~26 216 2 5 ~ 5 PCT~94/00571
l'homme sain et au repos la puissance maximale d'un
ventricule gauche est d'environ 3 watts.
On a constaté, chez certains sujets, qu'il est
possible de rendre partiellement simultanées les deux
étapes I et II, c'est-à-dire que l'on peut être amené,
au moins pendant un certain temps de recouvrement des
deux étapes, à augmenter à la fois et progressivement
la fréquence d'excitation du stimulateur et la quantité
de liquide introduite dans l'appareil d'entraînement 2.
Suivant une caractéristique complémentaire de
l'invention le matériau constituant les deux vessies
gonflables 2b est constitué par une silicone de type
élastique formant la paroi des vessies et par des
filets de polymère noyés dans cette paroi de telle
façon que l'on obtienne, pour chacune des vessies
gonflables 2b, une caractéristique pression/volume
comprise dans la plage délimitée entre les deux courbes
limites a et b sur la figure 3. Sur cette figure
l'élasticité C des vessies gonflables est donnée par le
rapport entre le volume V et la pression P de chaque
vessie. Les résultats les meilleurs ont été obtenus
avec une valeur de l'élasticité C comprise entre 1/4
(courbe a) et 2 (courbe b). Dans une forme d'exécution
particulièrement avantageuse la paroi de chaque vessie
2b est constituée de trois couches, à savoir une couche
interne et une couche externe en matériau connu sous le
nom de "Rehau SI 1511" et une couche médiane en
W094/2~26 ~ 62 ~ 8 5 PCT~94/00571
matériau connu sous le nom de "Dow Corning Q3-8111" ou
"Dow Corning MDX4-4210".
Les figures 4 et 5 illustrent une forme
d'exécution d'un coeur biomécanique suivant l'invention
constituant un "ventricule" à circulation axiale du
flux sanguin, utilisant comme moteur un muscle
squelettique entraîné dynami.quement de la façon décrite
précédemment. Ce ventricule biomécani~ue comporte ur
muscle 1, préalablement entraîné comme indiqué
précedemment, lequel est connecté à un myostimulateur 3
et est enroulé autour d'une cage de pompa~e tubulaire,
déformable 6. Cette cage 6, souple et élastique,
présente une partie centrale de grand diamètre se
prolongeant par deux parties extrêmes opposées de plus
lS petit diametre. La cage de pompage tubulaire 6 comporte
une enveloppe externe souple 7, par exemple en
silicone, et à l'intérieur de cette enveloppe plusieurs
lames de ressort cambrées 8, à convexité tournée vers
l'extérieur, s'etendant sur toute la longueur de
l'enveloppe 7, d'une extrémité à l'autre de la cage 6,
et réparties autour de l'axe de cette cage 6. Les
extrémités des lames de ressort 8 sont noyées dans deux
anneaux raidisseurs transversaux 9 logés respectivement
dans les deux extrémités ouvertes de la c~ge tubulaire
6. Une membrane interne 11, athrombogène, par exemple
en polyuréthanne, s'étend à l'intérieur de la cage 6,
en recouvrant les lames de ressort 8 auxquelles elle
W09412~26 PCT~94/00571
~162S8~
11
adhère de manière à délimiter, entre les lames de
ressort 8, des chambres individuelles étanches remplies
d'un fluide 12. Lorsque le muscle 1 n'est pas excité,
c'est-à-dire lorsqu'il est relâché, la cage tubulaire 6
a un grand diamètre et dans ce cas la membrane 11
délimite des chambres relativement aplaties, comme il
est représenté dans la partie supérieure de la figure
5. Par contre, lorsque le muscle 1 est excité, la cage
tubulaire 6 est contractée, ainsi qu'il est représenté
dans la partie inférieure de la figure 5, les lames de
ressort 8 sont aplaties et rapprochées les unes des
autres et la membrane 11 forme alors des chambres qui
s'étendent en saillie vers l'intérieur, entre les lames
de ressort 8, sensiblement dans des directions
radiales. Lorsque le muscle se relâche, les lames de
ressort 8 permettent la distension c'est-à-dire le
retour de la cage de pompage tubulaire 6 à sa forme
initiale à grand volume.
La figure 6 illustre une utilisation de la cage
de pompage tubulaire 6 réalisée de la façon illustrée
sur les figures 4 et 5, pour constituer un dispositif
de contre-pulsion extra-aortique. La cage de pompage
tubulaire 6 dont le muscle 1 est relié électriquement à
un myostimulateur 3, est branchée dans un conduit 13 en
dérivation sur l'aorte 14 d'un patient dont le coeur
est représenté en 15. Lorsque la valve aortique 16 est
fermée (diastole), le myostimulateur 3 envoie, en
W094/2~26 PCT~94/00571
216258~
- 12
synchronisme avec la diastole ventriculaire gauche, une
impulsion électrique au muscle 1 pour le stimuler. La
synchronisation est assurée par un capteur 17 d'écoute
des pulsations cardiaques en contact avec le coeur 15
et relié au myostimulateur 3. Du fait de l'excitation
du muscle 1, la cage de pompage tubulaire 6 est
comprimée et le sang est refoulé vers l'amont et vers
l'aval, comme il est indiqué par les flèches. Le
refoulement du sang vers l'amont se traduit par une
augmentation de la circulation dans les coronaires 18.
Par contre lorsque la valve aortique est ouverte
(systole) le muscle 1 n'est pas stimulé électriquement,
il se relâche et la cage tubulaire 6 se dilate en
créant une dépression favorisant la circulation du sang
dan8 l'aorte. Ce ventricule biomécanique à circulation
axiale du flux sanguin peut également être utilisé dans
des configurations topographiques autres, telles entre
l'oreillette gauche et l'aorte entre le ventricule
gauche et l'aorte, entre l'oreillette droite et
l'artère pulmonaire. Dans ce cas, ces ventricules
biomécaniques seront pourvus de deux raccords, à savoir
un raccord d'entrée muni d'une valve d'admission et un
raccord de sortie muni d'une valve de refoulement.
Dans la variante d'exécution d'ùn "ventricule"
biomécanique représentée sur la figure 7, laquelle est
prévue pour une circulation transversale du flux
sanguin, le muscle 1 entoure une poche souple non
wo 94/2~26 2 L 6 2 5 8 5 ~CT~94/00571
1~
expansible 19 s'étendant à l'extérieur d'un corps creux
21, à travers une ouverture de ce dernier. Le corps 21
est séparé en deux parties par une membrane étanche 22
(ou un piston) délimitant, d'un côté, une chambre de
pompage 23 à l'intérieur de la poche souple 19,
contenant un liquide tel que du sérum physiologique,
et, de l'autre côté, une chambre de chasse 24. La
chambre de chasse 24 est pourvue de deux raccords, à
savoir un raccord d'entrée 25 pourvu d'une valve
d'admission 26, et un raccord de sortie 27 pourvu d'une
valve de refoulement 28.
Le "ventricule" biomécanique repréaenté sur la
figure 7 peut être utilisé en assistance partielle ou
totale, aussi bien pour le coeur gauche, entre
ventricule gauche et artère aorte, que pour le coeur
droit entre oreillette droite et artère pulmonaire.
Dans ce cas les raccords d'entrée 25 et de sortie 27
sont branchés dans le système circulatoire. Il peut
être utilisé sans valves d'admission et de refoulement
en configuration aorto-aortique de contre-pulsion
extra-aortique.
L'appareil représenté sur la figure 7 peut être
également utilisé pour assurer l'entraînement dynamique
du muscle 1. Dans ce cas les raccords d'entrée 25 et de
sortie 27 ne sont pas branchés dans le système
circulatoire mais ils sont reliés entre eux par un
conduit 29 qui est coupé ensuite pour le supprimer lors
W094/2~26 PCT~94/00571
21~8~ 14
du passage à la mise en fonctionnement, afin de relier
les raccords 25 et 27 au système circulatoire.
Sur la figure 7 est également représenté un
cathéter 31 faisant communiquer la chambre de pompage
23 avec un dispositif de remplissage de cette chambre
de pompage en liquide propulseur, pendant la seconde
étape du procédé d'entraînement dynamique, afin de
permettre d'augmenter progressivement la quantité de
liquide se trouvant dans la chambre de pompage 23, et
de pouvoir mesuere régulièrement la pression de ce
liquide pour suivre l'évolution de la performance
musculaire. Le cathéter 18 peut être éventuellement
supprimé lors du passage au fonctionnement normal mais
il peut être aussi laissé en place pour servir à
mesurer la pression du liquide propulseur.
Les figures 8 et 9 représentent une variante
d'exécution dans laquelle le muscle 1 est préalablement
logé, avant la mise en oeuvre du procédé d'entraînement
dynamique, dans une gaine tubulaire 32 constituée par
une membrane en polymère qui protège le muscle pendant
le procédé d'entraînement dynamique et assure sa non
adhérence aux tissus environnants. La gaine 32 est
réalisée en n'importe quel polymère naturel, artificiel
ou synthétique mais de préférence elle est constituée
par un polymère substitué notamment par le fluor, tels
que les polymères du type polytétrafluoroéthylène.
W094/2~26 ~16 2 5 8 5 PCT~94/00571
La figure lO illustre un dispositif
péricardiaque comportant un muscle l, autour d'une cage
tubulaire 30 souple et élastique, ouverte à ses deux
extrémités.L'une des ouvertures de la cage 30 a un
diamètre suffisamment grand pour permettre
l'introduction d'un coeur humain à l'intérieur de la
cage 30. La stimulation du muscle l provoque alors la
contraction de la cage 30 et celle du coeur humain logé
étroitement dans cette cage. Si le muscle est
insuffisamment long, on peut prévoir un prolongement en
Y 33, fait d'un polymère résistant, comme par exemple
du Dacron ou du PTFE..
Les figures ll et 12 représentent une variante
d'exécution dans laquelle, pendant l'entraînement
dynamique du muscle, on interpose, entre le muscle l et
l'appareil d'entraînement dynamique 2 une membrane 34
enroulée autour d'un axe, à surface continue, ouverte à
ses deux extrémités. Cette membrane 34 est réalisée de
préférence en une matière "colonisable" par le tissu
conjonctif. Après la phase d'entraînement la "cage"
tubulaire souple 35 ainsi obtenue comprend, à
l'extérieur, le muscle l et, à l'intérieur la membrane
34 adhérant au muscle et colonisée par les cellules du
tissu conjonctif. La cage 35 peut être utilisée
directement comme chambre de pompage et elle peut être
raccordée à des prothèses artérielles 36.
W09412~26 PCT~94/00571
~162~ 8~ 16
La figure 1~ illustre une forme d'exécution
d'un dispositif péricardique dans la~uelle le muscle l
est enroulé autour d'une cage souple et élastique 37,
formant une chambre de pompage ou un émetteur
d'impulsions de pression, dont le volume interne
communique, par un conduit 38, avec une poche 39 en
forme de bol dans laquelle est logé un coeur humain 15.
La poche 39 qui forme un récepteur des impulsions de
pression, a une paroi creuse et elle comprend une
enveloppe externe 41 non dilatable et une enveloppe
interne 42 dilatable en contact avec le coeur. La cage
souple et élastique 37, à volume de pompage variable,
est ainsi reliée par un dispositif de transmission
hydraulique à la poche 39. Lorsque la cage 37 se
contracte, sous l'action du muscle l stimulé
électriquement, elle refoule du liquide, par
l'intermédiaire du conduit 38, à l'intérieur de la
poche 39, autrement dit elle crée une impulsion de
pression transmise à la poche 39. Comme son enveloppe
externe 41 n'est pas dilatable, le liquide en excédent
arrivant dans la poche provoque une dilatation de
l'enveloppe interne 42 et par conséquent une
contraction du coeur humain 15.
Le conduit 38 est relié, par l'intermédiaire
d'un conduit en dérivation 43, à une-chambre 44 située
sous la peau 45 d'un patient et obturée par une
membrane perforable 46. A travers cette membrane peut
W094l2~26 216 2 5 8 5 PCT~94/00571
être introduite une aiguille 47 pour la réalimentatlon
en liquide propulseur. Par ailleurs une aiguille pour
la mesure de la pression 48 peut être également
introduite à travers la membrane 46.
Dans la variante d'exécution représentée sur la
figure 14, le conduit 38 du dispositif de transmission
hydrauligue aboutit à un récepteur d'impulsions de
pression comportant une enveloppe dilatable 49 logée à
l'intérieur d'une poche externe 51 non dilatable, poche
à l'intérieur de laquelle se trouve également le coeur
humain 15. L'enveloppe dilatable 49 est en contact
d'une part avec la poche externe 51 et d'autre part
avec le coeur humain 15 si bien que les impulsions de
pression dans le conduit 38 se traduisent par une
augmentation de volume de l'enveloppe dilatable 49 et
une contraction du coeur 15.
On peut prévoir également, ainsi qu'il est
représenté sur la figure 13, un tuyau 52 raccordé au
circuit de transmission hydraulique, par exemple au
conduit 43 ou 38. Ce tuyau permet la connexion
transcutanée à un système de succion (aspiration)
pendant une courte période. Cette connexion
transcutanée peut être supprimée après quelques jours
quand la surface interne de la poche hydraulique 39 (en
silicone par exemple), adhère de façon permanente à
l'épicarde.