Note: Descriptions are shown in the official language in which they were submitted.
2~61~'1
~ ~ o 95/01451 PCT/FR94/00789
DISPOSITIF INDICATEUR DE STERILISATION
La présente invention concerne un dispositif destiné à évaluer
l'action d'un fluide sur une souche de microorganisme ou une enzyme, plus
particulièrement un dispositif indicateur de stéAlisation.
La stérilisation et la désinfection sont des procédés
extrêmement utilisés dans des domaines très divers.
La stérilisation est notamment mise en oeuvre dans des
établissements de soin tels que les hôpitaux, les cliniques, de fa~on à
disposer d'instruments médicaux, de verreAe, de linge, de façon générale de
tout matériel, totalement exempts de microorganisme afin de stopper la
propagation des maladies infectieuses.
Mais, la stérilisation est également utilisée dans l'industrie
pharmaceutique pour le matériel médico-chirurgical tel que les sutures ou
de facon générale un grand nombre d'objets à usage unique et également
pour les médicaments pour lesquels une absence totale de microorganisme
est nécessaire.
La stérilisation est mise en oeuvre également de plus en plus
souvent dans les industries agro-alimentaires afin de maîtriser la
biocont~min~tion de l'environnement, c'est le cas notamment des industries
laitières.
Il est également, dans ces mêmes domaines, d'usage courant
d'utiliser la désinfection, mais il s'agit dans le cas d'établissements de soin
par exemple, du traitement des surfaces, des linges, ceci pour diminuer la
proportion des germes pathogènes afin de limiter l'incidence des
infections. Dans l'industAe pharmaceutique et l'industrie agro-alimentaire
on pratique également la désinfection afin de respecter les bonnes
pratiques de fabAcation; ce procédé tendant d'ailleurs à se répandre dans
d'autres domaines comme par exemple les locaux des collectivités, les
cabinets dentaires, les coiffeurs, etc.
Les objets soumis à la stéAlisation et à la désinfection peuvent
être de nature excessivement vaAée, il peut s'agir aussi bien de verre, que
de métaux ou de matières synthétiques, de mêmes les configurations
géométAques peuvent être très vaAées, forme plate, creuse, lisse ou non.
Actuellement, pour juger de l'efficacité d'une stérilisation, par
exemple pour la chaleur humide, on utilise des moyens externes, il s'agit
WO 9S/01451 ~ 6 I 9 ~ PCT/FR94/00789
essentiellement de l'enregistrement de la température et de la pression
ainsi que des durées de stérilisation. En fonction d'abaque on peut
déterminer le couple temps/température permettant d'obtenir une
stérilisation dans des conditions données.
S Toutefois, ce moyen peut se révéler insuffisant, c'est pourquoi
dans la plupart des cas on prévoit également un dispositif interne
permettant la mise en évidence de la stérilisation.
Sous sa forme la plus simple, il s'agit d'un dispositif qui
comporte des microorganismes sous une forme végétative ou de résistance,
en particulier sous une forme sporulée, dont on contrôlera à la fin de la
stérilisation qu'effectivement il ne reste plus de microorganismes ou de
spores viables, ou du moins que le taux de microorg~ni.cmes ou de spores
viables restant est en dessous d'un certain seuil. On peut également utiliser
une enzyme pour révéler l'efficacité de la stérilisation.
Suivant le type de stérilisation appliqué, on utilisera des
microorganismes connus pour leur résistance sous forme sporulée, par
exemple pour la stérilisation par la chaleur humide on utilisera Bacillus
stearothermophilus. pour la stérilisation par la chaleur sèche ou les gaz on
utilisera Bacillus subtilis et pour la stérilisation par les rayonnements
ionisants on utilisera Bacillus pumilus.
Pour ce qui concerne les procédés de désinfection, seule cette
seconde méthode est utilisable, en effet il n'existe pas d'abaques permettant
de déterminer des conditions désinfectantes.
La présente invention concerne plus particulièrement les
dispositifs indicateurs comportant des microorganismes sous forme
végétative ou sporulée ou d'enzymes, destinés à tester, de facon générale,
l'action d'un fluide sur ledit microorg~nisme ou l'enzyme, en général afin
de tester la stérilisation ou la désinfection d'une enceinte.
Les dispositifs indicateurs de stérilisation comportent en
général, d'une part un support sur lequel se trouvent placées les spores de
la souche résistante qui pourront être amenées au contact du fluide de
stérilisation et, d'autre part, un compartiment dans lequel se trouve un
milieu permettant la culture du microorganisme sporulé et un agent de
révélation qui se change de couleur en présence du microorganisme en
culture.
2 ~ L ~ 7
--'O 9S/01451 PCT/FR94/00789
Le procédé de contrôle consiste donc à introduire le dispositif
dans l'enceinte de stérilisation, les spores sont alors mises en contact avec lefluide de stérilisation, puis, à la fin de la stérilisation on introduit, en
cassant une ampoule, le milieu de culture et l'agent de révélation au contact
5 avec les spores, et au bout d'un temps déterminé on visualise une couleur
dans le milieu si parmi les spores certaines d'entre elles étaient encore
viables.
Ce type d'appareillage est décrit par exemple dans le brevet
Fran$ais 2 045 855.
La plupart des dispositifs de la technique antérieure
présentent un certain nombre d'inconvénients:
- tout d'abord le support des spores est la plupart du temps en papier, or
les matériaux à stériliser dans la pratique ne sont pratiquement
jamais en papier mais en plastique, métal, caoutchouc, verre, etc.;
15 - en général les supports ont une forme plate qui est sans rapport avec
les conformations géométriques de la plupart des matériels à
stériliser qui sont généralement de forme extrêmement variée;
- enfin, le support absorbe, dans certains cas, facilement les agents
stérilisants, ce qui entraîne une destruction plus facile des spores
alors qu'en réalité les microorg~nismes contaminants le matériel à
stériliser sont portés sur des surfaces non-absorbantes.
Ainsi, certains des dispositifs suivant la faSon dont ils sont mis
en oeuvre peuvent conduire à des résultats faussement sécurisants.
En outre, la plupart des dispositifs indicateurs biologiques
actuellement proposés comportent le bris d'une ampoule en verre, ce qui
n'est en général pas souhaitable, notamment car les petits morceaux de
verre peuvent créer des microfissures du contenant extérieur, il y a donc
un risque de cont~min~tion.
Enfin, dans certains cas il peut être intéressant de pouvoir
contrôler la stérilisation en cours d'opération sans avoir à intervenir
directement dans l'enceinte de stérilisation, ceci n'est en général pas
possible avec les dispositifs existant actuellement.
C'est pourquoi la présente invention concerne un dispositif
destiné à évaluer l'action d'un fluide sur une souche de microorganisme ou
sur une enzyme, du type comportant:
WO 95/01451 21 ~ 6 ~ 9 7 PCT/FR94/0078"
- un compartiment (1) permettant la mise en contact du fluide et de
ladite souche ou l'enzyme et
- un compartiment (2) permettant la mise en évidence de ladite souche
ou de l'enzyme après mise en contact avec le fluide, à l'aide d'un
milieu de révélation ( 15),
caractérisé en ce qu'il est constitué d'un ensemble mobile pouvant
présenter au moins deux configurations (8, 11) présentant,
- dans une première configuration, un passage permettant la
circulation du fluide à l'intérieur de l'ensemble et sa mise en contact
avec la souche ou l'enzyme fixée sur un support (9) et
- dans une seconde configuration, un moyen permettant la mise en
contact du milieu de révélation avec le support sur lequel est fixée la
souche ou l'enzyme et, éventuellement, des moyens permettant
d'isoler le milieu de révélation contenant le support de l'atmosphère
extérieure, et des moyens permettant l'observation des modifications
éventuelles du milieu de révélation (18).
De façon préférentielle, ce dispositif est un indicateur
biologique de stérilisation et/ou de désinfection.
Dans ces conditions, le fluide en cause est la vapeur d'eau, un
20 gaz ou un liquide, mais également de facon très générale la chaleur sèche
ou un rayonnement ionisant, même s'il ne s'agit pas à proprement parler
d'un fluide.
Pour ce qui concerne le milieu de révélation, il s'agit la
plupart du temps d'un milieu permettant la culture de la souche à partir des
25 spores ou de forme végétative comportant un révélateur mettant en
évidence la présence de microorg~ni.~mes viables.
Enfin, les microorganismes seront la plupart du temps sous
forme de spores.
De façon préférée, le dispositif selon la présente invention
30 comportera également des moyens permettant l'observation des
modifications éventuelles du liquide de révélation.
De facon générale, le dispositif selon l'invention sera constitué
de deux compartiments mobiles l'un par rapport à l'autre, l'un des
compartiments comportant le support (9) ainsi qu'au moins un orifice (14)
197
- -'O 95/01451 PCTtFR94/00789
S
permettant d'amener un fluide extérieur à l'intérieur au contact du support,
et l'autre compartiment comportant le milieu de révélation, ledit
compartiment étant agencé pour que le déplacement de l'un par rapport à
l'autre amène le support de la souche (9) en contact avec le milieu de
S révélation et éventuellement en ce qu'un autre déplacement conduise à
isoler le milieu de révélation contenant le support du milieu extérieur.
Le déplacement des deux compartiments mobiles peut se faire
aussi bien par translation que par rotation autour d'un axe.
En général, le support de la souche est un élément mobile qui
10 peut avoir une configuration quelconque destiné en particulier à permettre
de représenter au mieux les surfaces qui devront être stérilisées au
décontaminées à l'extérieur.
Il peut s'agir notamment d'un support plan ou bien d'un
support comportant des évidements ou des ondulations, mais dans la plupart
15 des cas il s'agira plutôt d'un dispositif de forme tubulaire, de préférence
ayant la forme d'un petit tube et ce support sera mobile entre une première
position en contact avec le fluide et une seconde position en contact avec le
milieu de révélation.
Dans le mode préféré de r~lis~tion, le dispositif est constitué
2~) de deux conl~ ents mobiles en rotation l'un par rapport à l'autre autour
d'un axe et ayant deux surfaces en vis à vis perpendiculaires audit axe, le
compartiment supérieur comporte un conduit tubulaire (6) sensiblement
parallèle à l'axe de rotation débouchant à l'extérieur du compartiment par
deux orifices, un support est placé dans ledit conduit tubulaire et le support
25 repose sur la surface située en vis-à-vis du compartiment inférieur à la
surface duquel débouche un conduit tubulaire en vis-à-vis du précédent et
dont l'autre extrémité débouche à l'extérieur, on créé ainsi un canal qui
traverse l'ensemble du dispositif parallèlement à l'axe et dont une partie est
constituée par le support de la souche, le compartiment inférieur comporte,
30 en outre, sur sa surface en vis-à-vis un orifice, la dimension de l'orifice
étant telle que, par rotation des deux compartiments, le conduit tubulaire du
compartiment supérieur soit amené en coïncidence de l'orifice et que le
support tombe par cet orifice dans le milieu de révélation situé dans le
compartiment inférieur, ainsi qu'en ramenant l'ensemble à sa position
WO 9S/01451 ~ ~ ~ 6 ~ ~ 7 PCT/FR94/00789
initiale, on isole le milieu contenant le support du milieu extérieur, le
compartiment inférieur comportant, en outre, une ou deux fenêtres
transparentes ou étant complètement transparent, permettant de voir la
couleur du milieu de révélation.
En plus, le compartiment inférieur peut comporter en plus du milieu
de culture, dans la partie inférieure du conduit du fluide, un indicateur
physico-chimique (permettant de voir l'effet d'une stérilisation en
profondeur ou à distance sur un indicateur physico-chimique).
De faSon générale, le support du microorganisme sera
constitué par une surface qui pourra être identique aux surfaces à stériliser
et/ou à décontaminer, en pratique, notamment il pourra s'agir de surfaces
métalliques, de surfaces en papier si cela est nécessaire, de surfaces en
matière plastique, mais de préférence les surfaces seront en verre, en effet
comme on le constatera dans les exemples qui suivent, l'utilisation d'un
support en verre permet d'avoir des résultats qui sont les plus fiables.
Les microorg~nismes sont de préférence présents sous leur
forme la plus résistante, c'est-à-dire sous la forme de spores qui sont fixées
sur le support de microorganisme par des techniques qui sont connues . Il
est également possible d'utiliser des souches non-résistantes, par exemple
une flore réelle ou même une enzyme ayant la même résistance que les
spores de référence.
Comme cela a été indiqué précédemment, dans sa forme
préférée le support est constitué par un tube en verre à l'intérieur duquel
ont été déposées des spores de microorganismes selon des méthodes qui
seront décrites dans les exemples et le fluide sera amené à circuler à travers
ce tube.
Le milieu de révélation est de préférence constitué par un
milieu de culture permettant la croissance des spores lorsque celles-ci sont
encore viables, ledit milieu de culture comportant un indicateur, la plupart
du temps coloré, dont la coloration change ou apparâît lors de la croissance
des microorganismes, par exemple par modification du pH avec des produits
du type du rouge de phénol ou des produits qui réagissent à l'oxydoréduction
97
-'TO g5/01451 PCT/FR94/00789
tels que par exemple le bleu de méthylène, il peut s'agir également de
produits qui se colorent par mise en évidence d'une enzyme spécifique de la
souche en cause, il s'agira dans la plupart des cas d'un substrat coloré de
l'enzyme spécifique.
Dans le mode préféré de l'invention, le support, après avoir été
mis en contact avec le fluide à tester, va être amené à tomber dans le milieu
de révélation et donc incuber en sa présence, toutefois il est nécessaire de
pouvoir décrocher les spores fixées sur le support, pour ce faire on peut
procéder de facon mécanique, notamment en ajoutant un élément
d'agitation dans le milieu et/ou dans le tube, notamment une petite bille
métallique qui va permettre par agitation de racler les spores, il est possible
également de procéder à un passage aux ultrasons mais, comme cela
apparaîtra dans les exemples, la solution la plus rationnelle est d'introduire
dans le milieu de révélation un agent tensioactif, tel que le Tween 80 par
exemple, qui va permettre de décrocher facilement et complètement les
microorganismes sous forme de spores, mais n'a aucune influence sur la
viabilité des cellules.
De préférence la lecture du résultat pourra se faire à travers
une ou deux fenêtres en plastique transparent ou un compartiment
inférieur totalement transparent, ou en tout autre matériau transparent,
dans ce cas il est intéressant d'utiliser le verre comme support, ce qui
permet d'avoir une plus grande épaisseur visible, alors qu'un support
métallique sera au moins de ce point de vue moins efficace.
L'un des intérêts du dispositif de l'invention est que, compte
tenu du fait que le fluide à tester peut circuler dans une c~n~lis~tion dans
laquelle il est mis en contact avec le support portant les spores ou les
microorgani.smes sous forme végétative ou une enzyme, on peut prévoir aux
extrémités de cette canalisation deux ajutages sur lesquels on pourra venir
fixer des tubes en matière appropriée, non poreuse, afin de pouvoir tester la
stérilisation en profondeur ou la stérilisation à distance, c'est-à-dire que
l'on peut tester l'état de la stérilisation d'un endroit dans lequel l'indicateur
ne se trouve pas directement en plongeant les deux tubulures à l'endroit à
tester et en placant le dispositif à l'extérieur, il est d'ailleurs possible de
WO 95/01451 2 1 6 ~ ~ ~7 PCT/FR9410078g
tester la stérilisation d'une enceinte en maintenant le dispositif selon
l'invention à l'extérieur pour peu que l'on ait ajusté deux tubulures dans
lesquelles circule l'atmosphère que l'on doit stériliser.
Parmi les différents dispositifs permettant de tester la stérilité
5 d'une atmosphère, le dispositif selon la présente invention est le seul à
permettre, de façon simple, de tester la stérilité en profondeur grâce à
l'utilisation de tubulures plongeant en profondeur dans le produit ou
l'atmosphère à tester et reliées au dispositif par le ou les ajutages, ledit
dispositif n'étant pas lui-même placé en profondeur.
La présente invention concerne donc également un dispositif
tel que décrit précédemment auquel sont fixés par les ajutages des tuyaux
permettant notamment de tester la stérilité en profondeur, par exemple
dans un récipient de grande dimension de type allongé ou dans un endroit
difficilement accessible, en plaçant l'une des extrémités du tuyau à l'endroit
à tester. On peut d'ailleurs prévoir également d'aspirer l'atmosphère à l'une
des extrémités par l'intermédiaire d'une pompe reliée à l'autre ajutage.
Les exemples suivants sont plus particulièrement destinés à
mettre en évidence d'autres caractéristiques et avantages de la présente
invention .
Les exemples sont mis en oeuvre en utilisant un dispositif du
type de celui représe-lté aux figures annexées sur lesquelles:
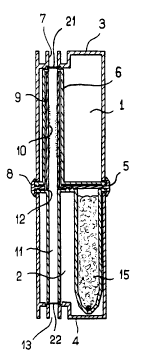
- la figure 1 re~résente une coupe selon un plan passant par
l'axe de rotation d'un dispositif selon l'invention en position de passage du
fluide;
- la figure 2 représente le même dispositif mais dans une autre
position où le support de microorganisme est placé dans le milieu;
- la figure 3 représente le dispositif après retour à la position
initiale;
- la figure 4 est une vue cavalière du dispositif des figures
là3.
La figure 1 représente un dispositif selon la présente
invention selon une section par un plan passant par l'axe de rotation des
deux compartiments l'un par rapport à l'autre.
~16~197
O 95/01451 PCT/FR94/00789
Ce dispositif est constitué de deux compartiments mobiles (1 et
2 ) reliés par une pièce de liaison ( 5 ), chacun des compartiments est
constitué de carters identiques ou pas (3 et 4) dans lequel est placé un
élément d'insertion qui, pour le compartiment supérieur, comporte un
S conduit tubulaire (6) sensiblement parallèle à l'axe de rotation, débouchant
à l'extérieur par un orifice (7) et par un orifice ( 8) en vis-à-vis du
compartiment inférieur. Le support (9) qui est sensiblement cylindrique et
appliqué dans le conduit tubulaire (6) est revêtu sur sa partie intérieure de
spores (10).
Le support (9) repose sur la surface située en vis-à-vis du
compartiment inférieur (12) à la surface de laquelle débouche un conduit
tubulaire en vis-à-vis du précédent (11) et dont l'extrémité (13) débouche à
l'extérieur. Le conduit tubulaire (11) peut contenir un indicateur physico-
chimique
Dans cette configuration on a ainsi constitué un canal qui
traverse l'ensemble du dispositif parallèlement à l'axe et dont une partie est
constituée par le support de la souche.
Le compartiment inférieur comporte, en outre, un orifice (14)
dont la dimension est telle qu'après rotation de 180 des deux compartiments
( 1 et 2 ) l'un par rapport à l'autre pour arriver à la configuration
représentée à la figure 4, le conduit tubulaire (6) est amené en coïncidence
avec ledit orifice et le support (9) tombe dans le milieu de révélation (15)
situé dans un réservoir (20) du compartiment inférieur.
Après une seconde rotation de 180, on ramène les deux
compartiments dans la position initiale représentée à la figure 3, mais le
support (9) est alors placé dans le milieu de révélation (15) mais isolé de
l'extérieur et peut alors être agité.
Il convient de remarquer qu'afin d'éviter des contaminations
extérieures, les orifices débouchant (7 et 13) comportent chacun un filtre
(21 et 22).
En outre, le canal tubulaire (11) est plus étroit à sa partie
supérieure afin de permettre le blocage du support (9).
Enfin, les extrémités du canal ( 7 et 13 ) sont pourvues
d'ajutages tels que 16 et 17 afin de permettre l'adaptation de tubulures si
cela est nécessaire afin de tester des stérilisations profondes ou afin de
W0 95/01451 ~ 7 lo PCT/FRg4/0078~
tester des atmosphères dans lesquelles on ne souhaite pas introduire le
dispositif.
La figure 4 représente une vue cavalière du dispositif selon la
présente invention sur laquelle on distingue les deux compartiments (1 et 2)
5 reliés par la pièce de liaison (5), l'un des conduits tubulaires débouchant
avec son ajutage (16) ainsi que la fenêtre de lecture (18) transparente qui
permet de voir les variations de couleurs du milieu de révélation ( 15).
E~EMPLE 1
Les essais n'ont été réalisés qu'avec les spores de Bacillus
stearothermophilus CIP 5281 = ATCC 7953 dans le cas de la stérilisation à la
vapeur d'eau.
1) Préparation de la sus~ension de spores, concentration de la suspension et
dénombrement microbien
1.1 Matériel
- Bouillon pour la congélation de la souche ( 1 )
. Extrait de viande de boeuf 3 g
. Peptone trypsique de caséine 5 g
. Glycérol 150 g
. Eau distillée Q~iP 1000 1
- Bouillon de première mise en culture (2)
. Extrait de levure 2,5 g
. Tryptone 5,0 g
. Glucose 1,0 g
. Eau distillée Q~P 1 000 1
25 - Gélose de sporuation répartie en fioles de Roux (3)
. Extrait de viande 10,0 g
. Extrait de levure 2,0 g
. MnSO4, H20
. Agar 23,0g
. Eau distillée Q~iP 1000 ml
1.2 Préparation de la suspension de spores
Ensemencement du bouillon (2) avec environ 106 spores
provenant d'un bouillon congélation à- 20C (1) dans lequel est conservé la
souche de Bacillus stearothermophilus CIP 5281 - Incubation à 56C pendant
35 24 heures.
1 9 7
- "o 95/01451 PCT/FR94/00789
- 11
Transfert de 3 ml environ de cette culture dans une fiole de
Roux contenant la gélose de sporulation. Faire subir à la fiole de Roux
diverses inclinaisons de facon à ce que l'inoculum vienne en contact avec
la totalité de la surface de la gélose ; rej eter ltinoculum en excès
Incubation de la fiole à 56C pendant 20 jours.
Observation de l'état de la culture au microscope: observer les
spores à la fuschine dilué ou au microscope à contraste de phase. Les
cellules végétatives doivent être lysées et les spores sont colorées en rose
très pâle.
Si la sporulation n'a pas débuté, recommencer l'essai.
Dans le cas où la sporulation a commencé, poursuivre
l'incubation jusqu'à ce que les cellules végétatives soient lysées.
Récupérer la culture solide avec de l'eau distillée stérile, en
grattant au besoin la surface de la gélose.
1.3 Concentration de la sus~ension
Répartir le liquide de récupération (coloré en jaune-brun)
dans des tubes à centrifuger. Réaliser trois lavages successifs de 15 minutes
chacun par centrifugation à 2 700 tours/minute: à chaque lavage, rejeter le
surnageant et reprendre le culot dans 5 ou 10 ml d'eau distillée stérile.
Transférer la dernière suspension (qui ne doit plus être
colorée en jaune-brun) dans un flacon Pyrex à bouchon vissé. Chauffer
30 minutes à 100C pour éliminer les formes végétatives restant éventuelles.
Conserver à + 4C.
Bien agiter la suspension avant chaque prélèvement, car les
spores sédimentent au fond du flacon.
1.4 Dénombrement de la suspension de s~ores
Dénombrement des spores après dilution convenable dans de
l'eau distillée stérile, inclusion en gélose Mueller Hinton Agar (Diagnostic
Pasteur, réf. 64884), 35 g/l, ~réparee extemporanément; incubation à 56C.
La suspension de spores doit titrer au minimum 107 spores/ml.
Vérifier l'absence d'amas de spores ou de débris organiques
volumineux par coloration à la fuschine diluée.
2) fixation des spores sur le support
On a testé différents supports:
WO 95tO1451 216 ~ 7 12 PCT/FRg4/00789
- de configuration plane, le verre, l'acier inoxydable, le caoutchouc et
le tissu,
- de configuration cylindrique, le verre, l'acier inoxydable et le
caoutchouc.
S Les dépôts ont été 100 ~11 de la suspension de spores à la surfacedes supports plans et dans la lumière des supports cylindriques et les spores
sont séchées à 37C .
3) RécuDération des spores fixées sur les supDorts
Après le dépôt de 100 ~,~1 d'une suspension de spores calibrées
10 sur les différents supports et séchage comme indiqué précédemment, le
support est mis dans un volume défini d'eau distillée stérile. La mise en
oeuvre de différentes méthodes permet de constater que l'utilisation de
Tween 80 à 0,5 % avec agitation est suffisante pour pouvoir décoller la plus
grande partie des spores alors que les autres méthodes se révèlent soit
lS difficiles à mettre en oeuvre soit insuffisantes dans leurs résultats.
La mise en oeuvre du dispositif tel que décrit précédemment
avec différents types de support permet la détermination du temps de
réduction décimale nommé DT à une température donnée. Cette réduction
décimale est le temps nécessaire pour inactiver 90 % des microorg~ni~mes
20 présents avant stérilisation, c'est-à-dire également le temps nécessaire pourréduire de 10 fois la valeur de la population microbienne initiale. Dans le
cadre d'une stérilisation on détermine la Dl2loc des supports en papier, en
verre, en acier inoxydable, en caoutchouc et en tissu de géométrie plane par
exposition des supports dans le dispositif selon la présente invention à
25 différents temps de stérilisation.
On trouve les résultats suivants:
Dl2loc papier = 1,9 min
Dl2lC verre = 2,3 min
Dl2lC acier inoxydable =2,4min
Dl2lC tissu = 2,3 min
Dl2lC caoutchouc =2,4min
Lorsqu'à la place des supports plans on prend des supports de
géométrie cylindrique, en verre, en acier inoxydable et en caoutchouc, on
trouve les résultats suivants:
~ 6~1~7
~~'0 95/01451 PCT/FR94/00789
13
Dl2lC verre = 2,5 min
Dl2lC acier inoxydable =2,4min
Dl2lC caoutchouc = 2,3 min
En conclusion, on peut retenir dans le nouvel indicateur
S biologique des supports dont la nature et la configuration sont
représentatifs des objets réellement soumis à la stérilisation, supports creux
en verre, acier ou caoutchouc, mais il paraît approprié d'utiliser de
préférence des supports cylindriques en verre qui donnent les temps de
réduction décimale les plus importants et donc la plus grande sécurité sur le
10 plan de la stérilisation.
4) Etude de la sensibilité
La technique mise en oeuvre dans le dispositif selon la
présente invention est une technique tout ou rienn. Pour tester la
sensibilité du dispositif on utilise un milieu de culture constitué d'un
15 bouillon de trypto-caséine-soja modiflé par addition de Tween 80 à 0,5 %. On
ajoute un rouge de phénol comme indicateur de pH. Cet indicateur de pH par
acidification du milieu passe de la couleur rouge à la couleur jaune lorsque
la culture est positive.
On effectue des essais avec un nombre très réduit de spores qui
20 ont conduit aux résultats suivants:
- pour 30 essais avec 2 + 1 spores, environ 80 % de cultures
positives en 24 h d'incubation,
- pour 30 essais avec 5 + 1 spores, 100 % de cultures positives en
24 h d'incubation.
Le seuil de sensibilité se situe donc à 5 + 1 spores.
Ainsi cette technique permet de mesurer une dimution en
logarithmes base 10 du nombre de spores après stérilisation, ce qui a pu être
vérifié par les essais en situation réelle.
Support cylindrique en verre portant 5.106 spores:
- temps d'exposition 3 min: 100 % de réponses positives
- temps d'exposition 6 min: 100 % de réponses positives
- temps d'exposition 9 min: 100 % de réponses positives
- temps d'exposition 12 min: 90 % de réponses positives
- temps d'exposition 15 min: 0 % de réponses positives
WO95/01451 2L6~197 14 PCT/FR94/0078
Le dispositif selon la présente invention permet d'obtenir des
résultats beaucoup plus satisfaisants que les indicateurs biologiques de la
technique antérieure, notamment ceux décrits par exemple dans Technique
Hospitalière n 493, Octobre 1986, p. 52-56.