Note: Descriptions are shown in the official language in which they were submitted.
21g9446
"GÉNÉRATEURS A ÉLECTROLYTE POLYMERE POSSÉDANT UN
SEL DE POTASSIUM PERMETTANT DE STABILISER LES
PERFORMANCES ET LA VIE UTILE DE LA BATTERIE"
La présente invention concerne les acc~1ml11ateurs à électrolyte
polymère, not~mment des génél~lew~ à électrolyte polymère comportant un
sel de potassium permettant de stabiliser les performances et la vie utile de
la batterie. Plus précisément, l'invention est relative à des génel~lew~ au
l0 lithium rechargeables contenant un sel de potassium distribué dans la
cathode, dans l'électrolyte polymère, ou dans ces deux derniers à la fois. En
particulier, la présente invention se rapporte à des générateurs
électrochimiques rechargeables, dalls lesquels les ions potassium introduits
sous forme d'ad~litifs tant au niveau de la cathode que de l'électrolyte
lS polymère établissent un traitement in situ et tout au long de la vie utile du générateur afin d'améliorer les performances en cyclage, notamment au
niveau de l'énergie et de la puissance. La présente invention concerne aussi
des a~l(lit1f~ à base de potassium distribués dans au moins un et meme deux
des const~ nt.C d'un générateur électrochirnique rechargeable au lithium,
20 de préférence l'électrolyte polymère et la cathode composite liée par un
polymère, dont l'effet est de stabiliser les performances d'énergie et de
puiss~nce au cyclage.
L'invention décrit aussi des moyens ~rerérés pour introduire le
25 potassium dans le générateur par l'un ou l'autre des constih1ant.~ de ce
dernier et décrit comment le potassium se distribue dans plus d'un
constituant de façon à optimiser le fonctionnement des électrodes au
cyclage. L'additif possède l'effet bénéfique du maintien de la morphologie
de l'anode de lithium au cyclage et d'optimiser le comportement de la
30 cathode au cyclage.
La vie utile d'une batterie est dépendante de plusieurs facteurs dont
la réversibilité des processus électrochimiques aux deux électrodes.
L'addition de métaux alcalins, alcalino-tell~u~ ou de transition à la matière
35 active des cathodes de piles au lithium est connue et utilisée généra1ement
pour stabiliser ou optimiser les cathodes à insertion (FR 2 616 013,
US 5 013 620, US S l 14 809, FR 2 573 250). Les a(l(litif~ utilisés visent
généralement à stabiliser les structures d'insertion et parfois à optimiser le
2~299~46
nombre de sites disponibles dans la structure hôte (WO 91/02383,
US 4 668 594). Dans certains cas, les ~ litif~ visent également à augmenter
la conductivité électronique des matériaux d'insertion (US 4 965 151,
JP 89/15317, JP 89/67063, US 5 114 811, US 5 147 737). Dans la plupart
des cas connus, les métaux d'addition sont intégrés dans la structure hôte et
sont présents à des taux relativement élevés variant entre 1 et 50%
relativement au métal de transition principal. Ces additifs sont généralement
immobilisés dans la structure hôte d'insertion et ne diffusent pas dans les
autres constituants du générateur, notamment l'électrolyte et l'anode.
Advenant le cas où des sels de ces métaux d'addition seraient solubles dans
l'électrolyte, ils seraient réduits par le lithium métallique et ne pourraient
pas rester en équilibre dans le générateur. De plus, à notre connaissance,
aucun exemple d'additif présent dans plus d'un constituant d'un générateur
au lithium n'a été décrit jusqu'à présent.
En effet, peu de ces métaux sont chimiquement compatibles avec
une anode de lithillm et capables de coexister avec les sels de lithillm en
solution dans l'électrolyte du générateur. Le potassium est, avec le
magnésium, un des seuls métaux non réduit (thermodynamiqllement et
cinétiquement) par le lithi-lm en milieu aprotique, et constitue donc un
m~tçri~l unique pour mettre en oeuvre la présente invention.
L'lltilis~tion d'électrolytes polymères à cations alcalin mixtes a été
mentionnée lors de mesures de conductivité (ACFAS 1993) et pour la
constihltion d'électrolytes à conduction véhiculaire ~J.S. 5 350 646). Dans
aucuns cas, il n'est fait mention d'un équilibre entre les cations mixtes de
l'électrolyte et les matériaux d'électrode ou d'un effet bénéfique sur le
cyclage du générateur ou sur l'anode de lithium.
L'invention a pour objet un effet bénéfique observé sur la
stabilisation des caractéristiques électrochimiques du matériau de cathode
V20s, présçntement utilisé dans la technologie des accllm~ teurs à
électrolyte polymère, et ~imlllt~1lémçnt une amélioration de la réversibilité
de la dissolution-redéposition de l'anode de lithium et de sa morphologie
afin d'améliorer les performances et la vie utile de la batterie.
21g9446
L'invention a aussi pour objet des améliorations obtenues par
l'introduction d'un sel de potassium, notamment le KTFSI
(trifluorométhanesulfonyl imidure de pot~csi~lm), dans le séparateur
polymère et/ou dans le polymère constituant la composite positive ou
5 cathode.
L'invention a aussi pour objet d'introduire des ions potassium dans le
polymère lesquels se retrouveront subséq~lemment aux électrodes par voie
électrochimique .
L'invention a aussi pour objet de permettre la fabrication d'une
batterie caractérisée par un cyclage amélioré, tant au niveau de l'énergie et
de la plli.cs~nce, obtenu par addition in situ d'un agent stabilisateur, en
l'occurrence le potassium, sans nécessairement passer par une voie
15 chimique.
L'invention a encore pour objet de permettre l'introduction d'un agent
stabilisateur, notamment dans le sépalateul à électrolyte polymère, et/ou
dans la cathode de fa,con à ce qu'il se répande uniformément dans toute la
20 pile, de l'interface Li au collecteur de la positive.
L'invention a aussi pour objet de produire des effets dépolarisants
lors de la recharge (baisse de voltage de plus de 20 mV en situation de
dendrites, contact de l'anode avec la cathode) suite au développement
25 morphologique du lithium (passage d'une surface de lithium plane à une
surface rugueuse), ce qui permet à la pile de cycler à nouveau de façon
réversible sur plusieurs dizaines de cycles sans qu'il y ait apparition de
dendrites.
~fin d'atteindre ces objets et surmonter les désavantages de l'art
antérieur, l'invention propose un générateur au lithium rechargeable
constitué d'au moins une anode de lithium, d'une cathode réductible aux
ions lithillm liée avec un premier polymère, et d'un électrolyte polymère
co~ lellant un second polymère, et un sel de lithillm en solution dans le
second polymère. Le générateur au lithi~lm selon l'invention est caractérisé
en ce qu'il renferme des ions pot~ccillm qui sont distribués dans au moins
l'un parmi la cathode et l'électrolyte polymère, la concentration à l'équilibre
2199~6
-4-
du lithium et du potassium dans le second polymère exprimée en O/(Li +
K), se situant entre environ 8/1 et 40/1, avec un rapport molaire Li/K
compris entre environ 0,2 et 15. Les ions potassium sont choisis de façon à
stabiliser les perforrnances du générateur au cyclage, au niveau de l'énergie
5 et de la puissance.
En général, les ions potassium sont introduits à l'aide de sels de
potassium. Le sel de potassium peut être distribué dans la cathode, dans
l'électrolyte polymère ou à la fois dans l'électrolyte polymère et la cathode.
Les premier et second polymères peuvent être identiques ou
dirrére~ selon les circonstances ainsi que cela apparâîtra évident à
l'homme de l'art.
Parmi les sels de potassium qu'on peut utiliser dans le cadre de
l'invention, on peut mentionner KN(RFS02)2, KN(FS02)RS02, BF4,
KPF6, KRFS03 où F est un perhalogénoallcyl ou perhalogénoaryl et où R
un radical organique pouvant être pareil ou différent, et autres sans que
cette liste soit li~llilalive. On peut incorporer les ions potassium dans la
20 cathode sous forme partiellement ou complètement réduite.
De préférence, la cathode comporte au moins un composé choisi
parmi les chalcogénures, les oxydes ou les sulfures de métaux de transition,
par exemple du pentoxyde de vanadium.
Le composé constituant la cathode peut être choisi parmi ceux
représentés par la formule
[ R Sx]n
dans laquelle les groupements R sont des di-ou tri-radicaux. Des exemples
30 de di-radicaux sont par exemple le soufre, les groupements aL~ylène de 2 à
10 atomes de carbone, les groupements oxyalkylène possédant de 4 à 12
atomes de carbone et de 1 à 4 atomes d'oxygène, les radicaux cycliques tels
que le phénylène substitué ou non, le thi~llia7.Qdi-yl, l'ox~ odi-yl. Un
exemple de tri-radical est dérivé de la 1,3,5-triazène sur laquelle sont
35 substitués trois atomes de soufre. n est le degré de polymérisation et est
compris entre 2 et 100,000, de pl~rélellce entre 10 et 10,000 et x 2 ~, le
potassium étant alors présent dans la cathode sous forme de R-S-K, où R
2199qg6
-5-
est tel que défini ci-dessus. Un mél~n~e de polymères colllplellant au
moins un polymère conducteur électronique et un composé de type [-R
Sx]n peut également constituer la cathode. Il peut aussi etre choisi parmi
ceux représentés par la formule
MXz
dans laquelle M est un métal de transition, X représente un chalcogène ou
un halogène, et z varie entre 1 et 3, le potassium étant alors présent dans la
cathode sous forme de KX, où X est tel que défini ci-dessus.
L'invention concerne aussi une cathode réductible par les ions
lithium pour générateur au lithium rechargeable, liée à un polymère, des
ions potassium étant distribués dans la cathode en une quantité telle que la
concentration en lithium et en potassium dans un électrolyte polymère d'un
générateur constitué de la cathode lorsque le générateur a atteint l'équilibre,
exprimée en O/(Li + K) varie entre environ 8/1 et 40/1 tandis que le rapport
molaire Li/K est compris entre environ 0,2 et 5.
L'invention concerne aussi un électrolyte polymère pour générateur
au lithium rechargeable, des ions potassium étant distribués dans
l'électrolyte en une quantité telle que la concentration en lithium et en
pot~ssillm dans l'électrolyte polymère d'un générateur comportant ce dernier
lorsque le générateur a atteint l'équilibre, exprimée en O/(Li + K) varie
entre environ 8/1 et 40/1 tandis que le rapport molaire Li/K est compris
entre environ 0,2 et 5.
La quantité de sel de potassium, notamment KTFSI par rapport au
sel de lithium utilisé cour~mment dans le générateur à électrolyte polymère,
est variable et se situe de préférence dans un ratio de KlLi inférieur à 5
préférentiellement entre 0,2 et 1.
Lorsque la cathode contient du V2Os, les concentrations m~im~les
en KaV2Os, sont de prérelellce celles où a < 0,06 ou encore K/V est
inférieur ou égal à 0,03.
D'autres caractéristiques et avantages de la présente invention
ressu~ onl des dessins annexés, sur lesquels:
2199q4,6
la figure 1 est un graphique représentant des résultats comparatifs
d'une pile selon l'invention avec ions potassium et une autre de l'art
antérieur, sans potassium;
la figure 2 est un graphique comparant les performances de trois~ géné~ selon l'invention dont la composition en Li/K est variable;
la figure 3 représente une analyse chimique par fluorescence des
rayons X(EDX) de l'électrolyte en coupe cryogénique pour une pile O/M -
40; Li/K= 0,8, après 200 cycles;
la figure 4 représente la même analyse que la figure 3, mais pour~0 l'électrode positive;
la figure 5 représente une analyse chimique par EDX de l'électrolyte
de la même pile que celle illustrée en figures 3 et 4, avant cyclage,
~lémonlrant une plus forte concentration de sel de potassium (rapport K/S)
qu'après le cyclage (figure 3);
la figure 6 est une micrographie obtenue par microscopie
électronique à transmission (MET) vérifiant la présence de potassium dans
la structure de l'oxyde de vanadium;
la figure 7 représente une analyse micrographique par microscopie
électronique en transmission selon le spectre EDX correspondant obtenu au~0 coeur d'un grain d'oxyde de vanadium démontrant la présence de potassium;
la figure 8 représente une analyse chimique par EDX de la surface
du lithium en contact avec l'électrolyte à l'int~rf~ce Li /Électrolyte
polymère;
la figure 9 est une coupe cryogénique d'une pile Li-Électrolyte~5 polymère/Électrolyte polymère-Li avec KTFSI dans l'électrolyte;
la figure 10 est une coupe cryogénique ~imil~ire à celle de la figure
9, sans KTFSI;
les figures 11 et 12 sont des vues comparatives (75 ) au microscope
électronique à balayage (MEB) de la surface du lithium à l'interface~0 Li /SPE des piles 6 et 7 dont il est question aux figures 9 et 10;
les figures 13 et 14 sont des coupes cryogéniques des piles 1 et 3
dont il est question sur les figures 1 et 2;
la figure 15 illustre l'évolution de la valeur m~im~le de la puissance
inst~nt~née Pi en fonction du cyclage pour les piles 1 et 2 dont il est~5 question à la figure 1;
la figure 16 illustre des courbes co~ )alalll le comportement des
piles 9 et 10 sans et avec K au niveau de leur puissance soutenue; et
2199~6
-7-
la figure 17 est un spectre EDX de l'électrolyte de la pile 11
mon~ l la présence de K (originalement inséré par voie chimique dans le
V2Os) équilibré entre la cathode et l'électrolyte polymère.
S L'addition de potassium, par exemple sous forme de KN(CF3SO2)2
dans l'électrolyte permet de m~ un taux d'lltilis~t10n de la matière
active de la cathode supérieur à ce qui est obtenu dans le cas d'un
générateur identique ne conten~nt pas de potassium. On montre également
par des analyses élémentaires après cyclage que le potassium introduit par
le biais de l'électrolyte se distribue également dans toutes les composantes
de la pile sans toutefois se déposer à l'anode ce qui confilme la stabilité des
électrolytes à cations alcalins mixte (Li+ + K+) utilisés dans les générateurs
de l'invention.
Un autre bénéfice de la présente invention concerne la qualité du
contact entre le lithium métallique et l'électrolyte polymère qui est
maintenue lors des cycles de décharge/charge, ce qui contribue grandement
aux excellentes propriétés de cyclage et de p~ s~nce des génélaleul~ de
l'invention.
La possibilité d'introduire du potassium en équilibre dans plus d'une
composante du générateur par le biais du matériau de la cathode est
également selon l'esprit de l'invention. Dans ces cas, l'addition de potassium
peut être faite en pré-insérant chimiqllement le potassium dans la structure
de l'oxyde de vanadium par le moyen d'une solution d'un sel oxydable tel
que le KI dans un solvant aprotique comme l'acétonitrile de façon à obtenir
du KXV2Os et de l'iode (ou triiodure). On montre également dans ces cas
par analyse élément~ire que le potassium est également présent dans
l'électrolyte du séparateur après cyclage et analyse de la pile.
Les exemples qui suivent sont donnés à titre purement illustratif et
sans caractère limitatif.
F.~emrle 1
Dans cet exemple, on compare les résultats obtenus en cyclage
(figure 1) d'une pile ayant du K+ incorporé in situ dans le film polymérique
sép~eur (pile 1) avec une pile n'ayant pas de K+ mais seulement du Li+
219944~
(pile 2). Le K~ est introduit dans la pile sous forme de sel de K appelé bis-
trifluorométhane sulfoneimidure de K (KTFSI) tout à fait compatible avec
la pile à électrolyte polymère ayant une anode métallique de litl~ m Les
piles 1 et 2 sont constituées d'une anode de lithium de 35 ~lm d'épaisseur
supportée sur feuillard mince de nickel et d'une cathode composite de
composition volumique approximative de 40% d'oxyde de vanadium, de
10% de noir d'acétylène et de 50% d'un copolymère d'oxyde d'éthylène. Ce
copolymère comporte environ 80% d'oxyde d'éthylène tel que décrit dans
les brevets Eur. N~O 013 199, U.S. N~ 4 578 326 et U.S. N~ 4 758 483,
auquel est ajouté l'électrolyte bis-trifluorométhane sulfoneimidure de
lithium (LiTFSI) et/ou de potassium (KTFSI) dans un rapport oxygène sur
métal ionique O/M de 30/1. La cathode d'une capacité utile voisine de
4C/cm2 (1 Li/V) est enduite sur un collecteur de nickel mince. L'épaisseur
du séparateur ou de l'électrolyte polymère est de 30,um et est également
composé de copolymère à base d'oxyde d'éthylène. Le rapport Li/K est égal
à 0,8 dans le cas de la pile 1. Les piles de surface utile de 3,89 cm2 sont
assemblées par pressage à chaud à 80~C.
Les piles sont cyclées à densité de courant imposé de l'ordre de
100 ~LA/cm2 en décharge et de 50 11A/cm2 en charge à 60~C entre des
limites de 3,3V et 1,5V permettant ainsi de réaliser des décharges profondes
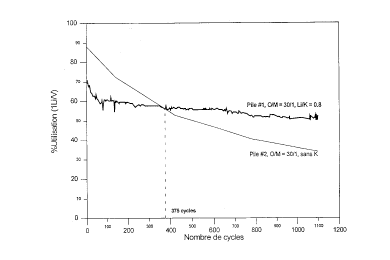
(100% DOD). La figure 1 illustre l'évolution de la capacité cyclée ou plus
exactement du ~/OUtilisation (capacité cyclée au cycle n sur la capacité
obtenue au cycle 1) en fonction du nombre de cycles. Le taux d'utilisation
initial de la pile 1 est plus faible que la pile 2. Par contre, la décroissance de
la capacité de la pile 1 se stabilise après environ 100 cycles à un taux
beaucoup plus faible (6 à 7 fois) que la pile 2. L'effet de stabilisation dû à la
présence de K dans la pile est donc perçu au-delà de 100 cycles et permet
ainsi une espérance de vie utile de plus de 1000 cycles pour le générateur.
Cette stabilisation devient très intéressante particulièrement vers 375 cycles
où a lieu le croisement des deux courbes de la perte de capacité en fonction
du nombre de cycles.
Exemple 2
Dans cet exemple, on compare les performances de 3 génélal~ws
dont la composition en Li/K est variable. Le KTFSI est introduit dans
l'électrolyte polymère du séparateur. Les piles sont essentiellement
2l994~6
composées du même type d'anode et de cathode que dans l'exemple 1. La
méthode d'assemblage est également identique ainsi que les densités de
courant imposées en décharge et en charge sous les mêmes limites de
voltage. Toutes les piles sont composées d'une quantité totale de sel
O/M=30/1. Le rapport Li/K dans le générateur est égal à 0,8 pour la pile 1,
de 7 pour la pile 3 et de 25 pour la pile 4. La figure 2 présente l'évolution
du %Utilisation de ces trois piles en fonction du nombre de cycles.
L'évolution de la pile 3 en cyclage et en résistance interne se comporte de
façon simil~ire à la pile 1. En effet, pour ce type de matériau d'électrode
une stabilisation de la pente de décroissance est également observée après
100 cycles et est tout à fait simil~ire à celle de la pile 1 alors que la
résistance interne se stabilise entre le looe et le 35oe cycle pour chacune
des piles, la résistance interne de la pile 3 étant légèrement supérieure. La
pente de décroissance de la pile 4 est beaucoup plus élevée (4 fois environ)
que celle de la pile 3 ou de la pile 1 et du même ordre de grandeur que celle
de la pile 2. La concentration de K dans le générateur est donc trop faible
pour avoir un effet bénéfique d'additif stabilisateur. Ce résultat permet de
conclure qu'un ratio inférieur ou égal à 25 en Li/K mais supérieur ou égal à
7 en Li/K est sllffisant pour stabiliser la perte de capacité en cyclage du
générateur. La concentration m~im~le en K peut être de Li/K=0,2 avec un
O/M=8 pour respecter la compatibilité électrochimique du générateur avec
son anode de lithium.
Exemple 3
Dans cet exemple, on désire illustrer que l'additif de potassium se
disperse de façon homogène dans tout le générateur, qu'il soit introduit dans
l'électrolyte séparateur etlou la cathode. L'exemple présent (pile 5) illustre
le cas où le KTFSI est introduit dans le séparateur. La quantité de sel O/M
est égale à 40/1 alors que le ratio Li/K dans le générateur est égal à 0,8.
L'épaisseur du séparateur est de 40 microns alors que les autres
composantes du générateur sont identiques à la pile 1. Après 200 cycles,
cette pile a été ~x~ ée par fluorescence des rayons X (EDX) suite à une
fracture cryogénique permettant d'avoir une vue en coupe de la pile.
La composition relative en "K+" dans l'électrolyte du séparateur et
dans la positive est identique, tel que démontré aux ~lgures 3 et 4 par le
ratio des int~n~ités des pics représentant le K et le S. La source de S dans le
219999~
-10-
générateur provient de l'anion TFSI des sels de Li et K. Il a été également
observé que le ratio K/S était supérieur dans l'électrolyte avant cyclage
(figure 5) démontrant bien que le K+ se redistribue dans tout le générateur
et qu'il existe en équilibre dans le générateur dans au moins deux
5 composantes.
La présence de K dans la stlucture de l'oxyde de vanadium (figure 6)
a également été vérifiée par microscopie électronique à tr~nsmission (TEM)
clarifiant également hors de tout doute la présence de K (en équilibre) à la
10 cathode au niveau des particules solides et de l'électrolyte polymère
s~nt comme liant. Par contre, la quantité de K intercalée dans la
st~ucture est faible par rapport à la concentration dans le liant (figure 7) et
ne perturbe donc pas, en fonction de l'utilisation du générateur, l'équilibre
entre le K+ et le Li+ dans l'électrolyte polymère.
Cet équilibre existe probablement également au niveau de l'int~ ce
Li/Électrolyte polymère. En effet, la figure 8 montre clairement l'absence de
potassium réduit (K) à la surface du Li métallique (confinn~nt ainsi la
stabilité apparente des ions K en présence de l'anode de lithi~ en milieu
20 électrolyte polymère justifiant par le fait même que le K+ est tout à fait
compatible avec l'anode). Le lithium n'est pas détecté par cette technique
mais l'oxygène (O) qui le recouvre est clairement visible sur le spechre. Il
est donc probable que le K+ soit également en équilibre très près de la
surface du lithillm puisqu'il n'y a pas de réduchon de potassium sur l'anode.
Ainsi, par ces analyses, il est établi que le K est présent dans plus de
2 composantes et/ou sections de la pile: le séparateur à élecholyte
polymère, le liant de la cathode qui est composé du même électrolyte que le
sépal~leur et le grain de l'oxyde de la positive. La probabilité de rehouver
30 du potassium ionique à l'interface Li/polymère n'est pas exclue également.
Exemple 4
Afin de démontrer à nouveau l'effet bénéfique de la présence de K+
à l'anode de lithillm 2 piles (6 et 7) symétriques ayant des anodes et des
35 cathodes en lithium métallique ont été asseml~lées. Les figures 9 et 10
illushrent encore une fois une vue en coupe cryogénique au microscope
électronique à balayage (MEB) de ces deux piles alors que les figures 11 et
2199~46
- 1 1-
12 représentent une vue de surface. La pile 7 a été assemblée avec du
m métallique initialement de 35 llm supporté sur un feuillard de
nickel de 10 ~n. L'épaisseur d'électrolyte étail d'environ 30 ~lm.
L'électrolyte contenait seulement du LiTFSI dans une concentration de
5 30/1. La pile 6 est simil~ire à la pile 7 à l'exception de deux dirrerellces: elle
est constituée de Li d'épaisseur de 22 ~lm et elle contient une quantité de sel
O/M=20/1 avec un ratio Li/K=2. Une autre pile (pile 8, non illustrée) a
également été expérimentée et contenait une quantité de sel O/M=25 avec
un ratio de Li/K=5. Chacune des piles a été cyclée à des densités de courant
10 et dans des conditions expérimentales simil~ires à celles décrites dans
l'exemple l; une électrode de lithium étant l'anode qui s'oxyde à un courant
double par rapport à sa réduction et une seconde électrode agicsant à titre
de cathode où l'on y observe les Cull~ S opposés. Les temps de cyclage
sont ajustés de façon à ce que la même quantité de coulombs soient
15 déchargés et rechargés. La pile 7 a réalisé 24 cycles avant de montrer des
courts-circuits internes alors que la pile 6 a été volonl~irclllent arrêtée après
39 cycles et n'avait toujours pas démontré de dendrites majeures comme la
pile 7. Les lithiums observés aux figures 9 à 12 sont ceux ayant été cyclés
comme anode donc une déposition ou un placage à une densité de courant
20 de l'ordre de 50 ~LA/cm2.
La morphologie déveioppée de l'anode de lithium de la pile 7 est
trois fois supérieure à celle de la pile 6 et ce pour une durée de cyclage
inférieure (presque la moitié moins de cycles). La seule dirrérence majeure
25 entre ces deux piles est la présence de KTFSI dans la pile 6. Ainsi, ces
photos démontrent très clairement l'effet très bénéfique du K sur la
profilométrie du lithium cyclé et ainsi sur la durée de vie de la batterie. Les
microscopies vues de face sont également très révélatrices. Des conclusions
~imil~ires ont été réalisées suite à l'observation de la pile 8 qui a réalisé 2030 cycles.
Exemple 5
Dans cet exemple, on reprend les piles 1 et 3 en analyse post-mortem
(vue en coupe cryogénique) pour illustrer (figures 13 et 14) l'état final de la
35 morphologie des différents constituants de la pile vus au microscope
électronique à balayage (MEB). Il faut rappeler que la pile 1 a réalisé 1100
cycles et la pile 3 près de 600 cycles. Comme on peut le constater, les films
219g4~6
-12-
d'électrolyte polymère et de cathode sont encore bien distants et on
remarque que la morphologie macroscopique du lithium est presque
inexistante we de la surface de l'électrolyte polymère (le lit~ m s'étant
dél~miné de l'électrolyte polymère amène à conclure sur une morphologie
de Li faiblement développée). En effet, des expériences antérieures ont bien
démontré que la vue de la surface de l'électrolyte polymère située à
l'interf~ce de l'anode représentait l'image miroir de la surface du lithium.
L'effet imhibiteur du potassium sur le développement de la morphologie du
lithillm est également (lémontré d'après ces résultats.
Exemple 6
Dans cet exemple, on confirme l'effet bénéfique de l'additif K+ sur
l'évolution de la puissance instantanée en fonction de la vie utile du
générateur. Les deux piles investiguées sont essentiellement les mêmes que
celles de l'exemple 1. La puissance inst~nt~née (Pi) est déle. ~ ée lorsque
le générateur est en pleine charge. Des (lensités de courant (I) de l'ordre de
1 à 5 mA/cm2 sont imposées sur la pile durant 20 secondes. Entre chaque
appel de puiSs~nce, la pile est laissée au repos durant 120 secondes. Le
voltage (V) final de chaque impulsion est alors enregistré et la puissance
inst~nt~née (mW) est donnée par la relation Pi=VI. La figure 15 illustre
l'évolution de la valeur m~xim~le de Pi en fonction du cyclage. On peut
constater que la puissance de la pile 1 se stabilise entre 200 et 600 cycles,
ce qui n'est pas observé pour la pile 2. De facon simil~ire au cyclage, la pile
2 présente une puiss~nce in~t~nt~née plus élevée lors des 200 premiers
cycles mais ne se stabilise jamais. La présence d'une quantité de K dans le
rapport Li/K=0,8 est donc très bénéfique pour la stabilisation de la
puissance instantanee. Les résistances internes des piles sont également
indiquées à la figure 15. La résistance interne de la pile 1 est légèrement
supérieure à celle de la pile 2 pour les 100 premiers cycles alors qu'au 3ooe
cycle, la valeur de la résistance interne de la pile 2 est plus élevée. Cette
différence peut être à l'origine des meilleures performances en pui~s~nce de
la pile 1.
F~mple 7
Dans cet exemple, on compare les comportement~ des piles sans et
avec K au niveau de leur puiss~nce soutenue (courbe de Ragone pour des
configurations de pile optimisée pour les collecteurs métalliques). La pile 9
2199~96
-13-
(figure 16) ne contient pas de K et est de même nature que la pile 2 citée
dans l'exemple 1. La pile 10 est exactement identique à la pile 3 citée à
l'exemple 2. La quantité de K est introduite dans l'électrolyte polymère par
le composé KTFSI à raison d'une concentration de Li/K = 7 (O/M=30).
L'assemblage et le cyclage des piles sont identiques aux exemples
précédents.
Comme déjà mentionné, l'énergie à fail)le puissance de la pile 9 est
supérieure à celle de la pile 10 étant donné son taux d'u~ tion (jusqu'à
environ 375 cycles) plus élevé. La puissance initiale est également plus
elevée que la pile ayant du K. Par contre, après 200 cycles, la pile 9 n'ayant
pas de K voit son énergie spécifique (Wh/~g) diminuer considérablement
spécialement à puissance élevée de l'ordre de plus de 200 W/l~g, ce qui n'est
pas le cas de la pile 10. En effet, quoique plus faible au début de la vie utiledu générateur, la puissance soutenue de la pile ayant du K se maintient et ce
pour plus de 300 cycles, ce qui démontre l'effet stabilisateur apporté par le
K dans le générateur au lithium à électrolyte polymère.
Exemple 8
Dans cet exemple, on démontre que l'équilibre des espèces Li et K
peut être obtenu dans au moins 3 composantes soit l'oxyde de v~n~ m le
polymère liant la cathode et le polymère de l'électrolyte grace à l'addition
chimique du potassium dans la structure de l'oxyde de vanadium par le
moyen d'une solution de KI dans l'acétonitrile de façon à ol~tenir du
KXV2Os et de l'iode (ou triiodure). Après cyclage du même type décrit
dans l'exemple 1, la pile 11 a été ex~minée par fluorescence des rayons X
(EDX) suite à une fracture cryogénique permettant d'avoir une vue en coupe
de la pile. La configuration électrochimique de la pile 11 est identique à
celle de la pile 1 à l'exception que l'électrolyte ne contient pas de sel de
potassium et que l'oxyde de vanadium V2Os contient environ 0,18 mole de
K. Le spectre EDX est illustré à la figure 17. On peut remarquer la présence
de K dans le polymère de l'électrolyte et/ou de la cathode alors qu'aucun
potassillm n'a été introduit dans l'électrolyte de départ ou le polymère liant
la cathode.
21g9~4.6
-14-
Il est entçndll que l'invention n'est pas reslleillle aux exemples
donnés ci-dessus, et que des modifications et altçrn~tives sont possibles
sans pour cela sortir du cadre de l'invention.