Note: Descriptions are shown in the official language in which they were submitted.
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
DISPOSITIF D'IONOPHORESE POUR L'ADMINISTRATION
TRANSCUTANEE D'UN PRINCIPE ACTIF
DE TYPE OLIGOSACCHARIDE ANIONIQUE
L'invention concerne un dispositif d'ionophorèse
pour l'administration transcutanée d'un principe actif de
médicament de type oligosaccharide anionique et en
particulier d'un oligosaccharide anionique de synthèse
ayant, entre autres, des activités antithrombotiques et/ou
anticoagulantes.
La coagulation sanguine est un phénomène
physiologique réputé pour être complexe. Certains stimuli
tels que l'activation de contact et les facteurs
tissulaires, déclenchent l'activation successive d'une série
de facteurs de coagulation présents dans le plasma sanguin.
Quelle que soit la nature du stimulus, les étapes
finales sont identiques : le facteur X activé (Xa) active le
facteur II (également appelé prothrombine), lequel sous sa
forme activée (facteur Iia, également appelé thrombine)
provoque la protéolyse partielle du fibrinogène soluble avec
libération de la fibrine insoluble, constituant principal du
caillot sanguin.
Dans les conditions physiologiques normales,
l'activité des facteurs de coagulation est régulée par des
protéines telles que l'antithrombine III (AT III) et le
cofacteur II de l'héparine (HC II), qui sont également
présentes dans le plasma. L'AT III exerce une activité
inhibitrice sur un certain nombre de facteurs de coagulation
et notamment sur les facteurs Xa et Iia.
L'inhibition du facteur Xa ou du facteur Iia
constitue donc un moyen privilégié pour obtenir une activité
anticoagulante et antithrombotique puisque ces deux facteurs
interviennent dans les deux dernières étapes de la
coagulation, lesquelles sont indépendantes du stimulus
déclencheur.
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
2
Le pentasaccharide de formule (I)
coo-
OS03 OS03 OS03
O O O O p t
OH OH O OS03 0 OKO O =OK
K~ ~ OH
t =
HHR OH UliSO3, O S 03- !tt{S03
avec R représentant -COCH3 ou - S03-
présente une structure appropriée pour la liaison à
l'AT III. Ce composé (R =-S03-) a été obtenu il y a environ
une dizaine d'années par synthèse chimique totale (P.Sina
et al, Carbohydrate Research (1984), 132 C5).
Depuis, un certain nombre d'oligosaccharides
anioniques de synthèse, obtenus par synthèse chimique totale
et ayant des activités antithrombotiques et anticoagulantes,
ont été décrits dans la littérature (cf, par exemple, EP-A-
0084999, EP-A-0113599, EP-A-0165134, EP-A-0301618, EP-A-
0454220 et EP-A-0529715).
Les activités anticoagulantes et antithrombotiques,
que peuvent posséder de tels oligosaccharides, font de ces
derniers des principes actifs utiles en thérapeutique
humaine.
Malheureusement, du fait de leur masse moléculaire
assez élevée, de leur forte charge anionique et de leur
hydrophilie, ils ne peuvent être administrés par voie orale
car ils ne passent pas la barrière gastrointestinale et ils
sont essentiellement administrables par voie parentérale,
par exemple, voie sous-cutanée ou voie intra-veineuse.
On sait en pareil cas qu'une alternative à la voie
parentérale, serait la voie transdermique puisque les
composés n'ont pas à traverser le tractus' gastrointestinal.
Mais on a pu constater que les oligosaccharides du type -
précité ne pénètrent pas dans la peau avec une vitesse
suffisante pour que les concentrations systémiques
atteignent des valeurs thérapeutiques efficaces.
On sait que l'ionophorèse peut permettre
d'administrer à un sujet, par voie transcutanée, certains
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
3
principes actifs, généralement consistant en composés de
faibles poids moléculaires à caractères ionique.
Pour ce faire, on opère à partir d'une solution
aqueuse ou d'un gel aqueux renfermant le principe actif sous
une forme au moins partiellement ionisée, en appliquant un
signal électrique entre, d'une part, une première électrode,
dite électrode active, ayant même polarité que les ions du
principe actif à administrer et se trouvant en contact avec
un élément réservoir, qui renferme le principe actif et se
trouve placé au contact d'une première zone de la peau du
sujet, et d'autre part, une deuxième électrode dite contre-
électrode ou électrode passive, de polarité opposée à celle
associée au principe actif, qui est placée, directement ou
par le biais d'un électrolyte indifférent, au contact d'une
deuxième zone de la peau du sujet distincte de la première
zone. Lors du passage du courant, généré_par application du
-
signal électrique entre les électrodes, dans le circuit
ainsi réalisé, les ions du principe actif migrent, à
l'opposé de l'électrode de même polarité (électrode active),
à travers la peau et les tissus du sujet, vers l'électrode
de polarité opposée (contre-électrode) et se retrouvent
ainsi à passer dans le système circulatoire du sujet.
En étudiant la possibilité d'un passage transcutané
de dérivés du type des oligosaccharides à caractère
anionique par la technique d'ionophorèse, en faisant appel à
des électrodes réutilisables habituellement employées en
ionophorèse telles que les électrodes en carbone, platine ou
titane, les demanderesses ont observé que les flux
transcutanés obtenus pour lesdit dérivés étaient très
inférieurs aux flux qu'il conviendrait d'atteindre pour
correspondre à une administration thérapeutique.
La citation EP-A-0556112 concerne un dispositif
d'ionophorèse pour l'administration transcutanée d'un
principe actif de médicament, notamment de type anionique,
qui comporte un ensemble électrode négative constitué d'une
électrode négative, dite électrode active, en contact avec
un élément réservoir contenant un électrolyte renfermant le
principe actif sous une forme au moins partiellement
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
4
ionisée, ledit élément réservoir étant agencé pour assurer,
lorsqu'il est placé au contact d'une zone de la peau d'un
sujet, un continuum conducteur ionique entre ladite
électrode négative et ladite zone, un ensemble électrode
positive constitué soit (i) d'une électrode positive seule
ou bien, de préférence, (ii) d'une électrode positive en
contact avec un élément réceptacle contenant au moins un
électrolyte, ledit élément réceptacle étant agencé pour
assurer, lorsqu'il est placé en contact d'une portion de la
peau du sujet, un continuum conducteur ionique entre
l'électrode positive et ladite portion, et un générateur de
signaux électriques connectable aux deux électrodes,
l'électrode négative en contact avec l'élément réservoir
étant formée, au moins en partie, d'un composé métallique
ionisable, dont les ions métalliques sont susceptibles
d'être réduits électrochimiquement en le métal correspondant
et de former avec ledit métal un système réversible
électrochimiquement, de manière à constituer, au moins au
cours du fonctionnement du dispositif, une électrode
négative réversible et le générateur étant agencé pour
appliquer entre les électrodes des signaux électriques de
tension moyenne telle que la densité du courant moyen généré
entre les électrodes soit comprise entre 0,03 et 0,5 mA/cm2.
La mise en oeuvre du dispositif d'ionophorèse de la
citation EP-A-0556112 avec des principes actifs de type
anionique est illustrée essentiellement par l'utilisation
d'un produit de masse moléculaire peu élevée, à savoir le
valproate de sodium, en concentration allant de 5 % à 15 %
en poids, soit 0,3 molaire à 0,9 molaire, ce qui représente
plus de 50 mg par cm2 d'électrode et par mAh de courant
passant par cm2 d'électrode.
On sait que, lorsque la masse moléculaire du
principe actif augmente, la diffusion et le nombre de
transport des ions du principe actif diminuent par rapport à
la diffusion et au nombre de transport des ions concurrents,
notamment ions C1- que l'on crée à l'électrode négative
(cathode) à base d'AgCl. Si l'on veut obtenir un passage
significatif du principe actif par unité de surface
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
d'électrode avec des densités de courant tolérables par la
peau, il faut augmenter les concentrations en principe actif
et donc la quantité totale du principe actif dans le
réservoir de l'électrode avec comme inconvénient de laisser
5 dans ledit réservoir une quantité non consommée du principe
actif pouvant aller jusqu'à plus de 99 % de la quantité
initiale. En outre, le phénomène d'électroosmose, qui se
produit lors de tout processus d'ionophorèse, génère un
courant d'eau dans la peau qui circule de l'électrode
positive vers l'électrode négative et s'oppose d'autant plus
fortement au déplacement des ions de principe actif
anionique que la taille desdits ions est plus grande, c'est-
à-dire que la masse moléculaire du principe actif est plus
élevée.
Il n'était donc pas évident de pouvoir réaliser une
administration transcutanée d'un principe actif anionique de
masse moléculaire substantiellement plus élevée que celle
des produits de type valproate à l'aide d'un dispositif
d'ionophorèse tel que décrit dans la citation EP-A-0556112,
qui concilierait des flux transcutanés ionophorétiques
acceptables de principe actif anionique et un taux
d'utilisation significatif du principe actif initialement
présent dans le réservoir associé à l'électrode négative.
Les demanderesses ont mis en évidence que l'on
pouvait faire appel à un dispositif d'ionophorèse à
électrode négative réversible d'un type comparable à celui
décrit dans la citation EP-A-0556112, pour réaliser une
administration transcutanée de dérivés du type des
oligosaccharides anioniques, avec obtention de flux
transcutanés ionophorétiques atteignant des concentrations
plasmatiques ayant des valeurs compatibles avec un
traitement thérapeutique et simultanément utilisation
significative du principe actif, si l'on appliquait entre
les électrodes des signaux électriques de tension moyenne
telle que la densité du courant moyen généré entre lesdites
électrodes ait une valeur allant de 0,05 à 0,25 mA/cm2 et si
le principe actif oligosaccharidique était présent
initialement dans l'élément réservoir associé à l'électrode
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
6
négative en quantité substantiellement inférieure à celle
enseignée par la citation EP-A-0556112 pour les principes
actifs anioniques de type valproate.
Le dispositif d'ionophorèse selon l'invention
comporte un ensemble électrode négative constitué d'une
électrode négative, dite électrode active, en contact avec
un élément réservoir contenant un électrolyte renfermant le
principe actif sous une forme au moins partiellement
ionisée, ledit élément réservoir étant agencé pour assurer,
lorsqu'il est placé au contact d'une zone de la peau d'un
sujet, un continuum conducteur ionique entre ladite
électrode négative et ladite zone, un ensemble électrode
positive constitué soit (i) d'une électrode positive seule
ou bien, de préférence, (ii) d'une électrode positive en
contact avec un élément réceptacle contenant au moins un
électrolyte, ledit élément réceptacle étant agencé pour
assurer, lorsqu'il est placé au contact d'une portion de la
peau du sujet, un continuum conducteur ionique entre
l'électrode positive et ladite portion, et un générateur de
signaux électriques connectable aux deux électrodes,
l'électrode négative en contact avec l'élément réservoir
étant formée au moins en partie d'un composé métallique
ionisable, dont les ions métalliques sont susceptibles
d'être réduits électrochimiquement en le métal correspondant
et de former avec ledit métal un système réversible
électrochimiquement, de manière à constituer, au moins au
cours du fonctionnement du dispositif, une électrode
négative réversible et le générateur étant agencé pour
appliquer, entre les électrodes, des signaux électriques de
tension moyenne telle que la densité du courant moyen généré
entre lesdites électrodes est comprise entre 0,03 et 0,5
mA/cm2, lequel dispositif se caractérise en ce que le
principe actif présent dans l'élément réservoir associé à
l'électrode négative est choisi parmi les oligosaccharides
anioniques représentés par les sels alcalins ou
alcalinoterreux d'oligosaccharides qui sont constitués de
deux à douze motifs saccharidiques, dont certains motifs ou
tous ont leurs groupements OH remplacés, au moins en partie,
CA 02211794 1997-07-17
WO 96122808 PCTIFR96/00114
7
par des groupements fonctionnels choisis parmi -OS03-,
-COO-, -NHSO3-, -NH-acyle, -OP03-- et -OT, T représentant un
radical hydrocarboné, et qui présentent un caractère ionique
propre à une administration ionophorétique, en ce que ladite
densité de courant possède des valeurs allant de 0,05 mA/cm2
à 0,25 mA/cm2 et en ce que la quantité de principe actif
présente initialement dans l'élément réservoir associé à
l'électrode négative représente 0,5 à 12 mg par cm2
d'électrode et par mAh de courant passant par cm2
d'électrode.
Parmi les composés métalliques susceptibles de
constituer au moins en partie l'électrode négative, on peut
citer, à titre non limitatif, les composés AgCl et CuCl.
En particulier, on peut constituer l'électrode
négative en associant le composé métallique au métal lui
correspondant.
La matière de l'électrode négative peut être déposée
sur un support, lequel support peut consister en un matériau
isolant et notamment en un matériau plastique isolant tel
que polypropylène, polyéthylène, PVC, polyester ou bien en
un matériau conducteur électronique métallique ou non
métallique résistant à la corrosion par l'électrolyte
renfermant le principe actif en l'absence de courant comme,
par exemple, argent, titane, platine, acier inoxydable,
carbone, graphite, polymère conducteur.
L'électrode positive que l'on utilise dans le
procédé de l'invention peut être en un métal ou alliage
métallique tel que titane, platine, acier inoxydable ou
encore en un matériau conducteur électronique non métallique
tel que carbone, graphite, polymère conducteur. On peut
encore constituer l'électrode positive, au- moins en partie,
par un métal susceptible d'être consommé par oxydation
électrochimique et, par exemple, par un métal tel que Al,
Cu, Mg, Zn et Ag. Dans ce cas, on peut en particulier
choisir ledit métal consommable par oxydation
électrochimique parmi ceux, tels que l'argent, susceptibles
de former un système réversible électrochimiquement avec les
ions métalliques résultant de l'oxydation électrochimique,
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
8
de manière à constituer une électrode positive réversible au
cours du fonctionnement du dispositif. Le matériau de
l'électrode positive consommable par oxydation
électrochimique peut être déposé sur un support consistant
en un matériau isolant et notamment en un matériau plastique
isolant tel que polypropylène, polyéthylène, PVC, polyester ou bien encore en
un matériau conducteur électronique
métallique ou non métallique tel que, par exemple, titane,
platine, acier inoxydable, carbone, graphite, polymère
conducteur.
L'électrode négative ou/et l'électrode positive
peuvent être agencées pour constituer des électrodes
composites formées d'une compositon à base d'un liant
polymère, d'une charge conductrice pulvérulente ou fibreuse,
notamment noir de carbone ou fibres courtes de graphite, et
du matériau actif de l'électrode sous forme divisée, à
savoir, dans le cas de l'électrode négative, composé
métallique électrochimiquement réductible seul ou associé au
métal correspondant, et, dans le cas de l'électrode
positive, métal ou alliage métallique choisi pour constituer
ladite électrode. Le liant polymère est de préférence un
polymère à base d'époxy-1,2 propane et/ou d'époxy-1,2 butane
comme décrit dans la demande de brevet français N 94 09231
déposée le 26.07.1994 par ELF AQUITAINE et SANOFI.
Selon une forme de réalisation du dispositif
d'ionophorèse selon l'invention, qui permet de réaliser
l'administration transcutanée d'une quantité totale donnée
du principe actif du type oligosaccharide anionique à un
sujet, l'une ou l'autre des électrodes négative et positive
est agencée pour constituer une électrode, dite électrode
limitante, formée d'une quantité limitée d'une matière
consommable électrochimiquement associée soit à un support =
conducteur électronique, soit à un support isolant, ladite
matière consommable électrochimiquement étant soit le
composé métallique électrochimiquement réductible lorsque
l'électrode limitante est l'électrode négative ou bien un
métal consommable par oxydation électrochimique, notamment
un métal tel que A1, Mg, Zn et Ag, lorsque l'électrode
CA 02211794 1997-07-17
WO 96122808 PCTIFR96/00114
9
limitante est l'électrode positive, et ledit support
conducteur électronique étant réalisé en un matériau qui
résiste à la corrosion par l'électrolyte associé à
l'électrode limitante en l'absence de courant et qui
présente, lorsque l'électrode limitante est l'électrode
négative, une surtension d'hydrogène en présence dudit
électrolyte au moins égale à celle de l'aluminium ou bien
qui n'est pas consommable par oxydation électrochimique
lorsque l'électrode limitante est l'électrode positive,
tandis que ladite quantité limitée de matière consommable
électrochimiquement est choisie pour que la quantité
d'électricité nécessaire à sa consommation électrochimique
corresponde à la quantité d'électricité nécessaire pour
administrer la quantité totale donnée de principe actif au
sujet, de telle sorte que la circulation du courant entre
les électrodes soit pratiquement interrompue lorsque la
matière consommable de l'électrode limitante a été
consommée, et le principe actif de type oligosaccharide
anionique est présent initialement dans l'élément réservoir
au contact de l'électrode négative, en quantité supérieure à
la quantité totale donnée à administrer au sujet.
Convient en particulier comme support isolant de
l'électrode limitante, un support en un matériau plastique
isolant tel que polypropylène, PVC, polyéthylène, polyester.
Comme support conducteur électronique de l'électrode
négative limitante, on peut choisir avantageusement un
support en un matériau choisi parmi aluminium, argent,
titane, tantale, vanadium, acier inoxydable, zinc, carbone,
graphite et polymère conducteur. Convient, par exemple,comme
support de l'électrode positive limitante un support en un
matériau choisi parmi platine, titane, acier inoxydable, or,
carbone, graphite et polymère conducteur.
Les supports conducteurs métalliques des électrodes
négative ou positive peuvent être massifs ou consister en
dépôts métalliques de très faible épaisseur sur des films
plastiques isolants. Ces dépôts métalliques peuvent être
réalisés par toute technique connue telle que, par exemple,
métallisation sous vide ou pulvérisation cathodique.
CA 02211794 1997-07-17
WO 96122808 PCTIFR96/00114
A titre d'exemples non limitatifs d'électrodes
utilisables comme électrodes négatives non limitantes ou
limitantes dans le dispositif selon l'invention, on peut
citer des électrodes à base d'AgCl ou de CuCl sur un support 5 d'argent, de
cuivre, d'acier inoxydable, de carbone, de
polypropylène, de polyéthylène ou d'un polymère conducteur.
Comme exemples d'électrodes positives consommables non
limitantes ou limitantes utilisables dans le dispositif
selon l'invention, on peut mentionner, à titre non
10 limitatif, les électrodes non limitantes à base d'un métal
consommable par oxydation électrochimique choisi parmi A1,
Ag, Cu, Mg et Zn et les électrodes limitantes à base d'un
tel métal déposé sur un support isolant tel que
polypropylène ou polyester ou sur un support choisi parmi
titane, acier inoxydable, platine, carbone, graphite et
polymère conducteur.
Comme indiqué précédemment, la matière consommable
électrochimiquement de l'électrode limitante est présente
dans ladite électrode en quantité telle que la quantité
d'électricité nécessaire à sa consommation électrochimique
corresponde à la quantité d'électricité à utiliser pour
administrer la quantité totale donnée du principe actif de
type oligosaccharide anionique au sujet. Cette dernière
quantité d'électricité, qui dépend du système ionophorétique
utilisé, c'est-à-dire des milieux réactionnels en contact
avec l'électrode négative réversible et l'électrode
positive, du signal électrique appliqué aux électrodes et de
la nature desdites électrodes, est déterminée par le biais
d'essais préalables pour chaque type de système
ionophorétique mis en oeuvre.
Le générateur électrique applique -entre l'électrode
négative (électrode active) et l'électrode positive (contre-
électrode) un signal électrique qui peut être soit un signal
intensiométrique, c'est-à-dire un signal d'intensité moyenne
imposée, par exemple constante (signal intensiostatique),
soit, de préférence, un signal potentiométrique, c'est-à-
dire un signal de tension moyenne imposée, par exemple
constante (signal potentiostatique). Le signal électrique de
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
11
type intensiométrique ou de type potentiométrique peut être
continu ou pulsé et permanent ou intermittent, avec ou sans
inversion temporaire de polarité. Sa fréquence peut aller de
O à 500 kHz et plus particulièrement de 0 à 100 kHz. Lorsque
le signal électrique est d'un type pulsé, il peut avoir un
rapport cyclique, c'est-à-dire un rapport entre la durée de
l'impulsion élémentaire, dont la répétition forme le signal
pulsé, et l'intervalle de temps séparant deux apparitions
consécutives de cette impulsion, allant de 0,05 à 0,95 et
plus particulièrement de 0,1 à 0,8.
Avantageusement, la tension moyenne du signal
appliqué par le générateur entre l'électrode négative et
l'électrode positive est choisie entre 0,1 et 50 volts et
plus spécialement entre 0,3 et 20 volts de telle sorte que
la densité du courant moyen généré entre lesdites électrodes
ait une valeur comprise entre 0,05 et 0,25 mA/cmZ et de
préférence entre 0,05 et 0,2 mA/cm2.
Le générateur de signaux électriques du dispositif
selon l'invention peut être de tout type connu permettant de
générer des signaux électriques d'intensité moyenne imposée
ou de tension moyenne imposée, qui sont continus ou pulsés
et permanents ou intermittents, avec ou sans inversion
temporaire de polarité, et qui présentent les
caractéristiques définies ci-dessus.
L'électrolyte, qui est présent dans l'élément
réservoir en contact avec l'électrode négative, contient
avantageusement une solution aqueuse ou un gel aqueux,
adhésif ou non, qui renferme le principe actif de type
oligosaccharide anionique à administrer sous la forme d'un
sel au moins partiellement ionisé d'un métal alcalin tel
que, par exemple, sodium ou potassium, ou sel d'un métal
alcalino-terreux tel que, par exemple, calcium. De même,
l'électrolyte, qui est éventuellement en contact avec
l'électrode positive, se présente, au moins en partie, sous
la forme d'une solution aqueuse ou d'un gel aqueux adhésif
ou non. Ces solutions ou gels aqueux peuvent constituer la
totalité de l'électrolyte présent dans l'élément réservoir
considéré ou bien peuvent former une partie seulement
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
12
desdits électrolytes et être alors dispersés dans un milieu
non aqueux formant le reste de l'électrolyte et choisi pour
ne pas interrompre le continuum conducteur ionique entre
l'électrode et la peau et pour accroître la qualité de
l'adhésion entre l'électrode et la peau. Ces solutions
aqueuses ou gels aqueux peuvent être obtenus comme il est
bien connu dans les techniques d'ionophorèse. Des exemples
de gels aqueux ou de solutions aqueuses épaisses sont
notamment décrits respectivement dans les citations US-A-
4766164 et US-A-3163166.
Le milieu aqueux renfermant le principe actif du
type oligosaccharide anionique, de même que le milieu aqueux
constituant l'électrolyte associé à l'électrode positive,
lorsque ledit électrolyte est utilisé, peuvent renfermer, si
besoin est, des agents susceptibles de favoriser le passage
transcutané du principe actif comme, par exemple, des agents
vasodilatateurs et/ou des agents amphiphiles parmi lesquels
on peut citer, à titre non limitatif, des composés du type
alcool ou du type ester. Ces agents sont utilisés en
concentrations permettant une bonne solubilité du principe
actif dans le milieu.
Comme indiqué précédemment, la quantité de principe
actif de type oligosaccharide anionique présente
initialement dans l'élément réservoir associé à l'électrode
négative représente 0,5 mg à 12 mg et de préférence 1 mg à 8
mg par cm2 de ladite électrode et par mAh de courant passant
par cm2 de cette électrode.
On peut introduire le principe actif à administrer
non seulement dans l'élément réservoir associé à l'électrode
négative, mais également dans l'élément réceptacle associé à
l'électrode positive et dans ce cas l'électrode négative et
l'électrode positive du dispositif d'ionophorèse consistent en une électrode
réversible à base du composé métallique
ionisable réductible et du métal lui correspondant, par
exemple une électrode réversible à base du couple Ag/AgCl.
Ceci permet, par inversion de la polarité des signaux
électriques appliqués aux électrodes, d'administrer le
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
13
principe actif alternativement à partir de l'élément
réservoir et de l'élément réceptacle.
Dans ce cas, la quantité de principe actif de type
oligosaccharidique anionique présente initialement dans
l'élément réservoir associé à chacune des électrodes
représente 0,5 mg à 6 mg et de préférence 0,5 mg à 4 mg par
cm2 d'électrode et par mAh de courant passant par cm2
d'électrode.
Les oligosaccharides anioniques concernés par
l'invention, consistent en sels alcalins ou alcalino-
terreux, notamment sels de sodium, potassium ou calcium, de
composés qui sont constitués de deux à douze motifs, et plus
particulièrement de trois à huit motifs saccharidiques, dont
certains motifs ou tous ont leurs groupements OH au moins en
partie remplacés par des groupements fonctionnels tels que,
par exemple, -OS03-, -COO-, -NHSO3-, -NH acyle, -OP03--, -OT
où T représente un radical hydrocarboné et notamment un
radical hydrocarboné aliphatique ou aromatique, -OT étant en
particulier un groupement fonctionnel alcoxy, et qui
présentent un caractère ionique propre à une administration
ionophorétique. Lesdits oligosaccharides sont plus
particulièrement des oligosacccharides anioniques obtenus
par synthèse chimique totale.
En particulier, lesdits oligosaccharides peuvent
être choisis parmi :
- les oligosaccharides de synthèse décrits dans la
citation EP-A-0084999, qui sont constitués de 2 à 12 motifs
monosaccharides alternés acides uroniques (glucuronique ou
iduronique) et glucosamine et renferment, en dehors des
groupes OH, des groupements fonctionnels, -OSO3-, -NHSO3- et
-N-acyle, notamment -N-acétyle et, dans certains cas, des
groupes alcoxy, notamment méthoxy, en remplacement des
groupes anomériques OH. Des exemples de tels
oligosaccharides sont les pentasaccharides à propriétés
antithrombotiques et/ou anticoagulantes, parmi lesquels on
trouve les composés représentés par la formule (I) donnée
précédement ;
CA 02211794 1997-07-17
WO 96/22808 PCT1FR96/00114
14
- les oligosaccharides de synthèse à activité
antithrombotique décrits dans la citation EP-A-0165134, qui
sont consitués de motifs monosaccharidiques acides uroniques
et glucosamine et contiennent des groupements fonctionnels
-OS03- et -O-PO3-- ;.
- les pentasaccharides à propriétés anti-
thrombotiques et/ou anticoagulantes décrits dans la citation
EP-A-0301618, qui sont constitués de motifs acides uroniques
et de motifs gluosamine et comportent un groupe -OS03- en
position 3 de l'unité glucosamine ;
- les oligosaccharides de synthèse à propriétés
antithrombotiques et/ou anticoagulantes décrits dans la
citation EP-A-0454220, qui sont des dérivés d'acides
uroniques et de glucose possédant un enchaînement
trisaccharidique spécifique et comportant des groupements
fonctionnels O-alkyle ou -O-S03- ;
- les dérivés glycosaminoglycanoides sulfatés de
synthèse, à propriétés antithrombotiques et à activité
inhibitrice de la prolifération des cellules musculaires
lisses, décrits dans la citation EP-A-0529715, pour lesquels
les groupements fonctionnels -NHS03-, N-acétate ou OH ont
été remplacés par des groupements alcoxy, aryloxy,
aralkyloxy ou -O-S03- ;
- les héparinoides de synthèse dérivés 3-désoxy à
activité antithrombotique décrits dans la demande de brevet
français N 93 04769 déposée le 22.04.1993 par ELF SANOFI et
AKZO, qui sont constitués de motifs acides uroniques et de
motifs glucosamine et pour lesquels les groupements
fonctionnels -NHSO3-, N-acétate du motif glucosamine et
éventuellement les groupes OH des motifs acides uroniques et
glucosamine ont été remplacés par des groupements alcoxy ou
-O-S03- ;
- les oligosaccharides de synthèse décrits dans la
citation EP-A-0113599, qui sont constitués de motifs
monosaccharidiques acides uroniques (glucuronique ou
iduronique) et D-galactosamine.
Les oligosaccharides anioniques utilisés selon
l'invention sont en particulier des tri-, tétra-, penta- ou
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
hexasaccharides et tout spécialement des pentasaccharides,
notamment des pentasaccharides de formule (II) suivante
-
OSO ' coo OSO - OS03
03 O 03 O
5 0 OH 0 OS03' 0 AE O OR
2
HO OQ3
NHR OH NHSO:I- OS03 NHS037
dans laquelle R est un groupement -S03' ou acyle,
notamment acétyle, R1 et R2, identiques ou différents,
10 représentent H ou -S03 et R3 désigne H ou un radical alkyle
inférieur, notamment -CH3.
Le dispositif selon l'invention peut être réalisé à
partir de tout dispositif d'ionophorèse connu, que l'on a
modifié pour que (i) son électrode négative soit une
15 électrode négative réversible, l'électrode positive étant
soit une électrode positive conventionnelle ou bien une
électrode positive consommable non réversible ou réversible
et l'élément réservoir associé à l'électrode négative
renfermant le principe actif du type oligosaccharide
anionique sous une forme au moins partiellement ionisée, que
(ii) son générateur de signaux électriques soit agencé pour
appliquer entre les électrodes des signaux électriques de
tension moyenne telle que la densité du courant moyen généré
entre les électrodes soit comprise entre 0,05 et 0,25 mA/cm2
et de préférence entre 0,05 et 0,2 mA/cm2 et que (iii) la
quantité de principe actif de type oligosaccharide anionique
présente initialement dans l'élément réservoir associé à
l'électrode négative ou dans l'élement réservoir ou
réceptacle associé à l'électrode négative ou positive ait
une valeur telle qu'indiqué précédemment.
Le cas échéant, l'électrode négative ou bien
l'électrode positive peut être agencée comme indiqué
précédemment pour constituer une électrode limitante.
En particulier, le dispositif selon l'invention peut
être un dispositif autonome portable, à fixer par bracelet
ou éventuellement à coller sur la peau, comportant des
électrodes ayant chacune une aire inférieure à 50 cm2 et
plus particulièrement comprise entre 1 et 30 cm2 et un
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
16
générateur de signaux électriques miniaturisé. Ainsi, un
dispositif portable autonome selon l'invention peut avoir
une structure analogue à celle des dispositifs d'ionophorése
portables autonomes décrits, par exemple, dans les citations
US-A-4325367, EP-A-0060452 et Fr-A-2509182 sous réserve que
l'électrode négative dudit dispositif soit une électrode
négative réversible et que le générateur de signaux
électriques et l'élément réservoir associé à chaque
électrode soient agencés comme indiqué précédemment.
L'électrode négative peut être par exemple une
électrode à base d'AgCl ou de CuCl sur un support d'argent,
de cuivre, de carbone, de polypropylène, de polyéthylène ou
d'un polymère conducteur. L'électrode positive peut être une
électrode positive conventionnelle, par exemple électrode en
un métal ou alliage métallique tel que titane, platine,
acier inoxydable ou encore en un matériau conducteur
électronique non métallique tel que carbone ou graphite, ou
bien encore une électrode positive consommable non
réversible ou réversible, par exemple électrode en un métal
tel que A1, Cu, Mg, Zn et Ag éventuellement déposée sur un
support isolant tel que polypropylène ou polyester ou sur un
support choisi parmi titane, acier inoxydable, platine,
carbone, graphite et polymère conducteur. Lesdites
électrodes négative et positive, dont l'une et/ou l'autre
peuvent être agencées comme indiqué plus haut pour
constituer une électrode limitante, ont chacune une aire
inférieure à 50 cm2 et plus particulièrement comprise entre
1 et 30 cmZ.
Lorsque l'ensemble électrode négative et l'ensemble
électrode positive sont fixés à la peau au moyen d'un
adhésif, ceci peut être réalisé en munissant d'une couche
d'un adhésif conduisant les ions, la face, destinée à venir
au contact de la peau, de l'élément réservoir de chaque
ensemble électrode ou une zone entourant ladite face.
Le dispositif d'ionophorèse selon l'invention,
lorsqu'il est équipé d'au moins une électrode négative à
base du couple Ag/AgCl et, de préférence, comporte une
électrode négative et une électrode positive à base dudit
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
17
couple Ag/AgCl, peut encore inclure un ensemble de contrôle
de l'état d'avancement de l'administration transcutanée du
principe actif tel que décrit dans la demande de brevet
français N 94 10541 déposée le 2 septembre 1994 par ELF
AQUITAINE et SANOFI.
L'invention est illustrée par les exemples suivants
donnés à titre non limitatif.
Exemple 1 :
Etude du passage transdermique d'un sel de sodium de
pentasaccharide par ionophorèse à tension constante.
Le pentasaccharide utilisé correspondait à celui
ayant la formule (I) donnée précédemment où R désigne -S03-.
On opérait dans des cellules d'ionophorèse de
structure identique. Chaque cellule d'ionophorèse était
constituée de trois compartiments cylindriques adjacents
coaxiaux de 2 cm2 de section transversale, à savoir, dans
cet ordre, un compartiment donneur, un compartiment receveur
et un compartiment de contre-électrode, ces trois
compartiments étant séparés, chacun du suivant et de façon
étanche, par un morceau de peau de rat nu (OFA/hr/hr)
servant de membrane pour l'étude de la diffusion
trancutanée. Le compartiment donneur, d'un volume de 0,5 ml
renfermait une solution aqueuse à 2-% en poids du sel de
sodium du pentasaccharide précité ayant une activité
antifacteur Xa de 0,65 unité "Golden standard" par micro
gramme, la quantité de pentasaccharide représentant 10 mg
pour 2 cm2 de surface active d'électrode. Le compartiment
receveur, d'un volume de 10 ml, renfermait du sérum
physiologique additionné de 500 ppm de NaN3 et était agité à
l'aide d'un barreau magnétique. Le compartiment de contre-
électrode, identique au compartiment donneur, renfermait
0,5 ml d'une solution aqueuse à 2% en poids de chlorure de
sodium ainsi que 500 ppm en poids de NaN3. A son extrémité
opposée au compartiment receveur le compartiment donneur
était équipé d'une électrode négative. De manière identique
au compartiment donneur, le compartiment contre-électrode
était équipé d'une électrode positive (contre-électrode).
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
18
Les échantillons de peau de rat avaient été
débarrassés des tissus sous-cutanés et conservés par
congélation à-40 C jusqu'à leur montage dans la cellule
d'ionophorèse, faces dermiques tournées vers le compartiment
receveur, après un passage de 15 minutes dans du sérum
physiologique additionné de 500 ppm de NaN3.
Pour chacun des essais réalisés, quatre cellules
d'ionophorèse identiques étaient mises en route
2
simultanément. La surface active d'échange était de 2 cm
pour chaque peau.
Un générateur de courant pulsé permettait d'établir
entre les électrodes des 4 cellules, montées en parallèle,
un signal électrique de type potentiostatique de tension
crête égale à 2,2 volts avec un rapport cyclique de 50%
(soit une tension moyenne de 1,1 volts) et une fréquence de
kHz.
Le courant pulsé produit par le générateur était
appliqué pendant 6 heures, l'électrode du compartiment
donneur de chaque cellule étant reliée au pôle négatif dudit
20 générateur et les contre-électrodes au pôle positif.
Au bout de ladite durée, on prélevait une partie
aliquote du milieu contenu dans le compartiment receveur et
déterminait par dosage la quantité de pentasaccharide ayant
traversé la peau séparant les compartiments donneur et
25 receveur de chaque cellule. Un deuxième prélèvement était
réalisé 24 heures après le début de chaque expérience soit
18 heures après l'arrêt du signal électrique.
Cinq essais la à le ont été réalisés comme suit
= Essai la : l'électrode négative et l'électrode
positive étaient constituées d'un film de titane ayant une
épaisseur égale à 10 m. Aucune tension n'était appliquée
aux électrodes dans le but de déterminer la diffusion
transcutanée passive.
= Essai lb : L'électrode négative et l'électrode
possitive étaient constituées d'une feuille de graphite
d'une épaisseur de 60 m.
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
19
= Essai lc : L'électrode négative et l'électrode
positive étaient constituées d'un film de titane ayant une
épaisseur égale à 10 m.
= Essais id et le : L'électrode négative était
constituée d'un film d'argent de 15 m d'épaisseur
préalablement chloruré sur une face pour renfermer une
couche de chlorure d'argent correspondant à 1,8 mAh/cm2
tandis que l'électrode positive était constituée d'un film
d'argent d'une épaisseur de 15 m très légèrement chloruré
sur une face (quantité de chlorure d'argent correspondant à
0,1 mAh/cm2) , la face chlorurée de chaque électrode étant
tournée du côté de la membrane en peau de rat.
La chloruration des films d'argent était réalisée
électrochimiquement par passage d'un courant continu de
5 mA/cm= alors que chaque film d'argent, dont l'une des
faces était protégée par un film plastique adhésif et
isolant, était plongé dans un bain d'acide chlorhydrique
0,1 N et constituait le pôle positif par rapport à une
électrode en graphite plongée dans le même bain de HC1, la
quantité de courant étant contrôlée par un coulomètre monté
en série dans le circuit, pour former la quantité désirée de
chlorure d'argent sur le film d'argent.
Dans les essais la à ld, les compartiments donneur
et receveur de chaque cellule renfermaient une composition
tampon 0,06 molaire à base de monohydrogénophosphate et de
dihydrogénophosphate de sodium en quantités équi-
moléculaires, de manière à maintenir le pH dans lesdits
compartiments à une valeur d'environ 7. Dans l'essai le,
aucun tampon n'était utilisé. Dans les essais ld et le, la
densité du courant moyen généré entre les électrodes était
égale à environ 0,20 mA/cm2.
Pour chacun des essais, on a déterminé sur des
parties aliquotes prélevées dans les compartiments receveurs
des quatre cellules, l'activité moyenne antifacteur Xa par
ml de milieu représentative de la quantité de
pentasaccharide ayant diffusé dans ces compartiments à
l'issue des 6 heures d'application du courant et 24 heures
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
après le début de chaque expérience, soit 18 heures après
l'arrêt dudit courant.
Le dosage du pentasaccharide dans le compartiment
récepteur était fondé sur la recherche de son activité
5 antifacteur Xa. Le dosage était réalisé, soit directement
sur le milieu prélevé dans le compartiment récepteur, soit
après dilution, à l'aide d'une trousse de dosage ROTACHROM
HEPARIN 8 , de tampon complémentaire pour appareil de dosage
et d'antithrombine III bovine, ces divers éléments étant
10 fournis par la société STAGO, en faisant appel à un appareil
de dosage HITACHI 717. L'établissement de la courbe
d'étalonnage était effectué à l'aide d'une solution étalon
de pentasaccharide dite étalon "Golden Standard" à laquelle
on a attribué une activité antifacteur Xa égale à 13 unités
15 par ml.
Les résultats obtenus sont rassemblés dans le
tableau I.
TABLEAU I
ESSAI la lb 1c Id le
Tension moyenne (volts) 0 1,1 1,1 1,1 1,1
Nature de l'électrode négative Titane Graphite Titane Ag/AgCI Ag/AgCI
Activité antifacteur Xa/ml à 6 heures <0,1 0,70 0,50 9,1 18,1
% variation par rapport à la moyenne 38 54 41 46
Taux d'utilisation du principe actif (%) - nul 0,1 0,08 1,4 2,8
Activité antifacteurXa/ml à 24 heures 0,25 1,13 0,95 9,7 21,4
% variation par rapport à la moyenne 60 45 51 43 39
Taux d'utilisation du principe actif (%) - nul 0,2 0,15 1,5 3,3
20 Le niveau de l'activité antifacteur Xa étant le
reflet de la concentration du pentasaccharide dans le
compartiment receveur, l'examen du tableau I montre
clairement que les quantités de pentasaccharide ayant
diffusé dans le compartiment receveur par ionophorèse sont
très faibles et proches du transport passif lorsque l'on
utilise des électrodes non réversibles comme le graphite ou
CA 02211794 1997-07-17
WO 96/22808 pCT/FR96/00114
21
le titane, alors que lesdites quantités augmentent très
fortement lorsque l'on fait appel à des électrodes négatives
Ag/AgCl (électrodes réversibles) même en présence d'un
tampon. Ces électrodes réversibles, à la différence des
électrodes non consommables comme le titane ou le graphite,
permettent d'éviter l'hydrolyse de l'eau et donc des
changements importants de pH en cours de traitement tant au
niveau des électrodes négatives que positives. La présence
de substances à effet tampon dans les compartiments donneurs
n'est donc plus nécessaire, ce qui constitue un avantage
supplémentaire des électrodes réversibles. Ainsi qu'on peut
le constater à la lecture de l'essai le, les flux
transdermiques sous ionophorèse obtenus en l'absence du
tampon sont encore accrus par rapport à tous les autres
essais. 137 g/cm2 par mAh).
Exemple 2 :
Etude du passage transdermique d'un sel de sodium de
pentasaccharide par ionophorèse à intensité imposée
on opérait comme décrit dans l'exemple 1 avec
toutefois les modifications suivantes :
= mise en oeuvre de l'ionophorèse en imposant une
intensité constante à travers chaque cellule
= utilisation d'un courant continu au lieu de
courant pulsé
= absence de tampon dans les compartiments donneurs
et de contre-électrode de l'essai 2d car ceux-ci sont
équipés d'électrodes de type Ag/AgCl qui évitent l'hydrolyse
de l'eau.
La mise en oeuvre était effectuée en imposant aux
électrodes de chacune des 4 cellules d'ionophorèse, pendant
une durée de 6 heures, un courant continu constant de
0,4 mA, soit 0,2 mA/cmZ, à l'aide d'un générateur permettant
d'imposer une intensité constante quelles que soient les
tensions générées aux bornes de chaque cellule.
Le courant continu d'intensité constante égale à
0,4 mA produit par le générateur était appliqué pendant
6 heures, le compartiment donneur de chaque cellule étant
CA 02211794 1997-07-17
WO 96122808 PCT/FR96/00114
22
relié au pôle négatif dudit générateur et les contre-
électrodes au pôle positif.
Pour chacun des essais 2a à 2d on a déterminé sur
des parties aliquotes, prélevées dans les compartiments
receveurs, l'activité moyenne antifacteur Xa par ml du
milieu receveur, représentative de la quantité de
pentasaccharide y ayant diffusé à l'issue des 6 heures
d'application du courant et 24 heures après le début de
chaque expérience, soit 18 heures après l'arrêt dudit
courant.
Les résultats obtenus sont rassemblés dans le
tableau II
TABLEAU II
ESSAI 2a 2b 2c 2d
Densité moyenne de courant (mA/cm2) 0 0,2 0,2 0,2
Nature de l'électrode négative Titane Graphite Titane Ag/AgCI
Activité antifacteur Xa/ml à 6 heures 0,12 6 3,2 18,1
% variation par rapport à la moyenne 35 42 22
Taux d'utilisation du principe actif (%) - nul 0,09 0,49 2,8
Activité antifacteur Xa/ml à 24 heures 0,6 5,8 4,9 24
% variation par rapport à(a moyenne 60 45 51 18
Taux d'utilisation du principe actif (%) 0,09 0,9 0,75 3,7
Les quantités totales diffusées, exprimées en g par
cm2 pour chacun des essais, sont respectivement égales à
4,64 (essai 2a), 45 (essai 2b), 38 (essai 2c) et 185 (essai
2d), soit 154 g/cm2 par mAh pour les électrodes Ag/AgCl.
Bien que, par rapport aux essais précédents conduits
à tension constante, la diffusion sous ionophorèse soit
devenue plus significative par rapport à la diffusion
passive pour les électrodes de graphite et de titane, les
performances des électrodes d'argent chloruré restent très
nettement supérieures.
CA 02211794 1997-07-17
WO 96122808 pCT/FR96/00114
23
EXEMPLE 3
Administration chez le microporc du sel de sodium d'un
pentasaccharide par ionophorèse à densité de courant imposée
Le microporc de souche YUCATAN est considéré par les
spécialistes comme un excellent modèle animal pour l'étude
de l'administration chez l'homme des médicaments par
ionophorèse. En effet la structure de la peau de cet animal
est très voisine de celle de la peau humaine.
Les essais suivants ont été conduits chez le
microporc précité dans le but de comparer l'administration
du sel de sodium du pentasaccharide utilisé dans les
exemples précédents par ionophorèse avec une administration
par injection sous-cutanée ou intraveineuse.
Pour ces essais, on constituait des paires
d'ensembles électrodes adhésifs, chaque paire comportant un
ensemble électrode donneur formé d'une électrode négative
réversible (électrode active) en contact avec un premier
élément réservoir renfermant le pentasaccharide à
administrer et un ensemble électrode passif formé d'une
électrode positive (contre-électrode) en contact avec un
deuxième élément réservoir (élément réceptacle) renfermant
un électrolyte indifférent.
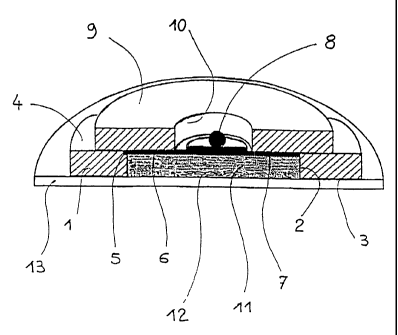
Chaque ensemble électrode avait une structure
analogue à celle qui est schématisée, à titre d'exemple non
limitatif, sur la figure.
En se référant à la figure, chaque ensemble
électrode comportait un disque 1 en mousse de polyéthylène
présentant un évidement cylindrique axial 2, ledit disque
comportant une face 3 adhésive et une face 4 non-adhésive,
chacune desdites faces ayant la forme d'une zone annulaire
de deux centimètres de largeur. L'extrémité 5 de l'évidement
du disque, côté face non-adhésive, était obturé par une
électrode 6 ayant la forme d'un disque d'argent chloruré sur
l'une de ses faces, ledit disque ayant une section de 20
cm2. La face chlorurée 7 du disque électrode était tournée
vers l'intérieur de l'évidement. La face non-chlorurée dudit
disque portait une prise de contact 8 du type bouton-
pression, soudée à ladite face au moyen d'un adhésif
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96100114
24
conducteur électronique, et elle s'appuyait contre un disque
support 9 en mousse de polyéthylène coaxial au disque 1 et
présentant un évidement axial 10 pour permettre l'acès à la
prise de contact 8. Ledit disque support, de diamètre
compris entre celui de l'électrode 6 et du disque 1, était
collé sur la face non-adhésive de ce dernier disque.
L'évidement 2 du disque 1 était rempli d'un hydrogel
conducteur 11 formant élément réservoir. La face adhésive 3
du disque 1 était enduite d'un adhésif sensible à la
pression agréé pour être appliqué sur la peau, ladite face 3
et la face 12 adjacente de l'élément réservoir il étant
initialement recouvertes par un film protecteur pelable
anti-adhérent en polyester, que l'on retirait avant
application sur la peau.
Dans l'ensemble électrode donneur, l'électrode
négative (électrode active) en argent chloruré renfermait
une quantité de chlorure d'argent équivalant à 1,8 mAh/cm2,
permettant ainsi à l'électrode de supporter la quantité de
courant traversant les électrodes pendant la durée du
traitement ionophorétique, à savoir 1,2 mAh/cm2. L'élément
réservoir associé à l'électrode négative était rempli sur
une épaisseur de 2 mm, soit une quantité de 4 g pour les 20
cm2 d'électrode, d'un hydrogel à base de xanthane et
d'extrait de caroube à 3 % d'extrait sec et contenant 2 % en
poids de sel de sodium du pentasaccharide de formule (I)
donnée précédemment. L'ensemble électrode donneur contenait
donc 80 mg de pentasaccharide à raison de 4 mg/cm2 pour
chacun des animaux traités.
Dans l'ensemble électrode passif, l'électrode
positive (contre-électrode) en argent chloruré renfermait
une quantité de chlorure d'argent équivalant à 0,1 mAh/cm2
et l'élément réservoir associé à cette électrode était
constitué du même hydrogel que celui présent dans l'ensemble
électrode donneur exempt toutefois de pentasaccharide, mais
renfermant, par contre, 4 % en poids de NaCl.
Un générateur de signaux électriques, connectable
aux électrodes de chaque paire d'ensembles électrodes
permettait de délivrer entre lesdites électrodes un signal
CA 02211794 1997-07-17
WO 96/22808 PCT1FR96/00114
électrique pulsé d'intensité régulée ayant une fréquence de
25 kHz et un rapport cyclique égal à 50 %.
Cinq jours avant chaque essai, les animaux étaient
cathétérisés au niveau des deux jugulaires, ainsi qu'il est
5 bien connu pour toute expérimentation d'administration de
médicaments, afin de permettre des prélèvements réguliers de
sang destinés à doser les activités antifacteur Xa et, par
là, à évaluer les quantités de principe actif ayant traversé
la peau pour pénétrer le système circulatoire et donc à
10 vérifier l'efficacité du traitement ionophorétique.
Les animaux, à jeun depuis la veille des
expérimentations, étaient placés dans des hamacs
spécialisés. On collait par simple pression sur le dos de
chaque animal préalablement nettoyé à l'aide d'un tissu
15 humide, de part et d'autre de la colonne vertébrale, une
paire d'ensembles électrodes préalablement débarrassés de
leur film protecteur pelable et on connectait, par
l'intermédiaire de câbles munis de pinces adaptées aux
prises de contact installées à cet effet, l'électrode
20 négative de l'ensemble électrode donneur au pôle négatif du
générateur et la contre-électrode de l'ensemble électrode
passif au pôle positif dudit générateur.
Entre les électrodes positive et négative de chaque
paire d'ensembles électrodes collés sur l'animal, on
25 établissait, grâce au générateur, un courant de 4,8 mA (soit
une densité de courant de 0,20 mA/cm2) pendant une durée.de
6 heures et on pratiquait divers prélèvements de sang sur
diatube H STAGO au cours du temps et ce jusqu'à 30 heures
après le début de chaque expérience soit 25 heures après la
fin du traitement ionophorétique. L'essai ionophorétique a
été reproduit sur cinq microporcs mâles de=poids égal à 11,4
kg en moyenne.
outre les essais d'administration du principe actif
par ionophorèse mis en oeuvre comme décrit ci-dessus (essai
3b), on effectuait également des essais comparatifs 3a, 3c
et 3d comme suit, chaque essai étant reproduit sur deux à
quatre microporcs, comme dans le cas de l'administration
ionophorétique
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
26
. essai 3a : mise en place des ensembles électrodes
comme dans l'essai d'ionophorèse 3b, mais sans application
de courant,
. essai 3c : injection intraveineuse en "bolus" de
0,240 mg/kg de pentasaccharide en solution injectable,
. essai 3d : injection sous-cutanée de 0,200 mg/kg
de pentasaccharide en solution injectable.
Dans ces essais 3a, 3c et 3d, on pratiquait un
certain nombre de prélèvements sanguins au cours du temps et
jusqu'à 30 heures après le début de chaque expérience comme
dans le cas du traitement ionophorétique de l'essai 3b.
Les teneurs plasmatiques des différents prélèvements
sanguins, exprimées en unités "Golden standard"
d'antifacteur Xa, sont indiquées dans le tableau III aux
fins de comparaison des taux plasmatiques moyens obtenus sur
des animaux de même souche et de même poids traités avec le
même principe actif dans les conditions des essais selon
l'invention (essai 3b) et comparatifs (essais 3a, 3c et 3d).
CA 02211794 1997-07-17
WO 96122808 PCTlFR96/00114
27
TABLEAU III
ESSAI 3a 3b 3c 3d
Nature du traitement passif ionophorèse injection I.V. injection
sous-cutanée
Nombre de microporcs traités 2 5 4 4
Densité de courant (mA/cm2) 0 0,20
Taux plasmatique à 0 minute 0 0 0 0
Taux plasmatique à 5 minutes 0 non dosé 1,04 0,12 non dosé
Taux plasmatique à 15 minutes 0 0,06 0,04 0,91 0,13 0,11 0,04
Taux plasmatique à 30 minutes 0 0,15 0,12 0,65 0,11 non dosé
Taux plasmatique à 1 heure 0 0,31 0,15 0,53 0,10 0,17 0,01
Taux plasmatique à 2 heures 0 0,45 t 0,2 0,30 0,09 0,22 0,04
- --- -
Taux plasmatique à 4 heures 0 0,64 0,18 0,29 0,08 0,26 0,06
Taux plasmatique à 6 heures 0 0,74 0,16 0,22 0,09 0,24 0,01
Taux plasmatique à 8 heures 0 0,52 0,13 0,17 0,06 0,15 0,07
Taux plasmatique à 12 heures 0 0,4 0,08 0,07 0,05 0,08 0,03
Taux plasmatique à 24 heures 0 0,11 t 0,03 0 0
Taux plasmatique à 30 heures 0 0 0 0
La comparaison des résultats du tableau III fait
apparaître que le traitement par voie ionophorétique
pratiqué selon l'invention conduit à des taux plasmatiques,
exprimés en antifacteur Xa, supérieurs à ceux que l'on peut
obtenir avec des injections intraveineuses ou sous-cutanées.
Les taux plasmatiques s'élèvent assez rapidement et
régulièrement au cours du traitement et décroissent
lentement apès arrêt du courant.
L'administration de ce type de principe actif par
voie ionophorétique,surtout si celle-ci est étalée sur une
durée quotidienne un peu plus longue et avec des densités de
courant encore plus faibles, permet d'obtenir une
concentration plasmatique de principe actif conduisant à une
CA 02211794 1997-07-17
WO 96122808 PCTiFR96/00114
28
bonne couverture antithrombotique, exprimée en termes
d'antifacteur Xa, sur une durée relativement importante en
évitant un passage par des taux plasmatiques de pointe
élevés.
La comparaison des aires sous les courbes
représentant l'évolution des taux plasmatiques au cours du
temps, lors des différents traitements, permet au pharmaco-
cinéticien de calculer, en fonction du poids des animaux,
les quantités de pentasaccharide qui ont été réellement
administrées par ionophorèse. Cette quantité a été estimée
dans le cas de l'essai 3b à 7 1,3 mg pour les 20 cm2, soit
350 g/cm2 pour 1,2 mAh/cm2, soit encore 292 g/cm2 pour 1
mAh/cm2.
La biodisponibilité, c'est-à-dire le taux de
principe actif réellement administré rapporté aux quantités
de principe actif présentes dans les électrodes, est donc
d'environ 9 %, ce qui est supérieur aux taux d'utilisation
qui ont été observés pour les essais in vitro.
Exemple 4
Administration chez le microporc du sel de sodium d'un
pentasaccharide par ionophorèse à densité de courant imposée
avec inversion périodique du sens du courant.
Les essais suivants d'administration ionophorétique
ont été conduits sur 4 microporcs en utilisant le même
générateur de courant et le même type d'électrodes que dans
l'exemple 3 et en appliquant les conditions suivantes :
Les électrodes de même structure que dans l'exemple
3 avaient une surface active de 20 cm2. Les électrodes
elles-mêmes étaient constituées de films d'argent, de 15 m
d'épaisseur, chlorurés par oxydation électrolytique à raison
de 0,5 mAh de chlorure d'argent par cm2: Les réservoirs,
également de 20 cm2, étaient constitués d'une feuille de
papier buvard en fibres de cellulose additionnées de
fibrilles de polypropylène, imbibée à raison de 50 mg/cm2
d'une solution aqueuse contenant 2 % en poids de
pentasaccharide et 0,2 % en poids de NaCl. Chaque électrode,
anode et cathode, contenait en tout 1 g de solution, soit 20
mg de pentasaccharide (1 mg/cm2) pour 20 cm2 de surface
CA 02211794 1997-07-17
WO 96122808 PCT/F.R96/00114
29
active. On a donc engagé 40 mg de pentasaccharide en tout
par animal.
Le générateur de courant délivrait une intensité
constante de 2,5 mA, soit 125 MA/cm2 de courant continu avec
des inversions régulières du sens du courant toutes les 30
minutes pendant une durée totale de 8 heures correspondant
au passage de 1 mA/cm2 de courant continu.
Chacune des électrodes, de structure et de
composition identique, se trouvait donc fonctionner
alternativement comme cathode puis comme anode, la présence
de chlorure de sodium dans chacun des réservoirs
garantissant leur fonctionnement permanent comme électrode
réversible, évitant ainsi toute réaction parasite
d'hydrolyse (avec changement du pH) ou d'oxydoréduction du
principe actif.
Dans l'essai 4a mettant en jeu 3 animaux de poids
moyen de 11,8 kg, les électrodes étaient mises en place
mais non connectées au générateur de courant alors que pour
l'ensemble des essais 4b, qui concernaient 4 animaux de
poids moyen de 12,3 kg, le courant de 2,5 mA était appliqué
pendant 8 heures avec une inversion automatisée du sens du
courant toutes les demi-heures.
On pratiquait, dans les essais 4a et 4b, un certain
nombre de prélèvements sanguins au cours du temps jusqu'à 30
heures après le début de chaque expérience, comme dans
l'exemple 3.
Les teneurs plasmatiques des différents prélèvements
sont indiquées dans le tableau IV aux fins de comparaison
des essais 4a et 4b entre eux et avec les résultats des
essais réalisés dans l'exemple 3, en particulier les essais
3c et 3d correspondant aux injections intraveineuses et
sous-cutanées.
La comparaison de l'aire sous la courbe représentant
l'évolution des taux plasmatiques au cours du temps pour
l'essai 4b avec celle des essais 3c et 3d permet au
pharmaco-cinéticien d'évaluer avec une bonne précision la
quantité moyenne de pentasaccharide administrée au cours du
CA 02211794 1997-07-17
WO 96122808 PCTIFR96/00114
traitement. Cette quantité est nulle pour l'essai passif 4a
et de 8, 45 1,5 mg de pentasaccharide pour l'essai 4b.
TABLEAU IV
5
ESSAI 4a 4b
Nature du traitement passif ionophorèse
Nombre d'animaux traités 2 4
Densité de courant (mA/cm2) 0 0,125
Taux plasmatique initial 0 0
Taux plasmatique à 0,5 heure 0 0,11 0,05
Taux plasmatique à 1 heure 0 0,16 0,05
Taux plasmatique à 2 heures 0 0,28 0,1
Taux plasmatique à 4 heures 0 0,64 0,2
Taux plasmatique à 6 heures 0 0,57 0,18
Taux plasmatique à 8 heures 0 0r.59 0,15
Taux plasmatique à 10 heures 0 0,61 0,16
Taux plasmatique à 12 heures 0 0?58 0,05
Taux plasmatique à 16 heures 0 0,2 0,05
Taux plasmatique à 26 heures 0 0,14 0,02
Taux plasmatique à 30 heures 0 0,05 t 0,02
Par rapport à l'essai précédent, pour lequel on
avait engagé 80 mg de pentasaccharide, on observe une
meilleure biodisponibilité, soit environ 21 % pour l'essai
10 4b contre environ 9 % pour l'essai 3b. On observe également
un meilleur rendement électrique, puisque la quantité de
pentasaccharide administrée par mAh était de 292 g/cm2 pour
l'essai 3b alors qu'elle est de 372 g/cm2 pour l'essai 4 b.
Cette approche par inversion périodique et
15 équilibrée du courant, qui permet de consommer dans chaque
réservoir une partie des ions chlorures générés par la
réduction du chlorure d'argent lors de la phase précédente,
diminue la compétition des ions chlorures par rapport aux
ions thérapeutiques et autorise la diminution des quantités
20 de principe actif par unité de surface. Elle a montré, en
CA 02211794 1997-07-17
WO 96/22808 PCT/FR96/00114
31
outre, l'intérêt d'employer des électrodes réversibles qui
empêchent les réactions d'oxydoréduction qui pourraient
affecter le principe actif qui se trouve alternativement
dans un compartiment anodique puis cathodique.
Les appareils d'ionophorèse pouvant désormais être
miniaturisés et d'un port tout à fait compatible avec une
vie quotidienne normale, l'ionophorèse pratiquée selon
l'invention constitue une voie galénique particulièrement
intéressante pour l'administration de pentasaccharides du
type précité et plus largement d'oligosaccharides anioniques
analogues ou voisins.