Note: Descriptions are shown in the official language in which they were submitted.
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
COMPOSITIONS COMPRENANT DES ACIDES NUCLEIQUES INCORPORES DANS DES PARTICULES
MINERALES BILAMELLAIRES
La présente invention se rapporte à des compositions comprenant au moins un
acide nucléique et une particule minérale ayant une structure à feuillets
échangeables,
leur procédé de préparatïon et leurs applications pour la transfection i~
vivo, in vitro
et/ou ex vivo d'acides nucléiques.
Avec le développement des biotechnologies, la possibilité de transférer
efficacement des acides nucléiques dans les cellules (c'est-à-dire de les
introduire
dans les cellules de façon à ce que le gène d'intérêt qu'ils portent y soit
exprimé) est
devenue une technique de base avec de nombreuses applications
biotechnologiques. Il
peut s'agir du transfert d'acides nucléiques dans des cellules ih vitro , par
exemple
pour la production de protéines recombinantes, ou au laboratoire pour l'étude
de la
régulation de l'expression des gènes, le clonage de gènes ou tout autre
manipulation
impliquant l'ADN. Il peut également s'agir du transfert d'acides nucléiques
dans des
cellules i~ vivo, par exemple pour la réalisation de vaccins, des études de
marquage
ou également des approches thérapeutiques. Il peut encore s'agir du transfert
de gènes
ex vivo dans des cellules prélevées d'un organisme, en vue de leur
réadministration
ultérieure, par exemple pour la création d'animaux transgéniques.
Il existe à ce jour de nombreuses méthodes de transfert d'acides nucléiques
dans des cellules : La précipitation au phosphate de calcium,
l'électroporation, la
microinjection, l'infection virale, l'injection d'ADN nu, ou encore
l'utilisation de
vecteurs non-viraux, comme par exemple les polymères cationiques, les vecteurs
biochimiques (constitués d'une protéine cationique associée à un récepteur
cellulaire),
ou encore les lipofectants, et plus particulièrement les lipides cationiques.
Toutefois, ces techniques développées à ce jour présentent de nombreux
inconvénients qui limitent l'efficacité de la transfection et ne permettent
pas de
résoudre de manière satisfaisante les difficultés liées au transfert de gènes
dans les
cellules et/ou l'organisme. Ainsi, la précipitation au phosphate de calcium
est une
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
2
méthode qui est assez inefficace, notamment par rapport à l'injection d'ADN
nu, et
elle a donc été abandonnée depuis longtemps. S'il a été montré que l'injection
d'acides nucléiques « nus », c'est-à-dire non-formulés, permet d'obtenir des
niveaux
de transfection acceptables dans certains types cellulaires ih vivo (voir
notamment la
demande de brevet W090/11092), les acides nucléique nus ne jouissent cependant
que d'une demi-vie plasmatique courte, en raison de leur dégradation par les
enzymes
et de leur élimination par les voies urinaires. Le niveau d'efficacité de
transfert de
gènes par injection d'acide nucléique nu reste trop faible pour la plupart des
applications envisagées. L'utilisation de polymères ou de lipides cationiques
constitue
ainsi un remède possible vis-à-vis des dégradations enzymatiques que subit
l'ADN à
transfecter, mais il a été souvent constaté que leur utilisation inhibe plus
ou moins
fortement l'efficacité de transfection dans le muscle et qu'ils induisent en
outre une
toxicité à l'égard des cellules. Si les virus recombinants permettent
d'obtenir une
bonne efficacité de transfert des acides nucléiques, leur emploi présente
cependant
certains risques liés à leur nature virale tels que la pathogénicité, la
transmission, la
réplication, la recombinaison, la transformation, fimmunogénicité, etc... Il
est donc
préférable d'éviter les techniques de transfection virale. Enfin, des
techniques telles
que l'électroporation constituent une alternative intéressante mais limitée à
une
administration locale. Elles provoquent bien souvent des dégats irréversibles
sur les
membranes cellulaires. Il apparaît donc qu'il serait souhaitable de disposer
d'un
vecteur de transfert qui permette à la fois de protéger les acides nucléiques
des
dégradations enzymatiques et d'obtenir une efficacité de transfert
satisfaisante dans
les cellules, sans pour autant les endommager ni induire de toxicité.
La présente invention apporte une solution avantageuse à ces problèmes. La
demanderesse a en effet montré que les compositions comprenant un acide
nucléique
et une particule minérale ayant une structure à feuillets échangeables
permettent le
transfert in vitro, ex vivo ou in vivo dudit acide nucléique dans une cellule
et/ou un
organe avec une efficacité supérieure à celles obtenues à ce jour avec les
techniques
classiques de transfert non-viral. Les compositions de l'invention permettent
en outre
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
3
d'éviter les inconvénients liés à l'emploi de vecteurs viraux ou de techniques
physiques de transfection.
Ainsi, un premier objet de la présente invention concerne les compositions
comprenant au moins un acide nucléique et une particule minérale ayant une
structure
à feuillets échangeables.
Au sens de l'invention, on entend par « particules minérales ayant une
structure à feuillets échangeables » des particules minérales dont la
structure est basée
sur un empilement de feuillets de composition M(OH)2 analogues à ceux bien
connus
de la brucite (Mg(OH)Z), M représentant un métal divalent, mais dans lesquels
une
partie des métaux divalents est remplacée par des métaux trivalents de façon à
rendre
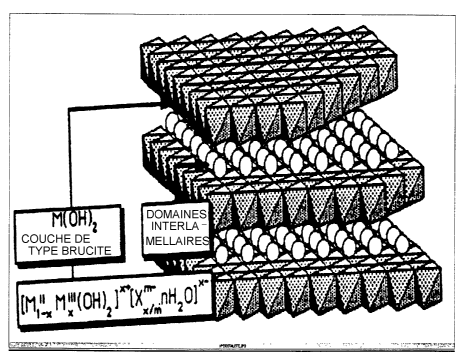
les feuillets globalement cationiques. Les espaces inter-feuillets comprennent
des
entités anioniques solvatées par des molécules d'eau. Une telle structure est
représentée à la figure 1 et est également appelée « hydroxyde double
lamellaire ».
Ces particules ont pour formule générale
II III x+ m- x-
~MI-x Mx WH)2j L~x~m .nHZOj
dans laquelle M~ représente un cation métallique divalent, MIn représente un
cation
métallique trivalent, Xm représente un anion interfoliaire et m est un entier
supérieur
ou égal à 1, x est compris entre 0 et 1 strictement, et n est strictement
supérieur à 0.
De telles particules minérales ont déjà été décrites pour des applications
dans
de nombreux domaines tels que la catalyse ou l' environnement. En effet, elles
forment des matériaux nanostructurés où des espèces moléculaires ou
colloïdales sont
intercalées dans une structure hôte lamellaire. Les propriétés de ces
stnlctures peuvent
ainsi être mises à profit en catalyse hétérogène ou homogène sur support, dans
des
techniques d'échanges et de séparation notamment des isomères optiques, pour
la
conception de membranes éventuellement sélectives pour filtration et
perméation,
pour le piégeage et la restitution contrôlée de molécules, ou encore pour la
conception
de matériaux et dépôts électro-actifs, d'électrodes et de dispositifs
électroniques.
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
4
Ainsi l'article de Choy et al (1999, J. Am. Chem. Soc. 121(6), 1399-1400)
décrit la préparation de nanoparticules hybrides composées de feuillets d'un
Hydroxyde Double Lamellaire (HDL), la pristine (Mg2Al(N03)-LDH), entre
lesquels
sont intercalés des nucléosides monophoshatés ou des fragments d'ADN de
testicules
de hareng. Les molécules nucléiques intercalées dans les particules décrites
dans cet
article présentent une taille inférieure à 1000 paires de bases. Aucune
utilisation de
ces molécules n'est décrite.
Cependant, de telles particules minérales n'avaient jamais été utilisées pour
le
transfert d'acides nucléiques et rien ne laissait prévoir qu'il serait
possible d'obtenir
une très nette amélioration de l'efficacité de transfert, en particulier par
rapport aux
résultats de transfection obtenus par injection d'ADN nu ou formulé avec les
vecteurs
synthétiques classiques tels que les lipides cationiques.
Les particules minérales ayant une structure à feuillets échangeables
utilisables dans le cadre de la présente invention sont souvent nommées
d'après la
I S nature des cations métalliques majeurs des feuillets : par exemple
l'hydrotalcite (Mg-
Al), la pyroaurite (Mg-Fe), la stichtite (Mg-Cr) ou encore la takovite (Ni-
Al). La
formule générale indiquée ci-avant sous-tend la grande variété des particules
minérales qu'il est possible de préparer en faisant varier la nature des deux
cations
métalliques Mai et MIII, leurs proportions respectives avec extension possible
à plus de
deux types de cations (par exemple Mg, Zn et Al), la nature des anions
interfoliaires,
ou encore l'état d'hydratation. En outre, la richesse de la formule générale
indiquée
ci-avant est encore accrue par une diversité structurale résultant de
l'existence de
polytypes différant par la séquence d'empilement des feuillets ainsi que de
l'apparition de surstructures dues par exemple à un classement cationique dans
le
feuillet hydroxylé.
Les cations métalliques divalents M° peuvent être choisis par
exemple parmi
le magnésium (Mg), le chrome (Cr), le manganèse (Mn), 1e fer (Fe), le nickel
(Ni), le
cobalt (Co), le cuivre (Cu), le calcium (Ca) ou encore le zinc (Zn). De
préférence, le
cation métallique divalent est Ie magnésium. Les cations métalliques
trivalents Muj
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
peuvent être choisis par exemple parmi l'aluminium (Al), le chrome (Cr), le
manganèse (Mn), le fer (Fe), le nickel (Ni), le cobalt (Co) ou encore le
gallium (Ga).
De préférence, le cation métallique trivalent est l'aluminium. En outre, les
deux
membres du couple M~ et M« peuvent également correspondre au même élément (par
5 exemple Fen/Fei~ ou MnB/MnIB).
Les anions interfoliaires Xm- peuvent être par exemple choisis parmi les
halogénures, les oxoanions, les iso- et hétéroanions, les anions complexes, ou
encore
les anions organiques. Citons à titre d'exemple les fluorures, les chlorures,
les
bromures, les carbonates, les nitrates, les sulfates ou encore les oxoanions
tétraédriques tels que Cr042-. De préférence, l'anion est choisi parmi les
carbonates
C032-.
La valeur de x est comprise strictement entre 0 et 1, c'est-à-dire que 0 et 1
sont des valeurs exclues. De préférence, x est compris entre 0,05 et 0,95, et
de
préférence entre 0,1 et 0,9. Encore plus préférentiellement, x est compris
entre 0,2 et
0,85. A titre d'exemple, x peut être égal à 0,25. En ce qui concerne la valeur
de n,
celle-ci indique l'état d'hydratation de la particule en question et elle est
strictement
supérieure à 0. De préférence, n est supérieur ou égal à 0,1. Par exemple, n
peut être
égal à 0,5. m est un entier supérieur ou égal à 1 qui représente la charge de
l'anion
interfoliaire. Par exemple, m peut être égal à l, 2, 3, 4, 5 ou 6.
Des particules minérales ayant une structure à feuillets échangeables selon la
présente invention peuvent être choisies par exemple parmi l'hydrotalcite de
formule
Mg6A1zC03(OH),6.4H20, la manasseite de formule Mg6A12C03(OH)i6..4H20, la
pyroaurite de formule Mg6Fe2C03(OH)16.4H~0, la stichtite de formule
Mg6Cr2C03(OH)16.4H20, la takovite de formule Ni6A12C03(OH)i6.4H20, la
reevesite
de formule Ni6Fe2C03(OH)16.4H20, ou encore la comblainite de formule
Ni6Co2C03(OH)16.4H20. D'autres particules minérales ayant une structure à
feuillets
échangeables peuvent également convenir.
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
6
De préférence, les compositions selon la présente invention comprennent au
moins un acide nucléique et de l'hydrotalcite de formule Mg6AlZC03(OH)I6.4H20.
Les particules minérales ayant une structure à feuillets échangeables selon la
présente invention sont soit commerciales, soït elles peuvent être préparées
selon des
méthodes qui s'apparentent aux méthodes connues dites de « chimie douce ».
Notamment, la préparation des particules minérales selon l'invention peut être
basée
sur la précipitation contrôlée de solutions ou de suspensions aqueuses
contenant à la
fois les cations métalliques destinés à prendre place dans la charpente
hydroxylée et
les anions destinés à occuper les domaines interlamellaires. Dans ces
conditions, il y a
simultanément construction des domaines interlamellaires constitués d'anions
et de
molécules d'eau, et du feuillet. La nature et la texture des phases obtenues
sont
fortement dépendantes des conditions opératoires (température, vitesse
d'addition et
concentration des réactifs, contrôle du pH), mais aussi de la géométrie du
réacteur et
de l'état d'association préalable des cations métalliques dans les réactifs
(existence
d'oligomères). Le procédé de préparation se ramène finalement toujours à
mettre en
présence, à concentration et réactivité adéquates, les espèces conduisant à la
construction des particules minérales dans des conditions optimales. Ces
conditions
optimales sont déterminées au cas par cas selon la méthode classique des
tâtonnements.
On entend au sens de l'invention par "acide nucléique" aussi bien un acide
désoxyribonucléique qu'un acide ribonucléique. Il peut s'agir de séquences
naturelles
ou artificielles, et notamment d'ADN génomique (ADNg), d'ADN complémentaire
(ADNc), d'ARN messager (ARNm), d'ARN de transfert (ARNt), d'ARN ribosomique
(ARNr), de séquences hybrides ou de séquences synthétiques ou semi-
synthétiques,
d'oligonucléotides modifiés ou non. Ces acides nucléiques peuvent être par
exemple
d'origine humaine, animale, végétale, bactérienne ou virale. Ils peuvent être
obtenus
par toute technique connue de l'homme du métier, et notamment par criblage de
banques, par synthèse chimique, ou encore par des méthodes mixtes incluant la
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
modification chimique ou enzymatique de séquences obtenues par criblage de
banques. Ils peuvent être modifiés chimiquement.
Concernant plus particulièrement les acides désoxyribonucléiques, ils
peuvent être simple ou double brin ou encore des oligonucléotides courts ou
des
séquences plus longues. En particulier, les acides nucléiqûes sont
avantageusement
constitués par exemple par des plasmides, des vecteurs, des épisomes ou des
cassettes
d'expression. Ces acides désoxyribonucléiques peuvent notamment porter une
origine
de réplication fonctionnelle ou non dans la cellule cible, un ou plusieurs
gènes
marqueurs, des séquences régulatrices de la transcription ou de la
réplication, des
gènes d'intérêt thérapeutique, des séquences antisens modifiées ou non ou
encore des
régions de liaison à d'autres composants cellulaires.
De préférence, Iedit acide nucléique présente une taille supérieure à 1000
paires de bases. Encore plus préférentiellement il présente une taille
comprise entre
environ 1000 paires de bases et environ 2.000.000 paires de bases (2 Mb),
environ
1000 paires de bases et environ 100.000 paires de bases ( 100 kb), et environ
1000
paires de bases et environ 20.000 paires de bases (20 kb).
De manière avantageuse l'acide nucléique comprend un ou plusieurs gènes
d'intérêt thérapeutique sous contrôle de séquences de régulation, par exemple
un ou
plusieurs promoteurs et un terminateur transcriptionnel actifs dans les
cellules cibles.
Au sens de l'invention, on entend par gène d'intérêt thérapeutique notamment
tout gène codant pour un produit protéique ayant un effet thérapeutique. Le
produit
protéique ainsi codé peut être notamment une protéine ou un peptide. Ce
produit
protéique peut être exogène homologue ou endogène vis-à-vis de la cellule
cible,
c'est-à-dire un produit qui est normalement exprimé dans la cellule cible
lorsque
celle-ci ne présente aucune pathologie. Dans ce cas, l'expression d'une
protéine
permet par exemple de pallier une expression insuffisante dans la cellule ou
(expression d'une protéine inactive ou faiblement active en raison d'une
modification,
ou encore de surexprimer ladite protéine. Le gène d'intérêt thérapeutique peut
aussi
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
8
coder pour un mutant d'une protéine cellulaire ayant par exemple une stabilité
accrue
ou une activité modifiée. Le produit protéique peut également être hétérologue
vis-à
vis de la cellule cible. Dans ce cas, une protéine exprimée peut par exemple
compléter
ou apporter une activité déficiente dans la cellule, lui permettant de lutter
contre une
pathologie, ou stimuler une réponse immunitaire.
Parmi les produits thérapeutiques au sens de la présente invention, on peut
citer plus particulièrement les enzymes, les dérivés sanguins, les hormones,
les
lymphokines (par exemple les interleukines, les interférons ou le TNF : voir
FR 92/03120), les facteurs de croissance, les neurotransmetteurs ou leurs
précurseurs
ou enzymes de synthèse, les facteurs trophiques (par exemple BDNF, CNTF, NGF,
IGF, GMF, aFGF, bFGF, VEGF, NT3, NTS ou HARP/pléiotrophine), les
apolipoprotéines (par exemple ApoAI, ApoAIV ou ApoE : voir FR 93/05125), la
dystrophine ou une minidystrophine (FR 91/11947), la protéine CFTR associée à
la
mucoviscidose, les gènes suppresseurs de tumeurs (par exemple p53, Rb, RaplA,
I S DCC ou k-rev : voir FR 93/04745), les gënes codant pour des facteurs
impliqués dans
la coagulation (Facteurs VII, VIII, IX), les gènes intervenant dans la
réparation de
l'ADN, les gènes suicides (thymidine kinase, cytosine déaminase), les gènes de
l'hémoglobine ou d'autres transporteurs protéiques, les enzymes du métabolisme
ou
catabolisme.
L'acide nucléique d'intérêt thérapeutique peut également être un gène ou une
séquence antisens, dont l'expression dans la cellule cible permet de contrôler
l'expression de gènes ou la transcription d'ARNm cellulaires. De telles
séquences
peuvent, par exemple, être transcrites dans la cellule cible en ARN
complémentaires
d'ARNm cellulaires et bloquer ainsi leur traduction en protéine, selon la
technique
décrite dans le brevet EP 140 308. Les gènes thérapeutiques comprennent
également
les séquences codant pour des ribozymes, qui sont capables de détruire
sélectivement
des ARN cibles (EP 321 201).
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
9
Comme indiqué plus haut, l'acide nucléique peut également comporter un ou
plusieurs gènes codant pour un peptide antigénique, capable de générer chez
(homme
ou l'animal une réponse immunitaire. Dans ce mode particulier de mise en
oeuvre,
(invention permet la réalisation soit de vaccins soit de traitements
immunothérapeutiques appliqués à l'homme ou à l'animal, notamment contre des
micro-organismes, des virus ou des cancers. il peut s'agir notamment de
peptides
antigéniques spécifiques du virus d'Epstein Barr, du virus HIV, du virus de
l'hépatite
B (EP 1 ~5 573), du virus de la pseudo-rage, du "syncitia forming virus",
d'autres virus
ou encore de peptides antigéniques spécifiques de tumeurs (EP 259 212).
Comme indiqué précédemment, (acide nucléique comprend de préférence
également des séquences permettant l'expression du gène d'intérêt
thérapeutique et/ou
du gène codant pour le peptide antigénique dans la cellule ou l'organe désiré.
Il peut
s'agir des séquences qui sont naturellement responsables de l'expression du
gène
considéré lorsque ces séquences sont susceptibles de fonctionner dans la
cellule
infectée. Il peut également s'agir de séquences d'origine différente
(responsables de
(expression d'autres protéines, ou même synthétiques). Notamment, il peut
s'agir de
séquences promotrices de gènes eucaryotes ou viraux. Par exemple, il peut
s'agir de
séquences promotrices issues du génome de la cellule que l'on désire infecter.
De
même, il peut s'agir de séquences promotrices issues du génome d'un virus. A
cet
égard, on peut citer par exemple les promoteurs des gènes EIA, MLP, CMV, RSV
ou
HSV. En outre, ces séquences d'expression peuvent être modifiées par exemple
par
addition de séquences d'activation ou de régulation. Il peut aussi s'agir de
promoteurs
inductibles ou répressibles.
Par ailleurs, (acide nucléique peut également comporter, en particulier en
amont du gène d'intérêt thérapeutique, une séquence signal dirigeant le
produit
thérapeutique synthétisé dans les voies de sécrétion de la cellule cible.
Cette séquence
signal peut être la séquence signal naturelle du produit thérapeutique, mais
il peut
également s'agir de toute autre séquence signal fonctionnelle, ou d'une
séquence
signal artificielle. L'acide nucléique peut également comporter une séquence
signal
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
dirigeant le produit thérapeutique synthétisé vers un compartiment particulier
de la
cellule.
Les çompositions selon la présente invention peuvent être préparées par
mélange d'une solution aqueuse contenant une particule minérale ayant une
structure
5 à feuillets échangeables et d'une solution contenant les acides nucléiques.
Plus
précisément, les compositions selon la présente invention peuvent être
préparées en
mettant les particules minérales ayant une structure à feuillets échangeables
en
solution aqueuse à un pH proche de la neutralité~(par exemple entre 6 et 8, et
plus
préférentiellement entre 6,5 et 7,5), puis en ajoutant la solution aqueuse
ainsi obtenue
10 à une solution contenant les acides nucléiques ou bien en ajoutant ladite
solution
contenant les acides nucléiques à la solution aqueuse de particules minérales
ayant
une structure à feuillets échangeables. La solution contenant les acides
nucléiques est
de préférence une solution isotonique dans du chlorure de sodium ou dans du
glucose.
De préférence, les particules minérales ayant une structure à feuillets
échangeables et
les acides nucléiques sont introduits dans la composition en quantités telles
que le
rapport massique entre les particules minérales ayant une structure à
feuillets
échangeables et les acides nucléiques est compris entre 0,01 et 1000, de
préférence
entre 0,01 et 500, plus préférentiellement entre 0,01 et 100, et encore plus
préférentiellement entre 0,5 et 100. En tout état de cause, les quantités
respectives de
chaque composant peuvent être ajustées et optimisées aisément par l'homme du
métier par la méthode habituelle des tâtonnements, en fonction de la particule
minérale ayant une structure à feuillets échangeables utilisée, de (acide
nucléique, et
des applications recherchées (notamment du type cellulaire à transfecter).
L'invention a également pour objet les compositions telles que défnies ci-
avant pour utilisation comme médicament.
L'invention a également pour objet l'utilisation des compositions telles que
définies ci-avant pour le transfert d'acides nucléiques dans les cellules in
vitro, in vivo
ou ex vivo. Plus précisément, la présente inventïon a pour objet l'utilisation
des
compositions telles que définies ci-avant pour la préparation d'un médicament
destiné
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
11
à traiter les maladies, en particulier les maladies qui résultent d'une
déficience en un
produit protéique ou nucléique. L'acide nucléique contenu dans ledit
médicament
code ledit produit protéique ou nucléique, ou constitue ledit produit
nucléique, apte à
corriger lesdites maladies in vivo ou ex vivo. Ledit médicament peut en outre
être un
vaccin et dans ce cas, l'acide nucléique transfecté induit une réponse
immunitaire.
Pour des utilisations in vivo, par exemple en thérapie ou pour l'étude de la
régulation de gènes ou la création de modèles animaux de pathologies, les
compositions selon l'invention peuvent être formulées en vue d'administrations
notamment par voie topique, cutanée, orale, rectale, vaginale, parentérale,
intranasale,
intraveineuse, intramusculaire, sous-cutanée, intraoculaire, transdermique,
intratrachéale ou intrapéritonéale. De préférence, les compositions de
l'invention
contiennent un véhïcule pharmaceutiquement acceptable pour une formulation
injectable, notamment pour une injection directe au niveau de l'organe désiré,
ou pour
une administration par voie topique (sur peau et/ou sur muqueuse). Il peut
s'agir en
particulier de solutions stériles, isotoniques, ou de compositions sèches,
notamment
lyophilisées, qui, par addition selon le cas d'eau stérilisée ou de sérum
physiologique,
permettent la constitution de solutés injectables. En outre, les compositions
selon
l'invention peuvent contenir un ou des adjuvants classiquement utilisés en
pharmacie.
Les doses d'acides nucléiques utilisées pour l'injection ainsi que le nombre
d'administrations peuvent être adaptées en fonction de différents paramètres,
et
notamment en fonction du mode d'administration utilisé, de la pathologie
concernée,
du gène à exprimer, ou encore de la durée du traitement recherchée. En ce qui
concerne plus particulièrement le mode d'administration, il peut s'agir . soit
d'une
injection directe dans les tissus, par exemple au niveau des tumeurs, ou dans
les voies
circulatoires, soit d'un traitement de cellules en culture suivi de leur
réimplantation ih
vivo, par injection ou greffe. Les tissus concernés dans le cadre de la
présente
invention sont par exemple les muscles, la peau, le cerveau, les poumons, le
foie, la
rate, la moelle osseuse, le thymus, le coeur, la lymphe, le sang, les os, les
cartilages, le
pancréas, les reins, la vessie, l'estomac, les intestins, les testicules, les
ovaires, le
rectum, le système nerveux, les yeux, les glandes ou les tissus conjonctifs.
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
12
Un autre objet de la présente invention concerne une méthode de transfert
d'acides nucléiques dans les cellules comprenànt les étapes suivantes
(1) la formation d'une composition comprenant au moins un acide nucléique et
une
particule minérale ayant une structure à feuillets échangeables telle que
définie
précédemment, et
(2) la mise en contact des cellules avec la composition formée en (1).
Plus particulièrement, la présente invention concerne une méthode de
traitement thérapeutique du corps humain ou animal comprenant les étapes
suivantes
(1) la formation d'une composition comprenant au moins un acide nucléique et
une
particule minérale ayant une structure à feuillets échangeables telle que
définie
précédemment, et
(2) la mise en contact des cellules du corps humain ou animal avec la
composition
formée en ( 1 ).
La mise en contact des cellules avec la composition selon la présente
invention
peut être réalisée par incubation des cellules avec ladite composition ou par
injection
de la composition dans l'organisme ou une partie de l'organisme. L'incubation
est
réalisée de préférence en présence de par exemple de 0,01 à 1000 ~g d'acide
nucléique pour 106 cellules. Pour une administration in vivo, des doses
d'acide
nucléique allant de 0,01 à 10 mg peuvent par exemple être utilisées.
Les compositions de l'invention peuvent en outre contenir un ou plusieurs
adjuvants pharmaceutiquement acceptables. Dans ce cas, le ou les adjuvants
sont
préalablement mélangés à la solution aqueuse contenant la particule minérale
ayant
une structure à feuillets échangeables selon (invention et/ou à la solution
d'acide(s)
nucléique(s).
La présente invention fournit ainsi une méthode particulièrement
avantageuse pour le transfert d'acides nucléiques, notamment pour le
traitement de
maladies, comprenant l'administration ifa vivo ou ex vivo d'un acide nucléique
codant
pour une protéine ou pouvant être transcrit en un acide nucléique apte à
corriger ladite
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
13
maladie, ledit acide nucléique étant associé à une particule minérale ayant
une
structure à feuillets échangeables telle que définie précédemment dans les
conditions
définies ci-avant.
Les compositions selon la présente invention sont particulièrement utiles pour
le transfert d'acides nucléiques dans des cellules primaires ou dans des
lignées établies.
Il peut s'agir par exemple de cellules fibroblastiques, musculaires, nerveuses
(neurones, astrocytes, cellules gliales), hépatiques, hématopoiétiques (par
exemple les
lymphocytes, CD34, ou dendritiques) ou épitheliales, sous forme différenciées
ou
pluripotentes (précurseurs).
Outre les dispositions qui précèdent, la présente invention comprend
également d'autres caractéristiques et avantages qui ressortiront des exemples
et
figures qui suivent, et qui doivent être considérés comme illustrant
l'invention sans en
limiter la portée.
FIGURES
Fi _ r~ structure idéalisée des particules minérales ayant une structure à
feuillets
échangeables (hydroxydes doubles lamellaires) selon la présente invention.
Fi vre 2 : représentation schématique de l'hydrotalcite Mg6A12C03(OH)i6.4H~0.
Fi.. u~ re 3 _ mesure du potentiel zéta de particules d'hydrotalcite seules en
solution.
Fore 4: mesure du potentiel zéta de compositions contenant des particules
d'hydrotalcite et de l'ADN dans un rapport massique égal à 0,5.
Fil: Mesure du pourcentage d'ADN restant dans le surnageant par râpport à la
quantité initiale d'ADN introduite, en fonction du rapport massique
hydrotalcite/ADN. Les mesures ont été faites pour trois concentrations
différentes
d'ADN introduites : 20 p,g d'ADN/ml, 50 pg d'ADN/ml, et 100 pg d'ADN/ml.
Figure 6 : Electrophorèse sur gel d'agarose de différentes formulations d'ADN.
La
colonne « a » constitue le contrôle (ADN non-formulé et non-soumis aux
nucléases),
la colonne « b » représente l'ADN non-formulé soumis aux nucléases, et les
colonnes
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
14
« c » à « f » représentent des compositions hydrotalcite/ADN à des rapports
massiques
de 0,125 ou 0,25 ou 0,5 ou 1 qui sont soumises aux nucléases.
Fi re 7 : visualisation sous forme d'histogramme de l'efficacité de transfert
de gène
in vivo (par injection dans le muscle tibial cranial de souris) de
compositions
ADN/hydrotalcite dans différents rapports massiques, comparativement à
l'injection
d'ADN nu.
Fi re 8: Représentation schématique du plasmide pXL3031 utilisé dans les
expériences de transfert d'ADN dans les cellules
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
EXEMPLES
A1 MATÉRIEL ET MÉTHODES
Souris utilisées
Les souris utilisées dans les expériences de transfert in vivo de gènes sont
des souris
5 femelles C57B16 âgées de 8 semaines, et réparties en 9 groupes de 12 souris.
Particule minérale selon l'invention utilisée
la particule minérale ayant une structure à feuillets échangeables utilisées
dans les
différents essais est l'hydrotalcite en solution aqueuse à une concentration
de 20 g/1 et
à pH 7. Cette hydrotalcite est commercialisée par la société Süd-Chemie AG
10 (Allemagne).
ADN
Le plasmide utilisé est le pXL3031 qui contient le gène luc codant pour la
luciférase
sous contrôle du promoteur P/E CMV du cytomégalovirus, représenté à la figure
8. Sa
taille est de 3671 bp. La solution de plasmide utilisée contient 320 pg
d'ADN/ml dans
15 une solution de chlorure de sodium (NaCI) à 150 mM.
Complexes hydrotalcite/ADN
Les complexes sont préparés par mélange équivolumétrique de deux solutions :
l'une
contenant l'hydrotalcite et l'autre l'ADN plasmidique.
Exemple I : Mesure des potentiels zéta de l'hydrotalcite seul et des complexes
ADN/hydrotalcite
Le but de cet exemple est de montrer que l'ADN est capable de s'associer avec
une
particule minérale ayant une structure à feuillets échangeables telle que
l'hydrotalcite.
La mesure du potentiel zéta renseigne sur la nature de la charge de surface
d'une
particule placée dans un liquide. Le potentiel zéta n'est pas une mesure
directe de la
charge de surface, mais est le potentiel qui existe autour de le particule
lorsque celle
ci se déplace dans une solution lorsqu'elle est soumise à un champs
électrique. Par
conséquent si les particules ont une charge de surface positive, le potentiel
zéta, qui
est la seule grandeur mesurable, sera lui aussi positif. Le potentiel zéta
joue un rôle
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
16
déterminant dans la stabilité colloïdale des particules en solution. En effet,
lorsque le
potentiel zéta est fortement positif ou négatif, les particules ne s'agrègent
pas car des
forces de répulsions électrostatiques les maintiennent isolées. Par contre,
les
particules qui possèdent un potentiel zéta proche de zéro ne sont pas stables
car les
forces de Van Der Waals attirent les particules entre elles, et les font
précipiter.
Le potentiel zéta de l'hydrotalcite et des complexes hydrotalcite/ADN a été
mesuré
par un zétamètre de marque Coulter (Delsa 440 SX). La solution d'hydrotalcite
contenait 0,15 mg d'hydrotalcite/ml dans une solution de chlorure de sodium
(NaCI) à
20 mM, soit une conductivité de 2,3 mS/cm. Les complexes hydrotalcite/ADN ont
été
préparés â des concentrations de 250 ~g d'ADN/ml dans une solution de chlorure
de
sodium (NaCI) à 20 mM, au rapport massique de 0,5. La mesure a été effectuée
en
appliquant un champs électrique de 1,5 mA pendant 60 secondes.
La figure 3 représente le potentiel zéta de l'hydrotalcite seul avant d'être
mélangé
avec l'ADN. Ce potentiel zéta est de + 32 mV et indique donc une charge en
surface
globalement cationique, ce qui est cohérent avec la structure et la
composition de
l'hydrotalcite (voir figures 1 et 2). La figure 4 représente le potentiel zéta
de
complexes hydrotalcite/ADN au rapport massique de 0,5. Dans ce cas, le
potentiel
zéta est de - 41 mV. La charge de surface a donc été modifiée et est à présent
globalement anionique, ce qui indique que les molécules d'ADN anioniques se
sont
associées sur la surface de l'hydrotalcite modifiant ainsi sa charge de
surface.
Exemple 2 : Mise en évidence de l'association entre l'ADN et les particules
minérales ayant une structure à feuillets échangeables telle que
I'hydrotalcite
Le but de cet exemple est de montrer que les particules minérales ayant une
structure
à feuillets échangeables telle que l'hydrotalcite s'associent avec l'ADN.
Des isothermes d'adsorption sont réalisées en mélangeant des quantités
croissantes
d'hydrotalcite avec une quantité constante d'ADN. Les mélanges
hydrotalcite/ADN
sont préparés par mélange équivolumétrique d'une solution contenant l'ADN et
d'une
solution contenant l'hydrotalcite. L'ensemble de ces mélanges est ensuite
ultracentrifugé à 50000 tour/minute pendant 10 minutes (Ultracentrifugeuse
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
17
Beckman TL100). Le graphique de la figure 5 indique que la quantité d'ADN
présente dans le surnageant diminue progressivement avec l'augmentation du
rapport
massique hydrotalcite/ADN. A un rapport hydrotalcite/ADN de 50 poids/poids, il
n'y
a plus d'ADN présent dans le surnageant. Ceci indique que toutes les molécules
d'ADN sont associées avec l'hydrotalcite et se trouvent dans le culot après
ultracentrifugation. Le même phénomène a été observé à trois concentrations
d'ADN
différentes : 20, 50 et 100 ~.g d'ADN/ml. Par conséquent, on peut en déduire
qu'il y a
bien association entre l'hydrotalcite et l'ADN. '
Exemple 3 : Protection de l'ADN vis-à-vis des dégradations causées par les
nucléases
Le but de cet exemple est de montrer que l'ADN est protégé vis-à-vis des
dégradations enzymatiques lorsqu'il est associé à une particule minérale ayant
une
structure à feuillets échangeables telle que l'hydrotalcite.
Des échantillons d'ADN nu et d'ADN formulé avec l'hydrotalcite ont été soumis
au
test de résistance aux dégradations causées par les nucléases. Pour cela, les
échantillons ont été incubés avec un prélèvement de liquide musculaire. La
figure 6
indique que lorsque l'ADN est associé avec l'hydrotalcite à différents
rapports
massiques (colonnes « c », « d », « e » et « f »), il n'est pas dégradé par
les nucléases
puisqu'il est tout à fait possible d'observer une bande d'ADN sur le gel. Par
contre, la
colonne « b » qui rëprésente l'ADN nu non-associé avec l'hydrotalcite est
totalement
dégradé par les nucléases car au lieu d'avoir une bande d'ADN bien identifiée
sur le
gel, on observe une multitude de petits fragments qui migrent dans Ie gel.
Ainsi, lorsque l'ADN est associé avec les particules minérales d'hydrotalcite,
il est
protégé de l'action de dégradation des nucléases, par opposition à l'ADN nu
qui est
rapidement dégradé. Cette propriété conférée par les particules minérales
ayant une
structure à feuillets échangeables telle que l'hydrotalcite est trés
intéressante car une
plus grande quantité d'ADN peut ainsi atteindre le noyau des cellules pour y
être
transcrit, avec les conséquences bénéfiques que cela implique en terme
d'efficacité de
transfection.
CA 02395742 2002-06-26
WO 01/49869 PCT/FR00/03702
18
Exemple 4 : Transfection in vivo de complexes hydrotalcite l ADN
a) Injections
Les injections ont été réalisées en bilatéral dans le muscle tibial cranial
des souris à
raison de 25 ~,l /muscle, soit 4 ~g d'ADN/muscle.
Les animaux sont anesthésiés avec 250 ~l de Ketamine/Xylazine par voie
intrapéritonéale (3,9 ml d'imalgène 1000, 0,6 ml Rompun à 2%, et 40,5 ml d'une
solution de chlorure de sodium NaCI à 150 mM). Ensuite, les animaux sont rasés
et
inj ectés au niveau des deux muscles tibial cranial.
b) Prélèvement des muscles
IO Les muscles tibial cranial sont repris 6 jours post-injection dans I ml de
tampon de
lyse/muscle (Lysis Buffer de Promega E) supplementé par des inhibiteurs de
protéase
(coktail tablets - Boehringer). Les muscles sont prélevés dans les tubes
spéciaux de
chez BIOl Ol et conservés à -20°C, avant broyage et lecture.
ç) Extraction de la luciférase exprimée par les cellules musculaires
L'extraction de la luciférase est réalisée avec un appareil « Fastprep machine
» dans
des conditions d'extraction utilisant 1 ml de tampon de lyse par tube à une
vitesse de
6,5 m/s, pendant 30 secondes. Les tubes sont ensuite mis dans la glace et
centrifugés à
12000 g pendant I O minutes à 4°C.
d) Détermination de l'activité luciférase
L'activité luciférase est mesurée en utilisant un kit de test de luciférase
(Promega) et
un luminomètre Dynex MLX. La lecture de cette activité est mesurée en RLU
(« Relative Light Unit » : Unité de Lumière Relative).
e) transfection i~z vivo dans le muscle
Les résultats du transfert de gène in vivo dans le muscle sont représentés à
la figure 7.
Ces résultats indiquent qu'au rapport massique hydrotalcite/ADN de 0,5 une
augmentation de l'activité Iuciférase d'un facteur 14 est obtenu par rapport à
l'ADN
nu. Plus généralement, les compositions ADNlhydrotalcite présentent une
efficacité
de transfection améliorée par rapport à celle obtenue par injection d'ADN nu.