Note: Descriptions are shown in the official language in which they were submitted.
CA 02413041 2002-11-29
Y
1
UN APPAREIL PERMETTANT D'EFFECTUER
DES VENTILATIONS LIQUIDES TOTALES
DOMAINE DE L'INVENTION
La présente invention concerne un appareil utilisé pour effectuer des
ventilations liquidiennes totales.
En particulier, mais non exclusivement, cet appareil utilise des
oxygénateurs et des condenseurs modulaires qui permettent de s'adapter à la
quantité de liquide à traiter et par le fait même au poids du patient, et
permet
de corriger le volume résiduel contenu dans les poumons du patient à l'aide
d'une mesure de la quantité de liquide dans l'appareil.
ARRI~RE-PLAN TECHNOLOGIQUE
Trois à 5% des nouveau-nés admis à l'unité des soins intensifs sont
affectés d'une détresse respiratoire, réfractaire à une ventilation
artificielle
optimale. L'inflammation pulmonaire est aggravée par les ventilations
artificielles conventionnelles. II en résulte une oxygénation très
insuffisante du
sang artériel et des différents organes, en particulier le cerveau. Une
alternative prometteuse dans le traitement du syndrome de détresse
respiratoire aiguë (SDRA) est la ventilation liquidienne avec l'emploi d'un
liquide respirable. Les avantages de cette technique reposent sur des bases
théoriques et expérimentales solides, connues depuis maintenant plusieurs
années.
CA 02413041 2002-11-29
i A
2
La ventilation liquidienne peut être réalisée de 2 façons, soit la
ventilation liquide partielle (VLP) et totale (VLT). La VLP utilise un
ventilateur
gazeux conventionnel, après avoir rempli partiellement les poumons avec du
PFC (perlluorocarbones). Cette technique ne requiert pas de ventilateur
spécialisé et elle a fait l'objet d'études cliniques depuis plusieurs années.
Cependant, il est clair que les bénéfices optimaux de la ventilation liquide
seront obtenus en utilisant la ventilation liquide totale, où les poumons sont
complètement remplis de liquide respirable oxygéné de façon externe. De
plus, l'idée de remettre te poumon très malade du nouveau-né dans sa
condition prénatale en attendant sa guérison (Praud, 2000), apparait
intuitivement trés séduisante.
L'avantage considérable de la ventilation liquide par rapport à la
ventilation gazeuse dans les dëfaillances respiratoires aiguës est la
possibilité, en annulant l'interface air-liquide, de permettre (expansion et
le
recrutement des alvéoles pathologiques « non-compliant » à des pressions
beaucoup plus basses. Le risque de vololbarotraumatisme est très diminué, la
ventilation alvéolaire est plus homogène, les atélectasies sont éliminées et
les
inégalités ventilationlperfusion diminuées. Ces bénéfices ont été retrouvés
dans toutes les études réalisées sur des modèles animaux de détresse
respiratoire du nouveau-né (Hirschl, 1996 ; Pedneault, 1999; Hirschl, 1995 ;
Pedneault, 1999 ; Shaffer, 1983 ; Wolfson, 1992).
Les perfluorocarbones sont les plus souvent sélectionnés comme
liquide respirable. Ils sont non toxiques, chimiquement stables et
biocompatibles. De plus, ils sont identifiés comme liquide "idéal", car ils
ont
une bonne diffusion dans les voies aériennes, une faible tension de surface et
une solubilité importante pour les gaz respiratoires, permettant ainsi
d'assurer
une oxygénation et une épuration efficace du C02 (Clark, 1966). Les PFC
permettent aussi de "laver" les voies aériennes des débris et molécules
inflammatoires (Wolfson, 1998), et d'administrer des médicaments à visée
CA 02413041 2002-11-29
i
locale, tels les dilatateurs d'artères pulmonaires (Wolfson, 1996). Un premier
PFC, le pertlubron, a été approuvé pour usage médical; d'autres, comme le
perfluorobutane, sont en cours d'examen par la FDA.
Plusieurs types de ventilateurs liquidiens ont été développés et rendus
public dans la littérature. Généralement, les études cliniques ont été
réalisées
avec des systèmes par gravité, ufilisant un réservoir au-dessus et en dessous
des poumons du patient pour réaliser l'inspiration et l'expiration. Par
contre,
ce type de montage ne permet pas de contrôler adéquatement tous les
paramètres de la ventilation.
Les laboratoires de recherches ont d'abord construits des ventilateurs
liquides à partir d'équipements existants d'oxygénation et de circulation
extracorporelle coGteux. Dans la plupart des cas, ils utilisaient un système
de
pompage complexe, composé de pompes péristaltiques, de réservoirs de
liquide ainsi que de plusieurs valves avec des systèmes de contournement.
La problématique majeure qui a alors été soulevée par les chercheurs est de
designer un ventilateur simple d'utilisation, efficace, sécuritaire et fiable
pour
amener la VLT dans les soins intensifs.
Dans le but de réduire la complexité mécanique des ventilateurs,
Hirsch et al. (1996) ont développé un connecteur avec venturi qui permet à la
fois d'inspirer et d'expirer sans utiliser de circuit de contournement et qui
fournit un écoulement continu de liquide dans tout le système.
Shaffer et al. (2000) ont par la suite développé un ventilateur liquidien
total qui utilise une pompe à rouleaux pour forcer le PFC au travers d'une
boucle de ventilation et de régénération. Cependant, ce type de pompe
génère un écoulement pulsé, ce qui induit des oscillations sur les mesures de
pression. Donc, les ventilateurs récemment développés (Sekin et al., Larrabe
et al. 2001 ) utilisent une pompe à double piston, dont l'un est dédié à
CA 02413041 2002-11-29
l'inspiration et le second à l'expiration. Ces pistons sont déplacés
simultanément par une plate-forme unique.
L'échangeur gazeux est un élément crucial dans l'efficacité de la VLT,
car il doit extraire complètement le C02 contenu dans le PFC, pour le
remplacer par de l'oxygène avant que le liquide ne soit réintroduit dans les
poumons du patient. Or, il est plus facile de dissoudre du C02 dans le PFC
que de l'oxygène. Donc, pour être en mesure d'effectuer efficacement
l'échange gazeux, plusieurs ventilateurs sont équipés d'un oxygénateur
sanguin extracorporel qui est coûteux. Cette pièce d'équipement renferme une
membrane de silicone à double paroi, entre lesquelles un écoulement
d'oxygène pur circule, l'écoulement de PFC s'effectuant à l'extérieur de celle-
ci. L'inconvénient majeur est que le liquide employé extrait les huiles
contenues dans le silicone, ce qui augmente les coûts de remplacement. De
plus, le liquide traverse la membrane et se retrouve dans l'écoulement
d'oxygène, augmentant alors les pertes de PFC.
Dans d'autres applications, la combinaison d'un atomiseur avec un
bulleur a été développée pour remplacer l'oxygénateur à membrane. La
colonne de cet oxygénateur est constituée principalement d'un tube
relativement long où le PFC est vaporisé par une buse au haut et l'oxygène
est injecté à la base par une pierre poreuse. L'échange gazeux est réalisé par
contact direct entre le liquide et les bulles de gaz. L'efficacité de cet
échange
est accrue en insérant des grilles dans la colonne pour favoriser le temps de
séjour des bulles dans le liquide (Sekin et al, 1999).
Cependant, la pertormance du bulleur avec atomiseur est fortement
dépendante du débit. Lorsqu'il est insuffisant, la surface de la pierre
poreuse
ne génère pas uniformément les bulles. Dans le cas où le débit de gaz est
trop important, les bulles générées se joignent pour former un amas de bulles,
CA 02413041 2002-11-29
ce qui diminue grandement la surface d'échange. De plus, la quantité de
liquide pour remplir la colonne est élevée.
Comme alternative aux systèmes d'oxygénation à membrane et au
5 bulleur avec atomiseur, Nugent a développé un nouveau type d'échangeur
gazeux pour les liquides respirables (Voir la demande internationale WO
99/62626). Cet échangeur gazeux est constitué d'une unité de dispersion de
fluide qui projette le liquide sous forme d'un mince film, mis en contact avec
un écoulement d'oxygène.
L'écoulement d'oxygène introduit dans l'oxygénateur est évacué,
entraînant avec lui le C02 et des vapeurs de PFC. Alors, durant la VLT, des
pertes significatives de liquide sont présentes. Une analyse multifactorielle,
portant sur l'efficacité des échangeurs et la conservation du liquide durant
les
VLTs, a démontré que les pertes de PFC sont plus importantes sur un bulleur
avec atomiseur que sur les oxygénateurs à membrane (Wolfson et al., 1999).
Ceci s'explique en bonne partie par le fait que le PFC atomisé est évacué
sous forme de minuscules gouttelettes hors de l'oxygénateur par l'écoulement
gazeux, en plus des pertes présentes par évaporation.
Globalement, les pertes de PFC doivent être minimisées, d'abord par
mesure d'économie, mais aussi pour éviter d'endommager le matériel médical
qui n'est pas compatible avec les vapeurs de PFC. Pour éviter cette situation,
un condenseur est généralement mis en place pour récupérer les vapeurs de
PFC s'échappant des oxygénateurs, tout en permettant une circulation
adéquate des gaz.
Cependant, au lieu d'utiliser un système de condensation, un circuit
fermé de recirculation des gaz pourrait permettre une rétention quasi complète
des vapeurs de PFC. Faithfull et Shutt (1999) ont développé une méthode et
un appareil pour ce genre de système, ce qui prolonge l'administration de
CA 02413041 2002-11-29
PFC sans pour autant avoir des pertes excessives reliées à l'évaporation. Par
contre, il faut alors un système d'extraction du COZ du circuit fermé.
Les intervenants sont conscients que le patient peut souffrir d'une
hyper distension des poumons, d'un écrasement des voies respiratoires ainsi
que d'une diffusion incomplète des gaz. Donc, le ventilateur doit informer les
intervenants de l'état du patient à l'aide de mesures comme la compliance, la
pression dans les voies respiratoires, le volume des poumons, etc. A titre
d'exemple, Shaffer et al. (1994) ont développé un procédé de contrôle pour un
ventilateur liquidien, basé sur la comparaison des conditions actuelles avec
un
intervalle de valeurs souhaitées qui détermine l'indication d'une alarme ou
l'activation d'une servo-valve sur le réseau de conduit.
Néanmoins, le problème n'est pas de décider quand indiquer une
alarme, mais d'avoir une mesure continuelle sur le volume de liquide dans les
poumons. Par exemple, si une légère erreur se produit entre le volume injecté
et retiré des poumons, l'erreur à long terme fait augmenter ou diminuer le
volume résiduel de liquide dans les poumons. Actuellement, il n'y a pas de
moyen efficace pour mesurer en continu ce volume de liquide (en sachant que
fa mesure de la variation du poids du patient ne peut pas être mis en place
aux soins intensifs comme moyen pratique).
SOMMAIRE DE L'INVENTION
Ainsi, la présente invention concerne un appareil pour effectuer des
ventilations liquides totales, comprenant au moins un oxygénateur. L'appareil
peut comprendre des pompes contrôlées indépendamment les unes des
autres, des moyens pour mesurer la quantité de liquide dans l'appareil, et des
moyens pour corriger le volume résiduel de liquide contenu dans les poumons
du patient à l'aide de cette mesure de la quantité de liquide dans l'appareil.
CA 02413041 2002-11-29
r
L'appareil peut par ailleurs présenter une modularité qui permet de l'ajuster
au poids du patient.
D'autres objets, avantages et caractéristiques de l'invention, ainsi que
ceux qui précèdent, deviendront plus apparents à la lecture de la description
non limitative qui suit d'un mode de réalisation illustratif de l'invention,
donné
à titre d'exemple seulement avec référence aux dessins annexés.
BR~VE DESCRIPTION DES DESSINS
Dans les dessins non limitatifs ci-joints
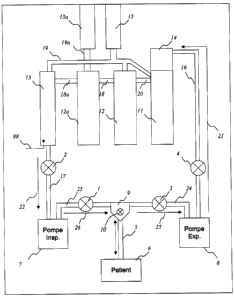
La figure 1 est un schéma du circuit liquide du mode de réalisation
illustratif d'un appareil pour effectuer des ventilations liquidiennes totales
conforme à l'invention, avec ses différentes composantes ;
La figure 2 illustre la séquence des actions des différentes
composantes du ventilateur de la figure 1 lors d'un cycle respiratoire ;
La figure 3 est une vue isométrique d'un module d'oxygénation du
liquide respirable faisant partie du mode de réalisation illustratif de la
figure 1,
ainsi que d'une coupe partielle permettant de montrer les composantes pour
le chauffage, intégrées à ce dernier ;
La figure 4 est une vue en coupe d'un module d'oxygénation et des
composantes du système chauffage faisant partie du mode de réalisation
illustratif de la figure 1, qui permet de montrer la compartimentation et le
parcours du PFC dans le module ;
La figure 5 est une vue en coupe regroupant les deux types de module
d'oxygénation ainsi que des composantes du système de chauffage et de
CA 02413041 2002-11-29
filtration faisant partie du mode de réalisation illustratif de la figure 1,
en plus
de démontrer le parcours du liquide dans ces composants ;
La figure 6 est un schéma qui présente un exemple de contrôle de la
température du liquide dans les 2 types de modules d'oxygénation ;
La figure 7 illustre, pour fins d'exemple, un aspect modulaire des
modules d'oxygénation;
La figure 8a est une vue en isométrie présentant un exemple de
module de condensation développé pour récupérer le PFC s'échappant des
modules d'oxygénation ainsi que du réservoir auxiliaire ;
La figure 8b est une vue de face présentant un exemple de parcours
de l'écoulement gazeux, s'échappant des modules d'oxygénation et du
réservoir auxiliaire, au travers du module de condensation ;
La figure 9 est un vue isométrique illustrant un exemple d'aspect
, modulaire des modules de condensation et présentant la façon dont le
contrôle de la température de ces modules s'effectue ;
La figure 10 est une vue en isométrie d'un exemple de pompe avec un
schéma qui décrit la façon dont le contrôle de la position du piston est
effectué ;
La figure 11 est une vue en isométrie d'un exemple de valve par
écrasement accompagnée de son schéma de contrôle ;
La figure 12 est un schéma présentant les éléments raccordés sur le
PLC (Programmable logic controller) du mode de réalisation illustratif de la
figure 1, ainsi que le pupitre de commande ; et
CA 02413041 2002-11-29
La figure 13 est un schéma présentant un exemple de contrôleur
typique, employé pour asservir les systèmes de pompage, de chauffage et de
condensation.
DESCRIPTION DÉTAILLÉE DU MODE DE RÉALISATION ILLUSTRATIF
La problématique majeure qui a été soulevée est de designer un
ventilateur simple d'utilisation, efficace, sécuritaire et fiable pour amener
la
VLT dans les soins intensifs. Ceci implique donc le développement et
l'intégration, de plusieurs composants dont la pompe, l'oxygénateur, le
système de chauffage, le condenseur, le filtre et le contrôleur. De plus, dans
l'optique d'utiliser cette technologie sur tous les types de patients allant
du
prématuré à l'adulte, cet équipement doit être en mesure de s'adapter
facilement sans avoir besoin de redimensionner et changer tous ces
composants.
L'aspect modulaire et intégré du mode de réalisation illustratif
rencontre cette problématique. Ce mode de réalisation illustratif est
constitué
de différents modules intégrant à la fois le système d'oxygénation, de
chauffage, de filtrage et de condensation. Ces modules peuvent être
dupliqués et mis en paralléle ou en série, dans le but de traiter davantage de
liquide respirable, s'il survient la nécessité de ventiler des personnes de
poids
supérieur.
De plus, le mode de réalisation illustratif permet la sélection de
différents cycles qui guident les intervenants dans les phases préalables à la
ventilation. Ainsi, la phase de démarrage augmente et maintient la
température du volume initial de liquide à la valeur désirée en plus de
l'oxygéner à 100%. La phase de remplissage, quant à elle, permet de remplir
les poumons de liquide à l'aide d'une pompe sur le montage. L'appareil
CA 02413041 2002-11-29
r
indique alors en temps réel la quantité qui a été injectée. Finalement, le
cycle
de respiration est enclenché, permettant ainsi d'insérer et de retirer un
volume
inspiratoire et expiratoire.
5 Les paramètres temporels, volumiques et fonctionnels pour chacun de
ces cycles sont entrés sur un pupitre de commande, lequel communique
continuellement avec le PLC qui contrôle l'ensemble du ventilateur liquidien.
Ces paramètres peuvent être modifiés pendant le déroulement des cycles.
Différentes options sont aussi disponibles comme la modification des profils
10 inspiratoire et expiratoire, l'arrêt ou la mise en marche des systèmes,
etc.
Pour réaliser ces cycles, le liquide est transporté jusqu'au patient à
l'aide de conduits, créant un circuit liquide simple et complet. Le mode de
réalisation illustratif de la présente invention contient seulement un
circuit,
mais il donne accès à toutes les composantes actives du ventilateur
développé. Cinq valves et deux pompes indépendantes, dont une valve
manuelle au niveau du tube endotrachéal permettant d'isoler le circuit liquide
des poumons du patient, permettent de diriger le liquide respirable dans la
composante désirée.
Le système de pompage indépendant permet aussi de corriger le
volume résiduel, contenu dans les poumons du patient pendant les cycles de
respiration. Ceci n'est pas possible à réaliser si les pistons des pompes sont
déplacés simultanément par la même plate-forme. La grandeur de la
correction à effectuer, si nécessaire, est déterminée grâce à la présence d'un
réservoir auxiliaire instrumenté, indiquant le volume de liquide dans le
ventilateur. Cette donnée permet de déduire la quantité de liquide dans le
patient. De plus, la motorisation indépendante permet de gagner du temps
d'oxygénation pendant la phase d'inspiration. Ainsi, le PFC expiré bénéficie
de secondes supplémentaires pour évacuer son C02.
CA 02413041 2002-11-29
11
Le liquide expiré entrant dans l'oxygénateur n'est pas en contact direct
avec le liquide sortant de ce dernier, car l'intérieur est divisé en 2
sections
distinctes, séparées par une paroi. Ainsi, le temps d'oxygénation est accru et
l'élimination du C02 est grandement favorisée.
Circuit liquide
Le système de la figure 1 comprend un tube endotrachéal 5 dont une
extrémité est insérée dans la trachée du patient 6. Ce tube 5 permet d'insérer
ou de retirer du liquide des poumons. La seconde extrémité du tube
endotrachéal 5 est branchée sur un connecteur en « Y » 9, muni d'une valve
manuelle 10. Lorsque cette valve 10 est fermée, elle isole le circuit liquide
du
ventilateur des poumons du patient 6. II est alors possible de mettre en place
des cycles qui autrement enverraient du liquide dans les poumons du patient
6.
Le connecteur en « Y » 9 permet de joindre l'une des extrémités des
conduits 23 et 24 au tube endotrachéal 5. La seconde extrémité du conduit 23
est branchée sur la pompe d'inspiration 7, qui est reliée au réservoir
auxiliaire
13 via le conduit 17. Finalement, la seconde extrémité du conduit 24 est
reliée
à la pompe d'expiration 8, qui communique au filtre 14 (intégré à
l'oxygénateur 11 J, via le conduit 16.
Les éléments 1, 2, 3 et 4 de la figure 1 sont des valves par
écrasement. Lorsqu'elles sont ouvertes, elles permettent l'écoulement dans le
conduit auquel elles sont associées. Ainsi, il est possible de diriger le
liquide
dans toutes les composantes du circuit global selon les différentes
combinaisons d'ouverture et de fermeture de ces valves 1, 2, 3 et 4.
Le réseau de conduits 19 sert à acheminer l'écoulement gazeux
s'échappant des oxygénateurs 11, 12 et du réservoir tampon 13, vers le
CA 02413041 2002-11-29
s
12
condenseur 15. Le PFC condensé retourne sous forme liquide, à
l'oxygénateur 11, par les conduits 19.
Pour amliorer l'oxygnation, il de mettre second
est possible un
oxygnateur12a en srie avec l'oxygnateurL'coulementde
12. gaz
s'chappant de ce nouvel oxygnateur 12a dirig par conduit
sera un
indépendant 19a vers un condenseur 15a attitré exclusivement à ce dernier.
Le conduit 20 achemine le liquide en trop de l'oxygénateur 11 vers
l'oxygénateur 12. Le conduit 18, quant à lui, dirige le liquide en trop de
l'oxygénateur 12 vers un troisième oxygénateur 12a ou vers le réservoir
auxiliaire 13.
(Cycle avec pafienf)
Lorsque la valve 2 est ouverte et la valve 1 est fermée, la pompe
d'inspiration 7 est en mesure d'aspirer du liquide contenu dans le réservoir
auxiliaire 13 via le conduit 17. Le liquide circule alors dans le sens de la
flèche
22. Dans le cas où la valve 1 est ouverte, les valves 2 et 3 sont fermées et
la
pompe d'inspiration 7 est remplie de liquide et peut alors le pomper par le
conduit 23 jusqu'au « Y » 9. Ce connecteur 9 dirigera le PFC vers les
poumons du patient 6 par le tube endotrachéal 5. L'écoulement suit alors le
sens de la flèche 26.
Quand la valve 3 est ouverte et les valves 2 et 4 sont fermées, la
pompe d'expiration 8 peut aspirer du liquide contenu dans les poumons du
patient 6 par le tube endotrachéal 5, le « Y » 9 et le conduit 24.
L'écoulement
ainsi créé, suit le sens de la flèche 25. Dans le second cas où la valve 3 est
fermée, la valve 4 est ouverte et la pompe 8 contient du liquide, elle peut
alors
l'expulser par le conduit 16 jusqu'au filtre 14, intégré à l'oxygénateur 11,
dans
le sens de la flèche 21.
CA 02413041 2002-11-29
r
13
(Cycle sans patient)
Lorsque les valves 1, 2 et 3 sont ouvertes et les valves 4 et 10 sont
fermées, la pompe d'expiration 8 peut aspirer du liquide du réservoir tampon
13 par les conduits 17, 23 et 24 et par le connecteur en « Y » 9. Dans un cas
similaire, si les valves 1, 3 et 4 sont ouvertes et les valves 10 et 2 sont
fermée, il est possible pour la pompe d'inspiration 7 d'envoyer du liquide
directement au filtre 14 par les conduits 23, 24 et 16 et par le connecteur en
< Y»9.
Ainsi, la valve 10 au niveau du « Y » 9 permet de faire circuler le
liquide dans le ventilateur ou de brancher un ventilateur gazeux durant le
remplissage des poumons. De plus, elle facilite le changement de tube lors
des remplissages.
Séquences
Cycle de démarrage
Lors du remplissage initial de la machine, le PFC est à la température
de la pièce et renferme peu d'oxygène. Pour corriger cette situation, un cycle
de démarrage est mis en marche pour faire circuler le liquide dans les
conduits et les composants du ventilateur. II passe alors au travers des
oxygénateurs 11 et 12 où sa concentration en oxygène est augmenté à
100%. Par le fait même, le PFC est réchauffé par le système de chauffage
intégré aux oxygénateurs 11 et 12. Lorsque la température visée est atteinte,
le système de chauffage ne fait que compenser les déperditions thermiques
pour maintenir la température désirée. Ce cycle permet donc d'oxygéner, de
réchauffer et de maintenir le liquide à la température désirée avant de passer
aux cycles de remplissage et de respiration.
CA 02413041 2002-11-29
14
Pour effectuer ce cycle, la valve 10 du « Y » 9 est fermée, les valves 1
et 2 sont ouvertes en permanence et le piston 73 (Figure 10) de la pompe
d'inspiration 7 est à la position supérieure. Ensuite, la valve 4 est
maintenue
fermée et la valve 3 s'ouvre pour permettre à la pompe d'expiration 8 de se
remplir de PFC, via les conduits 17, 23, 24 ainsi que le « Y » 9. Une fois
remplie, la valve 3 se ferme tandis que la valve 4 s'ouvre pour permettre au
liquide d'être injecté au niveau du filtre 14 de l'oxygénateur 11 par le
conduit
16.
Séquence de remplissage
La séquence de remplissage est utilisée pour remplir les poumons du
patient 6 à l'aide de la pompe d'expiration 8 et du circuit liquide du
ventilateur.
Les intervenants fixent les paramètres de remplissage sur le pupitre 97
(Figure 12), pour imposer par exemple, le débit de la pompe 8 et le volume de
la CRF (capacité résiduelle fonctionnelle).
L'utilisation de la pompe d'expiration 8 permet à la pompe d'inspiration
7 de se remplir à son tour d'un volume courant déterminé par les intervenants
75 (Figure 10) durant la séquence de remplissage. Ainsi, le cycle respiratoire
peut immédiatement débuter, lorsque le remplissage est terminé.
Cette séquence de remplissage débute par l'ouverture des valves 1, 2
et 3 et la fermeture des valves 4 et 10. La pompe d'expiration 8 se remplit
ensuite de liquide à partir du réservoir auxiliaire 13 par l'intermédiaire des
conduits 17, 23 et 24, ainsi que par le « Y » 9. Par la suite, la valve 1 est
fermée et la valve 10 est ouverte. Finalement, les intervenants appuient sur
un bouton pour remplir les poumons 6 du volume désiré, avec la pompe
d'expiration 8.
CA 02413041 2002-11-29
Cycle de respiration
Le cycle respiratoire se divise en 4 étapes, soit l'inspiration, l'expiration
5 et les arrêts en fin d'inspiration et d'expiration. La figure 2 montre les
différentes actions exécutées par le PLC lors d'un cycle de respiration.
Les paramètres temporels et volumiques 75 (Figure 10) sont
déterminés par les intervenants et communiqués au PLC via le pupitre 97
10 (Figure 12). Ces paramètres peuvent être modifiés en cours de ventilation
pour améliorer ou corriger différentes situations rencontrées.
ÉTAPE 1 : INSPIRATION
Pendant l'étape 1, la valve 1 est ouverte et la valve 2 est fermée. Le
liquide contenu dans la pompe d'inspiration 7 est acheminé par le conduit 23
15 au « Y » 9 où l'écoulement est dirigé dans les poumons du patient 6 par le
tube endotrachéal 5. La valve 1 est refermée à la fin de cette étape.
Pendant l'étape 1 a, la valve 4 est ouverte et la valve 3 est fermée. La
pompe d'expiration 8 expulse alors très rapidement son liquide via le conduit
16 dans le filtre 14 intégré à l'oxygénateur 11. Lorsque la pompe 8 s'est
complètement vidée, la valve 4 est de nouveau fermée.
La phase 1 b illustre le temps caché qui est gagné en temps
d'oxygénation, dû au fait que les pompes sont commandées individuellement.
Ainsi le PFC bénéficie de secondes supplémentaires pour éliminer son C02.
ÉTAPE 2 : TEMPS D'ARRET #1 - FIN D'INSPIRATION
Lorsque l'étape d'inspiration 1 est terminée, il est souhaitable de faire
un temps d'arrêt pour prendre des mesures de pression au niveau des
CA 02413041 2002-11-29
16
poumons du patient 6. Ces mesures serviront à évaluer certains paramètres
des poumons, dont la compliance statique.
ÉTAPE 3 : EXPIRATION
Durant la phase d'expiration 3, la valve 3 est ouverte et la valve 4 est
maintenue fermée. La pompe d'expiration 8 retire du liquide des poumons par
le tube endotrachéal 5, le « Y » 9 et le conduit 24, dans le sens indiqué par
la
flèche 25.
Durant la phase 3a, le piston 73 de la pompe d'inspiration 7 ne bouge
pas et les valves 1 et 2 sont fermées. II est alors possible de mesurer le
niveau du réservoir auxiliaire 13 à l'aide du capteur 88. En sachant
l'efficacité
du condenseur 15, cette donnée nous informe sur la possibilité de la
présence de pertes dans le circuit liquide ou d'erreurs au niveau des volumes
insérés et retirés des poumons.
C'est seulement durant la phase 3b que la pompe d'inspiration 7 se
remplit de liquide par le conduit 17 relié directement au réservoir auxiliaire
13.
Pour ce faire, la valve 2 est ouverte permettant ainsi au liquide de s'écouler
dans le sens de la flèche 22. Lorsque la pompe 7 est remplie au volume
déterminé par les intervenants, la valve 2 est alors refermée.
ÉTAPE 4 : TEMPS D'ARRET #2 - FIN D'EXPIRATION
Lorsque la phase d'expiration 3 est terminé, il est possible de faire un
second temps d'arrêt pour prendre des mesures de pression au niveau du
poumons. Ces mesures serviront à évaluer certains paramètres des
poumons, dont la compliance statique.
Le cycle retourne alors à l'étape 1 et ce, jusqu'à ce qu'un intervenant
mette fln à la ventilation.
CA 02413041 2002-11-29
17
Séquence de vidange
Lorsque l'on désire vider les poumons du patient 6, il faut d'abord
mettre fin au cycle de respiration. Ce dernier se termine par l'étape
d'expiration. II suffit alors de fermer la valve manuelle 10, de débrancher le
tube endotrachéal 5 du connecteur en « Y » 9, puis de pencher le patient 6
pour favoriser l'évacuation du liquide des poumons 6 par gravité.
Estimation de la CRF
Le capteur 88 permet de mesurer le niveau de PFC contenu dans le
réservoir auxiliaire 13. En connaissant l'efficacité du condenseur 15, cette
donnée nous informe sur la possibilité de la présence de pertes dans le
circuit
liquide ou d'erreurs au niveau des volumes injectés et retirés des poumons.
La capacité résiduelle fonctionnelle (CRF) théorique est calculée selon
l'équation 1 tandis que la CRF estimée, est calculée selon l'équation 2.
L'indice k indique les cycles.
V~,.[k+1]=Vr~.[k~+Vrr[k~-V~e[k] (1 )
V~,~[k+1]=V~,~(0)-(Vu.[0]*(1-at)-Vu.[k]) {2)
où,
- V~rf; volume de la capacité résiduelle fonctionnelle (ml);
- Vt;, volume courant {tidal volume) dans la pompe d'inspiration 7 à
l'étape 4 (ml);
- Vte, volume courant (tidal volume) dans la pompe d'expiration 8 à
l'étape 4 (ml);
- Vas[0], volume initial dans le réservoir auxiliaire 13 (ml);
- a, perte au niveau du condenseur en fonction du temps (ml/s); et
- Var, volume dans le réservoir auxiliaire durant l'étape 3a (ml).
CA 02413041 2002-11-29
18
Les deux valeurs doivent concorder pour s'assurer que le volume de
liquide dans le patient 6 reste constant. L'augmentation de la valeur de V~,~
par rapport à V~rf indique que le volume de liquide dans les poumons diminue.
Dans le cas contraire, la diminution de V~,~ par rapport à V~,~ indique une
augmentation du volume de PFC dans les poumons du patient.
La motorisation indépendante des pompes ? et 8, permet de corriger la
CRF en cours de ventilation en assignant un volume inspiratoire différent du
volume expiratoire ou vice-versa. Ainsi, si l'on désire augmenter la CRF, le
volume inspiré sera supérieur au volume expiré pendant un nombre de cycles
déterminés. Inversement, si l'on veut diminuer la CRF, le volume inspiré sera
supérieur au volume expiré pendant un nombre de cycles prescrits.
Ainsi
- Le réservoir auxiliaire permet d'estimer la quantité de PFC présent
dans tout le ventilateur et donc de déduire le volume résiduel de PFC
dans les poumons du patient 6;
- La motorisation indépendante et asservie des deux pistons facilite la
procédure de mise en fonction du ventilateur;
- La motorisation indépendante des deux pistons maximise le temps de
séjour du PFC dans l'échangeur gazeux. En effet, dès que le PFC est
retiré des poumons, le piston vide rapidement son contenu dans
l'échangeur gazeux à un débit supérieur au débit fourni par la pompe
d'inspiration;
- La motorisation indépendante permet de corriger le volume de la CRF
au cours d'un ou de plusieurs cycles de ventilation
o II est possible d'augmenter ou de diminuer le volume lors de
l'expiration et laisser constant le volume d'inspiration; et
CA 02413041 2002-11-29
19
o II est possible d'augmenter ou de diminuer le volume lors de
l'inspiration et laisser constant le volume expiration; et
II est possible de modifier les paramètres suivants en cours de
ventilation
~ Le volume courant d'inspiration et d'expiration;
~ Le temps d'inspiration;
~ Le temps d'expiration;
~ Le temps de plateau #1 (temps d'arrêt);
~ Le temps de plateau #2 (temps d'arrét);
~ Le profil de l'étape d'inspiration; et
~ Le profil de l'étape d'expiration.
Oxygénateur
La fonction première de l'oxygénateur est de maintenir la quantité
d'oxygène dans le liquide à 100%. Pour être en mesure de réaliser cet
objectif, un oxygénateur de type bulleur a été développé. La figure 3 présente
l'oxygénateur 12 en isométrique et la figure 4 en coupe. La figure 5 présente
les oxygénateurs 11 et 12 en coupe, avec le lien qui les unit.
Les bulles d'oxygène pures sont générées à la base de chaque
oxygénateur 11 et 12 par une membrane perforée 29 qui est maintenue
fermement entre les pièces 27 et 30. L'oxygène est amené sous la membrane
29 par !'entrée 39. Les bulles ainsi générées entrent directement en contact
avec le PFC contenu dans les sections 35 et 40. L'écoulement gazeux,
s'échappe par le haut des oxygénateurs 11 et 12 pour être acheminé au
condenseur par les conduits 19. Le PFC contenu dans cet écoulement sera
récupéré par le condenseur 15 et retourné sous forme liquide par les conduits
19 à l'oxygénateur 11.
CA 02413041 2002-11-29
L'intérieur de chaque l'oxygénateur 11 et 12 est divisé en deux
sections, soit la section intérieure 35, délimitée par le tube 37, et la
section
annulaire 40 qui est délimitée par les tubes 31 et 37. Ces sections 35 et 40
communiquent entre elles au bas de l'oxygénateur, car le tube 37 ne descend
5 pas jusqu'à la membrane 29. La capacité des sections 35 et 40 est de l'ordre
d'un volume courant.
Selon le poids du patient 6 et la quantité de liquide à oxygéner, il est
possible de modifier soit la section et la hauteur des tubes 31 et 37 et/ou le
10 nombre d'oxygénateurs. L'augmentation du nombre d'oxygénateur peut se
faire en série ou en parallèle selon le besoin. La figure 1 présente l'option
en
série tandis que la figure 7 présente l'option en parallèle.
A chaque cycle de respiration, le liquide amené par le conduit 16
15 traverse l'élément filtrant 55 du filtre 14 intégré à l'oxygénateur 11. Le
liquide
s'écoule ensuite dans la section intérieure 35 de l'oxygénateur 11.
L'augmentation du volume dans la section 35 chasse le liquide déjà présent
vers la section annulaire 40 en suivant le sens des flèches 79. Ceci évite que
le PFC entrant soit en contact avec le PFC sortant de l'oxygénateur,
20 favorisant l'élimination du C02 et le temps de séjour dans chaque
oxygénateur 11 et 12.
L'écoulement, décrit précédemment par les flèches 79, tend à
équilibrer le niveau des sections 35 et 40. Cependant, dès que le niveau de la
section 40 atteint le conduit 20, le liquide en surplus est alors dirigé dans
la
section intérieure 35 du second oxygénateur 12. Ce mécanisme de
transvasement maintient le niveau global des oxygénateurs 11 et 12 à la
hauteur des conduits de débordement 18 et 20.
Ainsi
CA 02413041 2002-11-29
21
- La compartimentation de l'échangeur par section impose un circuit du
haut vers le bas puis du bas vers le haut au liquide avant de sortir.
Ceci évite au liquide entrant d'ëtre directement en contact avec le
liquide sortant augmentant ainsi le temps de contact du PFC avec
l'oxygène.
- Les échangeurs modulaires 11 et 12 sont raccordables en série ou en
parallèle par de simples tuyaux, car le transfert d'un module à l'autre
s'effectue par débordement.
- Le nombre d'échangeurs modulaires fixe la qualité de l'échange
gazeux, et le raccord en série ou en parallèle augmente cette
efficacité.
- Le nombre d'échangeurs modulaires est ajustable en fonction du poids
du patient. En effet, en connaissant le poids du patient on détermine la
quantité de C02 dissous dans le PFC par expiration, et donc le temps
de séjour nécessaire dans le bulleur.
- Le filtre est d'un accès facile et peut être changé en cours de
ventilation.
- Le filtre est intégré directement à l'oxygénateur, ce qui réduit la
quantité de liquide nécessaire pour remplir le ventilateur en plus
d'éliminer les tuyaux pour le relier aux autres composants
Système de chauffage
La fonction du système de chauffage est de réchauffer la quantité
initiale de PFC dans le ventilateur et ensuite de maintenir cette température
au niveau désiré. Dans le but de minimiser la quantité de liquide pour remplir
CA 02413041 2002-11-29
22
le ventilateur, ce système de chauffage est intégré à la base de chaque
oxygénateur 11 et 12.
Selon ce qui est présenté à la figure 3, l'élément chauffant 28 de
120W, augmente la température de la pièce métallique 27 qui chauffe alors le
PFC qu'elle contient. Les bulles générées par la membrane 29 assurent un
brassage constant du PFC, ce qui permet d'obtenir une répartition uniforme
de la température dans les sections 35 et 40. La matière isolante 33 empéche
les intervenants de toucher les éléments chauds 27 et 28.
La figure 6 présente la façon dont l'augmentaüon et le maintien de la
température du PFC sont réalisés. Des capteurs de température 32 sont
montés sur 1a paroi 31 des oxygénateurs 11 et 12 et permettent de mesurer la
température du PFC dans la section 40. Ces mesures de température sont
d'abord interprétées par un module d'entrée 41 du PLC puis la température
de l'oxygénateur 12 est filtrée par un filtre discret 42. Cette donnée est
ensuite transmise à un contrôleur 46 qui compare la valeur avec une
température de consigne 45 indiquée par les intervenants sur le pupitre de
commande 97 (Figure 12). La sortie du contrôleur 46 est finalement envoyée
é une électronique 48 qui module la puissance 49 fournie aux éléments
chauffants 28 de chaque oxygénateur 11 et 12.
Les températures non filtrées des oxygénateurs 11 et 12 sont aussi
utilisées pour indiquer des alarmes 44, comme un mauvais fonctionnement du
système de chauffage en situation d'incohérence entre les valeurs de
température mesurées.
Par conséquent
- L'utilisation d'un fil électrique chauffant externe au module réduit
l'encombrement du système tout en permettant un contrôle précis.
CA 02413041 2002-11-29
23
- Le système est directement intégré à la base des oxygénateurs, ce qui
réduit le volume de remplissage du ventilateur.
Système condenseur
Le rôle des condenseurs 15 et 15a (Figure 1 ) est de récupérer le PFC
qui s'échappe, sous forme de vapeur et de brouillard, des oxygénateurs 11,
12 et 12a et du réservoir auxiliaire 13. Dans le mode de réalisation
illustratif
présenté, le condenseur 15 est dédié pour les oxygénateurs 11 et 12
uniquement alors que le condenseur 15a récupère le PFC qui s'échappe de
l'oxygénateur 12a lorsqu'il est en série avec l'oxygénateur 12. Lors de la
mise
en parallèle d'une seconde série d'oxygénateurs 11 et 12, comme présenté à
la figure 7, une seconde unité 15 est nécessaire pour récupérer les vapeurs
de PFC. En plus, s'il survient un moment où l'écoulement de gaz à traiter
dépasse la capacité d'un seul condenseur 15 ou 15a, il est alors possible de
partager l'écoulement gazeux entre plusieurs condenseurs mis en parallèle,
puisqu'il se présente sous forme modulaire.
Le condenseur 15 et 15a développé est un échangeur de chaleur à
ailettes. Ces ailettes 63 et 64 (Figures 8a et 8b) sont montées sur une base
métallique 61 refroidie par des modules thermoélectriques (MTE) 57 et 58.
Pour maximiser la surface d'échange thermique et augmenter l'efficacité,
l'alternance des ailettes courtes 63 et longues 64 bornées par les cloisons 65
et 67, force l'écoulement à suivre le chemin indiqué par les flèches 66.
Pendant toute la durée de son parcours, la température de l'écoulement
gazeux diminue et les vapeurs de PFC se condensent à la surface des
ailettes 43 et 64, pour finalement s'écouler par les fentes 68 entre les
ailettes
63 et 64 et retourner à l'oxygénateur 11 ou 12a selon le cas.
CA 02413041 2002-11-29
24
La figure 9 présente l'aspect modulaire du condenseur qui est exploité
dans cette présente invention. La mise en série de deux unités de
condensation 15 identiques a pour but d'accroître l'efficacité globale au
niveau de la récupération des vapeurs de PFC contenues dans l'écoulement
gazeux s'échappant des oxygénateurs 11 et 12 ou 12a. Pour ce faire, deux
stratégies de contrôle sont mises en place, soit une pour le stade 98 et une
seconde pour le stade 99.
Le rôle du premier stade de condensation 98 est de retirer la majeure
partie des vapeurs de PFC. Le condenseur doit donc être maintenu à une
température évitant toute formation de givre, mais maximisant l'efficacité de
la
récupération. C'est au contrôleur 52 que revient la tâche de maintenir la
température idéale. II compare alors la température mesurée par le capteur
59 avec une consigne 51 fournie par les intervenants sur le pupitre 97 et
envoie le résultat de cette comparaison à une électronique 56 qui module la
puissance 54 transmise aux éléments thermoélectriques 57 et 58 de ce
même stade de condensation.
Le travail du second stade 99 vise l'extraction du PFC encore présent à
la sortie du premier stade 98. Le contrôleur 53 effectue alors des cycles de
givrage/dégivrage. Dans un premier temps, la plaque métallique 61 a est
refroidie à basse température pour givrer le PFC encore présent dans
l'écoulement gazeux. Lorsqu'une quantité suffisante s'est accumulée sur les
ailettes 63 et 64, le contrôleur 53 active l'étape de dégivrage en inversant
la
polarité de la tension sur les modules thermoélectriques 57a et 58a. Ils
chauffent alors pendant un court instant la plaque froide 61 a pour liquéfier
le
givre de PFC. Une fois que les ailettes 63 et 64 sont complètement
déglacées, la phase de givrage est remise en marche. Le contrôleur 53
effectue ce cycle à l'aide du capteur 60 et de l'électronique de puissance 62,
dédiée aux modules thermoélectriques 57a et 58a.
CA 02413041 2002-11-29
Par conséquent
- Le condenseur réduit considérablement les pertes de PFC tout en
assurant la bonne circulation des gaz.
5
- Le contrôleur du condenseur inclut des cycles de givrage/dégivrage, ce
qui favorise la conservation du PFC en réduisant les pertes jusqu'à
zéro et améliore l'efficacité.
10 - La modularité du condenseur permet différentes configurations dont
une permettant de traiter un volume plus important de gaz s'échappant
des oxygénateurs et une seconde augmentant l'efficacité de la
récupération du PFC.
15 - L' intégration du condenseur à l'oxygénateur diminue les raccords aux
autres composants du ventilateur le rendant ainsi plus simple.
- Le contrôle indépendant des unités de condensation permet de mettre
en place différentes stratégies de contrôle dans le but d'augmenter
20 l'efficacité de la récupération du PFC.
Système pompe
Les pompes 7 et 8 permettent d'insérer et de retirer une certaine
25 quantité de liquide des poumons du patient 6 selon les paramètres indiqués
sur le pupitre de commande 97. Dans le présent mode de réalisation
illustratif,
la pompe d'expiration 8 est le miroir de la pompe d'inspiration 7, donc le
fonctionnement global de chacune est décrit à partir la pompe 7. La figure 10
présente cette dernière plus en détail.
CA 02413041 2002-11-29
26
La pompe d'inspiration 7 est constituée d'un moteur 70 monté sur une
boîte d'engrenage 71 qui transforme le mouvement rotatif du moteur 70 en
mouvement de translation. La boîte d'engrenage met donc en translation une
crémaillère 72 qui déplace à son tour un piston 73. C'est ce piston 73 qui met
en mouvement le liquide contenu à l'intérieur du cylindre 74. Un potentiomètre
linéaire 69, monté sur la crémaillère 72 de la boîte d'engrenage 71, indique
la
position du piston 73 dans le cylindre 74. Le potentiomètre linéaire 69 peut
être remplacé par d'autres capteurs permettant de déduire, de calculer ou de
mesurer la position du piston 73.
Selon le poids du patient, il est possible d'augmenter le diamètre du
piston 73 et du cylindre 74 pour augmenter le volume par pompe, tout en
conservant ou en augmentant la longueur du cylindre 74 et par le fait même la
course du piston 73. Les cylindres des pompes 74 peuvent être faits d'une
matière opaque ou transparente selon les besoins.
Le contrôleur
La tâche du contrôleur est d'insérer et de retirer avec précision le
volume, demandé par les intervenants sur le pupitre de commande 97 (Figure
12). Pour se faire, la position mesurée par le potentiomètre 69 est comparée
à une référence 76 à l'intérieur du contrôleur 77. Cette référence est
modifiable selon les différents paramètres 75 imposés par les intervenants sur
le pupitre 97. De plus, elle peut prendre différentes formes, comme par
exemple un sinus, une rampe, une exponentielle, etc. et sa durée dans le
temps est variable. Le résultat de cette comparaison est alors transmis au
servo amplificateur 78 qui ajuste la vitesse du moteur 70.
CA 02413041 2002-11-29
27
La largeur du piston monté sur l'appareil est ajustable en fonction du
poids du patient. Ainsi, le diamètre actuel convient pour un nouveau-né ou un
petit nourrisson de poids inférieur à 9 kg. En doublant le diamètre du piston
on peut ventiler un enfant de poids inférieur à 36 kg, et en triplant on peut
ventiler un adulte de 81 kg au maximum.
L'asservissement en position de chacun des pistons autorise des
profils de ventilation complexes, et la motorisation indépendante des pompes
permet de faire des séquences qui ne sont pas possibles autrement.
~stème valve
Les éléments 1, 2, 3 et 4 de la figure 1 sont des valves par
écrasement. Les critères qui ont motivé ce choix sont le volume de la valve
versus la force disponible et la facilité de stérilisation. Entre chaque
utilisation,
il n'est pas nécessaire de stériliser la valve, car il suffit simplement de
changer la tuyauterie. Pour le concept global, il est tout de même possible
d'utiliser d'autres types de valves qui seraient en mesure d'effectuer le même
travail.
Le cylindre pneumatique 80 fournit la force nécessaire pour écraser le
tube 17 qui la traverse et ainsi bloquer l'écoulement. Les régulateurs de
débit
82 et 83 permettent de fixer le temps de fermeture et d'ouverture de la valve,
évitant ainsi les sauts de pression dans le circuit liquide. Le capteur 81
monté
sur le corps du cylindre 80 indique au PLC (Programmable Logic Controller)
84 si !a valve est fermée. Le PLC 84 commande l'ouverture et la fermeture de
la valve en envoyant une commande au distributeur 85, qui est alimenté par
une source pneumatique 86.
CA 02413041 2002-11-29
28
La taille des tuyaux admissibles dans la valve peut varier de très petit à
'/ de pouce. Cependant, si l'on désire utiliser des tubes ayant un diamètre
supérieur à 3/ de pouce, il suffît simplement d'augmenter la distance entre
les
pièces 100 et 101 et la course du cylindre pneumatique 80.
Contrôleur
Le contrôleur typique employé pour le système de chauffage, de
pompage et de condensation, est présenté é la figure 13. La variable du
procédé 89 est comparée à une référence 90. La différence 91 entre ces
valeurs est alors multipliée par un gain proportionnel 92, intégrateur 93 et
dérivateur 94. Le résultat de chaque produit est ensuite sommé par un
sommateur 95 pour former la commande. Cette commande est alors envoyée
au système à contrôler, par l'intermédiaire de différent médium.
La boîte de saturation 96 limite la commande à l'intérieur d'un intervalle
prédéfini de valeurs analogiques. Pour éviter les problèmes causés par
l'imposition de cette saturation, l'intégrateur 93 doit être équipé d'une
bouche
c anti wind-up ».
Avantages
Un premier avantage de !'invention est l'échangeur gazeux modulaire
qui permet d'ajuster l'appareil au poids du patient. L'intérét du module pour
enfant est qu'il est optimisé pour traiter un débit de PFC correspondant à un
patient de 9 kg (prototype actuel). Avec deux (2) et quatre {4) modules pour
enfant en parallèle, l'appareil peut ventiler un patient respectivement de 18
et
de 36 kg. Pour les adultes, un module dont la surface d'échange gazeux est
le double du module pour enfant permet de prendre en charge 36 kg de
masse corporelle. Ainsi, avec trois (3) modules pour adulte, l'appareil peut
ventiler un patient pesant jusqu'é 108 kg.
CA 02413041 2002-11-29
29
Un autre avantage provient du système de pompage avec pompes
indépendantes et d'un réservoir auxiliaire instrumenté. Cette configuration
permet d'estimer avec précision le volume complet de PFC dans le
ventilateur, et donc d'en déduire le volume de PFC dans les poumons du
patient. Elle permet aussi d'optimiser le temps de séjour du PFC dans
l'échangeur gazeux, de modifier etlou corriger le volume pulmonaire en cours
de ventilation, et de planifier des profils de ventilation variés. !n fine,
cela
permet au clinicien de moduler et d'optimiser les échanges gazeux grâce à
une intertace utilisateur/machine performante et simple d'accès.
Ainsi, jusqu'à maintenant, les ventilateurs liquidiens développés
résultent de l'assemblage de plusieurs composants disparates: une pompe,
un système de chauffage, une unité de contrôle, un condenseur et un
oxygénateur. Bien que ce choix de conception peut donner des résultats
acceptables pour la ventilation de nouveau-nés qui nécessite de traiter de
faibles débits de PFC il s'avère délicat à mettre en oeuvre pour la
ventilation
liquide totale des adultes car les débits de PFC peuvent être dix fois plus
importants. La présente invention répond à ce problème par l'intégration du
condenseur et de (élément chauffant dans ce qu'on appele un oxygénateur
modulaire. Par modularité on entend que foxygénateur peut être raccordé en
série ou en parallèle avec d'autres oxygénateurs modulaires afin de traiter de
grandes quantités de PFC sans avoir à les redimensionner. De plus, la mise
en oeuvre de deux pompes contralées indépendamment l'une de l'autre et
d'un moyen pour mesurer la quantité de liquide dans l'appareil permet
d'estimer en tout temps le liquide contenu dans les poumons, et de corriger le
volume résiduel de PFC (volume de PFC contenu dans les poumons à la fin
de l'expiration).
CA 02413041 2002-11-29
Bibliographie
Hirschl RB et al. (1995) Liquid ventilation in adults, children and full-terni
neonates. Lancet 346:1201-2.
Hirschl RB, Tooley R, Parent A, Johnson K, Bartlett RH. (1996) Evaluation of
5 gas exchange, pulmonary compliance, and lung injury during total and partial
liquid ventilation in the acute respiratory distress syndrome. Crit Care Med
24:1001-8.
Wolfson MR, Greenspan JS, Deoras KS, Rubenstein SD, Shaffer TH. (1992)
Comparison of gas and liquid ventilation: clinicat, physiological, and
10 histological correlates. J Appl Physiol 72:1024-31.
Woifson MR, Greenspan JS, Shaffer TH. (1996) Pulmonary administration of
vasoactive substances by perfluorochemical ventilation. Pediatrics 97:449-55.
Wolfson MR, Greenspan JS, Shaffer, TH. (1998) Liquid-assisted ventilation:
an alternative respiratory modality. Pediatr Pulmonol 26: 42-63.
15 Pedneault C, Renolleau S, Gosselin R, Letoumeau P, Praud JP. (1999)Total
liquid ventilation using a modified extra-corporeal gas exchange circuit:
preliminary results in lambs. Pediatr Pulmonol Suppl 18: A241.
Larrabe JL., Alvarez FJ., Gatiasoro Cuesta E., Valls-i-Solers A., Alfonso
LF.,Arnaiz A., Fernandez MB., Loureiro B., Publicover NG., Roman L., Caste
20 JA., Gomez MA. (2001 ), Development of a time-cycled volume -control(ed
Pressure-limited respirator and lung mechanics system for total liquid
ventilation., IEEE Transactions on Biomedical engineering 48:1134-1144
Sekins KM, Nugent L, Mazzoni M, Flanagan C, Neer L, Rozenberg A,
Hoffman J. (1999) Recent innovations in total liquid ventilation system and
25 component design. Biomed Instrum Technoi 33 :277-84.