Note: Descriptions are shown in the official language in which they were submitted.
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
1
Paroi de séparation d'électrolytes pour le transfert
sélectif de cations à travers la paroi, procédé de
fabrication et procédé de transfert.
DOMAINE DE L'INVENTION
L'invention concerne une paroi de séparation
d'électrolytes pour le transfert sélectif de cations à
travers la paroi, un procédé de fabrication de ladite
paroi et un procédé de transfert sélectif de cations à
travers ladite paroi. L'invention concerne en outre un
procédé de type électrolytique assurant un transport de
cations, au travers d'une paroi adaptée, depuis une
première solution d'électrolyte contenant une ou
plusieurs catégories d'ions de même charge ou de charge
différente, vers une deuxième solution électrolytique.
TECHNIQUE ANTÉRIEURE
On connaît déjà un procédé de ce type utilisant
comme paroi de séparation une paroi formée de
chalcogénures à cluster de molybdène, notamment les
phases Mo6X8 appelées phases de Chevrel, décrit dans la
demande de brevet internationale WO 2009/007598. Ce
procédé a fait également l'objet des publications
suivantes :
- Electrochemical reactions of reversible intercalation
in Chevrel compounds for cationic transfer - Principle
and application on Co2+ ion ; S. Seghir, C. Boulanger,
S. Diliberto, J.M. Lecuire, M. Potel, O. Merdrignac-
Conanec ; dans Electrochemistry Communications, 10,
2008, 1505-1508.
- Selective transfer of cations between two electrolytes
using the intercalation properties of Chevrel phases ;
S. Seghir, C. Boulanger, S. Diliberto, M. Potel, J-M.
Lecuire ; dans Electrochimica Acta, 55, 2010, 1097-
1106.
Ces documents exposent que des cations peuvent être
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
2
transportés à travers la paroi en matériau de formule
M06X8 (avec X= S, Se, Te) dénommé Phases de Chevrel où se
produisent des systèmes d'oxydoréduction réversibles du
type :
Mo6X8 + xMn+ + xn e <=> MxMo6X8
x étant un nombre variant typiquement entre 0 et 4.
Ces systèmes sont diversifiés par la nature du
cation Mn+, du chalcogène X et de la stoechiométrie x du
ternaire.
Dans un montage expérimental mettant en uvre le
procédé de transfert sélectif, la paroi de transfert est
placée entre deux compartiments comportant respectivement
une électrode en titane platiné qui fonctionne en anode
et une électrode en inox qui fonctionne en cathode. Le
premier compartiment contient un premier électrolyte qui
contient différents cations d'un effluent à traiter. Le
deuxième compartiment contient un deuxième électrolyte
destiné à recevoir les cations sélectionnés.
Un courant électrique continu est établi entre
l'anode et la cathode. Dans le fonctionnement
électrochimique global de l'ensemble des deux
compartiments, il se produit l'intercalation du cation à
l'interface M.xMo6S8/ premier électrolyte (effluent à
traiter, mélange des cations Mn+, M'n+, M"n+ différents
entre eux par exemple), selon :
Mo6X8 + x1\411+ + xn e- = MxMo6X8
La désintercalation de ce même cation Mn+ à
l'interface MxMo6S8/ deuxième électrolyte (solution de
valorisation de Mn+ par exemple) s'effectue réciproquement
selon
MxMo6X8 = Mo6X8 + xn e-+ xlVfl+
La mobilité du cation métallique dans la phase de
Chevrel permet ainsi le transfert du cation Mn+ désolvaté
d'un milieu à l'autre sans transfert d'aucune autre
espèce chimique de l'un ou de l'autre des compartiments.
Une paroi de transfert sous forme de pastille est
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
3
obtenue par frittage à chaud d'un mélange de poudre de
composition adaptée à la stoechiométrie du matériau
désiré. On obtient ainsi des disques de matière active
d'une épaisseur de 2 à 5 millimètres.
Les essais avec des parois composées de phases
séléniées et sulfurées ont montré qu'en particulier les
cations des métaux suivants peuvent être transférées d'un
électrolyte à l'autre : fer, manganèse, cobalt, nickel
chrome, cuivre, zinc, cadmium. Les limites de densités de
courant obtenues sont comprises entre 10 et 20 A/m2, avec
des rendements faradiques supérieurs à 90%, voire
supérieurs à 98%, et une très bonne sélectivité.
Les essais ont aussi démontré que la limite de
vitesse de transfert augmentait avec la diminution de
l'épaisseur de la paroi. Cependant, la résistance
mécanique nécessaire de la paroi limite la diminution de
son épaisseur.
Par ailleurs, le transfert de lithium n'a pas pu
être obtenu avec de telles parois. Or, le lithium est de
plus en plus sollicité industriellement, en particulier
pour les batteries de véhicules électriques.
OBJECTIFS DE L'INVENTION
L'invention vise donc à fournir une paroi de
transfert sélectif permettant une bonne vitesse de
transfert et avec un choix élargi de cations
transférables.
EXPOSÉ DE L'INVENTION
Avec ces objectifs en vue, l'invention a pour objet
une paroi de séparation d'électrolytes comportant une
couche active étanche d'un matériau apte à développer des
réactions d'intercalation et de désintercalation pour le
transfert sélectif de cations à travers la paroi,
caractérisée en ce qu'elle comporte une couche de support
constituée d'un matériau poreux servant de support à la
couche active.
WO 2012/010766 CA 02805998 2013-01-18 PCT/FR2011/051602
4
Les inventeurs ont réussi à réaliser une paroi avec
un support poreux qui apporte la résistance mécanique et
une couche active dont l'épaisseur peut être très
réduite. Ils ont constaté que le support poreux ne
faisait pas obstacle aux réactions électrochimiques qui
se produisent au niveau de la couche active. En diminuant
l'épaisseur de la couche active, la vitesse de transfert
atteinte est largement supérieure à la limite de vitesse
selon l'art antérieur, ce qui est l'un des objectifs de
l'invention.
Le matériau poreux est choisi par exemple parmi la
mullite, la silice, la fibre de verre, le quartz ou une
céramique. Ces matériaux présentent les qualités
nécessaires pour remplir le rôle de la paroi, à savoir la
résistance mécanique, la résistance aux produits contenus
dans les électrolytes et la porosité.
La porosité du matériau poreux est comprise par
exemple entre 0,4 et 0,6. Cette valeur exprime le taux de
matière par rapport au volume occupé. Elle constitue un
bon compromis entre le volume de l'électrolyte présent
dans le support poreux et la résistance mécanique dudit
support.
De manière particulière, le matériau de la couche
active est un matériau binaire ou ternaire se comportant
en réseau hôte et ayant des propriétés d'accueil
réversible de cations selon une réaction
d'oxydoréduction. Les inventeurs ont constaté que les
phases de Chevrel ne sont pas les seuls matériaux qui
peuvent développer des réactions
d'intercalation/désintercalation pour former une paroi de
transfert sélectif, mais plus généralement des réseaux
hôtes qui sont stables et où se produisent des réactions
d'oxydoréduction.
Le matériau de la couche active est par exemple un
chalcogénure métallique.
De manière particulière, le chalcogènure métallique
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
5
est un chalcogénure à cluster de molybdène (Mor,X,+2 ou
MxMor,X+2), X étant un chalcogène pris parmi S (Soufre), Se
(Sélénium) ou Te (Tellure), et M étant un métal. Le
nombre n est choisi par exemple parmi 1 ; 1,5 ; 2 ; 3 ;
4 ; 5 ; 6 ou 9.
Selon une autre composition, le matériau de la
couche active est un composé de lithium et d'un métal
sous forme d'oxyde, de phosphate ou de fluorure ou d'une
combinaison de ces formes, le métal étant choisi parmi le
nickel, le cobalt, le fer, le manganèse, le vanadium, le
titane ou le chrome. On constate que ces matériaux sont
aptes à développer des réactions d'intercalation et de
désintercalation, et de transférer des cations de manière
sélective, en particulier le lithium.
Selon un procédé de fabrication de la paroi de
transfert, on prépare une solution comprenant un matériau
actif sous forme de poudre, un liant et un solvant, puis
on enduit la surface d'une couche de support en matériau
poreux avec ladite solution et on fait évaporer le
solvant pour former une couche active étanche sur la
couche de support.
On constate que la couche active obtenue est
étanche, ce qui garantit que les électrolytes ne se
mélangent pas quand la paroi les sépare. De plus, malgré
la formulation initiale en poudre, la couche active est
conductrice électriquement, ce qui montre que les grains
sont en contact les uns avec les autres et ce qui permet
que les réactions d'oxydoréduction se développent sur
toute la surface de la couche active. La couche obtenue
est très fine, conformément à l'objectif fixé au départ.
Le liant est par exemple du poly(fluorure de
vinylidène).
Le solvant est par exemple de la 1-méthy1-2-
pyrrolidone.
Le résultat est déjà satisfaisant lorsque le
matériau en poudre est présent dans une proportion de 80%
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
6
en masse hors le solvant.
Le matériau en poudre a par exemple une
granulométrie comprise entre 30 et 100 pm.
Selon un perfectionnement, la solution comporte en
outre du graphite en poudre. Celui-ci permet de compléter
la conductivité électrique de la couche active.
Selon un perfectionnement, on polit la couche
active jusqu'à faire apparaître la couche de support à
travers la couche active. On diminue ainsi l'épaisseur de
la couche active. Malgré cette diminution, l'étanchéité
est préservée et le rendement de la paroi n'est pas
affecté. On constate une augmentation de la valeur limite
de la densité de courant électrique.
L'invention a aussi pour objet un procédé
d'extraction sélective de cations par transfert
électrochimique caractérisé en ce qu'on utilise comme
paroi de séparation des électrolytes une paroi de
transfert telle que décrite précédemment, et on assure un
transfert des cations à travers ladite paroi de transfert
en générant une différence de potentiel entre d'une part
le premier électrolyte, et d'autre part le deuxième
électrolyte ou la dite paroi de transfert, de manière à
provoquer une intercalation des cations dans la paroi de
transfert du côté du premier électrolyte, une diffusion
des cations dans celle-ci, puis leur désintercalation
dans le deuxième électrolyte.
Selon d'autres caractéristiques :
- au moins un des électrolytes est non aqueux. Les
électrolytes peuvent être différents entre les
compartiments, notamment par différentiation de la
nature des sels de fond, par le niveau d'acidité, par
la présence de complexants, par la nature des solvants
notamment solvants non aqueux organiques ou minéraux
tels que par exemple DMSO, DMF, liquides ioniques,
électrolytes solides, etc_
- la paroi de transfert est raccordée électriquement à un
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
7
appareil de mesure du potentiel entre la dite paroi et
des électrodes de référence situées respectivement
dans chaque électrolyte et on ajuste en conséquence le
potentiel appliqué entre les dits électrolytes.
- la différence de potentiel est générée entre le premier
électrolyte et la paroi de transfert, et la
désintercalation des cations du côté du deuxième
électrolyte est une désintercalation chimique par un
oxydant chimique dans le deuxième électrolyte.
- on assure une succession de transferts de cations à
travers des parois de transfert disposées
successivement entre des électrolytes d'extrémité, et
avec un ou des électrolytes intermédiaires entre les
différentes parois de transfert.
- le métal transféré est électrodéposé sur la cathode.
- au moins deux parois de transfert de nature différente
séparent le premier compartiment de compartiments
respectifs en parallèle pour des transferts sélectifs
de différents cations avec électrolyses modulées
d'intercalation spécifiques sur chacune des parois de
transfert engagées. Les transferts vers des
compartiments séparés permettent la récupération
simultanée spécifique de chacun des métaux, par exemple
pour une solution source contenant des ions Cobalt et
Lithium avec utilisation d'une couche active en Mo6S8
pour le transfert du cobalt et une seconde en LiMn204
sélective du transfert du lithium.
BREVE DESCRIPTION DES FIGURES
L'invention sera mieux comprise et d'autres
particularités et avantages apparaîtront à la lecture de
la description qui va suivre, la description faisant
référence aux dessins annexés parmi lesquels :
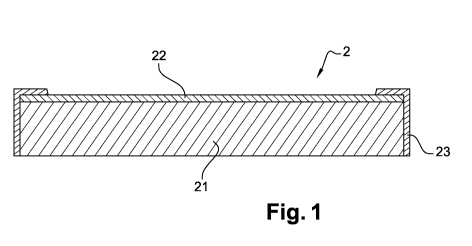
- la figure 1 est une vue en coupe d'une paroi de
transfert conforme à l'invention ;
WO 2012/010766 CA 02805998 2013-01-18 PCT/FR2011/051602
8
- la figure 2 est un graphique d'analyse par diffraction
de rayons X du matériau poreux pour la fabrication
d'une paroi selon la figure 1 ;
- les figures 3 et 4 sont des vues schématiques d'un
montage d'essai pour vérifier la porosité ou
l'étanchéité de la paroi de la figure 1 ;
- la figure 5 est un schéma de principe du dispositif,
- la figure 6 illustre une disposition utilisant
plusieurs compartiments et parois de transfert en
série ;
- la figure 7 illustre une disposition utilisant
plusieurs compartiments et parois de transfert en
parallèle.
DESCRIPTION DETAILLÉE
Une paroi de transfert sous forme de pastille 2
conforme à l'invention est formée d'un support poreux 21
sur lequel une fine couche active 22 est déposée. La
fabrication de pastilles étanches est effectuée en une
première phase de fabrication du support poreux 21, et
une deuxième phase d'application de la couche active 22
sur le support 21.
Elaboration du support poreux
Le support poreux 21 peut se trouver dans le
commerce en mullite, en quartz ou en céramique. A titre
d'exemple, un mode de réalisation est détaillé ci-après,
qui est issu du protocole donné par l'article de Garcia-
Gabaldon et co//, sur la fabrication de membranes
céramiques à base de kaolin et d'alumine développant une
porosité modulable pour leur application en tant que
membrane de séparation en électrochimie : Effect of
porosity on the effective electri cal conductivity of
different ceramic membranes used as separators in
electrochemi cal reactors, Journal of Membranes Sciences
280 (2006) 536-544.
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
9
Le protocole est le suivant : dans un premier temps
un mélange prévu pour 5 g de matériau est constitué de :
- 2,52 g de Kaolin (silicate d'aluminium hydraté
Al2Si205(OH)4,
- 3,80 g d'Alumine A1203
- 1 g de fécule de pomme de terre commerciale.
Le mélange des poudres est homogénéisé dans un
mortier en porcelaine puis mouillé avec un volume minimal
d'acétone pour éviter la formation d'agrégats. Ce mélange
est séché à l'air libre durant 14 h. La poudre obtenue
est ensuite rebroyée manuellement au mortier durant 10
min puis par fraction d'environ 1 g, elle est mise en
forme de pastille par pressage dans une matrice de 25 mm
de diamètre sous une pression de 2 tonnes pendant 5 min.
Les pastilles compactées forment un disque de 1 mm
d'épaisseur. Les échantillons sont soumis à deux
traitements thermiques successifs.
Un premier chauffage à 300 C permet l'oxydation à
l'air de la fécule de pomme de terre. Ce liant organique
est éliminé en 1 heure et crée ainsi la porosité. Un
traitement supplémentaire à 1100 C durant 8 à 24 heures
permet d'assurer une tenue mécanique satisfaisante. Après
ce traitement thermique, on obtient des disques de 24 mm
de diamètre et de 1 mm d'épaisseur. La surface est de 4,5
cm2.
Une analyse par diffraction des rayons X a été
réalisée sur la pastille poreuse (Figure 2). Le spectre
enregistré montre l'absence d'impuretés ainsi que la
formation d'une phase d'alumine et d'une phase de
mullite.
L'évaluation de la porosité de la pastille a été
testée à l'aide de papier pH et d'acide nitrique HNO3 de
la manière suivante représentée sur le schéma de la
figure 3 : le virage du papier pH a permis de confirmer
une bonne porosité de la pastille. Les contrôles de
porosité donnent des valeurs moyennes de 0,553 en volume
CA 02805998 2013-01-18
WO 2012/010766
PCT/FR2011/051602
10
pour des teneurs initiales de 10% en fécule et de 0,501
pour des teneurs de 5%.
Elaboration de la couche active
La deuxième phase de la fabrication de la pastille
consiste en l'enduction physique d'une face du support
poreux 21. Dans l'exemple qui est montré, l'enduction est
réalisée avec une suspension de phase de Chevrel, de
formule M06X8, avec X étant un chalcogène, dans un solvant
volatil. L'électrode de travail est préparée à partir de
composés pulvérulents Mo6S8 ou Mo6Se8 qui constitue la
masse active. Une addition de poly(fluorure de
vinylidène), appelé aussi PVDF, joue le rôle de liant.
La phase Mo6Se8 est issue d'une synthèse céramique à
partir du mélange Mo + 2 MoSe2 homogénéisé et compressé à
froid en cylindre à une pression de 250MPa, effectuée en
creuset de Molybdène scellé au four à arc, sous pression
partielle d'argon, puis chauffé pendant 50h à 1300 C. Le
même traitement de broyage tamisage à 50 pm est également
appliqué à ce composé.La pureté des poudres synthétisées est vérifiée par
leur diagramme de diffraction des Rayons X obtenu sur un
diffractomètre.
La synthèse de la phase de Chevrel à base de
souffre est réalisé par l'intermédiaire d'une phase
ternaire avec un métal intermédiaire tel que par exemple
du Cu3Mo6S8. La synthèse de ce composé ternaire est
effectuée en ampoule de silice scellée sous vide à 1000 C
durant 50h. Le mélange initial est constitué de poudres
micrométriques de Cu, M0S2 et Mo homogénéisé dans un
broyeur à boules pendant 30 minutes et compressé à froid
sous une pression de 250 MPa.
La poudre de molybdène est désoxydée sous courant
d'hydrogène à 1000 C durant 3h et la poudre de M0S2 est
préparée en ampoule scellée de silice par chauffage
progressif du mélange stoechiométrique des éléments
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
11
jusqu'à 800 C.
La granulométrie des produits pulvérulents engagés
est comprise dans une gamme de 30 à 100 micromètres.
La phase Mo6Se8 est issue d'une synthèse céramique à
partir du mélange Mo + 2MoSe2 homogénéisé et compressé à
froid en cylindre à une pression de 250 MPa, effectuée en
creuset de molybdène scellé au four à arc, sous pression
partielle d'argon, puis chauffé pendant 50h à 1300 C. La
pureté des produits de réaction obtenus est vérifiée par
leur diagramme de diffraction des Rayons X obtenu sur un
diffractomètre.
Application de la couche active sur support poreux par enduction
Cas de la matrice en phase de Chevrel
Une suspension constituée de 95% de phases de
Chevrel en poudre et 5% de PVDF est formée dans de la 1-
méthy1-2-pyrrolidone, appelée NMP par la suite, à raison
de 0,1 g de la phase M06X8 solide, 0,005 g de PVDF
dispersé dans 1 mL de NMP. L'ensemble est soumis à une
agitation durant 2 heures.
A l'aide d'une pipette pasteur, on place quelques
gouttes de la suspension de Mo6X8 NMP-PVDF sur la surface
du disque de support poreux pour recouvrir le plus
uniformément toute la surface. Ensuite l'ensemble est mis
à l'étuve pendant 1h pour éliminer le solvant NMP. Dans
ces conditions, le film de M06S8 ou Mo6Se8 résultant est
adhérent à la surface du disque avec des épaisseurs de
l'ordre de 80 pm. De plus les tests d'étanchéité
conformément à la figure 4 confirment la bonne occlusion
des pores du disque poreux, du fait que le papier pH ne
vire pas. Des tests de conductance électrique démontrent
un bon contact électrique entre les grains.
Des techniques d'enduction sur le principe
répartition par centrifugation (spin-coating) ont été
également pratiquées. Elles conduisent à des revêtements
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
12
de même configuration que précédemment.
Pour la synthèse de la phase binaire Mo6S8, on
procède à la désintercalation chimique du cuivre par voie
électrochimique après la réalisation de l'enduction.
Cas de la matrice oxyde de type LixMy0,
Selon un autre exemple, la paroi est fabriquée avec
comme matériau actif une matrice répondant à la formule
générale LixMy0õ dans lequel y et z sont des entiers, par
exemple à titre non limitatif LixCo02, LiMn204, LiV30e,
LiNi02 ou LiMn02. Le matériau actif peut aussi comporter
un mélange de métaux M. Le principe d'élaboration reste
une enduction du support poreux par une suspension de
Li,My0, .
La solution d'enduction est préparée à partir d'un
mélange pulvérulent Li,My0, qui constitue le matériau
actif à 80% en masse, de PVDF à 10% qui joue le rôle de
liant et de carbone à 10% qui assure la conductivité
électrique. Le mélange est homogénéisé intimement dans un
mortier.
Une suspension est réalisée dans de la 1-méthy1-2-
pyrrolidone avec une agitation durant 2 heures à raison
de 0,2 grammes de mélange de poudre pour 1 ml de NMP.
A l'aide d'une pipette pasteur, on place quelques
gouttes de la suspension de Li,My0, NMP-PVDF sur la surface
du disque de support poreux pour recouvrir le plus
uniformément toute la surface. Cette opération peut
également être faite dans une technique de répartition
par centrifugation. Ensuite l'ensemble est mis à l'étuve
pendant 1h pour éliminer le solvant NMP. Dans ces
conditions le film d'oxyde résultant est adhérent à la
surface du disque avec des épaisseurs de l'ordre de 80
pm. De plus, les tests d'étanchéités confirment la bonne
occlusion des pores du disque poreux. Des tests de
conductance électrique démontrent un bon comportement
électrique du film.
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
13
Quel que soit le type de matrice, pour suivre les
potentiels d'interface, il est nécessaire de mettre en
place un contact électrique autour de la pastille à
l'aide de laque de graphite 23. On badigeonne le contour
de la pastille et on déborde sur la face de la couche
active 22.
Procédé de transfert sélectif
Le schéma de la figure 5 montre un dispositif pour
mettre en uvre un procédé de transfert sélectif
utilisant des parois de transfert selon l'invention. Le
dispositif comporte une cuve 1 comportant deux
compartiments 11 et 12, adaptés pour recevoir un
électrolyte et séparés par une cloison de séparation 13
dans laquelle est placée une paroi de transfert 2
constituée d'une pastille 2 en forme de disque, montée
dans la cloison 13 de manière étanche.
Le dispositif comporte aussi une anode Al placée
dans le premier compartiment 11 et une cathode C2 placée
dans le deuxième compartiment 12. Une différence de
potentiel AE peut être appliquée entre l'anode Al et la
cathode C2 par des moyens connus en soi, afin d'imposer
et de contrôler un courant i entre les électrolytes El et
E2.
La couche active 22 est placée du côté du premier
compartiment 11, même si le système fonctionne aussi
lorsqu'elle est du côté du deuxième compartiment 12. Un
système de contact mobile à ressort 44 assure une
connexion électrique avec le contour de la pastille 2
recouvert de laque de graphite, et permet de relier
celle-ci à un appareil de contrôle, adapté notamment pour
mesurer le potentiel d'interface Eil, Ei2 de la pastille
par rapport à des électrodes de référence 33, 34
disposées respectivement dans chaque compartiment 11, 12
de la cuve 1, comme illustré figure 5.
La mise en uvre du dispositif s'effectue
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
14
typiquement de la manière suivante :
On remplit les compartiments 11 et 12 avec
l'électrolyte souhaité, par exemple, et de manière
nullement limitative, 100 ml Na2SO4 0,5 M + M(i)SO4 comme
premier électrolyte El dans le premier compartiment 11,
et 100 ml Na2SO4 0,5 M comme deuxième électrolyte E2 dans
le deuxième compartiment 12, avec 1,4(2) étant un ou
plusieurs cations métalliques que l'on souhaite séparer.
On place l'anode Al dans le premier compartiment 11 et la
cathode C2 dans le deuxième compartiment 12, et on relie
le contact 44 de la pastille avec des moyens de contrôle
potentiométrique, raccordés aux électrodes de référence
33, 34 plongées dans les électrolytes El et E2. On peut
ainsi contrôler les potentiels d'interface et ajuster en
conséquence le potentiel global AE appliqué entre l'anode
Al et la cathode C2, de manière à obtenir une densité de
courant rapportée à la surface opérationnelle de la paroi
de transfert 2, ou de l'ensemble des parois de transfert
disposées en parallèle, comprise par exemple entre 2 et
200 A/m2.
Un régime intensiostatique global est établi entre
l'anode Al et la cathode C2. Nommons RH, pour réseau
hôte, le matériau de la couche active 22. Dans le
fonctionnement électrochimique global de l'ensemble des
deux compartiments, l'électrolyte El étant une solution
d'origine à traiter comportant un mélange des cations de
différents métaux et de charges identiques ou
différentes, Mn+, M'n+, M"n-F par exemple, et l'électrolyte
E2 étant une solution de valorisation du métal M, il se
produit :
- l'intercalation du cation Mn+ à l'interface de la couche
active 22 avec l'électrolyte El, selon :
RH + x Mn+ + xn e =* 1,4,RH
- la désintercalation de ce même cation à l'interface de
la couche active 22 avec l'électrolyte E2 (solution de
valorisation de Mn+ par exemple), qui s'effectue
WO 2012/010766 CA 02805998 2013-01-18PCT/FR2011/051602
15
réciproquement selon
MxRH = RH + xn e + X Mn+
La mobilité du cation métallique dans le réseau
hôte permet ainsi le transfert du cation Mn+ désolvaté
d'un milieu à l'autre sans transfert d'aucune autre
espèce chimique de l'un ou de l'autre des compartiments.
On notera encore de manière générale que les
électrolytes placés dans les deux compartiments 11, 12
comportant l'anode Al et la cathode C2 peuvent être
différents, notamment par la nature des sels de fond, par
le niveau d'acidité, par la présence de complexants, par
la nature des solvants, notamment solvants non aqueux
organiques ou minéraux (DMSO, DMF, liquides ioniques,
électrolytes solides, etc.). On peut ainsi par exemple
effectuer un transfert ionique d'un milieu sulfate à un
milieu chlorure sans diffusion du dit milieu.
Dans la variante de la figure 6, la cuve comporte
trois compartiments. Les deux compartiments extrêmes 11',
12' sont équivalents aux compartiments 11 et 12 de
l'exemple représenté figure 1. Un compartiment
supplémentaire 15, contenant un électrolyte E3 est situé
entre les deux compartiments 11' et 12' et séparé de
ceux-ci par des cloisons de séparation 13', 13"
comportant chacune une ou des parois de transfert 2', 2"
selon l'invention. Ces parois de transfert 2', 2"
peuvent être de même nature, pour simplement accroître la
sélectivité du transfert du compartiment 11' au
compartiment 12'. Elles peuvent aussi être de nature
différente, et être gérées de manière différente par un
contrôle spécifique des potentiels appliqués entre les
divers compartiments par exemple, pour effectuer une
séparation de différents cations. Par exemple, on peut
transférer deux types de cations du compartiment 11' au
compartiment 15, et un seul du compartiment 15 au
compartiment 12'. Diverses combinaisons de pastilles et
de paramètres de transferts peuvent ainsi être utilisées
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
16
pour effectuer des séparations et traitements divers
souhaités.
Dans le cas de la variante de la figure 6, le ou
les électrolytes intermédiaires E3 peuvent aussi être
identiques ou différents de l'un ou des deux électrolytes
El ou E2.
Dans une autre variante, illustrée par la figure 7,
la cuve comporte trois compartiments. Le compartiment
central 11" est équivalent au premier compartiment 11 de
l'exemple représenté figure 2. Le compartiment de gauche
12" est équivalent au deuxième compartiment 12 de
l'exemple représenté figure 2. Un compartiment
supplémentaire 16, contenant un électrolyte E3 est situé
à droite du premier compartiment et séparé de celui-ci
par une cloison de séparation 13"' comportant une ou
plusieurs parois de transfert 2" selon l'invention. Ces
parois de transfert 2" sont de nature différente selon
la cloison de séparation 13, 13", pour transférer
sélectivement un cation spécifique pour chaque
compartiment. Par exemple le premier électrolyte El est
une solution source contenant des ions cobalt et lithium.
La première paroi de transfert 2, entre le premier et le
deuxième compartiment 11", 12", a un matériau actif en
M06S8 pour le transfert sélectif du cobalt, tandis que la
deuxième paroi de transfert 2", entre le premier et le
troisième compartiment 11", 16, a un matériau actif en
LiMn204 pour le transfert sélectif simultané du lithium.
Le premier compartiment 11" comporte une anode Al" de
manière à créer un courant de transfert entre ladite
anode Al" et une cathode C2" dans le deuxième
compartiment, et un autre courant de transfert entre
ladite anode Al" et une cathode 03 dans le troisième
compartiment 16.
CA 02805998 2013-01-18
WO 2012/010766
PCT/FR2011/051602
17
Exemple 1
Une pastille poreuse 21 recouverte d'une couche
active 22 à base de phase de Chevrel sulfurée est
utilisée comme paroi de transfert 2, telle que décrite
précédemment, dans un montage conforme à la figure 5. Le
transfert de cations entre le premier compartiment 11
contenant le premier électrolyte El (solution de cation
M2+ 0,1 M en milieu Na2SO4 0,1 M, H2SO4 0,1 M) et le
deuxième compartiment 12 contenant le deuxième
électrolyte E2 de valorisation à 0,1 M de Na2SO4, et 0,1 M
de H2SO4 a été étudié pour les deux types de pastilles à
base respectivement de Mo6S8 et de Mo6Se8, et à différentes
densités de courant. L'étude s'est attachée à vérifier
pour différents cations Mn+ les rendements faradiques des
transferts, à déterminer les conditions limites pour des
pastilles poreuses de Mo6S8 et Mo6Se8 et à évaluer la
limite de densité de courant. Le procédé de transfert
repose sur un conditionnement préalable avec une quantité
de cation intercalé estimé à partir de la masse Mo6X8
déposé pour une stoechiométrie de Mx/2Mo6X8. Les tableaux 1
et 2 montrent les résultats obtenus pour un matériau
actif respectivement M06S8 et Mo6Se8.
Mo6S8
Métal M Co Ni Cd Zn Mn In
Rendement Pas de
Faradique de 98 90 98 96 92 transfert
transfert(%)
Densité de courant Pas
de
limite (A/m2) 70 70 70 70 70 transfert
Tableau 1.
Mo6Se8
Métal M Co Ni Cd Zn Mn In
Rendement Pas de Pas de
Faradique de 99 97 94 97
transfert(%) transfert transfert
Densité de courant Pas de Pas de 70 70 70 70
limite (A/m2) transfert transfert
Tableau 2.
CA 02805998 2013-01-18
WO 2012/010766
PCT/FR2011/051602
18
On constate que les rendements faradiques sont
intéressants en étant supérieurs à 90% et que les
densités de courant sont très supérieures à celles de
l'art antérieur (de l'ordre de 16 A/m2).
Pour la phase sulfurée, le transfert quantitatif
s'établit à des vitesses entre 2.10-2 mol/h/m2 à faible
densité de courant (3,2 A/m2) et 3 mol/h/m2 à forte
densité de courant (70 A/m2). Cette dernière valeur
apparait comme une vitesse limite pour des épaisseurs de
jonction en Mo6S8 estimées à 80 pm. Concernant la pastille
à matériau actif Mo6Se8, les vitesses de transfert dans
ces phases séléniées se situent dans un même ordre de
grandeur que pour la phase sulfurée : soit 5.10-2 mol/h/m2
pour 3,2 A/m2 et 4 mol/h/m2 pour 70 A/m2 uniquement pour
les cations Cd2+, Zn2+, Mn2+, Cu2+ et In3+. Les tableaux 3 et
4 suivants précisent pour chaque élément les vitesses de
transfert pour une densité de courant de 70 A/m2.
M06S8
Métal M Ce' Ni=2+ Fe2+ ce Zn2+ Mn2+ CU2+
In3+
Vitesse de 1,32 1,11 1,65 3,07 1,43 3,89 4,15
0
transfert
(mol/h/m2)
Tableau 3.
Mo6Se8
Métal M Ce' Ni=2+ Fe2+ ce Zn2+ Mn2+ CU2+
In3+
Vitesse de 0 0 0 3,43 4,17 3,23 2,08
4,08
transfert
(mol/h/m2)
Tableau 4.
Sélectivité
Dans le procédé de transfert sélectif des cations,
le premier électrolyte El contient un mélange de cations
dont seul un type est transféré à travers la paroi. La
sélectivité découle du fait que pendant l'opération
d'électrolyse, la tension appliquée entre les deux faces
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
19
de la couche active 22 ne permet l'intercalation et la
désintercalation que d'un type de cations. Pour
transférer les autres cations, il faudrait appliquer un
potentiel plus élevé, ce qui n'est pas le but du procédé.
Le type de cation qui est transféré a un potentiel
d'intercalation minimal et un potentiel de
désintercalation maximal qui sont exprimés par rapport au
potentiel de référence donné par une électrode au calomel
saturée (ECS).
Des expérimentations de transfert ont été exécutées
pour des mélanges synthétiques de cations tels que :
Co/Ni, Cd/Zn, Cd/Ni, Zn/Mn, Cd/Co, Co/Fe, Ni/Fe et
Cd/Co/Ni.
Dans les exemples suivants, réalisés à partir de
mélanges de deux cations équimolaires (0,1 M), la
sélectivité du transfert est exprimée par un taux de
sélectivité de transfert du cation Mn+ représenté par le
rapport Mtn+ / E MItn+ de la quantité de cations transférés
Mtn+ pour l'espèce considérée à la somme des cations
transférés de toute espèce MItn+ dans le compartiment 2,
par exemple Cot/(Cot+Nit) pour le mélange 002+ + Ni2+.
Ce rapport est donc d'autant plus proche de 100%
que la sélectivité est grande et prend une valeur de 50%
si aucune sélectivité ne se développe.
Les tableaux 5 et 6 récapitulent les taux de
sélectivité obtenus pour les différents mélanges à
différentes densité de courant. Les valeurs indiquées
pour les différentes densités de courant correspondent à
la moyenne des taux de sélectivité obtenus à chaque heure
pendant l'électrolyse de 1 à 7 heures.
Mélanges Matériau actif de la paroi de transfert : 1VIo6S8
Cation Autres Potentiel Potentiel Densité de Densité de
transféré cations intercalation désintercalation courant courant
minimal maximal 3,2 A/m2 70 A/m2
(mV/ECS) (mV/ECS) (Vo) (Vo)
Cd Zn -592 -327 93 93
Co Ni -624 -250 99 99
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
20
Cd Ni -582 -278 70 78
Zn Mn -814 -196 57 60
Cd Co -585 -373 47 89
Co Fe -751 -175 60 59
Ni Fe -756 -118 49 53
Cd Co/Ni -660 -250 63 77
In Cd/Zn / / / /
Tableau 5.
Mélanges Matériau actif de la paroi de transfert : 1VIo6Se8
Cation Autres Potentiel Potentiel Densité de Densité de
transféré cations intercalation désintercalatio courant courant
minimal n maximal 3,2 A/m2 70 A/m2
(mV/ECS) (mV/ECS)
Cd Zn -603 -153 100 100
Co Ni / / / /
Cd Ni -582 -200 100 100
Zn Mn -741 -345 93 98
Cd Co -647 -180 100 100
Co Fe / / / /
Ni Fe / / / /
Cd Co/Ni -656 -166 100 100
In Cd/Zn -540 -340 52 60
Tableau 6.
On constate que le taux de sélectivité dépend de la
densité de courant. La sélectivité est élevée pour des
densités de courant fortes induisant ainsi des vitesses
de transfert élevées. La nature de la couche active 22 de
la paroi joue un rôle important dans le transfert
sélectif de cation. La sélectivité du transfert de Ce' ou
de Zn2+ en présence de Ni2+ est vraiment améliorée jusqu'à
99% en utilisant une matrice séléniée. La même
observation peut être faite dans le cas de Ce' dans le
mélange Cd/Co. La sélectivité n'est pas affectée par la
faible épaisseur de la couche active 22.
Exemple 2
Dans cet exemple, la couche active 22 est réalisée
avec le matériau LiCo02 avec une épaisseur d'environ 80
pm. Un tel matériau est exploité par exemple dans
CA 02805998 2013-01-18
WO 2012/010766
PCT/FR2011/051602
21
l'électrode positive des batteries Lithium ions. Le
premier électrolyte est une solution aqueuse Li+ à 1 M en
milieu Na2SO4 1M. Le deuxième électrolyte qui sert de
solution de valorisation est une solution aqueuse de
Na2SO4 à 1M. Les résultats sont présentés dans le tableau
7.
Densité de courant 4 8 12 16 32 41
(A/m2)
Rendement 98 99 98 99 99 41
faradique de
transfert (%)
Vitesse de 0,14 0,2 0,41 0,6 1,21 0,82
transfert
(mol/h/m2)
Tableau 7.
io Exemple 3
Cet exemple est similaire à l'exemple 2, hormis que
le deuxième électrolyte qui sert de solution de
valorisation est une solution d'un solvant en carbonate
de propylène et de tétrabutyl ammonium perchlorate.
L'anode est en titane platiné et la cathode en inox. Les
résultats sont présentés dans le tableau 8.
LiCo02 sur support poreux
à 10 A/m2
Rendement faradique de transfert 75
(Vo)
Vitesse de transfert (mol/h/m2) 0,401
Tableau 8.
Exemple 4
A partir d'un film élaboré par dépôt de Mo6S8-PVDF
sur une pastille poreuse selon le protocole présenté ci-
dessus, on élimine l'excès de matériau du film par
polissage manuel, par une abrasion au disque SiC de
granulométrie 2400 durant quelques secondes jusqu'à
CA 02805998 2013-01-18
WO 2012/010766 PCT/FR2011/051602
22
apparition de la coloration du support poreux. Ainsi, on
ne laisse la partie des matériaux de transfert que dans
les pores. Cette opération pratiquée et testée de la même
manière que les expérimentations précédentes se signale
par des performances de transfert nettement plus
avantageuses, avec une densité de courant applicable
d'environ 80 A/m2, plus grande que précédemment, sans
perturbation des rendements faradiques.
+,
Exemple 5 : transfert de Li a partir d'un électrolyte mixte Li2SO4 et
COSO4
Dans cet exemple la couche active est réalisée avec
le matériau LiMn204 avec une épaisseur d'environ 80 pm. Le
premier électrolyte est une solution aqueuse contenant
les cations Li+ (1M) et Co2+ (0.5M) en milieu sulfate. Le
deuxième électrolyte qui sert de solution de valorisation
est une solution de Na2SO4 à une concentration de 1M. Les
résultats sont présentés dans le tableau 9.
LiMn204 sur support poreux
Densité de courant (A/m2) 40 70 90 110
Rendement faradique de
transfert de lithium (%) 94 96 97 98
Vitesse de transfert du lithium
(mol/h/m2) 1,43 2,24 3,06 3,67
Tableau 9.