Note: Descriptions are shown in the official language in which they were submitted.
1
Description
Titre : Dispositif et procédé de conversion de composés aromatiques par
alkylation de
benzène par l'éthanol
Domaine technique
L'invention porte sur la conversion d'aromatiques dans le cadre de la
production d'aromatiques
pour la pétrochimie (benzène, toluène, paraxylène, orthoxylène). Plus
particulièrement, l'objet
de l'invention est de pouvoir contrôler les quantités respectives de benzène
et de paraxylène,
et en particulier de pouvoir produire uniquement du paraxylène.
Le complexe aromatique (ou dispositif de conversion de composés aromatiques)
est alimenté
par des charges majoritairement composées de six à dix atomes de carbones ou
plus notées
charges C6 à C10+. Différentes sources de composés aromatiques peuvent être
introduites
dans un complexe aromatique, la plus répandue étant le procédé de reformage
catalytique
des naphtes. Des mélanges de composés aromatiques obtenus par procédé de
conversion
de la biomasse lignocellulosique peuvent également, après traitement de
purification, être
introduits dans un complexe aromatique. On peut par exemple considérer le
procédé de
pyrolyse catalytique de la biomasse lignocellulosique comme source
d'aromatiques.
Au sein d'un complexe aromatique, quel qu'en soit la source d'aromatiques, le
benzène et les
alkyles aromatiques (e.g. toluène, paraxylène, orthoxylène) y sont extraits
puis convertis en
intermédiaires souhaités. Les produits d'intérêt sont des aromatiques avec 0
(benzène), 1
(toluène) ou 2 (xylènes) groupes méthyles, et en particulier, au sein des
xylènes, le paraxylène,
ayant la plus forte valeur marchande.
Il convient donc de disposer de groupes méthyles pour que tous les noyaux
aromatiques en
sortie du complexe aromatique possèdent 2 groupes méthyles (e.g. paraxylène,
orthoxylène)
Technique antérieure
A ce jour les complexes aromatiques permettent de produire du benzène,
éventuellement du
toluène, et des xylènes (souvent le paraxylène, quelques fois l'orthoxylène).
Un complexe
aromatique dispose généralement d'au moins une unité catalytique présentant au
moins une
des fonctions suivantes :
Date Reçue/Date Received 2020-12-11
2
- l'isomérisation des composés aromatiques à 8 atomes de carbone notés
composés A8
permettant de convertir l'orthoxylène, le métaxylène et l'éthylbenzène en
paraxylène;
- la transalkylation permettant de produire des xylènes à partir d'un
mélange de toluène
(et optionnellement de benzène) et de composés A9+ tels que les
triméthylbenzènes et
les tétraméthylbenzènes ; et
- la dismutation du toluène, qui permet de produire du benzène et des
xylènes.
La boucle aromatique permet de produire du paraxylène haute pureté par
séparation par
adsorption ou par cristallisation, opération bien connue de l'art antérieur.
Cette boucle C8-
aromatique inclut une étape d'élimination des composés lourds (i.e., C9+)
dans une colonne
de distillation appelée colonne des xylènes . Le flux de tête de cette
colonne, qui contient
les isomères en C8-aromatiques (i.e., A8), est ensuite envoyé dans le procédé
de séparation
du paraxylène qui est très généralement un procédé de séparation par
adsorption en lit mobile
simulé (LMS) pour produire un extrait et un raffinat, ou un procédé de
cristallisation dans lequel
une fraction de paraxylène est isolée du reste des constituants du mélange
sous forme de
cristaux.
L'extrait, qui contient le paraxylène est ensuite distillé pour obtenir du
paraxylène de haute
pureté. Le raffinat, riche en métaxylène, orthoxylène et éthylbenzène est
traité dans une unité
catalytique d'isomérisation qui redonne un mélange d'aromatiques en C8, dans
lequel la
proportion des xylènes (ortho-, méta-, para- xylènes) est pratiquement à
l'équilibre
thermodynamique et la quantité d'éthylbenzène est amoindrie. Ce mélange est à
nouveau
envoyé dans la colonne des xylènes avec la charge fraiche.
Tous les procédés industriels d'isomérisation des C8-aromatiques permettent
d'isomériser les
xylènes. La transformation de l'éthylbenzène dépend, en revanche, du type de
procédé et de
catalyseur choisis. En effet, les complexes pétrochimiques utilisent une unité
d'isomérisation
dite isomérisante (i.e., isomérisation de l'éthylbenzène en un mélange de
C8 aromatiques)
ou désalkylante (i.e., désalkylation de l'éthylbenzène en benzène), afin
de privilégier la
production (à la sortie de la boucle aromatique) respectivement soit de
paraxylène seul, soit
de benzène et paraxylène.
Le choix d'une isomérisation isomérisante permet, comme indiqué ci-dessus,
de
maximiser la production de paraxylène, qui est le composé ayant la plus forte
valeur ajoutée
en sortie du complexe aromatique. L'association au sein d'un complexe
aromatique d'une
isomérisation isomérisante et d'une isomérisation en phase liquide telle
que décrite par
exemple dans les brevets US8697929, US7371913, US4962258, US6180550,
US7915471,
Date Reçue/Date Received 2020-12-11
3
US10035739 et US10029958 permet notamment de maximiser la quantité de
paraxylène
produite tout en ayant une perte en cycles aromatiques réduite par rapport à
un complexe
aromatique selon l'art antérieur.
Résumé de l'invention
Dans le contexte précédemment décrit, un premier objet de la présente
description est de
surmonter les problèmes de l'art antérieur et de fournir un dispositif et un
procédé de
production d'aromatiques pour la pétrochimie permettant, pour tout type de
charge alimentant
un complexe aromatique, d'ajuster les quantités respectives de benzène et
paraxylène, voire
de ne produire que du paraxylène. L'objet de l'invention permet également
d'augmenter la
quantité d'aromatiques produits, et de conserver le caractère biosourcé des
aromatiques dans
le cas où ces derniers sont issus d'un procédé de conversion de la biomasse
lignocellulosique.
L'invention repose sur l'introduction d'éthanol dans le complexe aromatique,
et sur la
disposition d'une ou plusieurs unités permettant de convertir l'éthanol et
notamment de pouvoir
ne produire que du paraxylène. Spécifiquement, l'objet de la présente
invention peut se
résumer à ajouter une unité catalytique au complexe aromatique, cette unité
catalytique
permet de convertir le benzène en éthylbenzène par réaction entre du benzène
et de l'éthanol.
Cette unité comprend une section réactionnelle d'alkylation produisant de
l'éthylbenzène. Une
section réactionnelle optionnelle de transalkylation peut également permettre
de convertir les
polyéthylbenzènes, éventuels sous-produits de la réaction d'alkylation du
benzène par
l'éthanol, en éthylbenzènes. L'éthylbenzène ainsi produit est converti en
paraxylène dans la
boucle aromatique du complexe aromatique.
Selon un premier aspect, les objets précités, ainsi que d'autres avantages,
sont obtenus par
un dispositif de conversion d'une charge de composés aromatiques, comprenant :
- un train de fractionnement adapté pour extraire au moins une coupe
comprenant du
benzène, une coupe comprenant du toluène et une coupe comprenant des xylènes
et
de l'éthylbenzène de la charge ;
- une unité de séparation des xylènes adaptée pour traiter la coupe
comprenant des
xylènes et de l'éthylbenzène et produire un extrait comprenant du paraxylène
et un
raffinat comprenant de l'orthoxylène, du métaxylène et de l'éthylbenzène;
- une unité d'isomérisation adaptée pour traiter le raffinat et produire un
isomérat enrichi
en paraxylène envoyé vers le train de fractionnement ; et
Date Reçue/Date Received 2020-12-11
4
- une section réactionnelle d'alkylation adaptée pour traiter au moins une
partie de la
coupe comprenant du benzène avec une source d'éthanol et produire un effluent
d'alkylation comprenant de l'éthylbenzène envoyé vers l'unité d'isomérisation.
Selon un ou plusieurs modes de réalisation, le dispositif comprend en outre
une section
réactionnelle de transalkylation adaptée pour transalkyler des
polyéthylbenzènes présents
dans l'effluent d'alkylation et produire une coupe enrichie en éthylbenzène.
Selon un ou plusieurs modes de réalisation, le dispositif comprend en outre
une unité de
fractionnement adaptée pour traiter l'effluent d'alkylation et produire une
pluralité de coupes
de fractionnement comprenant au moins une coupe d'éthylbenzène envoyée vers
l'unité
d'isomérisation, une coupe aqueuse comprenant de l'eau et une coupe de
benzène.
Selon un ou plusieurs modes de réalisation, l'unité de fractionnement est
disposée en aval de
la section réactionnelle de transalkylation et est adaptée pour traiter la
coupe enrichie en
éthylbenzène.
Selon un ou plusieurs modes de réalisation, l'unité de fractionnement est
adaptée pour
produire en outre au moins une coupe de polyéthylbenzènes, et la section
réactionnelle de
transalkylation est disposée en aval de l'unité de fractionnement et est
adaptée pour traiter au
moins une partie de ladite coupe de polyéthylbenzènes.
Selon un ou plusieurs modes de réalisation, le train de fractionnement est
adapté pour extraire
une coupe de mono-aromatiques en C9-C10 de la charge.
Selon un ou plusieurs modes de réalisation, le dispositif comprend en outre
une unité de
transalkylation adaptée pour traiter la coupe de mono-aromatiques en C9-C10
avec la coupe
comprenant du toluène et produire des xylènes envoyés vers le train de
fractionnement.
Selon un ou plusieurs modes de réalisation, le dispositif comprend en outre
une unité de
dismutation adaptée pour traiter au moins en partie la coupe comprenant du
toluène et
produire une coupe enrichie en xylènes recyclé vers l'unité d'isomérisation.
Selon un deuxième aspect, les objets précités, ainsi que d'autres avantages,
sont obtenus par
un procédé de conversion d'une charge de composés aromatiques, comprenant les
étapes
suivantes :
Date Reçue/Date Received 2020-12-11
5
- fractionner la charge dans un train de fractionnement pour extraire au
moins une coupe
comprenant du benzène, une coupe comprenant du toluène et une coupe comprenant
des xylènes et de l'éthylbenzène ;
- séparer la coupe comprenant des xylènes et de l'éthylbenzène dans une
unité de
séparation des xylènes et produire un extrait comprenant du paraxylène et un
raffinat
comprenant de l'orthoxylène, du métaxylène et de l'éthylbenzène ;
- isomériser le raffinat dans une unité d'isomérisation et produire un
isomérat enrichi en
paraxylène;
- envoyer l'isomérat enrichi en paraxylène vers le train de fractionnement
;
- alkyler au moins une partie de la coupe comprenant du benzène avec une
source
d'éthanol dans une section réactionnelle d'alkylation et produire un effluent
d'alkylation
comprenant de l'éthylbenzène ; et
- envoyer l'effluent d'alkylation comprenant de l'éthylbenzène vers l'unité
d'isomérisation.
Selon un ou plusieurs modes de réalisation, la section réactionnelle
d'alkylation comprend au
moins un réacteur d'alkylation utilisé dans les conditions opératoires
suivantes :
- température comprise entre 20 C et 400 C;
- pression comprise entre 1 et 10 MPa ;
- rapport molaire benzène/éthanol compris entre 3 et 15;
- PPH comprise entre 0,5 et 50 h-1.
Selon un ou plusieurs modes de réalisation, le réacteur d'alkylation est opéré
en présence
d'un catalyseur comprenant une zéolithe.
Selon un ou plusieurs modes de réalisation, l'unité d'isomérisation comprend
une zone
d'isomérisation en phase gaz et/ou une zone d'isomérisation en phase liquide,
dans lequel la zone d'isomérisation en phase gaz est utilisée dans les
conditions opératoires
suivantes :
- température supérieure à 300 C;
- pression inférieure à 4,0 MPa ;
- vitesse spatiale horaire inférieure à 10 h-1;
- rapport molaire hydrogène sur hydrocarbure inférieur à 10;
- en présence d'un catalyseur comportant au moins une zéolithe présentant
des canaux
dont l'ouverture est définie par un anneau à 10 ou 12 atomes d'oxygène, et au
moins
un métal du groupe VIII de teneur comprise entre 0,1 et 0,3% poids, bornes
incluses,
et
Date Reçue/Date Received 2020-12-11
6
dans lequel la zone d'isomérisation en phase liquide est utilisée dans les
conditions
opératoires suivantes :
- température inférieure à 300 C;
- pression inférieure à 4 MPa ;
- vitesse spatiale horaire inférieure à 10h-1;
- en présence d'un catalyseur comportant au moins une zéolithe présentant
des canaux
dont l'ouverture est définie par un anneau à 10 ou 12 atomes d'oxygène.
Selon un ou plusieurs modes de réalisation, le procédé comprend en outre
l'étape suivante :
- transalkyler des polyéthylbenzènes présents dans l'effluent d'alkylation
dans une section
réactionnelle de transalkylation et produire une coupe enrichie en
éthylbenzène, et
- envoyer la coupe enrichie en éthylbenzène vers l'unité d'isomérisation.
Selon un ou plusieurs modes de réalisation, la section réactionnelle de
transalkylation
comprend au moins un réacteur de transalkylation utilisé dans les conditions
opératoires
suivantes :
- température comprise entre 200 C et 400 C;
- pression comprise entre 1 et 6 MPa ;
- PPH comprise entre 0,5 et 5 h-1.
Selon un ou plusieurs modes de réalisation, le réacteur de transalkylation est
opéré en
présence d'un catalyseur comprenant une zéolithe.
Des modes de réalisation selon le premier aspect et le deuxième aspect ainsi
que d'autres
caractéristiques et avantages des dispositifs et procédés selon les aspects
précités vont
apparaître à la lecture de la description qui va suivre, donnée à titre
uniquement illustratif et
non limitatif, et en référence aux dessins suivants.
Liste des figures
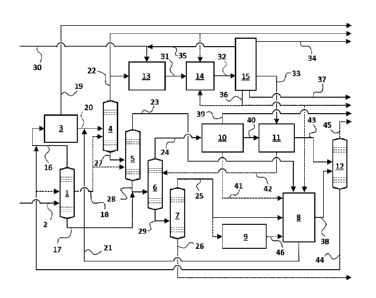
[Fig 1] La figure 1 représente une vue schématique d'un procédé selon la
présente invention
permettant d'augmenter la production de paraxylène.
[Fig 2] La figure 2 représente une vue schématique d'un procédé selon la
présente invention
permettant d'augmenter la production de paraxylène dans lequel l'unité de
transalkylation est
remplacée par une unité de dismutation et dans lequel la section réactionnelle
de
transalkylation est disposée en aval de l'unité de fractionnement.
Date Reçue/Date Received 2020-12-11
7
Description des modes de réalisation
Des modes de réalisation du dispositif selon le premier aspect et du procédé
selon le deuxième
aspect vont maintenant être décrits en détail. Dans la description détaillée
suivante, de
nombreux détails spécifiques sont exposés afin de fournir une compréhension
plus
approfondie du dispositif. Cependant, il apparaîtra à l'homme du métier que le
dispositif peut
être mis en oeuvre sans ces détails spécifiques. Dans d'autres cas, des
caractéristiques bien
connues n'ont pas été décrites en détail pour éviter de compliquer inutilement
la description.
Dans la présente demande, le terme comprendre est synonyme de (signifie la
même chose
que) inclure et contenir , et est inclusif ou ouvert et n'exclut pas
d'autres éléments non
récités. Il est entendu que le terme comprendre inclut le terme exclusif
et fermé
consister . En outre, dans la présente description, un effluent comprenant
essentiellement
ou uniquement des composés A correspond à un effluent comprenant au moins 80
ou 90%
poids, préférablement au moins 95% poids, très préférablement au moins 99%
poids, de
composés A.
La présente invention peut se définir comme un dispositif et un procédé
comprenant un
enchainement d'opérations unitaires permettant de produire soit exclusivement
du paraxylène,
soit du paraxylène et du benzène.
Le dispositif et le procédé selon l'invention sont caractérisés en ce qu'ils
comprennent et
utilisent les unités catalytiques et les unités de séparation connus de
l'homme du métier pour
produire du benzène et du paraxylène, unités que l'on trouve habituellement
dans les
complexes aromatiques, et en ce qu'ils comprennent et utilisent une section
réactionnelle
d'alkylation du benzène par de l'éthanol, et optionnellement une section
réactionnelle de
transalkylation de sous-produits de type polyéthylbenzènes. Ladite section
réactionnelle
d'alkylation du benzène par l'éthanol permet d'obtenir de l'éthylbenzène. Une
des
caractéristiques de la présente invention consiste en la transformation
sélective de cet
éthylbenzène obtenu par alkylation au sein d'une unité d'isomérisation des
composés C8
aromatiques, ladite unité d'isomérisation traitant des composés aromatiques du
complexe
aromatique auxquels s'ajoute l'éthylbenzène produit par alkylation du benzène
avec l'éthanol.
D'une façon surprenante, la combinaison de la section réactionnelle
d'alkylation du benzène
par l'éthanol, et de l'unité d'isomérisation permet à la fois d'augmenter la
quantité
d'aromatiques produits, d'avoir la possibilité de n'obtenir que du paraxylène,
et de conserver
Date Reçue/Date Received 2020-12-11
8
le caractère biosourcé du paraxylène dans le cas où la source de composés
aromatiques en
entrée du complexe aromatique est issue d'un procédé de conversion de la
biomasse
lignocellulosique, comme par exemple un procédé de pyrolyse catalytique de la
biomasse et
dans le cas où l'éthanol est également biosourcée.
En référence à la figure 1, selon un ou plusieurs modes de réalisation, le
dispositif de
conversion de composés aromatiques comprend :
- une unité optionnelle de séparation de charge 1 pour séparer la charge
d'entrée 2 du
complexe aromatique en une coupe hydrocarbonée à 7 atomes de carbones ou moins
(C7-) et une coupe aromatique à 8 atomes de carbones ou plus (A8+) ;
- une unité optionnelle d'extraction des aromatiques 3 entre l'unité de
séparation de
charge 1 et un train de fractionnement 4-7 pour séparer les composés
aliphatiques du
benzène et du toluène de la coupe en C7- de la charge du complexe ;
- le train de fractionnement 4-7 en aval de l'unité optionnelle
d'extraction des aromatiques
3 permettant d'extraire du benzène, du toluène et des xylènes des autres
aromatiques ;
- une unité optionnelle de transalkylation 8 convertissant en xylènes du
toluène (et
optionnellement du benzène) et des méthylalkylbenzènes tels que des
triméthylbenzènes - avantageusement cette unité peut également traiter des
tétraméthylbenzènes ;
- une unité optionnelle d'hydrogénolyse sélective 9 adaptée pour traiter une
coupe
comprenant des composés aromatiques à 9 et 10 atomes de carbones et produire
un
effluent d'hydrogénolyse enrichi en composés aromatiques substitués en
méthyles ;
- une unité optionnelle de séparation (non montrée) pour séparer l'effluent
d'hydrogénolyse disposée (e.g. directement) en aval de l'unité d'hydrogénolyse
sélective
9, pour produire une pluralité de coupes d'effluents liquides ;
- une unité de séparation des xylènes 10 (e.g. de type cristallisation ou
lit mobile simulé
utilisant un tamis moléculaire et un désorbant tel que du toluène) permettant
d'isoler le
paraxylène des xylènes et de l'éthylbenzène ;
- une unité d'isomérisation 11 du raffinat obtenu comme effluent de l'unité
de séparation
des xylènes 10 pour convertir notamment l'orthoxylène, le métaxylène et
l'éthylbenzène
en paraxylène;
- une colonne optionnelle de stabilisation 12, permettant notamment de
retirer les espèces
plus volatiles (e.g. C5-) du complexe aromatique, notamment des effluents de
l'unité de
transalkylation 8 et/ou de l'unité d'isomérisation 11 ;
- une section réactionnelle d'alkylation 13 pour alkyler une fraction
comprenant du
benzène avec de l'éthanol et produire de l'éthylbenzène ;
Date Reçue/Date Received 2020-12-11
9
- une section optionnelle de transalkylation 14 pour transalkyler les
polyéthylbenzènes
issus de la section réactionnelle d'alkylation 13 et produire un effluent
enrichi en
éthylbenzène ;
- une unité de fractionnement 15 pour séparer les produits d'alkylation
disposée en aval
de la section réactionnelle d'alkylation 13.
Avantageusement, la section réactionnelle d'alkylation 13 permet de produire
un surplus
d'aromatiques par l'ajout d'éthanol (ajout de deux atomes de carbone sur
chaque molécule de
benzène) et donne la possibilité de pouvoir convertir l'intégralité du benzène
en paraxylène.
De plus, la faible quantité de composés lourds issus de la section
d'alkylation du benzène par
l'éthanol, et qui n'est pas utilisée pour être transalkylée avec du benzène,
peut être valorisée
en carburant (e.g. kérosène ou gazole).
En référence à la figure 1, l'unité de séparation de charge 1 traite la charge
d'entrée 2 du
complexe aromatique pour séparer une coupe de tête comprenant (e.g.
essentiellement) des
composés à 7 atomes de carbones ou moins 16 (C7-) contenant notamment du
benzène et
du toluène, et une coupe de fond comprenant (e.g. essentiellement) des
aromatiques à 8
atomes de carbones ou plus 17 (A8+) envoyée vers la colonne de xylène 6. Selon
un ou
plusieurs modes de réalisation, l'unité de séparation de charge 1 sépare
également une
première coupe de toluène 18 comprenant au moins 90% poids, préférablement au
moins 95%
poids, très préférablement au moins 99% poids de toluène. Selon un ou
plusieurs modes de
réalisation, la première coupe de toluène 18 est envoyée vers la première
colonne de
distillation de composés aromatiques 4, appelée également colonne de benzène,
et/ou vers la
deuxième colonne de distillation de composés aromatiques 5, appelée également
colonne de
toluène.
Selon un ou plusieurs modes de réalisation, la charge d'entrée 2 est une coupe
hydrocarbonée
contenant majoritairement (i.e., > 50% poids) des molécules dont le nombre de
carbone
s'étend de 6 à 10 atomes de carbone. Cette charge peut également contenir des
molécules
ayant plus de 10 atomes de carbone et/ou des molécules à 5 atomes de carbone.
La charge d'entrée 2 du complexe aromatique est riche en aromatiques (e.g. >
50% poids) et
contient préférablement au moins 20% poids de benzène, préférentiellement au
moins 30%
poids, très préférablement au moins 40% poids de benzène. La charge d'entrée 2
peut être
produite par reformage catalytique d'un naphta ou être un produit d'unité de
craquage (e.g. à
la vapeur, catalytique) ou tout autre moyen de production d'alkyle
aromatiques.
Date Reçue/Date Received 2020-12-11
10
Selon un ou plusieurs modes de réalisation, la charge d'entrée 2 est
biosourcée. Selon un ou
plusieurs modes de réalisation, la charge d'entrée 2 provient d'un procédé de
conversion de
la biomasse lignocellulosique. Par exemple, un effluent produit par conversion
de la biomasse
lignocellulosique peut être traité pour être aux spécifications requises de la
charge d'entrée 2
telle que décrite ci-dessus afin de présenter des teneurs en éléments soufrés,
azotés et
oxygénés compatible avec un complexe aromatique. Selon un ou plusieurs modes
de
réalisation, la charge d'entrée 2 comprend moins de 10 ppm poids,
préférablement moins de
5 ppm poids, très préférablement moins de 1 ppm poids en azote élémentaire,
et/ou moins de
ppm poids, préférablement moins de 5 ppm poids, très préférablement moins de 1
ppm
10 poids en soufre élémentaire, et/ou moins de 100 ppm poids,
préférablement moins de 50 ppm
poids, très préférablement moins de 10 ppm poids en oxygène élémentaire.
La coupe de tête 16 de l'unité de séparation de charge 1, optionnellement
mélangée au produit
de fond (benzène et toluène) de la colonne de stabilisation 12 qui sera
définie ci-après, est
envoyée vers l'unité d'extraction des aromatiques 3 afin d'extraire un
effluent comprenant des
espèces aliphatiques en C6-C7 19 qui est exporté comme co-produit du complexe
aromatique.
La coupe aromatique 20 (essentiellement du benzène et du toluène) appelée
extrait de l'unité
d'extraction des aromatiques 3, optionnellement mélangée à la fraction lourde
21 de l'unité de
transalkylation 8 qui sera définie ci-après, est envoyée vers la colonne de
benzène 4. Selon
un ou plusieurs modes de réalisation, la coupe aromatique 20 est une charge
hydrocarbonée
(e.g. essentiellement) aromatique en C6-C7 (A6-A7).
Selon un ou plusieurs modes de réalisation, le train de fractionnement
comprend les colonnes
de distillation de composés aromatiques 4, 5, 6 et 7 permettant de séparer les
5 coupes
suivantes :
- une coupe comprenant (e.g. essentiellement) du benzène 22;
- une coupe comprenant (e.g. essentiellement) du toluène 23;
- une coupe comprenant (e.g. essentiellement) des xylènes et de
l'éthylbenzène 24;
- une coupe comprenant (e.g. essentiellement) des composés aromatiques à 9
et 10
atomes de carbones 25;
- une coupe comprenant (e.g. essentiellement) des composés aromatiques dont
les
espèces les plus volatiles sont des aromatiques à 10 atomes de carbones 26.
La colonne de benzène 4 est adaptée pour : traiter la coupe aromatique 20 qui
est une charge
hydrocarbonée (e.g. essentiellement) aromatique en C6-C10 (A6+) ; produire en
tête la coupe
comprenant du benzène 22 qui peut être un des produits recherchés en sortie du
complexe
Date Reçue/Date Received 2020-12-11
11
aromatique ; et produire en fond un effluent (e.g. essentiellement) aromatique
en C7-C10 27
(A7+).
La colonne de toluène 5 est adaptée pour : traiter l'effluent aromatique en C7-
C10 27 (A7+),
produit de fond de la colonne de benzène 4; produire en tête la coupe
comprenant du toluène
23 qui est dirigée vers l'unité de transalkylation 8; et produire en fond un
effluent (e.g.
essentiellement) aromatique en C8-C10 28 (A8+).
La troisième colonne de distillation de composés aromatiques 6, appelée
également colonne
de xylène est adaptée pour : traiter la coupe aromatique à 8 atomes de
carbones ou plus 17
(A8+) de la charge du complexe aromatique et optionnellement l'effluent de
fond de la colonne
de toluène 28; produire en tête la coupe comprenant des xylènes et de
l'éthylbenzène 24 qui
est dirigée vers l'unité de séparation des xylènes 10; et produire en fond un
effluent (e.g.
essentiellement) comprenant des aromatiques en C9-C10 29 (A9+).
La quatrième colonne de distillation de composés aromatiques 7, appelée
également colonne
des aromatiques lourds est optionnelle et est adaptée pour : traiter
l'effluent de fond de la
colonne de xylène 29; produire en tête la fraction comprenant des mono-
aromatiques en C9-
C10 25; et produire en fond la coupe comprenant (e.g. essentiellement) des
composés
aromatiques dont les espèces les plus volatiles sont des aromatiques à 10
atomes de
carbones 26 (Al 0+). Préférablement, la coupe de fond 26 comprend des composés
en C11+.
En tête de la colonne de benzène 4 est obtenue la coupe comprenant du benzène
22 qui est
envoyée au moins en partie vers la section réactionnelle d'alkylation 13 pour
réaction avec
une source d'éthanol 30 pour produire un effluent d'alkylation 31 comprenant
de
l'éthylbenzène, de l'eau et potentiellement du benzène et/ou de l'éthanol
et/ou des
polyéthylbenzènes (sous-produits) et/ou des oligomères formés à partir de
l'éthanol. Selon un
ou plusieurs modes de réalisation, la section réactionnelle d'alkylation 13
est alimentée par un
mélange constitué (e.g. essentiellement) de benzène et d'éthanol (et
optionnellement d'eau).
Selon un ou plusieurs modes de réalisation, l'effluent d'alkylation 31
comprend au moins 5%
poids, préférablement au moins 8% poids, très préférablement au moins 10%
poids
d'éthylbenzène. Le complément à 100 est principalement (e.g. > 50% poids),
voire
essentiellement, constitué de benzène car généralement utilisé en excès.
Selon un ou plusieurs modes de réalisation, la section réactionnelle
d'alkylation 13 comprend
au moins un réacteur d'alkylation adapté pour être utilisé dans au moins une
des conditions
opératoires suivantes :
Date Reçue/Date Received 2020-12-11
12
- température comprise entre 20 C et 400 C, préférentiellement comprise
entre 150 C et
400 C, et plus préférentiellement encore comprise entre 250 C et 310 C;
- pression comprise entre 1 et 10 MPa, préférentiellement comprise entre 2
et 7 MPa, et
plus préférentiellement comprise entre 3 et 5 MPa;
- rapport molaire benzène/éthanol compris entre 3 et 15, et préférentiellement
compris
entre 5 et 12;
- PPH comprise entre 0,5 et 50 h-1, préférentiellement comprise entre 1 et
10 h-1, et plus
préférentiellement comprise entre 1,5 et 3 h-1.
Le terme PPH correspond au poids de charge hydrocarbonée horaire injecté
rapporté au poids
de catalyseur chargé.
Selon un ou plusieurs modes de réalisation, le réacteur d'alkylation est opéré
en présence
d'un catalyseur comprenant une zéolithe. Selon un ou plusieurs modes de
réalisation, le
catalyseur à base de zéolithe, préférablement à base de zéolithe Y, très
préférablement à base
de zéolithe Y désaluminée, comprend de 1 à 100 % poids, de préférence 20 à 98
% poids, par
exemple 40 à 98 % poids de ladite zéolithe et 0 à 99 % poids, de préférence 2
à 80 % poids,
et, par exemple, 2 à 60 % poids d'une matrice. Selon un ou plusieurs modes de
réalisation, le
catalyseur comprend une zéolithe Y désaluminée de rapport atomique Si/AI
global supérieur
à 4, de préférence compris entre 8 et 70 et préférablement ne contenant pas
d'espèces
aluminiques extra-réseau. Ladite zéolithe Y désaluminée peut être employée
seule ou en
mélange avec un liant ou une matrice généralement choisis dans le groupe formé
par les
argiles, les alumines, la silice, la magnésie, la zircone, l'oxyde de titane,
l'oxyde de bore et
toute combinaison d'au moins deux de ces oxydes comme la silice-alumine, la
silice-magnésie.
Toutes les méthodes connues d'agglomération et de mise en forme sont
applicables, telles
que, par exemple, l'extrusion, le pastillage ou la coagulation en gouttes. Les
zéolithes telles
que les zéolithes Y désaluminées et leur préparation sont bien connues. On
pourra par
exemple se référer au brevet U54738940.
Selon un ou plusieurs modes de réalisation, le réacteur d'alkylation est de
type lit fixe.
Selon un ou plusieurs modes de réalisation, l'éthanol 30 est biosourcée. Selon
un ou plusieurs
modes de réalisation, l'éthanol 30 provient d'un procédé de fermentation de
sucres. Selon un
ou plusieurs modes de réalisation, l'éthanol 30 provient d'un procédé de
fermentation de
sucres dont la teneur en eau est comprise entre 0,5% poids et 40% poids.
Date Reçue/Date Received 2020-12-11
13
Selon un ou plusieurs modes de réalisation, l'effluent d'alkylation 31 est
transalkylé dans la
section optionnelle de transalkylation 14 pour produire une coupe enrichie en
éthylbenzène
32. Selon un ou plusieurs modes de réalisation, la section réactionnelle de
transalkylation 14
est alimentée en benzène, par exemple lorsqu'un excès de groupes éthyles est
observé dans
l'effluent d'alkylation 31 pour la production d'éthylbenzène.
Selon un ou plusieurs modes de réalisation, la coupe enrichie en éthylbenzène
32 est envoyée
vers l'unité de fractionnement 15 pour produire une coupe d'éthylbenzène 33,
une coupe
aqueuse 34 comprenant de l'eau et optionnellement de l'éthanol, une coupe de
benzène 35
qui pourra par exemple être recyclée au moins en partie vers la section
réactionnelle
d'alkylation 13, éventuellement une ou plusieurs coupes de polyéthylbenzènes
36 et 37, et
éventuellement des oligomères formés à partir de l'éthanol. Selon un ou
plusieurs modes de
réalisation, la coupe d'éthylbenzène 33 alimente l'unité d'isomérisation 11.
De cette façon, tout
l'éthylbenzène, initialement présent dans la charge et produit par alkylation
dans la section
réactionnelle d'alkylation 13, est introduit et converti en paraxylène dans la
boucle aromatique
contenant l'unité d'isomérisation 11 et l'unité de séparation des xylènes 10.
Selon un ou plusieurs modes de réalisation, l'effluent d'alkylation 31 est
envoyé directement
vers l'unité de fractionnement 15.
Selon un ou plusieurs modes de réalisation, l'unité de fractionnement 15
comprend une série
de colonnes de fractionnement (e.g. série de trois colonnes) adaptée pour
extraire la coupe
de benzène 35 (par exemple en tête de la première colonne de fractionnement),
la coupe
d'éthylbenzène 33 (par exemple en tête de la deuxième colonne de
fractionnement), une
première coupe de polyéthylbenzènes 36 comprenant du diéthylbenzène et
optionnellement
du triéthylbenzène (par exemple en tête de la troisième colonne de
fractionnement), et une
deuxième coupe de polyéthylbenzènes 37 comprenant notamment du
tétraéthylbenzène (par
exemple en fond de la troisième colonne de fractionnement).
Selon un ou plusieurs modes de réalisation, la première coupe de
polyéthylbenzènes 36 est
au moins partiellement recyclée vers la section réactionnelle de
transalkylation 14. Selon un
ou plusieurs modes de réalisation, la première coupe de polyéthylbenzènes 36
est au moins
partiellement recyclée vers l'unité de transalkylation 8. Selon un ou
plusieurs modes de
réalisation, la deuxième coupe de polyéthylbenzènes 37, dite coupe de goudron
ou coupe
lourde, est extraite du complexe aromatique. Selon un ou plusieurs modes de
réalisation, la
deuxième coupe de polyéthylbenzènes 37 est évacuée avec la coupe de fond 26 de
la colonne
des aromatiques lourds 7.
Date Reçue/Date Received 2020-12-11
14
Dans l'unité de transalkylation 8, la fraction comprenant des mono-aromatiques
en C9-C10 25
(et/ou l'effluent d'hydrogénolyse enrichi en composés aromatiques substitués
en méthyles
décrit ci-après) est mélangée à la coupe comprenant du toluène 23 en
provenance de la tête
de la colonne de toluène 5, et alimente la section réactionnelle de l'unité de
transalkylation 8
pour produire des xylènes par transalkylation d'aromatiques en défaut de
groupes méthyles
(toluène), et en excès de groupes méthyles (e.g. tri- et tétra-
méthylbenzènes). Selon un ou
plusieurs modes de réalisation, l'unité de transalkylation 8 est alimentée en
benzène (ligne
non représentée sur la figure 1), par exemple lorsqu'un excès de groupes
méthyles est
observé pour la production de paraxylène.
Selon un ou plusieurs modes de réalisation, l'unité de transalkylation 8
comprend au moins un
premier réacteur de transalkylation adapté pour être utilisé dans au moins une
des conditions
opératoires suivantes :
- température comprise entre 200 C et 600 C, préférentiellement comprise entre
350 C
et 550 C, et plus préférentiellement encore comprise entre 380 C et 500 C;
- pression comprise entre 2 et 10 MPa, préférentiellement comprise entre 2
et 6 MPa, et
plus préférentiellement comprise entre 2 et 4 MPa;
- PPH comprise entre 0,5 et 5 h-1, préférentiellement comprise entre 1 et 4
h-1, et plus
préférentiellement comprise entre 2 et 3 h-1.
Selon un ou plusieurs modes de réalisation, le premier réacteur de
transalkylation est opéré
en présence d'un catalyseur comprenant de la zéolithe, par exemple de la ZSM-
5. Selon un
ou plusieurs modes de réalisation, le deuxième réacteur de transalkylation est
de type lit fixe.
Selon un ou plusieurs modes de réalisation, la section réactionnelle de
transalkylation 14
comprend au moins un deuxième réacteur de transalkylation adapté pour être
utilisé dans au
moins une des conditions opératoires suivantes :
- température comprise entre 200 C et 400 C, préférentiellement comprise
entre 220 C
et 350 C, et plus préférentiellement encore comprise entre 250 C et 310 C;
- pression comprise entre 1 et 6 MPa, préférentiellement comprise entre 2
et 5 MPa, et
plus préférentiellement comprise entre 3 et 5 MPa;
- PPH comprise entre 0,5 et 5 h-1, préférentiellement comprise entre 0,5 et
4 h-1, et plus
préférentiellement comprise entre 0,5 et 3 h-1.
Selon un ou plusieurs modes de réalisation, le deuxième réacteur de
transalkylation est opéré
en présence d'un catalyseur comprenant de la zéolithe, par exemple une
zéolithe Y
Date Reçue/Date Received 2020-12-11
15
désaluminée (par exemple, une zéolithe similaire à celles décrites dans la
partie catalyseur
d'alkylation) Selon un ou plusieurs modes de réalisation, le deuxième réacteur
de
transalkylation est de type lit fixe.
Selon un ou plusieurs modes de réalisation, les effluents de la section
réactionnelle de l'unité
de transalkylation 8 sont séparés dans une première colonne de séparation (non
représentée)
en aval de ladite section réactionnelle de l'unité de transalkylation 8. Une
coupe comprenant
au moins une partie du benzène et les espèces plus volatiles 38 (C6-) est
extraite en tête de
la première colonne de séparation et est envoyée vers une colonne optionnelle
de stabilisation
12, permettant notamment de retirer les espèces plus volatiles (e.g. C5-) du
complexe
aromatique. La fraction lourde des effluents de la première colonne de
séparation comprenant
(e.g. essentiellement) des aromatiques au moins 7 atomes de carbone 21 (A7+),
est
optionnellement recyclée vers le train de fractionnement 4-7, par exemple vers
la colonne de
benzène 4.
La coupe comprenant des xylènes et de l'éthylbenzène 24 est traitée dans
l'unité de séparation
des xylènes 10 pour produire une fraction ou un extrait 39 comprenant du
paraxylène et un
raffinat 40. L'extrait 39 peut être ensuite distillé (e.g. si séparation par
adsorption LMS), par
exemple au moyen d'une colonne d'extrait puis d'une colonne de toluène
supplémentaire (non
montrées) dans le cas où le toluène est utilisé comme désorbant, pour obtenir
du paraxylène
de haute pureté exporté comme produit principal. Le raffinat 40 de l'unité de
séparation des
xylènes 10 comprend (e.g. essentiellement) de l'orthoxylène, du métaxylène et
de
l'éthylbenzène et alimente l'unité d'isomérisation 11.
Selon un ou plusieurs modes de réalisation, l'unité de séparation des xylènes
10 sépare
également une deuxième coupe de toluène 41 comprenant au moins 90% poids,
préférablement au moins 95% poids, très préférablement au moins 99% poids de
toluène. La
coupe de toluène 41 peut être par exemple une partie du toluène utilisé comme
désorbant
lorsque l'unité de séparation des xylènes 10 comprend une unité d'adsorption
dite à lit mobile
simulé. Selon un ou plusieurs modes de réalisation, la deuxième coupe de
toluène 41 est
envoyée vers l'unité de transalkylation 8.
Dans la section réactionnelle d'isomérisation (non représentée) de l'unité
d'isomérisation 11,
les isomères du paraxylène sont isomérisés alors que l'éthylbenzène peut être
: isomérisé en
un mélange de C8 aromatiques, par exemple si on souhaite produire
principalement du
paraxylène; et/ou désalkylé pour produire du benzène, par exemple si on
souhaite produire à
la fois du paraxylene et du benzène. Selon un ou plusieurs modes de
réalisation, les effluents
Date Reçue/Date Received 2020-12-11
16
de la section réactionnelle d'isomérisation sont envoyés vers une deuxième
colonne de
séparation (non représentée) pour produire en fond un isomérat 42 enrichi en
paraxylène
préférablement recyclé vers la colonne de xylène 6; et produire en tête une
coupe
hydrocarbonée comprenant des composés à 7 atomes de carbone ou moins 43 (C7-)
envoyée
vers la colonne optionnelle de stabilisation 12, par exemple avec la coupe
comprenant au
moins une partie du benzène et les espèces plus volatiles 38.
Selon un ou plusieurs modes de réalisation, l'unité d'isomérisation 11
comprend une première
zone d'isomérisation travaillant en phase liquide, et/ou une deuxième zone
d'isomérisation
travaillant en phase gaz, comme cela est décrit dans les brevets précédemment
répertoriés.
Selon un ou plusieurs modes de réalisation, l'unité d'isomérisation 11
comprend une première
zone d'isomérisation travaillant en phase liquide, et une deuxième zone
d'isomérisation
travaillant en phase gaz. Selon un ou plusieurs modes de réalisation, on
envoie dans l'unité
d'isomérisation en phase liquide une première partie du raffinat 40, pour
obtenir un premier
isomérat alimentant directement et au moins en partie l'unité de séparation
10, et on envoie
dans l'unité d'isomérisation en phase gaz une seconde partie du raffinat 40
pour obtenir un
isomérat qui est envoyé dans la colonne de xylène 6. Selon un ou plusieurs
modes de
réalisation, on envoi la coupe d'éthylbenzène 33 majoritairement (i.e., au
moins 50% poids,
e.g. au moins 60% poids, préférablement au moins 70% poids) dans la première
zone
d'isomérisation travaillant en phase gaz pour être préférentiellement
isomérisée en
paraxylène.
Avantageusement, l'unité d'isomérisation 11 permet de pouvoir convertir avec
une très haute
sélectivité le surplus d'éthylbenzène pourvu par la section réactionnelle
d'alkylation 13.
Selon un ou plusieurs modes de réalisation, la zone d'isomérisation en phase
gaz est adaptée
pour être utilisée dans au moins une des conditions opératoires suivantes :
- température supérieure à 300 C, de préférence de 350 C à 480 C;
- pression inférieure à 4,0 MPa, et de préférence de 0,5 à 2,0 MPa ;
- vitesse spatiale horaire inférieure à 10 h-1(10 litres par litre et par
heure), de préférence
comprise entre 0,5 h-1 et 6 h-1;
- rapport molaire hydrogène sur hydrocarbure inférieur à 10, et de
préférence compris
entre 3 et 6;
- en présence d'un catalyseur comportant au moins une zéolithe présentant
des canaux
dont l'ouverture est définie par un anneau à 10 ou 12 atomes d'oxygène (10 MR
ou 12
MR), et au moins un métal du groupe VIII de teneur comprise entre 0,1 et 0,3%
poids
(forme réduite), bornes incluses.
Date Reçue/Date Received 2020-12-11
17
Selon un ou plusieurs modes de réalisation, la zone d'isomérisation en phase
liquide est
adaptée pour être utilisée dans au moins une des conditions opératoires
suivantes :
- température inférieure à 300 C, de préférence 200 C à 260 C;
- pression inférieure à 4 MPa, de préférence 2 à 3 MPa ;
- vitesse spatiale horaire (VVH) inférieure à 10h-1 (10 litres par litre et
par heure), de
préférence comprise entre 2 et 4 h-1;
- en présence d'un catalyseur comportant au moins une zéolithe présentant
des canaux
dont l'ouverture est définie par un anneau à 10 ou 12 atomes d'oxygène (10 MR
ou 12
MR), préférentiellement un catalyseur comportant au moins une zéolithe
présentant des
canaux dont l'ouverture est définie par un anneau à 10 atomes d'oxygène (10
MR), et
de manière encore plus préférée un catalyseur comportant une zéolithe de type
ZSM-5.
Le terme VVH correspond au volume de charge hydrocarbonée horaire injecté
rapporté au
volume de catalyseur chargé.
Selon un ou plusieurs modes de réalisation, la colonne optionnelle de
stabilisation 12 produit :
en fond une coupe stabilisée comprenant (e.g. essentiellement) du benzène et
du toluène 44
optionnellement recyclée en entrée de l'unité de séparation de charge 1 et/ou
de l'unité
d'extraction des aromatiques 3; et en tête une coupe d'espèces plus volatiles
45 (e.g. C5-)
retirée du complexe aromatique.
Selon un ou plusieurs modes de réalisation, l'unité d'hydrogénolyse sélective
9 est adaptée
pour :
- traiter les mono-aromatiques ayant entre 9 et 10 atomes de carbone 25 ; et
- produire un effluent d'hydrogénolyse enrichi en composés aromatiques
substitués en
méthyles 46.
Spécifiquement, l'unité d'hydrogénolyse sélective 9 peut être adaptée pour
traiter les
aromatiques ayant entre 9 et 10 atomes de carbone 25 en transformant un ou
plusieurs
groupe(s) alkyle(s) à au moins deux atomes de carbone (groupes éthyle,
propyle, butyle,
isopropyle, etc..) fixé(s) sur un noyau benzénique, en un ou plusieurs
groupe(s) méthyle(s),
c'est-à-dire formé(s) d'un seule groupe CH3. L'intérêt majeur l'unité
d'hydrogénolyse sélective
9 est d'augmenter la teneur en groupements CH3 et baisser la teneur en
groupements éthyle,
propyle, butyle, isopropyle, etc..., dans la charge de l'unité d'isomérisation
11 pour augmenter
.. le taux de production de xylènes, et notamment de paraxylène, dans ladite
unité
d'isomérisation 11.
Date Reçue/Date Received 2020-12-11
18
Selon un ou plusieurs modes de réalisation, l'unité d'hydrogénolyse sélective
9 comprend au
moins un réacteur d'hydrogénolyse adapté pour être utilisée dans au moins une
des conditions
opératoires suivantes :
- température comprise entre 300 C et 550 C, préférentiellement comprise
entre 350 C
et 500 C, et plus préférentiellement encore comprise entre 370 C et 4500;
- pression comprise entre 0,1 et 3 MPa, préférentiellement comprise entre
0,2 et 2 MPa,
et plus préférentiellement comprise entre 0,2 et 1 MPa;
- rapport molaire H2/HC (charge hydrocarbure) compris entre 1 et 10, et
préférentiellement
compris entre 1,5 et 6 ;
- PPH comprise entre 0,1 et 50 h-1 (e.g. 0,5-50 h-1), préférentiellement
comprise entre 0,5
et 30 h-1 (e.g. 1-30 h-1), et plus préférentiellement comprise entre 1 et 20 h-
1 (e.g. 2-20 h-
1, 5-20 h-1).
Selon un ou plusieurs modes de réalisation, le réacteur d'hydrogénolyse est
opéré en
présence d'un catalyseur comportant au moins un métal du groupe VIII de la
classification
périodique, de préférence le nickel et/ou cobalt, déposé sur un support poreux
comprenant au
moins un oxyde réfractaire cristallin ou non, à porosité structurée ou non.
Selon un ou plusieurs
modes de réalisation, le métal du groupe VIII est le nickel. La présence d'un
promoteur
(Groupe VIB VIIB VIII IB IIB) est également possible. Le catalyseur est
supporté sur un oxyde
réfractaire (e.g. alumine, silice), éventuellement traité par une base pour le
neutraliser.
Selon un ou plusieurs modes de réalisation, le réacteur d'hydrogénolyse est de
type lit fixe, et
le support de catalyseur se présente sous la forme d'extrudés. Selon un ou
plusieurs modes
de réalisation, le réacteur d'hydrogénolyse est de type lit mobile, et le
support de catalyseur
se présente sous la forme de billes approximativement sphériques. Un lit
mobile peut être
défini comme étant un lit à écoulement gravitaire, tels que ceux rencontrés
dans le reformage
catalytique des essences.
La figure 2 représente une vue schématique d'un procédé selon la présente
invention
permettant d'augmenter la production de paraxylène dans lequel la section
réactionnelle de
transalkylation 14 est disposée en aval de l'unité de fractionnement 15. Selon
un ou plusieurs
modes de réalisation, l'effluent d'alkylation 31 est séparé dans l'unité de
fractionnement 15
pour produire la coupe d'éthylbenzène 33, la coupe aqueuse 34 comprenant de
l'eau et
optionnellement de l'éthanol, la coupe de benzène 35 qui pourra par exemple
être recyclée au
moins en partie vers la section réactionnelle d'alkylation 13 et/ou la section
réactionnelle de
transalkylation 14, éventuellement une ou plusieurs coupes de
polyéthylbenzènes 36 et 37, et
Date Reçue/Date Received 2020-12-11
19
éventuellement des oligomères formés à partir de l'éthanol. La coupe
d'éthylbenzène 33
alimente l'unité d'isomérisation 11.
Toujours en référence à la figure 2, selon un ou plusieurs modes de
réalisation, au moins une
portion de la première coupe de polyéthylbenzènes 36 est envoyée vers la
section
réactionnelle de transalkylation 14 pour produire une coupe enrichie en
éthylbenzène 47
renvoyée vers l'unité de fractionnement 15. Selon un ou plusieurs modes de
réalisation, la
zone de transalkylation 14 est au moins en partie alimentée par au moins une
portion de la
coupe de benzène 35 venant de la section de fractionnement 15.
Le dispositif et le procédé de conversion de composés aromatiques décrit ci-
dessus
comprennent une unité de transalkylation 8 permettant de convertir en xylènes
du toluène
et/ou du benzène avec des méthylbenzènes. Il est entendu que le dispositif et
le procédé de
conversion de composés aromatiques peuvent comprendre une unité de dismutation
en
combinaison ou en remplacement de l'unité de transalkylation 8, l'unité de
dismutation
permettant de convertit du toluène en benzène et xylène. Par exemple, en
référence à la figure
2, lorsque une unité de dismutation 48 est utilisée à la place de l'unité de
transalkylation 8,
l'effluent de fond 29 de la colonne de xylène 6 peut être évacué du complexe
aromatique
(suppression de la colonne des aromatiques lourds 7 et de l'unité
d'hydrogénolyse sélective 9
présentes dans la figure 1).
Selon un ou plusieurs modes de réalisation, les effluents de la section
réactionnelle de l'unité
de dismutation 48 sont séparés dans une troisième colonne de séparation (non
représentée)
en aval de ladite section réactionnelle de l'unité de dismutation 48 pour
produire : une coupe
enrichie en xylènes (50) préférablement recyclée vers l'unité d'isomérisation
11 ; et produire
une coupe de benzène et de toluène 49 envoyée préférablement vers la colonne
de benzène
4.
En référence aux figures 1 et 2, le dispositif et le procédé de conversion de
composés
aromatiques décrits ci-dessus sont adaptés pour envoyer la première coupe de
toluène 18
vers la colonne de benzène 4, et/ou la colonne de toluène 5 et envoyer la
deuxième coupe de
toluène 41 vers l'unité de transalkylation 8 ou l'unité de dismutation 48. Il
est entendu que le
dispositif et le procédé de conversion de composés aromatiques peuvent être
adaptés pour
envoyer la première coupe de toluène 18 vers l'unité de transalkylation 8 ou
l'unité de
dismutation 48 et/ou envoyer la deuxième coupe de toluène 41 vers la colonne
de benzène 4,
et/ou la colonne de toluène 5.
Date Reçue/Date Received 2020-12-11
20
Le dispositif et le procédé selon l'invention permettent ainsi d'obtenir des
gains allant jusqu'à
100% en paraxylène quand la totalité du benzène est alkyle par l'éthanol.
Dans la présente demande, les groupes d'éléments chimiques sont donnés par
défaut selon
la classification CAS (CRC Hand book of Chemistry and Physics, éditeur CRC
press, rédacteur
en chef D.R. Lide, 81ème édition, 2000-2001). Par exemple, le groupe VIII
selon la
classification CAS correspond aux métaux des colonnes 8, 9 et 10 selon la
nouvelle
classification IUPAC ; le groupe Vlb selon la classification CAS correspond
aux métaux de la
colonne 6 selon la nouvelle classification IUPAC.
Exemples
Exemple de dispositif de référence
On utilise un exemple de dispositif de référence de transformation d'une
charge comprenant
un mélange de composés aromatiques issus d'un procédé de conversion de la
biomasse
lignocellulosique à base d'une conversion par pyrolyse catalytique.
L'exemple de dispositif de référence est similaire au dispositif représenté
sur la figure 1 à la
différence que l'unité de transalkylation 8 est remplacée par une unité de
dismutation 48. De
plus, l'exemple de dispositif de référence ne met pas en oeuvre les unités
suivantes :
- colonne des aromatiques lourds 7;
- unité d'hydrogénolyse sélective 9;
- colonne de stabilisation 12;
- section réactionnelle d'alkylation 13;
- section réactionnelle de transalkylation 14 ; et
- unité de fractionnement 15.
Les débits desdits composés aromatiques de la charge à traiter, en entrée du
dispositif de
référence sont les suivants :
- benzène : 2,63 t/h ;
- toluène : 5,64 t/h;
- éthylbenzène : 0,15 t/h ; et
- xylènes : 3,56 t/h.
Soit un total de 11,98 t/h de composés aromatiques.
Date Reçue/Date Received 2020-12-11
21
Dans le dispositif de référence, la totalité du toluène est converti, par une
unité de dismutation
en benzène et xylènes. Les xylènes de la charge et produits par dismutation
sont isomérisés
en paraxylène, lequel est séparé du mélange de xylènes à l'équilibre
thermodynamique à la
sortie de l'unité d'isomérisation, au moyen d'une unité d'adsorption en lit
mobile simulé. Cet
ensemble d'opérations unitaires permet, dans le meilleur des cas (dans
l'hypothèse d'une
sélectivité de 100% pour chaque opération unitaire) de produire les composés
suivants :
- benzène : 5,02 t/h ;
- paraxylène: 6,96 t/h
- total aromatique : 11,98 t/h.
Exemple de dispositif selon l'invention
L'exemple de dispositif selon l'invention permet d'augmenter à la fois la
quantité totale
d'aromatiques produite pour le même débit de charge que dans le dispositif de
référence et
de ne produire que le composé à plus haute valeur ajoutée : le paraxylène.
L'exemple de dispositif selon l'invention est similaire au dispositif
représenté sur la figure 1 à
la différence que l'unité de transalkylation 8 est remplacée par une unité de
dismutation 48.
De plus, l'exemple de dispositif selon l'invention ne met pas en oeuvre les
unités suivantes :
- colonne des aromatiques lourds 7;
- unité d'hydrogénolyse sélective 9; et
- colonne de stabilisation 12.
Par rapport au schéma de dispositif de référence, sont notamment ajoutés la
section
réactionnelle d'alkylation 13 et la section réactionnelle de transalkylation
14 pour alkyler le
benzène par de l'éthanol et transalkyler les polyéthylbenzènes en
éthylbenzènes. Le produit
issu de la transalkylation 14, c'est-à-dire l'éthylbenzène est introduit dans
la boucle aromatique
comprenant l'unité d'isomérisation 11 mise en oeuvre avec un réacteur
d'isomérisation en
phase liquide et un réacteur d'isomérisation en phase gaz, et l'unité de
séparation des xylènes
10.
Selon l'exemple de dispositif selon l'invention, et avec la même charge en
entrée du complexe
et les mêmes rendements des opérations unitaires que dans l'exemple de
dispositif de
référence, on obtient sur la table 1 les performances suivantes comparées à
celles du dispositif
de référence.
[Table 1]
Date Reçue/Date Received 2020-12-11
22
Exemple de dispositif Exemple de dispositif
de référence selon l'invention
Charge (t/h) - -
Et0H 0 2,95
Benzène 2,63 2,63
Toluène 5,64 5,64
Ethylbenzène 0,15 0,15
Xylènes 3,56 3,56
Produits (tlh) - -
Benzène 5,02 0
p-xylène 6,96 13,78
Ethylbenzène 0 0
H20 0 1,15
Total 11,98 13,78
aromatiques
La table 1 montre que la mise en oeuvre selon l'invention permet de produire
15% poids de
plus d'aromatiques (13,78 t/h au lieu de 11,98 t/h) et de ne produire que du
paraxylène avec
une augmentation de production de paraxylène de presque 100%.
Date Reçue/Date Received 2020-12-11