Note: Descriptions are shown in the official language in which they were submitted.
CA 03121693 2021-06-01
1
AMPHIPOLS
[0001] L'invention concerne de nouveaux polymères amphiphiles appelés
amphipols .
[0002] Ces
polymères amphipatiques sont connus dans l'état de l'art pour permettre la
stabilisation des protéines membranaires en solution aqueuse une fois celles-
ci
extraites des membranes via l'utilisation de détergents.
[0003] Les
protéines membranaires représentent environ 30% des protéines codées
par le génome des cellules et sont impliquées dans de nombreuses fonctions
cellulaires importantes (signalisation, sécrétion, migration, adhérence,
homéostasie,
production d'énergie, etc). Les protéines membranaires peuvent être
monomériques
ou oligomériques. De par leur intégration dans les membranes, elles sont
fortement
structurées en hélices oc ou feuillets p pour les parties transmembranaires
interagissant
avec les chaînes alkyles des lipides membranaires.
[0004] Les
nombreuses fonctions et activités enzymatiques qu'elles assument en font
des cibles pharmacologiques ou des outils biotechnologiques de choix.
Cependant,
leur étude fonctionnelle et structurale en solution et leur utilisation dans
le
développement d'outils thérapeutiques ou biotechnologiques impliquent leur
production en quantité importante, leur purification et leur maintien dans une
conformation active or celles-ci sont le plus souvent instables une fois
extraites de la
membrane. Cette instabilité en solution aqueuse est notamment due à
l'utilisation
obligatoire de tensioactifs pour empêcher leur agrégation. En effet, la
surface des
domaines extra membranaires de ces protéines est principalement recouverte
d'acides
aminés à chaînes latérales hydrophiles tandis que la surface de leur domaine
transmembranaire est recouverte d'acides aminés à chaînes hydrophobes ; les
protéines membranaires sont donc hautement insolubles dans l'eau en raison de
l'effet
hydrophobe qui les pousse à s'agréger en solution afin de minimiser les
perturbations
du réseau de liaisons hydrogène entre les molécules d'eau.
[0005] II
existe de nombreuses stratégies pour produire les protéines membranaires
en quantité suffisante ainsi qu'un grand choix de molécules chimiques
permettant leur
purification (les rendements étant souvent limités), solubilisation et
stabilisation en
solution aqueuse.
[0006] Les
détergents disponibles sur le marché permettent de solubiliser les protéines
mais provoquent, comme mentionné, leur dénaturation et inactivation plus ou
moins
rapides notamment du fait du pouvoir dissociant des détergents ; en outre il
est
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
2
nécessaire de maintenir ceux-ci en solution à des concentrations au-dessus de
leur
concentration micellaire critique (CMC). D'un autre côté, les tensioactifs
tels que les
amphipols (WO 98/27434) permettent de stabiliser les protéines mais offrent
des
propriétés de solubilisation beaucoup plus faibles. Les amphipols sont des
polymères
amphiphiles définis comme étant capables de maintenir les protéines
membranaires
dans leur conformation native, soluble, sous la forme de petits complexes
(Zoonens &
Popot, 2014). L'amphipol le plus communément utilisé et étudié est l'A8-35. Il
est
constitué d'un squelette d'acide polyacrylique sur lequel sont greffées des
chaînes
latérales d'octylamine et d'isopropylamine : 35% de groupes acides
carboxyliques non
greffés, 25% de dérivés carboxyliques greffés avec des chaînes octyle
(octylamine) et
40% de groupes carboxyliques greffés avec des groupes isopropyliques
(isopropylamine). Les amphipols de type A8-35 nécessitent généralement la
solubilisation préalable des membranes en utilisant un détergent,
subséquemment
remplacé par l'amphipol au moyen de la dilution du détergent sous sa CMC (ce
qui a
le désavantage de diluer également les protéines) ou de son adsorption sur des
billes.
D'autres polymères amphiphiles ont été développés. Parmi ceux-ci on peut noter
les
SMAs (pour Styrene Maleic Acid copolymers, W02011004158) et leurs dérivés qui
présenteraient la particularité de pouvoir solubiliser les protéines
membranaires
directement à partir des fractions membranaires, sans la solubilisation
préalable au
moyen d'un détergent. Cependant les SMAs, au contraire des amphipols qui se
purifient simplement à l'issue de leur synthèse, présentent toujours des
impuretés qui
préemptent l'utilisation ultérieure des protéines pour des applications
biotechnologiques.
[0007] Les
stratégies de purification des protéines et notamment des protéines
membranaires, recombinantes ou non, sont généralement empiriques et
difficilement
prédictibles, dépendant notamment de la protéine, du (micro)organisme ou
encore de
la composition de la membrane ; il est généralement procédé à des essais
successifs
de différents agents pour solubiliser et/ ou stabiliser les protéines
membranaires, afin
d'identifier l'agent le plus efficace dans ces conditions.
[0008] Dans ce
contexte, la fourniture de nouveau outils alternatifs pour la production
des protéines membranaires d'un haut intérêt biotechnologique est désirable.
Notamment, des polymères possédant à la fois des propriétés de solubilisation
et de
stabilisation des protéines membranaires seraient particulièrement avantageux
et
n'existent pas à l'heure actuelle. Les nouveaux Amphipols objets de
l'invention
répondent à ce besoin.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
3
RESUME
[0009] L'invention a donc pour but de fournir de nouveaux composés
pour permettre
la solubilisation et la stabilisation de protéines membranaires. Plus
particulièrement
l'invention concerne des nouveaux amphipols, polymères vinyliques amphiphiles
ayant
des propriétés de solubilisation améliorées tout en permettant une
stabilisation
satisfaisante des protéines membranaires.
[0010] A cet effet, l'invention porte sur des polymères vinyliques
amphiphiles de
formule I,
Ri R5 R8
I 4
1¨CH¨CH4 CH CH [ CH CH _______________
CH¨CH
w
R4 -1-X
y ;
R2
MO 'O R6 C R5
N ====;:,0
0 4' 0
X X Rio
R3==%.,
R7
Formule I
dans laquelle :
NI+ est un métal alcalin, de préférence sélectionné parmi Lit, Na, KE,
Ri, R4, R5, R8 sont, chacun indépendamment, l'atome d'hydrogène ou le radical
méthyle,
R2, R6, R9 sont, chacun indépendamment, un groupe sélectionné parmi l'atome
d'hydrogène et les (C1-C8) alkyles linéaires ou ramifiés,
Rio est un groupe sélectionné parmi les (C1-05) alkyles linéaires ou ramifiés,
R3 et R7 sont, chacun indépendamment, un groupe sélectionné parmi :
- l'hydrogène, X étant alors une simple liaison
- les alkyles linéaires ou ramifiés d'au moins 6 atomes de carbone, les
alcényles linéaires ou ramifiés d'au moins 6 atomes de carbone, ou les
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
4
alcynyles linéaires ou ramifiés d'au moins 6 atomes de carbone, X étant
alors une simple liaison,
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C1-C8)
alcényles linéaires ou ramifiés et les (C1-08) alcynyles linéaires ou
ramifiés,
- les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro) cycloalcényles, poly
ou monoinsaturés, substitués ou non par un ou des radicaux sélectionnés
parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés , X étant alors
une simple liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou
ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8)
alcynylènes linéaires ou ramifiés,
- des polycycles poly ou monoinsaturés, substitués ou non par un ou des
radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou
ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles
linéaires ou ramifiés, X étant alors une simple liaison ou sélectionné parmi
les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8) alcénylènes linéaires
ou ramifiés et les (C2-C8) alcynylènes linéaires ou ramifiés,
- un phényle, substitué ou non par un ou des radicaux
sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés , X une simple liaison
ou étant alors sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés,
(C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires ou ramifiés,
étant entendu que lorsque que l'un des groupes R3 OU R7 est un alkyle linéaire
ou
ramifié d'au moins 6 atomes de carbone, un alcényle linéaire ou ramifié d'au
moins 6
atomes de carbone, ou un alcynyle linéaire ou ramifié d'au moins 6 atomes de
carbone,
ou un atome d'hydrogène, X étant alors une simple liaison, alors, l'autre
groupe R3 OU
R7 est sélectionné parmi :
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
C8) alcynyles linéaires ou ramifiés , X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8)
alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
5 - les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro)
cycloalcényles, poly
ou monoinsaturés, substitués ou non par un ou des radicaux sélectionnés
parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés , X étant alors
une simple liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou
ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8)
alcynylènes linéaires ou ramifiés,
- des polycycles poly ou monoinsaturés, substitués ou non par un ou des
radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou
ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles
linéaires ou ramifiés, X étant alors une simple liaison ou sélectionné parmi
les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8) alcénylènes linéaires
ou ramifiés et les (C2-C8) alcynylènes linéaires ou ramifiés, et
- un phényle, substitué ou non par un ou des radicaux
sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors une simple
liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés,
(C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires ou ramifiés,
w, x, y, z correspondant aux pourcentages respectifs des motifs,
- x étant compris entre 20 et 90 %,
- y étant compris entre 0 et 80 %,
- w étant compris entre 0 et 80%, et
- z étant compris entre 0 et 60 %, étant entendu que
w+x+y+z=100 % et que
y ou w est au moins égal à 10%.
Selon une caractéristique optionnelle le polymère vinylique amphiphile de
formule I est
tel que w=0 et R7 est un groupement sélectionné parmi :
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
6
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
C8) alcynyles linéaires ou ramifiés, ou
- - un phényle, substitué ou non par un ou des radicaux sélectionnés parmi
les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés,
X étant alors une simple liaison ou sélectionné parmi les (C1-C8) alkylènes
linéaires
ou ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8)
alcynylènes
linéaires ou ramifiés.
[0011] Selon d'autres caractéristiques optionnelles le polymère
vinylique amphiphile
de formule I est tel que:
- R3 et/ou R7 sont des (C6-C8) cycloalkyles tels que
précédemment spécifiés,
ou
- R3 et/ou R7 sont un phényle, préférentiellement ledit
phényle est substitué
en para par un groupe méthyle ou éthyle,
X étant une simple liaison, ou sélectionné parmi les (C1-C8) alkylènes
linéaires ou
ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires
ou ramifiés.
[0012] Selon d'autres caractéristiques optionnelles le polymère
vinylique amphiphile
de formule I est tel que:
- R3 et/ou R7 sont des (C6-C8) cycloalkyles tels que précédemment spécifiés,
X étant préférentiellement une simple liaison ou CH2,
- R3 et/ou R7 sont un phényle, préférentiellement ledit
phényle est substitué
en para par un groupe méthyle ou éthyle, X étant une simple liaison, ou
- R3 et/ou R7 sont un groupe styrényle. X étant une simple
liaison.
[0013] Selon d'autres caractéristiques optionnelles, le polymère vinylique
amphiphile
de formule I est tel que:
- le métal M est Na+,
- R10 est un groupe isopropyle,
- x est inférieur ou égal à 75%,
- w et/ou y est supérieur ou égal 25%,
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
7
- w et/ou y est compris entre 25 % et 50 % et z est compris
entre 0 % et 40
%, préférentiellement entre 15 % et 40%, ou
- il est fonctionnalisé par greffage de tag d'affinité, de
sonde fluorescente ou
de molécule immunostimulatrice.
[0014] Selon une autre caractéristique optionnelle, le polymère vinylique
de formule I
est tel que:
- R1, R2, R4, R5, R6, R8, R6 sont l'atome d'hydrogène,
- R3 et/ou R7 est un (Co-Co) cycloalkyle et X est une simple
liaison,
- Rio est un groupe isopropyle,
- x est égal à 35% ou 50%,
- y est supérieur ou égal à 25 %,
- w est égal à 0%, ou 25%, et
- z est égal à 0%, 15% ou 40%, étant entendu que w+x+y+z=100
%.
[0015] Selon une autre caractéristique optionnelle, le polymère
vinylique de formule I
est sélectionné parmi les composés listés dans le tableau I.
[0016] Les polymères vinyliques de l'invention sont des amphipols,
c'est à dire qu'ils
sont capables de maintenir solubles les protéines membranaires dans leur
conformation native, sous la forme de petits complexes. Ainsi, dans un autre
de ses
aspects, l'invention concerne donc le complexe hydrosoluble formé par i) une
protéine
membranaire ou bien un mélange de protéines membranaires et ii) au moins un
composé, polymère vinylique amphiphile, tel que décrit ci-dessus.
[0017] Selon une caractéristique optionnelle le complexe hydrosoluble
ainsi formé est
tel qu'il comprend en outre des composés lipidiques.
[0018] En outre les polymères de l'invention permettent de stabiliser
les protéines
membranaires en solution aqueuse. Ainsi un objet de l'invention est le
complexe
hydrosoluble formé par i) une protéine membranaire ou bien un mélange de
protéines
membranaires et ii) au moins un composé, polymère vinylique amphiphile de
l'invention
au sein duquel les protéines membranaires sont stabilisées en solution
aqueuse. Un
autre objet de l'invention est donc une solution comprenant un tel complexe.
[0019] L'invention porte également sur un procédé de préparation d'une
solution
aqueuse de protéine(s) membranaire(s), ledit procédé comprenant une étape de
solubilisation et/ou stabilisation dans laquelle la fraction protéique
provenant d'une
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
8
membrane biologique ou synthétique contenant ladite protéine membranaire, ou
ledit
mélange de protéines membranaires, est mis en présence du polymère vinylique
tel
que décrit ci-dessus.
[0020] Selon des caractéristiques optionnelles, ce procédé est tel
que:
- la ou les
protéines membranaires sont des protéines recombinantes exprimées
dans des cellules procaryotes ou eucaryotes, et/ou des protéines natives
exprimées dans des membranes spécialisées à haute densité protéique,
- une étape de solubilisation de ladite protéine membranaire ou dudit
mélange de
protéines membranaires est préalablement réalisée au moyen d'un milieu
détergent,
- une étape de fusion de la fraction de protéique contenant ladite protéine
membranaire, ou ledit mélange de protéines membranaires, est préalablement
réalisée au moyen de vésicules de phospholipides ou de mélange de
phospholipides, de préférence de 1,2-Dimyristoyl-sn-glycero-3-phosphocholine
(DMPC), ou
- la solution de fraction protéique contenant ladite protéine membranaire
n'est pas
une solution de protéine(s) membranaire(s) en milieu détergent sous forme
micellaire.
[0021] Les
complexes de l'invention protéine(s) membranaire(s)-amphipols de
l'invention en permettant la solubilisation et la stabilisation de ces
protéines sous leur
forme native, permettent les applications biotechnologiques de ces protéines.
Ainsi, un
objet de la présente invention est également l'utilisation des complexes de
l'invention
comme réactifs dans des kits de réactifs, et notamment un kit de diagnostic
comprenant
au moins un complexe de l'invention à titre de réactif immunologique.
Également, les
complexes de l'invention peuvent être fixés sur un dispositif faisant usage de
l'activité
de ladite protéine membranaire ainsi purifiée et solubilisée par les amphipols
de
l'invention à des fins de diagnostic ou de mesure d'activité.
[0022]
D'autres avantages et caractéristiques de l'invention apparaitront à la
lecture
de la description suivante donnée à titre d'exemple illustratif et non
limitatif, en
référence aux figures annexées qui représentent :
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
9
- Figure 1 : Analyse par chromatographie d'exclusion stérique des particules
formées
par les amphipols de l'invention, l'A8-35, ainsi que de leur complexe avec la
bactériorhodopsine (BR). Vo=volume mort ; Vr=volume total.
-
Figure 2: Complexation de la BR avec des amphipols selon l'invention, avant
(barres
noires) ou après centrifugation (barres grises).
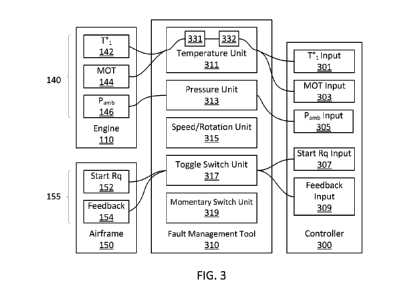
- Figure 3: Dénaturation thermique de la BR dans différents
environnements.
- Figure 4: Solubilisation de la membrane pourpre de Halobacterium salinarum
avant
(A) ou après (B) fusion avec des vésicules de DMPC avec l'A8-35, les SMAs ou
des
amphipols de l'invention.
- Figure 5: Quantification de la BR extraite de la membrane pourpre,
préalablement
fusionnée aux vésicules de DMPC, par l'A8-35, les SMAs, ou de polymères de
l'invention (A) et analyse de la stabilité thermique de ces complexes après 6
heures
d'incubation à 50 C (B). Les ratios des valeurs d'absorbance mesurées au début
et à
la fin de chaque expérience sont reportés.
- Figure 6: Extraction de la membrane pourpre. (A) Quantification de la
solubilisation
(barres grises) et stabilité thermique (barres noires) de la BR de la membrane
pourpre,
préalablement fusionnée aux vésicules de DMPC, par l'A8-35, les SMAs, ou de
polymères de l'invention chaque condition réalisée au moins en triplicat
valeurs +/-
SD ; (B). Cinétique de déstabilisation thermique des complexes formés avec les
SMAs
ou les polymères 19 et 23 sur 6 heures d'incubation à 50 C. Les valeurs
d'absorbance
mesurées à 554 nm ont été normalisées avec celles mesurées avant incubation
des
échantillons.
- Figure 7: Cinétique de solubilisation de la protéine YidC-GFP surexprimée
dans la
membrane plasmique d'Escherichia coli en présence de SMAs, de polymères de
l'invention ou de DDM. (A) Photographies des gels d'électrophorèse révélant la
fluorescence de la GFP fusionnée à la protéine membranaire YidC et (B)
représentation graphique de la quantification de la fluorescence à partir de
l'image des
gels en prenant comme référence la fluorescence mesurée en présence de DDM
après
1 heure d'incubation.
- Figure 8 : Solubilisation des membranes riches en AChR de Torpedo marmorata
avec
l'A8-35, les SMAs et des amphipols de l'invention. Les échantillons
correspondant aux
surnageants (S) et culots (C) de chaque condition ont été déposés sur gel
d'acrylamide,
qui après migration a été coloré au bleu de Coomassie. Les flèches indiquent
l'emplacement des bandes correspondant aux sous-unités de AchR et à la Na /K-E
ATPase de Torpedo marmorata. Les protéines présentent dans les culots ne sont
pas
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
solubilisées, les protéines dans le surnageant correspondent aux protéines
solubilisées.
5 DESCRIPTION DE L'INVENTION ET AUTRES MODES DE REALISATION
[0023] L'invention concerne de nouveaux amphipols qui permettent la
solubilisation et
la stabilisation de protéines membranaires en milieu aqueux. Notamment les
nouveaux
amphipols de l'invention ont des propriétés de solubilisation et/ou de
stabilisation
améliorées par rapport aux polymères de référence utilisés pour solubiliser
les
10 protéines membranaires. Les complexes ainsi formés avec les protéines
membranaires sont particulièrement adaptés pour les applications
biotechnologiques
et l'étude de ces protéines membranaires.
[0024] Dans la suite de la description, l'expression amphipol
désigne des
polymères vinyliques capables de maintenir solubles les protéines membranaires
dans
leur conformation native, sous la forme de petits complexes.
[0025] L'expression vinylique englobe dans sa signification
générale les
polymères acryliques.
[0026] L'expression protéine membranaire est indifféremment
utilisée au singulier
ou au pluriel, elle englobe les mélanges de protéines membranaires ou bien des
préparations comprenant substantiellement un seul type de protéine. Au sens de
l'invention une protéine membranaire est une protéine traversant de part et
d'autre la
membrane, elle comprend alors au moins un domaine transmembranaire ou bien une
protéine comprenant au moins un domaine hydrophobe interagissant avec la
membrane. La protéine membranaire peut être monomérique ou bien oligomérique,
associée ou non à des cofacteurs.
[0027] Au sens de l'invention, une protéine membranaire stabilisée
correspond à
une protéine membranaire solubilisée conservant une conformation native et, de
préférence, au moins une part de son activité biologique, même si celle-ci
peut être
transitoirement bloquée.
[0028] L'expression membranes spécialisées englobe, au sens de
l'invention, les
membranes des organelles eucaryotes telles que, par exemple, les crêtes des
mitochondries, les thylakoïdes des chloroplastes, le réticulum endoplasmique
ou
sarcoplasmique ; membrane spécialisée englobe également des membranes à
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
11
haute densité protéique comprenant au moins 50% de protéines membranaires,
intégrales ou non, voire au moins 60% ou encore au moins 70% de protéines
membranaires, telle que, par exemple, la membrane pourpre de la bactérie
Halobacterium salinarum (qui peut comprendre jusque 75% de
bactériorhodopsine), le
reste comprenant des lipides ou autres molécules.
[0029] L'expression membrane biologique s'entend, au sens de
l'invention, de
toute membrane lipidique extraite ou provenant d'une cellule ou d'un organisme
tels
que bactérie, champignon, cellules eucaryotes etc. L'expression membrane
biologique synthétique désigne toute membrane lipidique reconstituée,
recomposée
ou modifiée avec des lipides de synthèse ou d'origine naturelle. Ainsi, par
exemple et
de manière non limitative, une membrane synthétique peut correspondre à une
membrane lipidique extraite d'un organisme à laquelle on adjoint un ou des
lipides
synthétiques, une membrane fabriquée à partir de lipides synthétiques ou une
membrane lipidique reconstituée à partir de lipides naturels et ou
synthétiques
mélangés à dessein.
[0030] L'expression fraction protéique comprend, au sens de
l'invention, la fraction
cellulaire contenant la protéine membranaire recherchée ou analysée. Ainsi il
peut
s'agir d'homogénat cellulaire plus ou moins clarifié et/ou purifié. S'agissant
de
protéines membranaires, l'expression fraction protéique désigne notamment
une
fraction de cet homogénat comme la fraction membranaire ou bien la fraction
correspondant à un compartiment cellulaire.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
12
[0031] L'invention concerne donc un polymère vinylique amphiphile de
formule I:
R5 R8
ii 4
1-CH-CH4w __________________ CH CH [ CH CH ________ CH-CH
R4 -I- I
X
y ;
R2 N-C
0
R5
N0
le0 0 " 0
X X R10
R3 ==%,
R7
Formule I
dans laquelle :
M+ est un métal alcalin, de préférence sélectionné parmi Lit, Na, K+,
R1, R4, R5, R8 sont, chacun indépendamment, l'atome d'hydrogène ou le radical
méthyle,
R2, R6, R9 sont, chacun indépendamment, un groupe sélectionné parmi l'atome
d'hydrogène
et les (C1-C8) alkyles linéaires ou ramifiés,
R10 est un groupe sélectionné parmi les (C1-05) alkyles linéaires ou ramifiés,
R3 et R7 sont, chacun indépendamment, un groupe sélectionné parmi :
- l'hydrogène, X étant alors une simple liaison
- les alkyles linéaires ou ramifiés d'au moins 6 atomes de carbone, les
alcényles linéaires ou ramifiés d'au moins 6 atomes de carbone, ou les
alcynyles linéaires ou ramifiés d'au moins 6 atomes de carbone, X étant
alors une simple liaison,
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8)
alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
13
- les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro) cycloalcényles, poly
ou monoinsaturés, substitués ou non par un ou des radicaux sélectionnés
parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors
une simple liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou
ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8)
alcynylènes linéaires ou ramifiés,
- les polycycles poly ou monoinsaturés, substitués ou non par un ou des
radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou
ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles
linéaires ou ramifiés, X étant alors une simple liaison ou sélectionné parmi
les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8) alcénylènes linéaires
ou ramifiés et les (C2-C8) alcynylènes linéaires ou ramifiés, ou
- un phényle, substitué ou non par un ou des radicaux
sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors une simple
liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés,
(C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires ou ramifiés,
étant entendu que lorsque l'un des groupes R3 OU R7 est un alkyle linéaire ou
ramifié d'au
moins 6 atomes de carbone, un alcényle linéaire ou ramifié d'au moins 6 atomes
de carbone,
ou un alcynyle linéaire ou ramifié d'au moins 6 atomes de carbone, ou un atome
d'hydrogène,
X étant une simple liaison, alors, l'autre groupe R3 OU R7 est sélectionné
parmi :
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8)
alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
- les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro) cycloalcényles, poly
ou monoinsaturés, substitués ou non par un ou des radicaux sélectionnés
parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors
une simple liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
14
ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8)
alcynylènes linéaires ou ramifiés,
- des polycycles poly ou monoinsaturés, substitués ou non par un ou des
radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou
ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles
linéaires ou ramifiés, X étant alors une simple liaison ou sélectionné parmi
les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8) alcénylènes linéaires
ou ramifiés et les (C2-C8) alcynylènes linéaires ou ramifiés, ou
- un phényle, substitué ou non par un ou des radicaux
sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors une simple
liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés,
(C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires ou ramifiés,
w, x, y, z correspondant aux pourcentages respectifs des motifs,
- x étant compris entre 20 et 90 %,
- y étant compris entre 0 et 80 %,
- w étant compris entre 0 et 80%, et
- z étant compris entre 0 et 60 %, étant entendu que
w+x+y+z=100 % et que
y ou w est au moins égal à 10%.
[0032] II découle de manière évidente de la définition du paragraphe
précédent que,
lorsque l'un des groupes R3 OU R7 est un alkyle linéaire ou ramifié d'au moins
6 atomes de
carbone, un alcényle linéaire ou ramifié d'au moins 6 atomes de carbone, ou un
alcynyle
linéaire ou ramifié d'au moins 6 atomes de carbone, ou un atome d'hydrogène, X
étant une
simple liaison, alors, l'autre groupe R3 OU R7 étant tel que spécifié et
défini ci-dessus, alors w
et y sont différents de 0.
[0033] Dans un mode de réalisation particulier, le polymère de formule
I est tel que:
M+ est un métal alcalin, de préférence sélectionné parmi Li+, Na+, K+,
R1, R4, R5, R8 sont, chacun indépendamment, l'atome d'hydrogène ou le radical
méthyle,
R2, R6, R9 sont, chacun indépendamment, un groupe sélectionné parmi l'atome
d'hydrogène
et les (C1-C8) alkyles linéaires ou ramifiés,
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
Rio est un groupe sélectionné parmi les (C1-05) alkyles linéaires ou ramifiés,
R3 et/ou R7 sont, chacun indépendamment, un groupe sélectionné parmi :
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
5 cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou
ramifiés et les (C1-
C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8)
alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
10 - les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro)
cycloalcényles, poly
ou monoinsaturés, substitués ou non par un ou des radicaux sélectionnés
parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés , X étant alors
une simple liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou
15 ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-
C8)
alcynylènes linéaires ou ramifiés,
- des polycycles poly ou monoinsaturés, substitués ou non par un ou des
radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou
ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles
linéaires ou ramifiés, X étant alors une simple liaison ou sélectionné parmi
les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8) alcénylènes linéaires
ou ramifiés et les (C2-C8) alcynylènes linéaires ou ramifiés,
- un phényle, substitué ou non par un ou des radicaux
sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X une simple liaison ou
étant alors sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés,
(C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires ou ramifiés,
w, x, y, z correspondant aux pourcentages respectifs des motifs,
- x étant compris entre 20 et 90 %,
- y étant compris entre 0 et 80 %,
- w étant compris entre 0 et 80%, et
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
16
- z
étant compris entre 0 et 60 %, étant entendu que w+x+y+z=100 % et que
y ou w est au moins égal à 10%.
[0034] Dans un mode de réalisation particulier, le polymère de formule
I est tel que:
M+ est un métal alcalin, de préférence sélectionné parmi Lit, Na, K ,
Ri, Ra, R5, Rs sont, chacun indépendamment, l'atome d'hydrogène ou le radical
méthyle,
R2, R6, R9 sont, chacun indépendamment, un groupe sélectionné parmi l'atome
d'hydrogène
et les (C1-C8) alkyles linéaires ou ramifiés,
Rio est un groupe sélectionné parmi les (C1-05) alkyles linéaires ou ramifiés,
R3 et R7 sont, chacun indépendamment, un groupe sélectionné parmi :
- l'hydrogène, X étant alors une simple liaison
- les alkyles linéaires ou ramifiés d'au moins 6 atomes de carbone, les
alcényles linéaires ou ramifiés d'au moins 6 atomes de carbone, ou les
alcynyles linéaires ou ramifiés d'au moins 6 atomes de carbone, X étant
alors une simple liaison,
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles, substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8)
alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
- les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro) cycloalcényles, poly
ou monoinsaturés, substitués ou non par un ou des radicaux sélectionnés
parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors
une simple liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou
ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8)
alcynylènes linéaires ou ramifiés, ou
- un
phényle, substitué ou non par un ou des radicaux sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors une simple
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
17
liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés,
(C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires ou ramifiés,
étant entendu que lorsque l'un des groupes R3 ou R7 est un alkyle linéaire ou
ramifié d'au
moins 6 atomes de carbone, un alcényle linéaire ou ramifié d'au moins 6 atomes
de carbone,
ou un alcynyle linéaire ou ramifié d'au moins 6 atomes de carbone, ou un atome
d'hydrogène,
X étant une simple liaison, alors, l'autre groupe R3 ou R7 est sélectionné
parmi :
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou
non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8)
alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
- les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro) cycloalcényles, poly
ou monoinsaturés, substitués ou non par un ou des radicaux sélectionnés
parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors
une simple liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou
ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8)
alcynylènes linéaires ou ramifiés, ou
- un phényle, substitué ou non par un ou des radicaux
sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors une simple
liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés,
(C2-C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes
linéaires ou ramifiés,
w, x, y, z correspondant aux pourcentages respectifs des motifs,
- x étant compris entre 20 et 90 %,
- y étant compris entre 0 et 80 %,
- w étant compris entre 0 et 80%, et
- z étant compris entre 0 et 60 %, étant entendu que
w+x+y+z=100 % et que
y ou w est au moins égal à 10%.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
18
[0035]
Dans un mode de réalisation particulier, quand R3 et/ou R7 est un groupe
sélectionné parmi les alkyles linéaires ou ramifiés d'au moins 6 atomes de
carbone, les
alcényles linéaires ou ramifiés d'au moins 6 atomes de carbone, ou les
alcynyles
linéaires ou ramifiés d'au moins 6 atomes de carbone, X étant alors une simple
liaison,
alors lesdits alkyles, alcényles, ou alcynyles comptent moins de 18, de 17, de
16, de
15, de 14, de 13, de 12, de 11, de 10, de 9, de 8, ou moins de 7 atomes de
carbone.
[0036] La
masse molaire moyenne des amphipols selon l'invention est inférieure
à100000 g.mo1-1, de préférence comprise entre 2000 et 50000 g.mo1-1.
[0037] II
est indiqué ci-après des modes de réalisation de l'invention, qui peuvent être
pris ou non en combinaison avec un autre ou entre certains d'entre eux.
[0038] Dans un mode de réalisation particulier, Pl+ est Na.
[0039]
Dans un mode de réalisation particulier, y et/ou w est supérieur ou égal à
25%.
En effet les polymères greffés à ce pourcentage sont particulièrement
efficaces,
comme le montre la partie expérimentale.
[0040] Dans un mode de réalisation particulier, R2, R6, R9 sont
l'hydrogène.
[0041]
Dans un mode de réalisation particulier, w=0 et R7 est un groupement
sélectionné parmi les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou non par un ou des radicaux sélectionnés parmi les (C1-C8)
alkyles
linéaires, cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés
et les (C1-
C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné
parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8) alcénylènes
linéaires ou
ramifiés et les (C2-C8) alcynylènes linéaires ou ramifiés. De préférence, X
est une
simple liaison et R7 est un C6 cycloalkyle, de préférence, un C7 cycloalkyle,
de manière
encore plus préférée un C8 cycloalkyle. Alternativement, X est un (C1-C8)
alkylène
linéaire ou ramifié, de préférence un méthyle ou un éthyle.
[0042]
Dans un autre mode de réalisation particulier w=0 et R7 est un phényle,
substitué ou non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles
linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-
C8)
alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi
les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8) alcénylènes linéaires ou
ramifiés
et les (C2-C8) alcynylènes linéaires ou ramifiés. De préférence, X est une
simple liaison
et ledit phényle est substitué en para. De manière encore plus préférée,
lorsqu'il est
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
19
monosubstitué, ledit phényle est substitué en para par un alkyle linéaire en
C1-C8, de
manière encore plus préférée, ledit alkyle linéaire en position para est
sélectionné
parmi les groupes méthyle ou éthyle.
[0043]
Dans un mode de réalisation, w.--0 et R7 est un phényle substitué ou non par
un
ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou
ramifiés,
(C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou
ramifiés et X est
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, de préférence,
un Cl
alkylène ou un C2 alkylène.
[0044]
Dans un mode de réalisation particulier, w et y sont différents de 0 et R3 et
R7
sont, indépendamment l'un de l'autre :
- les
(C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles, substitués ou non
par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-
C8)
alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné
parmi les (C1-C8) alkylènes linéaires ou ramifiés, les (C2-C8) alcénylènes
linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou ramifiés,
- les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro) cycloalcényles, poly ou
monoinsaturés, substitués ou non par un ou des radicaux sélectionnés parmi
les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles
linéaires
ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, X étant alors une simple
liaison ou sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, (C2-
C8) alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
- des polycycles poly ou monoinsaturés, substitués ou non par un ou des
radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou
ramifiés,
(C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou
ramifiés,
X étant alors une simple liaison ou sélectionné parmi les (C1-C8) alkylènes
linéaires ou ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-
C8)
alcynylènes linéaires ou ramifiés, ou
- un phényle, substitué ou non par un ou des radicaux sélectionnés parmi les
(C1-C8) alkyles linéaires ou ramifiés, (C1-C8) alcényles linéaires ou
ramifiés,
(C1-C8) alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8)
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
alcénylènes linéaires ou ramifiés et les (C2-C8) alcynylènes linéaires ou
ramifiés,
de manière préférée, R3 et R7 sont alors indépendamment l'un de l'autre :
- un C6 cycloalkyle, de préférence, un C7 cycloalkyle, de manière encore plus
5 préférée un C8 cycloalkyle,
- un phényl, de manière encore plus préférée substitué en para par un alkyle
linéaire en Cl -C8 lorsqu'il est monosubstitué, de manière encore plus
préférée,
ledit alkyle linéaire en position para est sélectionné parmi les groupes
méthyle
ou éthyle, X étant alors une simple liaison, ou
10 - un
phényle substitué ou non par un ou des radicaux sélectionnés parmi les (C1-
C8) alkyle linéaires ou ramifiés, (C1-C8) alcényles linéaires, cycliques ou
ramifiés, (C1-C8) alcynyles linéaires ou ramifiés et X est sélectionné parmi
les
(C1-C8) alkylènes linéaires ou ramifiés, de préférence, un Cl alkylène ou un
C2 alkylène,
15 de manière encore plus préférée, R3 et R7 sont différents l'un de
l'autre.
[0045]
Dans un autre mode de réalisation particulier, R3 et/ou R7 est un groupement
sélectionné parmi les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles,
substitués ou non par un ou des radicaux sélectionnés parmi les (C1-C8)
alkyles
linéaires, cycliques ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés
et les (C1-
20 C8)
alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné
parmi les (C1-C8) alkylènes linéaires ou ramifiés, de préférence un méthyle ou
un
éthyle.
[0046]
Dans un autre mode de réalisation particulier, R3 et/ou R7 est un phényle,
substitué ou non par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles
linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-
C8)
alcynyles linéaires ou ramifiés, X étant alors une simple liaison ou
sélectionné parmi
les (C1-C8) alkylènes linéaires ou ramifiés, de préférence un méthyle ou un
éthyle. De
préférence, X est une simple liaison et ledit phényle est substitué en para.
De manière
encore plus préférée, lorsqu'il est monosubstitué, ledit phényle est substitué
en para
par un alkyle linéaire en Cl -C8, de manière encore plus préférée, ledit
alkyle linéaire
en position para est sélectionné parmi les groupes méthyle ou éthyle.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
21
[0047] Dans un autre
mode de réalisation, z est différent de 0; de manière préférée
Rio est alors un groupe isopropyle, de manière encore plus préférée, R10 est
un groupe
isopropyle et, concernant les motifs comprenant R3 et/ou R7, X est sélectionné
parmi
les (C1-C8) alkylènes linéaires ou ramifiés, (C2-C8) alcénylènes linéaires ou
ramifiés
et les (C2-C8) alcynylènes linéaires ou ramifiés, R3 et/ou R7 étant
sélectionnés parmi :
- les (C3-C10) cycloalkyles ou (C3-C10) (hétéro) cycloalkyles, substitués ou
non
par un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires,
cycliques
ou ramifiés, les (C1-C8) alcényles linéaires ou ramifiés et les (C1-C8)
alcynyles
linéaires ou ramifiés,
- les (C3-C10) cycloalcényles ou les (C3-C10) (hétéro) cycloalcényles, poly ou
monoinsaturés, substitués ou non par un ou des radicaux sélectionnés parmi les
(C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires
ou
ramifiés, (C1-C8) alcynyles linéaires ou ramifiés,
- des polycycles
poly ou monoinsaturés, substitués ou non par un ou des radicaux
sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-
C8)
alcényles linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés, ou
- un phényle,
substitué ou non par un ou des radicaux sélectionnés parmi les (C1-
C8) alkyles linéaires, cycliques ou ramifiés, (C1-C8) alcényles linéaires ou
ramifiés, (C1-C8) alcynyles linéaires ou ramifiés.
[0048] Dans un mode de
réalisation particulier, le polymère vinylique amphiphile de
formule I est choisi parmi les composés listés dans le tableau I ci-dessous,
IVI étant un
métal alcalin, de préférence sélectionné parmi Lit, Na, ;
dans un mode de
réalisation particulier, IVI est Na.
¨CH-CH2I----- cH-CH2
Y
C
-
----0 ---
M+-0 N1+-0"" 0
A
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
22
CH-CH2 -----CH-CH2 -E.
I I --CH-CH2 -----CH-
CHI
I I
X Y Y
C x
'0 HN %, r%
ltdr-V helD .0 HN 0
111: lb
C D-
ICH-CH21-------E-CH-CF121
CH-CH2----- CH-CH2
1
I x I Y I
C
C
HN---- -.."--0 Y
-
NI --0*-0 O HN''''
10) 110
E
_
F
_ -
-CH-CH2 -------CH-CH2l
X y IcH-GH21-----
IcH-cH21----101-1-CH21
I I I I z
I ..,..c,,,.,
hel.-Cr.%0 HN m+-o- -0 HN- -CI 0- NH
ô
H
G _
ICH -C H21---- --CH-CH21-=-+CH-CH2/ -[C1H-C1H21-------[¨CH-CH21-----[¨CH-
CH21
PA"0"- '"-0 HNr '' Ce Ce -.." NH fire '''C) He- '---
;-'0 Ce NH
Cir) ---"L,
il ..--1---..
I J
x Y
-Er-CH21------H-CH21._
-I-CH-CH21------CH-CH21
õC,--- I I
Deo- -...c, 0 HN C, x - C--- Y
R4+-0"- O HN ---C)
à
L _
K _
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
23
ICH-CH21-----+CH-CH21
MO O Y _x
Y
HN
C---
0
M+-0 0 HN
gOl
-F-CH-CH21---+CH-C1121------ECH-CH21
I . I
c, Y .441Z._ er x Y z
MO - HM' -NH e/1.-0"- O HN O O NH
0
Tableau I
[0049] Comme
mentionné, au sein des polymères vinyliques de l'invention, les
pourcentages w, x, y et z des différents motifs peuvent varier, étant entendu
que
w+x+y+z = 100%. Les pourcentages étant spécifiés avec une précision de plus ou
moins 10%. Ainsi, par exemple, si un pourcentage pour un motif est spécifié
comme
étant de 50%, il doit être entendu que ce motif peut être présent entre 45% et
55%
dans le polymère de l'invention.
[0050] Dans un mode de
réalisation particulier, x est inférieur ou égal à 75%.
[0051] Dans un autre
mode de réalisation w et/ou y est compris entre 25 % et 50 % et
z est compris entre 0 % et 40 %, préférentiellement entre 15 % et 40%.
[0052] Dans un mode de
réalisation particulier, w+y est supérieur ou égal à 25%, de
préférence inférieur à 50%.
[0053] Dans un autre
mode de réalisation particulier, les polymères selon l'invention
sont sélectionnés parmi les composés du tableau I avec les proportions w, x, y
et z
telles que spécifiées dans le tableau II ci-dessous.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
24
(x;y) ou
(x;y) ou
(x;y;z) ou
Formule (x;y;z) ou Formule
(x;Y;w)
(x;Y;w) (%) (%)
-E CH-CH2----- cH-CH2 Y
1 i ¨cH-cH2 ---- oH-cH2
1 I
x
INa ri
ie +-0-0 H ---- Na4-0", -0 HW --
à (75;25)
1011 (75;25)
1 2
cii-cH2----- oH-cH2-
1
--CH-CH2 ---- CH-CH2
I x I
Ne -0- -0 HWC----r% Na --- o -0 HWc,, Y ----
à (50;50)
1111 (50;50)
3 4
-E.Ci H-CH2-----CH-CH21
i Y
Nee '''`O HW' ---0
Na+-0- -0 HN- -0
(50;50) (50;50)
6
_
-i-CH-cH21----4-cH-cH21
¨CH-cH2 ---- CH-CH I i
_,C.,...>õ x ,,,e7,=_,.., Y
I 21.
x Na4-0 -0 HN- -0
,.- ,,C--n Y
Net)" -0 HW -..-
0) (75;25) (50;50)
7
8
[-?1-1-cH21----- cH-CE121 f -ECH-cH21-------cH-
cH21------H-cH2
i
c x c y c z
,,C,,õ x _õ6---rt Y Hee .0 He- 0 01 µ14H
Na+-0 -0 HW --- )N,
[Cr) (70;30)
. (35;50;15)
9
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
- .
C¨ -H-CH2 --- CH CH2/ ¨CH-CH2 ---- CH-CH2
i i i y
x x
-3C HN-
-: --C-"zzo Y ,Cz..,
Na+-0 -0 Na+-0- "=0 HN
Crj (50;50)
E. (75;25)
11 12
_
-FCH-cH,- ¨ ----cH-cH, -----cii-cH,
I i i
Il 1 1
,c, x .õ..C.,
Na*-0"--C.k-'0 x Hif"'0 Y 0'NH z NeCr -0 HW '0 O' -NH
Cr) 7.1.,, (35;25;40) _A,., (35;50;15)
13 14 _
_
tr-cH1-----r-cH4-----r-cH2 Ir-cH21-----1-cii-cH21-----cH-cH4
z
Ne-ec%ci x IHN'e'''-0 Y ONII Na*-0"'`O x Ille-LO Y Ole &'Nli z
Cri . ...)-",.. (35;50;15) ),, ..
(35;25;40)
15 16 _
_
_
-1-CH-CH2------CH-CH21
x I y ¨CH-CH2 ---- cH-CH2
- C--
..-C.,-,
HN.- ---0 I 1
Na+-0 -0 x y
C--
(75;25) ,...-
INa+-0- "'01. '''' --ID
18 HN (65;35)
_
17 _ _
-[-CH-CH21-----CH-CH21
I.i x I y ir-CH21------H-CH2
Na+-0"-00 HN e) ;- [ y
Na+-0- -"0 HN''' .
(50;50) ---C)
20 C-- (50;50)
_
19
_
CH-CH2--- CH-CH2-
1
x
1 I y -ECH-CH------[-CH-CH2-
i I
,C..:,.., -x C---- Y
Na+-0" '10 RN"- ---O
Na+-0"-CO HNõ..C.,-,:-zo -
O(50;50) (75;25)
21 _
22 _
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
26
,.
, [
CH-CH2 ..õ...-.[cH-CH2-
1
1 x I 0 T Y CH-CH -
Na+-0 0 HW CH
---%., Na 10 +-0- .*".' HW--
ô(50;50) (50;50)
23
24
iI cH-cH21---f0H-cH2I-----cH-cH,}
-rH-cH,¨ --CH-cH21
-C -----cH-042 1 1 . i
,,c, x õ.c.,.. x
i p I
Net)" -CI HW -0 O' -NH
,C,,, x C, Y , Cõ w
Ne"0" '`C) FIN-, -"C: Cr NH
,.
0) 41 (50;25;25)
(35;50;15)
26
Tableau 2
[0054] Comme démontré dans la partie expérimentale les composés de
l'invention,
5 polymères vinyliques amphiphiles, sont des nouveaux amphipols
particulièrement
aptes à solubiliser et stabiliser les protéines membranaires, notamment au
regard
d'autres polymères tels que l'A8-35 ou le SMA. Ainsi les complexes formés avec
les
protéines membranaires sont d'un intérêt particulier concernant l'étude des
protéines
membranaires ainsi que pour les applications biotechnologiques de ces
protéines. La
10 stabilisation des protéines dans leur état natif et/ou au moins en
partie la préservation
de leur activité est essentielle pour ces applications ; comme démontré dans
la partie
expérimentale, les polymères de l'invention permettent la solubilisation des
protéines
membranaires et cette stabilisation. Notamment la solubilisation peut s'opérer
sans
détergent ce qui est particulièrement avantageux.
15 [0055] II n'y a pas de limitation quant au type de protéines
membranaires au sein des
complexes objets de l'invention. D'un point de vue biotechnologique, les
protéines
membranaires, connues pour être impliquées dans des pathologies, comme étant
des
cibles médicamenteuses ou susceptibles d'être immunogènes sont
particulièrement
préférées.
20 [0056] Les applications envisageables pour ces complexes, sont donc,
par exemple :
- la RMN dans un milieu liquide ou solide, la microscopie
électronique,
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
27
- le diagnostic : la recherche d'anticorps circulants, solubles ou
portés par des
lymphocytes,
- la vaccination ou production d'anticorps: présentation des protéines
membranaires
comme immunogènes,
- détection/utilisation de l'activité enzymatique des protéines
membranaires lorsque
celles-ci sont des enzymes,
- en pharmacologie, mesure de l'affinité des récepteurs cellulaires
pour des molécules
d'intérêt pharmaceutique.
[0057] De ce point de vue les polymères de l'invention fonctionnalisés
sont
particulièrement avantageux. L'homme de l'art saura identifier les moyens de
fonctionnalisation pertinents pour l'utilisation envisagée des polymères de
l'invention.
A titre d'exemple, et de façon non limitative, de tels moyens peuvent être
sélectionnés
parmi ceux présentés par Le Bon et al. (2014).
[0058] Comme mentionné, un objet de l'invention est les complexes
formés par les
polymères de l'invention tels que décrits dans la présente demande et les
protéines
membranaires. Dans un mode de réalisation particulier, pour les applications
susmentionnées, les complexes de l'invention peuvent être présents au sein
d'une
solution aqueuse, sous forme lyophilisée ou bien immobilisés dans une matrice
ou sur
une surface via les groupements fonctionnels greffés sur le polymère de
l'invention.
[0059] L'homme de l'art saura déterminer expérimentalement le ratio
massique
optimum entre le polymère de l'invention et la protéine membranaire pour
obtenir une
solubilisation et/ou une stabilisation de la protéine membranaire
satisfaisante. Dans un
mode de réalisation particulier d'échange du détergent pour l'amphipol A8-35,
le ratio
protéine:amphipol est compris entre 1:0,1 et 1:10, de préférence entre 1:1 et
1 :7,5, de
manière encore plus préférée entre 1:1,5 et 1:5.
[0060] Comme exposé dans la partie expérimentale, ces composés sont
des
amphipols, ils permettent la stabilisation et/ou la solubilisation des
protéines
membranaires sans l'utilisation de détergent qui sont connus pour avoir un
effet négatif
sur la stabilité et donc l'activité des protéines. Avantageusement, dans un
mode de
réalisation, ce complexe est donc substantiellement dépourvu de détergent.
[0061] Dans un autre mode de réalisation, les complexes hydrosolubles
de l'invention
comprennent des lipides ou un mélange de lipides. Ceux-ci peuvent être utiles
pour
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
28
diluer les protéines membranaires, comme exposé dans la partie expérimentale,
ou
bien provenir de la membrane de l'organisme ou de l'organelle dont provient la
protéine
membranaire solubilisée et stabilisée au sein du complexe. Dans un mode de
réalisation particulier, ledit lipide est de la 1,2-Dimyristoyl-sn-glycero-3-
phosphocholine
(DMPC).
[0062]
Avantageusement, le complexe hydrosoluble peut comprendre l'ensemble des
sous-unités d'une protéine multimérique ou tout cofacteur associé avec la
protéine
membranaire, comme le montrent les expérimentations de solubilisation et de
stabilisation de la bactériorhodopsine présentées dans la partie
expérimentale.
[0063] Comme évoqué,
l'invention concerne également un procédé de préparation
d'une solution aqueuse de protéine(s) membranaire(s) stabilisées et présentes
au sein
de complexes avec les polymères de l'invention.
[0064] II
est connu dans l'art antérieur un procédé de préparation des complexes
protéines membranaires avec des amphipols de l'état de l'art tels que A8-35,
ce
procédé impliquant la solubilisation préalable des protéines membranaires via
leur
mise en présence avec un milieu détergent. Un tel procédé implique par la
suite le
remplacement du détergent par l'amphipol en abaissant la concentration du
détergent
à une concentration inférieure à la concentration micellaire critique.
L'abaissement de
la concentration du détergent pouvant être réalisée par dilution, adsorption
des
détergents par exemple sur des billes Bio-Beads SM-2, dialyse, séparation sur
tamis
moléculaire ou sur gradient. Cependant cette étape supplémentaire s'effectue
la
plupart du temps au détriment du rendement ou de la concentration finale en
complexe
contenant la protéine membranaire.
[0065] Les
nouveaux amphipols de l'invention ont la capacité de solubiliser les
protéines membranaires sans cette étape préliminaire de solubilisation par
l'utilisation
d'une préparation détergente. Ainsi un objet de l'invention est l'utilisation
de polymères
de l'invention pour solubiliser et/ou stabiliser les protéines membranaires.
[0066]
Dans un autre mode de réalisation particulier, le procédé de préparation d'une
solution de protéine membranaire ou d'un mélange de protéines membranaires,
selon
l'invention ne comprend pas l'étape de dissolution au moyen d'une préparation
détergente, la solubilisation étant réalisée au moyen d'un des polymères de
l'invention.
Dans un mode de réalisation encore plus particulier, le polymère est
sélectionné parmi
les polymères de formule I sélectionnés tels que
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
29
- w=0
et R7 est un groupe sélectionné parmi les (C3-C10) cycloalkyles ou (C3-
C10) (hétéro) cycloalkyles, substitués ou non par un ou des radicaux
sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, les
(C1-C8) alcényles linéaires ou ramifiés et les (C1-C8) alcynyles linéaires ou
ramifiés, X étant alors une simple liaison ou sélectionné parmi les (C1-C8)
alkylènes linéaires ou ramifiés, les (C2-C8) alcénylènes linéaires ou ramifiés
et les (C2-C8) alcynylènes linéaires ou ramifiés. De préférence, X est une
simple liaison et R7 est un C6 cycloalkyle, de préférence, un C7 cycloalkyle,
de manière encore plus préférée un C8 cycloalkyle.
- w=0 et R7 est un phényle, substitué ou non par un ou des radicaux
sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques ou ramifiés, (C1-
C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles linéaires ou ramifiés,
X
étant alors une simple liaison ou sélectionné parmi les (C1-C8) alkylènes
linéaires ou ramifiés, (C2-C8) alcénylènes linéaires ou ramifiés et les (C2-
C8)
alcynylènes linéaires ou ramifiés. De préférence, X est une simple liaison et
ledit phényle est substitué en para. De manière encore plus préférée,
lorsqu'il
est monosubstitué, ledit phényle est substitué en para par un alkyle linéaire
en C1-C8, de manière encore plus préférée, ledit alkyle linéaire en position
para est sélectionné parmi les groupes méthyle ou éthyle.
[0067] Dans un mode
de réalisation, w=0 et R7 est un phényle substitué ou non par
un ou des radicaux sélectionnés parmi les (C1-C8) alkyles linéaires, cycliques
ou
ramifiés, (C1-C8) alcényles linéaires ou ramifiés, (C1-C8) alcynyles linéaires
ou
ramifiés et X est sélectionné parmi les (C1-C8) alkylènes linéaires ou
ramifiés, de
préférence, un Cl alkylène ou un C2 alkylène.
[0068] Les amphipols
de l'invention ont pour précurseur l'acide polyacrylique. Leur
synthèse est donc très similaire à celle d'autres amphipols décrite dans Gohon
et al.
(2006). L'homme de l'art saura adapter sans difficulté particulière le
protocole pour
greffer aléatoirement les groupements spécifiés sur le précurseur d'acide
polyacrylique
via la formation de liaisons amide entre une amine primaire portée par lesdits
groupements et une fraction des groupes carboxylate portés par le précurseur.
De
préférence, la réaction se fait dans de la N-methylpyrrolidone (NMP) en
présence de
dicyclohexylcarbodiimide (DCC). La synthèse peut se faire de façon
séquentielle,
chaque étape consistant dans le greffage d'un motif particulier.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
EXEMPLES
[0069] Les abréviations suivantes ont été utilisées dans les exemples
qui suivent.
- OTG : Octylthioglucoside
- DM PC : dimyristoylphosphatidylcholine
5 - BR : bactériorhodopsine
- SERCA1a : sarco/endoplasmic reticulum Ca2+-ATPase la
- SMA: Styrene maleic acid copolymer, formule :
¨(CH¨CH)¨(C142¨CH)y^^4;
Nem"01 LiNa*
411
Le SMA (2:1) est composé de deux tiers de styrène et un tiers d'acide
maléique. Le SMA (3:1)
10 comporte trois quart de styrène et un quart d'acide maléique.
- A8-35 : Amphipol de formule :
n
HN HN
avec x=-35%, y=-40% and z=-25%
- A8-75: comme ci-dessus mais avec x=-75%, y=-25% and z= 0%
- E. col!: Escherichia col!
15 - DDM : n-dodécyl-p-D-maltopyranoside
- GFP : green fluorescent protein
- AChR : récepteur de l'acétylcholine
- EDTA : acide éthylènediaminetétraacétique
- CHAPS : 3-[(3-Cholamidopropyl)diméthylammonio]-1-propanesulfonate hydrate
20 - SDS : sodium dodécyl sulfate
- Tris : Tris(hydroxyméthyl)aminométhane
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
31
[0070] Les
données expérimentales ci-dessous ont été obtenues en utilisant des
fractions membranaires et/ou protéines pour étudier les propriétés des
nouveaux
amphipols de l'invention. Ces exemples ne sont pas limitatifs, notamment, les
efficacités relatives des amphipols de l'invention peuvent varier en fonction
de la
fraction membranaire ou de la protéine membranaire considérée. Néanmoins, les
propriétés de solubilisation et/ou de stabilisation améliorées des amphipols
de
l'invention vis-à-vis des polymères de référence sont d'application générale.
1. Exemple 1, synthèse des amphipols de l'invention
[0071]
Comme mentionné, les amphipols de l'invention ont pour précurseur l'acide
polyacrylique. Leur synthèse est donc très similaire à celle de l'A8-35
décrite dans
Gohon et al. (2006). Elle consiste à greffer aléatoirement les groupements sur
le
précurseur d'acide polyacrylique via la formation de liaisons amide entre une
amine
primaire portée par les groupements à greffer et une fraction des groupes
carboxylate
portés par le précurseur. La réaction se fait dans de la N-méthylpyrrolidone
(NMP) en
présence de dicyclohexylcarbodiimide (DCC). Le greffage et l'obtention des
différents
motifs peut se faire de façon séquentielle. Notamment, quand z est différent
de 0, le
greffage des groupes correspondant à une fraction des groupes carboxylate du
précurseur a lieu dans un deuxième temps, dans de la NMP en présence de 1-
hydroxybenzotriazole (HOBt)/DCC.
[0072]
L'amphipol est alors obtenu sous sa forme acide. Après synthèse, le polymère
est purifié par trois cycles de précipitation à pH=3 suivis d'une
solubilisation à pH=10.
Le polymère est ensuite dialysé contre de l'eau déionisée puis lyophilisé.
[0073] La
composition chimique du polymère est déterminée par une analyse RMN du
proton et du carbone, couplée à un dosage pH-métrique.
Exemple de synthèse du composé 23
[0074]
Dans un ballon bicol de 100 mL, 1,00 g d'acide polyacrylique (1éq., 13,89
mmol)
est dissous dans 20 mL de N-Méthy1-2-pyrrolidone (NMP). Le milieu est placé
sous
agitation à 60 C pendant 4 heures. 884,3 mg de cyclooctylamine (0,50 éq., 6,94
mmol)
sont dissous dans 2 mL de NMP et la solution obtenue est additionnée goutte à
goutte
au milieu réactionnel sous agitation. Après addition complète de l'amine,
l'agitation est
poursuivie pendant 10 min puis 1,58 g de DCC (0,55 éq., 7,64 mmol)
préalablement
dissous dans 4 mL de NMP sont ajoutés goutte à goutte au milieu réactionnel.
Une fois
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
32
la totalité du réactif ajoutée, le milieu réactionnel est maintenu sous
agitation à 60 C
pendant 1 heure, puis laissé sous agitation sans chauffage pendant 4 heures.
[0075] Une
fois à température ambiante, le milieu réactionnel est filtré sur fritté
(porosité 4) puis 1,5 g de méthanolate de sodium (2 éq., 27,8 mmol) sont
ajoutés au
filtrat. L'agitation est poursuivie pendant environ 15 minutes.
[0076] Le
milieu réactionnel est ensuite versé dans 260 mL (10 volumes équivalents)
d'eau purifiée et déionisée (Milli-Q ) et le pH est ajusté à 10 (papier pH)
avec de la
soude (11N). La solution est maintenue sous vive agitation pendant une
trentaine de
minutes puis filtrée sur fritté (porosité 4). Le filtrat obtenu est ajouté
manuellement
goutte à goutte à 21 mL d'acide chlorhydrique 2N (3 éq., 42 mmol) sous vive
agitation.
L'addition est effectuée via une seringue dont l'embout est connecté à un
système de
filtres millipore (préfiltre PES 0,45 pm et filtre acétate de cellulose 0,2 pm
en série).
[0077] Une
fois l'addition terminée, la suspension obtenue est filtrée sur fritté
(porosité
4) et le précipité est dissous dans 50 mL d'eau Milli-Qc après addition de
1,9 mL
(1,5 éq., 21 mmol) de soude 11 N. Ce cycle de précipitation / solubilisation
est réitéré
quatre fois, puis la solution basique finalement obtenue est dialysée
(membrane
Spectrapore avec seuil de coupure à 8000 g.mo1-1) pendant 24 heures contre une
solution de soude à 4,5.10-3 N puis lyophilisée.
[0078]
L'homme de l'art saura adapter ce protocole pour obtenir les autres amphipols
de l'invention sans difficulté particulière, notamment en adaptant le choix
des amines
devant réagir avec les groupes carboxylate de l'acide polyacrylique.
2. Exemple 2, analyse des particules d'amphipols selon l'invention par
chromatographie d'exclusion stérique (SEC).
Matériel et méthodes
[0079] Une
colonne Superose 12/HR ou 12 10/300 GL (GE Healthcare) a été utilisée.
[0080] La
colonne a été équilibrée en tampon Tris 20 mM pH8.0, 100 mM NaCI (Figure
1A), ou en tampon 20 mM phosphate de sodium pH7.0, 100 mM NaCI (Figure 1B).
[0081]
Concernant les complexes BR/amphipols (Figure 1C), la membrane pourpre a
été solubilisée en OTG (cf exemple 2), puis la BR complexée avec les amphipols
à un
ratio massique BR/amphipol de 1:5. La colonne a été équilibrée en 20 mM
phosphate
de sodium pH 7.0, 100 mM NaCI.
[0082]
L'élution a été effectuée en 20mM phosphate de sodium pH 7.0, 100 mM NaCI.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
33
Résultats
[0083] Les
profils d'élution des polymères de l'invention obtenus par SEC ont été
comparés à celui de l'A8-35 (Figure 1A et B). En solution, il est connu que
l'A8-35
forme des particules homogènes, compactes et globulaires de 40 kDa comprenant
environ 9-10 molécules (Giusti et al., 2014; Gohon et al., 2006). Comparés à
l'A8-35,
les polymères de l'invention testés présentent des pics d'élution plus larges.
Ce résultat
peut s'expliquer par la présence des cycles dans les amphipols selon
l'invention qui
sont moins flexibles que les chaines octyle linéaires de l'A8-35 et donc moins
favorables à la formation de particules sphériques, résultant en la formation
de
particules plus grosses et moins homogènes.
[0084]
Aussi, le nombre d'atomes de carbone entre la liaison amide et le groupe
cycloalkyle des amphipols selon l'invention semble influencer la taille et
l'homogénéité
des particules qu'ils forment. En effet, l'addition d'un carbone entre la
liaison amide et
le cycle cycloalkyle (cf. les profils d'élution du composé 3 et du composé 11,
Figure
1A) résulte en des particules plus homogènes ayant un profil d'élution
comparable à
celui de l'amphipol A8-35. Toutefois, la présence de deux atomes de carbone
(composé 17, Figure 1A) a pour conséquence la formation de particules plus
grosses
et moins homogènes. Concernant les amphipols greffés avec un groupe phényle
(e.g.
composés 2 ou 4), les profils d'élution indiquent que les particules formées
par ces
polymères ont une taille supérieure à 40 kDa et sont moins homogènes
comparativement à l'A8-35. L'homogénéité est très nettement améliorée par
l'addition
d'un groupe éthyle (e.g. profile d'élution du composé 8) et aboutit à des
particules de
taille plus en rapport avec celles de l'A8-35
[0085] De
manière intéressante, les profils d'élution des complexes formés par les
composés 11 et 8 et la bactériorhodopsine (BR) sont d'une homogénéité et d'une
taille
comparable avec celle des complexes BR/A8-35 (Figure 1C).
[0086] Les
polymères de l'invention constituent donc des outils modulables à façon qui
présentent en milieu aqueux des propriétés d'auto-organisation en particules
compatibles avec les procédés de purification de protéines en termes
d'homogénéité.
Ces particules sont comparables avec celles formées par l'amphipol A8-35 qui
fait
référence dans la communauté.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
34
3. Exemple 3, étude de l'effet stabilisateur.
[0087]
L'effet stabilisateur pour les protéines membranaires des amphipols selon
l'invention a été testé sur deux protéines membranaires modèles, SERCA1 a
(sarco/endoplasmic reticulum Ca2 -ATPase la) et la bactériorhodopsine de
Halobacterium salinarum.
Matériel et méthodes
Protéines membranaires modèles utilisées
[0088]
SERCAla est une pompe à calcium qui nécessite l'hydrolyse d'une molécule
d'ATP pour réaliser sa fonction de transport. Cette protéine appartient à la
famille des
ATPase de "type P" et ses segments transmembranaires adoptent des changements
conformationnels de grandes amplitudes pour permettre le passage des ions
calcium.
[0089] La
couleur violette de la BR est indicatrice de sa conformation native. Dans sa
forme repliée la BR lie de façon covalente mais réversible le rétinal (un
chromophore)
via la formation d'une base de Schiff. La protonation de cette base provoque
le
déplacement du pic d'absorption du rétinal de ¨380 nm (forme libre) à 570 nm
ou ¨555
nm (forme liée) selon que la BR est imbriquée dans la membrane ou solubilisée
en
solution aqueuse. L'absorbance à 554 nm est donc indicative de la conformation
native
de la BR.
Production de SERCAl a et mesure de l'activité
[0090] Les
vésicules du réticulum sarcoplasmique de lapin ont été préparées à partir
de tissus musculaires selon le protocole décrit dans Champeil et al. (1985).
Ces
membranes sont très riches en SERCAla.
[0091]
L'activité ATPasique de SERCA1 a a été mesurée de façon indirecte en
couplant plusieurs réactions enzymatiques. Le dosage a été fait en présence de
pyruvate kinase (0,1 mg/mL) et de lactate déshydrogénase (0,1 mg/mL) afin,
d'une
part, de maintenir constante la concentration d'ATP dans l'échantillon et,
d'autre part,
de suivre la consommation d'ATP en mesurant la diminution de l'absorbance à
340 nm
du NADH au cours du temps. Le tampon de l'échantillon contient du KCI 100 mM,
Mg2
1 mM, Ca2 0,1 mM, Tes-Tris 50 mM (pH 7,5 à 20 C) et 1-5 mM d'ATP. Pour
réaliser
le dosage, le milieu réactionnel contient également du phosphoénolpyruvate 1
mM et
du NADH 0,15 mM.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
Production de la membrane pourpre et préparation des complexes BR/amphipol
[0092] La
préparation des complexes BR/amphipols a lieu selon les étapes suivantes :
i) Une culture de Halobacterium salinarum a été réalisée et la fraction
membranaire
correspondant à la membrane pourpre a été purifiée selon le protocole déjà
décrit
5 dans Oesterhelt & Stoeckenius (1971).
ii) La membrane pourpre a été solubilisée en tampon phosphate de sodium 10
mM,
NaCI 100 mM, OTG 100 mM, pour une incubation de 48 heures en chambre froide
sous agitation et dans l'obscurité. L'échantillon a été centrifugé 20 min. à
200.000
g à 6 C. Le surnageant a été dilué avec du tampon sans OTG pour abaisser la
10 concentration de détergent de 100 mM à 18 mM.
iii) Remplacement du détergent et préparation des complexes BR/amphipol
La concentration de la BR a été déterminée par mesure de l'absorbance à 554
nm.
La quantité d'amphipol ajouté a été calculée en fonction de la masse de BR
présente dans l'échantillon, correspondant à un ratio massique BR/amphipol de
15 1:5.
Après 20 min d'incubation à 4 C, des billes de polystyrène (Bio-Beads SM2,
BioRad) ont été ajoutées de façon à ce que leur masse corresponde à 20 fois
celle
du détergent présent dans l'échantillon. Après 2 h d'incubation à 4 C sous
agitation,
les billes ont été retirées.
20 [0093] La
formation de complexes BR/A8-35 ou BR/A8-75 (contrôles positifs) d'une
part, et des complexes BR avec les amphipols de l'invention d'autre part, a
été
effectuée selon le protocole de remplacement et élimination du détergent par
adsorption sur des billes de polystyrène (Bio-Beads , BioRad).
[0094]
Après les 20 min d'incubation en présence d'OTG et d'amphipols, les Bio-
25 Beads
ont été rajoutées au mélange dans un ratio massique Bio-Beads /OTG 20:1 et
incubées pendant 2 heures à 4 C. L'absorbance à 554 nm de chaque échantillon a
été
mesurée avant et après centrifugation à 100000 g pendant 20 min. Le
pourcentage de
BR est calculé en référence à l'absorbance mesurée en OTG avant
centrifugation.
30 Dénaturation thermique de la BR
[0095] Le
ratio de la protéine BR avec les différents agents de solubilisation testés
est de 1:5, dans un tampon phosphate de sodium 20 mM, pH 7.0, NaCI 100 mM.
Les échantillons ont été incubés à chaque température pendant 30 min puis
refroidis sur glace avant lecture de l'absorbance à 554 nm. Concernant les
35
échantillons de BR en détergent (OTG, Octylthioglucoside) une étape de
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
36
centrifugation a été effectuée pour supprimer les agrégats de protéine.
L'absorbance des échantillons à 554 nm a été mesurée avec un
spectrophotomètre UV-visible en prenant comme référence du tampon sans
protéine. Les valeurs d'absorbance sont normalisées par rapport à l'absorbance
mesurée à 4 C.
Résultats
[0096] II
a été observé que le composé 11 semble inhiber de façon plus importante
l'activité ATPasique de SERCA1a que l'A8-35 (non présenté). L'effet inhibiteur
des
amphipols pouvant être lié à leur effet stabilisateur, on peut donc supposer
que le
composé 11 stabilise de manière plus efficace SERCA1a que l'A8-35.
[0097] La
stabilité thermique de la BR complexée avec l'A8-35, l'A8-75 ou les
amphipols de l'invention a été analysée. Dans un premier temps, la capacité de
ces
polymères à maintenir la BR soluble sous sa forme native a été analysée par la
mesure
de l'absorbance des surnageants à 554 nm.
[0098]
Après avoir éliminé le détergent avec les Bio-Beads , le pourcentage de BR
sous sa forme native dans les échantillons après complexation avec les
amphipols de
l'invention comprenant 25% de groupes cycliques hydrophobes et 75% de groupes
carboxylate non modifiés est plus élevé que celui observé en utilisant l'APol
A8-75
comme référence (figure 2 A et B), qui est particulièrement peu efficace pour
ce qui est
de la stabilisation de la BR. Ce résultat montre que les groupes cycliques
augmentent
l'effet stabilisateur des amphipols. Les composés 7 et 1 sont plus doux
que l'A8-75
quant à la dénaturation. Cependant, la stabilité de la BR diminue avec le
nombre
croissant de carbones entre le cycle et la liaison amide jusqu'à atteindre un
niveau de
déstabilisation similaire à celui de l'A8-75 (e.g. BR complexé avec le composé
17). Cet
effet est plus prononcé avec les amphipols greffés avec des groupes
cycloalkyle
qu'avec les groupes phényle (figure 2B composés 2, 12, 22).
Effet de la charge de l'amphipol
[0099]
L'influence de la charge des amphipols de l'invention a été étudiée en
augmentant le taux de greffage des polymères avec des groupes isopropyle, ce
qui a
pour effet de réduire la charge globale de l'amphipol. La réduction de la
charge (via un
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
37
taux de greffage des groupes isopropyle jusque 40%) ainsi obtenue améliore le
taux
de BR présente sous sa forme native dans les échantillons après remplacement
du
détergent par l'amphipol en présence de Bio-Beads (comparer, e.g., les
absorbances
pour composés 7 et 13). Inversement, une plus faible quantité de BR est
retrouvée
dans le surnageant quand on diminue la densité de charge (comparer e.g.
composé
11 vs. composé 15), ce qui pourrait être dû à de l'agrégation de BR.
[00100] Pour les amphipols comprenant un taux de greffage plus important (50%
de
groupes cycloalkyle et/ou phényle et 50% de groupe carboxylate non modifiés),
l'effet
déstabilisateur du nombre croissant de carbone entre les cycles et la liaison
amide est
considérablement diminué (Figure 2C).
[00101] Les
amphipols de l'invention greffés avec des groupes cycloalkyle et/ou des
groupes phényle à hauteur de 50% ont une densité de charge équivalente au SMA
(2 :1) ou supérieure au SMA (3 :1). Pourtant, exception faite du composé 4,
tous les
amphipols de l'invention testés permettent d'obtenir plus de BR sous sa forme
native
que les deux SMAs. (Figure 2).
[00102] La
stabilité thermique de la BR complexée avec les amphipols selon l'invention
a été testée sur la fraction de BR restée native après échange du détergent
par les
amphipols en utilisant les Bio-Beads . Labsorbance à 554 nm des échantillons a
été
suivie en fonction de la température, une chute d'absorbance signant la
dénaturation
de la protéine (Figure 3).
[00103] Dans le cas des complexes BR/A8-35, la dénaturation de la protéine a
lieu dans
un intervalle de température très étroit, comme l'indique la pente de la
sigmoïde
obtenue, avec une température de fusion moléculaire (Tm) autour de 63 C
(Figure 3A).
La Tm de la protéine dans le détergent OTG est significativement plus bas (-47
C,
Figure 3A), ce qui indique une plus faible stabilisation de la protéine en
OTG. Un Tm
similaire est observé pour la protéine complexée au SMA (3:1) ou au SMA (2:1),
respectivement de ¨45 C et ¨49 C. A l'inverse, les Tm obtenues avec les
amphipols
selon l'invention sont significativement plus élevées que ceux en SMA et pour
certains
comparables voire plus importants que celui des complexes BR/A8-35 (e.g.
composés
4 et 3, avec des Tm ¨57 C et ¨66 C respectivement, Figure 3B).
[00104]
Ainsi, en termes de stabilisation, les amphipols selon l'invention sont plus
efficaces que les SMAs et peuvent être au moins aussi efficaces que l'amphipol
de
référence A8-35, voire plus efficaces comme le suggèrent les résultats obtenus
concernant SERCA1.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
38
4. Exemple 4, évaluation de l'effet solubilisateur des amphipols de
l'invention
sur des membranes à haute densité en protéines membranaires.
[00105] A la différence des détergents, l'A8-35 est connu pour ne pas
solubiliser
efficacement SERCA1 des vésicules du réticulum sarcoplasmique (Champeil et
al.,
2000). Typiquement les protéines membranaires sont toujours solubilisées en
utilisant
des détergents, qui sont par la suite échangés avec l'A8-35 pour les
stabiliser.
[00106] A l'inverse, le Styrene Maleic Acid copolymer (SMA) est un polymère
connu
pour permettre la solubilisation des protéines membranaires, sans nécessiter
l'étape
de solubilisation avec un détergent, ce qui résulte en la formation de
particules
lipidiques (SMALPs pour SMA
particles) qui comprennent la protéine membranaire
et des lipides, entourés par le SMA. Cependant, comme vu plus haut, la
stabilité de la
BR en SMA est relativement médiocre comparée à celle de la même protéine
complexée avec l'A8-35.
[00107] Les
propriétés de solubilisation du SMA, A8-35 et des amphipols selon
l'invention ont été comparées pour différents types de membranes plus ou moins
riches
en protéines membranaires (membrane d'E. co/i, des organes électriques de T.
marmorata, des thylakoïdes de C. reinhardtii, membrane pourpre de H.
salinarum). Les
résultats obtenus sont spécifiques des membranes testées et illustrent les
propriétés
différentes des différents polymères. Ainsi un polymère faiblement efficace
pour l'une
de ces membranes modèles pourrait être tout à fait efficace pour un autre type
de
membrane du fait de sa composition spécifique en protéines et/ou lipides.
Matériel et méthodes
Préparation des fractions de membrane pourpre de Halobacterium salinarum, de
membranes de thylakoides de Chlamydomonas reinhardtii, de membrane d'organes
électriques de Torpedo marmorata ou de membrane dEscherichia coli.
[00108] Comme mentionné précédemment, la membrane pourpre de Halobacterium
salinarum est préparée selon le protocole décrit dans Oesterhelt & Stoeckenius
(1971).
[00109] Les membranes extraites d'organes électriques de Torpedo marmorata
naturellement riches en récepteur d'acétylcholine (AChR) sont préparées selon
le
protocole décrit dans Sobel et al. (1977).
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
39
[00110] Les membranes de thylakoïdes de Chlamydomonas reinhardtti sont
préparées
selon le protocole décrit dans Pierre et al. (1995).
[00111] Les membranes d'Escherichia colisurexprimant la protéine YidC,
fusionnée en
position C-terminale à la GFP, sont préparées après lyse mécanique des
bactéries
avec un broyeur de cellules (Constant Systems). Les débris cellulaires et les
cellules
non cassées sont éliminés par centrifugation à basse vitesse. Le surnageant
est
récupéré et les membranes sont culotées par centrifugation à haute vitesse
(100000 g
pendant une heure). Le protocole de préparation des membranes d'E. cou est
décrit
dans Angius et al. (2018).
Dilution de la fraction de membrane pourpre avec des vésicules de DMPC
[00112] Des vésicules de DMPC (50 mg/mL) ont été formées par extrusion après
10
passages à travers une membrane en polycarbonate (Whatman) calibrée avec des
pores de 100 nm de diamètre. Les vésicules de DMPC et la membrane pourpre sont
mélangées de façon à obtenir un ratio massique BR:DMPC de 1:5, puis incubées
30
min dans un bain à sonication selon le protocole déjà décrit par Knowles et
al. (2009).
Le tampon de l'échantillon contient 20 mM phosphate de sodium pH 7.0, 100 mM
NaCI.
Solubilisation de la membrane pourpre en OTG
[00113] La solubilisation en OTG (100 mM) a été effectuée comme exposé plus
haut.
Les échantillons ont été incubés une heure à 4 C avant centrifugation (20 min
100000
g), et les surnageants prélevés pour la mesure d'absorbance à 544 nm.
Solubilisation de la membrane pourpre avec les SMAs ou les amphipols de
l'invention
[00114]
Pour chaque condition, le ratio massique BR/SMA ou amphipol est 1:6,25 et le
ratio massique BR/DPMC est 1:5. Le tampon utilisé est du phosphate de sodium
20
mM, pH 7.0, NaCI 100 mM comme mentionné ci-dessus.
[00115] Les
échantillons ont été incubés sur la nuit à température ambiante, sous
agitation, puis centrifugés 20 min à 100000g, et les mesures d'absorbance
effectuées
sur les surnageants.
[00116] Les absorbances sont normalisées sur la valeur d'absorbance mesurée
avant
l'étape d'ultracentrifugation.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
Solubilisation des membranes d'E. cou i surexprimant une protéine membranaire
recombinante
avec les amphipols de l'invention, les SMA ou le DDM
[00117] YidC est une protéine membranaire conservée au cours de l'évolution
qui
5 compte
6 domaines transmembranaires chez les bactéries à coloration de gram
négative. Une forme recombinante fusionnée à la GFP est utilisée comme
protéine
reporter de la solubilisation des membranes pour l'étude des propriétés des
amphipols de l'invention.
[00118] Les protéines membranaires totales présentes dans les extraits de
membranes
10 d'E.
co/i sont dosées à l'aide d'un test colorimétrique. La concentration en
protéines
est ajustée à 2 mg/mL avec du tampon Tris 20 mM pH 8, NaCI 150 mM.
[00119]
Pour la solubilisation, le ratio massique protéine totale/amphipols ou SMA est
de 1:1. Dans le cas de l'échantillon contrôle en présence de détergent, le
ratio
massique protéine totale/DDM est de 1 :5. Comme mentionné ci-dessus, le tampon
15 utilisé dans toutes les conditions est composé de Tris 20 mM, pH 8.0,
NaCI 150 mM.
[00120] Les
échantillons sont incubés deux heures à 4 C, sous agitation. Pour suivre la
cinétique de solubilisation, un aliquot est prélevé de chacun des tubes tous
les quarts
d'heure au cours de la première heure d'incubation, puis toutes les demi-
heures au
cours de la seconde heure.
20 [00121]
A chaque prélèvement, les échantillons sont centrifugés 10 min à 250000 g.
Les culots, séparés des surnageants, sont re-suspendus dans le volume initial
de
solubilisation avec du tampon Tris 20 mM pH 8, NaCI 150 mM contenant du SDS à
5 %.
[00122] A ces échantillons est ajouté du bleu de charge compatible avec une
mesure
25 de
fluorescence sur gel d'acrylamide. Il s'agit d'un bleu de charge préparé
suivant le
protocole décrit dans Drew et al. (2008). Les échantillons, correspondant aux
surnageants et culots de chaque condition et prélevés aux temps indiqués, sont
déposés sur un gel d'acrylamide 12%.
[00123] L'électrophorèse est faite en présence de SDS dans le tampon de
migration
30
contenant du Tris-glycine pH 8,3. La migration des protéines dans le gel est
faite
pendant 1 heure en appliquant un courant de 100 V et 20 mA par gel.
[00124] Une
fois la migration terminée, chaque gel est placé dans de l'eau Milli-Q
et une photo de fluorescence des gels, prise grâce à un scanner laser
(?excitation- = 495
nm ; ?émission = 519 nm), permet de mesurer la fluorescence de la GFP.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
41
[00125] Le
logiciel ImageJ permet d'intégrer les aires de chaque bande pour quantifier
la fluorescence. Les résultats sont normalisés par rapport à la fluorescence
obtenue
en détergent (DDM ¨ 1heure).
Solubilisation de la membrane de Torpedo marmorata enrichie en AChR avec les
amphipols
de l'invention, les SMAs ou le CHAPS -solubilisation de l'AChR.
[00126] AChR est une protéine membranaire intrinsèque. Les organes électriques
de
Torpedo Marmorata sont particulièrement riches en cette protéine. Ces organes
constituent de ce fait une source et un modèle d'étude important du récepteur
à
l'acétylcholine.
[00127] Les protéines membranaires totales présentes dans les extraits de
membranes
de Torpedo marmorata sont dosées à l'aide d'un test colorimétrique. La
concentration
en protéines est ajustée à 1 mg/mL avec du tampon NaP 5 mM pH 7,2, NaCI 100
mM,
EDTA 1 mM.
[00128] Pour la
solubilisation, le ratio massique protéine totale/amphipols ou SMA est
de 1:5. Dans le cas de l'échantillon contrôle, c'est à dire en présence de
détergent, le
ratio massique protéine totale/CHAPS est de 1:4.
[00129] Les
échantillons sont incubés une heure à 4 C, sous agitation avant d'être
centrifugés 20 min à 100000 g. Les culots, séparés des surnageants, sont re-
suspendus dans le volume initial de solubilisation avec du tampon NaPi 5 mM pH
7,2,
NaCI 100 mM, EDTA 1 mM.
[00130] Les
échantillons, correspondant aux surnageants et culots de chaque condition,
sont mélangés à du bleu de charge préparé suivant le protocole décrit dans
Laemmli
(1970) avant d'être déposés sur un gel d'acrylamide 10%.
[00131] L'électrophorèse est faite en présence de SDS dans le tampon de
migration
contenant du Tris-glycine pH 8,3. La migration des protéines dans le gel est
faite
pendant 1 heure en appliquant un courant de 100 V et 20 mA par gel.
[00132] Une fois la migration terminée, chaque gel est coloré au bleu de
Coomassie et
une photo des gels, en lumière blanche, est prise.
Résultats
[00133] II
a été observé que l'efficacité de solubilisation des polymères est étroitement
liée à la composition de la membrane dont on souhaite extraire les protéines
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
42
membranaires (aussi bien en termes de protéines que de lipides). En effet
aucun des
polymères testés que ce soit l'A8-35, les amphipols selon l'invention ou bien
même les
SMAs, n'est capable de solubiliser les membranes riches en protéines comme la
membrane pourpre de Halobacterium salinarum (Figure 4A), ou celle des
thylakoïdes
de Chlamydomonas reinhardtii (non présenté), alors que la plupart peuvent
solubiliser
les membranes de E. coli surexprimant une protéine recombinante telle que YidC-
GFP
(voir Figure 7). Néanmoins les amphipols de l'invention s'avèrent d'une
manière
générale plus efficaces que le polymères A8-35 ou les SMAs.
[00134] La
membrane pourpre de Halobacterium salinarum comprend 75% de BR pour
25% de lipides. Du fait de cette composition singulière, sa solubilisation par
le SMA
n'est possible que lorsque la membrane est préalablement fusionnée avec des
vésicules de DPMC, afin de diluer la protéine BR dans des lipides (Knowles
et al.,
2009; Orwick-Rydmark et al., 2012). Dans ces conditions, les amphipols de
l'invention
sont également capables de solubiliser la BR, alors que l'A8-35 reste
inefficace (Figure
4B).
[00135] Concernant les amphipols de l'invention comprenant un greffage avec un
groupe phényle, il est observé que l'ajout d'un groupement éthyle sur le site
aromatique
permet d'augmenter les propriétés de solubilisation (comparer le pourcentage
de BR
solubilisée pour les composés 4, 6 et 8). A noter que l'emplacement du groupe
éthyle
en position para (position 4) ou ortho (position 1) ne semble pas avoir
d'importance,
les composés 8 et 24 permettant une solubilisation comparable (Figure 4B).
[00136] Les
amphipols de l'invention présentant un greffage avec un cycloalkyle sont
particulièrement efficaces concernant la solubilisation de la BR. Le composé
23
notamment est trouvé aussi efficace que le SMA (2 :1) (comparer la taille des
culots)
mais la quantité de BR présente sous sa forme native dans le surnageant est
plus
élevée que celle obtenue avec le SMA (2 :1) ou le SMA (3 :1); le composé 21
étant
sensiblement plus efficace que le SMA (2 :1).
[00137] En
outre, l'analyse en chromatographie d'exclusion stérique des complexes
BR/lipides/amphipols selon l'invention montrent que ceux-ci sont beaucoup plus
homogènes en taille que ceux obtenus en utilisant du SMA, ce qui est
particulièrement
avantageux dans les techniques de caractérisation des protéines (non
présenté).
[00138]
L'efficacité des polymères de l'invention à extraire la protéine membranaire
YidC-GFP surexprimée dans les membranes d'E. co/i, ici il s'agit de la
protéine, a
également été testée et comparée avec. l'A8-35 et les SMAs. En fixant le ratio
protéine/polymère à 1 :1, c'est à dire en travaillant à des concentrations
basses en
polymères, les polymères amphipols de l'invention présentent une meilleure
efficacité
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
43
d'extraction de la protéine recombinante d'intérêt que l'A8-35 et les SMAs. En
effet,
après deux heures d'incubation, en présence des polymères amphipols de
l'invention,
la quantité de protéine extraite est d'environ 80 %, contre environ 35 % en
présence
d'A8-35 ou de SMAs. De plus, la cinétique d'extraction de la protéine
membranaire
d'intérêt est plus rapide (Figure 7). Ainsi, les amphipols de l'invention sont
efficaces à
de faibles concentrations et permettent une extraction plus rapide ce qui est
particulièrement avantageux, notamment dans le contexte de production de
protéines
membranaires recombinantes.
[00139] L'efficacité des polymères de l'invention à extraire le récepteur de
l'acétylcholine (AChR) de la membrane des organes électriques de Torpedo
marmorata a également été testée. A un ratio protéine/polymère fixé à 1:5, les
polymères de l'invention présentent une efficacité d'extraction de la protéine
membranaire d'intérêt meilleure que celle de l'A8-35 et du SMA (2 :1) et
comparable à
celle du SMA (3 :1) (Figure 8, comparer les colonnes notées S). De manière
surprenante, le polymère contrôle (A8-50), comportant des chaînes octylamine,
donc
ayant le même nombre d'atomes de carbone que dans les groupes
cyclohexyléthylamine (comme dans le composé 19), et cyclooctylamine (comme
dans
le composé 23), et greffées au même pourcentage (50%), est moins efficace à
extraire
AchR que les polymères de l'invention. Ce résultat indique que l'architecture
moléculaire du groupe hydrophobe peut jouer un rôle important dans les
amphipols de
l'invention.
[00140] A noter que les amphipols de l'invention sont également
particulièrement plus
efficaces à solubiliser la pompe sodium potassium des membranes des organes
électriques de T. marmorata que A8-50 ou A8-35.
[00141] A une plus
faible concentration en polymère, les amphipols de l'invention
s'avèrent là aussi plus efficaces à solubiliser AchR ou la pompe sodium
potassium que
A8-35, A8-50 et SMA 3-1 (données non présentées).
5. Exemple 5, Etude de l'effet stabilisateur des amphipols sur les protéines
membranaires après extraction directe de la membrane
[00142]
L'effet stabilisateur des amphipols selon l'invention vis à vis de la BR a été
testé
directement après solubilisation de la membrane pourpre sans avoir recours aux
étapes de solubilisation par l'OTG, puis échange de l'OTG par les amphipols.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
44
Deux séries d'expérimentations indépendantes ont été effectuées. Les résultats
de la
première sont présentés figures 5A et B. Pour la deuxième série
d'expérimentation
chaque condition a été réalisée au minimum en triplicats (Figure 6).
Matériel et méthodes
[00143] Solubilisation de la membrane pourpre après fusion avec des vésicules
de
DMPC préformées.
i) Comme mentionné précédemment, la membrane pourpre a été fusionnée à des
vésicules de DMPC selon le protocole décrit par Orwick-Rydmark et al. (2012)
avant d'initier l'étape de solubilisation avec les amphipols. Après 24 heures
d'incubation à température ambiante, les échantillons ont été centrifugés à
100000x g pendant 20 min. Les surnageants ont été séparés du culot.
ii) L'absorbance à 554 nm (qui reflète la quantité de BR native) des
surnageants est
mesurée. La quantification de l'efficacité de solubilisation a été faite en
reportant
cette valeur sur celle mesurée avant centrifugation (Figure 5A, barres grises
de la
Figure 6A). On obtient ainsi le pourcentage de BR native solubilisée dans le
surnageant.
[00144] Evaluation de la stabilité de la BR.
Après solubilisation, les échantillons ont été incubés à 50 C pendant 6h puis
l'absorbance
à 554 nm est mesurée. Les valeurs d'absorbance ont été normalisées sur la
valeur de
l'absorbance initiale mesurée avant incubation (Figure 5B et figure 6B). Les
barres noires
de la Figure 6A correspondent à la quantité de BR stable, normalisée par
rapport à la
quantité initiale de BR avant centrifugation (Le avant l'étape de
solubilisation). Pour suivre
la cinétique de dénaturation de la BR, cette expérience a été répétée en
mesurant toutes
les heures l'absorbance à 554 nm des échantillons (Figure 6B).
[00145] Lorsque l'on compare les polymères de référence, Le. l'A8-35 et les
deux SMAs,
le pouvoir solubilisateur des SMAs est corrélé à un faible pouvoir
stabilisateur de la
BR. A l'inverse, l'A8-35 qui solubilise peu la BR la stabilise efficacement
(Figures 5A
et B et Figure 6A).
[00146] Les polymères
de l'invention testés permettent de solubiliser la BR aussi
efficacement que le SMA (3:1) tout en stabilisant la protéine au moins aussi
efficacement que l'A8-35 (comparer les absorbances pour les composés 19 et 23
avec
les polymères de référence, Figures 5 A et B et Figure 6).
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
6. Conclusion
[00147] Ainsi, les données expérimentales fournies montrent que les nouveaux
amphipols de la présente invention constituent de nouveaux polymères
5 particulièrement avantageux. En effet, la purification de protéines
membranaires
nécessite de les solubiliser tout en préservant leur conformation et leur
stabilité, ces
deux étapes peuvent sembler antinomiques, la solubilisation impliquant
notamment
l'utilisation de tensioactifs au pouvoir dissociant qui généralement
conduisent au cours
du temps à la dénaturation au moins partielle des protéines membranaires.
Basés sur
10 des protéines membranaires modèles, les résultats montrent que les
nouveaux
amphipols de l'invention présentent des propriétés de solubilisation
intéressantes pour
la purification des protéines membranaires, tout en préservant la stabilité de
ces
protéines et donc leur conformation et leur activité biologique, ce qui est
essentiel pour
leur étude ou leur utilisation dans des applications biotechnologiques et non
observé
15 avec les polymères de l'art antérieur. En outre, les polymères de
l'invention sont
efficaces également à de faibles concentrations, ce qui est particulièrement
avantageux pour ces applications.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
46
REFERENCES
Angius F, Ilioaia 0, Amrani A, Suisse A, Rosset L, Legrand A, Abou-Hamdan A,
Uzan M,
Zito F, Miroux B. (2018) A novel regulation mechanism of the T7 RNA polymerase
based
expression system improves overproduction and folding of membrane proteins.
Sci Rep.. 8,
8572.
Champeil, P., Guillain, F., Vénien, C., Gingold MP. (1985). Interaction of
magnesium and
inorganic phosphate with calcium-deprived sarcoplasmic reticulum
adenosinetriphosphatase
as reflected by organic solvent induced perturbation. Biochemistry 24(1), 69-
81.
Champeil, P., Menguy, T., Tribet, C., Popot, J.-L. and le Maire, M. (2000).
Interaction of
amphipols with the sarcoplasmic reticulum Ca2+-ATPase. J. Biol. Chem. 275,
18623-18637.
Drew, D., Newstead, S., Sonoda, Y., Kim, H., von Heijne, G., and lwata, S.
(2008). GFP-
based optimization scheme for the overexpression and purification of
eukaryotic membrane
proteins in Saccharomyces cerevisiae. Nat. Protoc. 3, 784-798.
Giusti, F., Rieger, J., Catoire, L., Qian, S., Calabrese, A. N., Watkinson, T.
G., Casiraghi,
M., Radford, S. E., Ashcroft, A. E. and Popot, J.-L. (2014). Synthesis,
characterization and
applications of a perdeuterated amphipol. J. Membr. Biol. 247, 909-924.
Gohon, Y., Giusti, F., Prata, C., Charvolin, D., Timmins, P., Ebel, C.,
Tribet, C. and Popot,
J.-L. (2006). Well-defined nanoparticles formed by hydrophobic assembly of a
short and
polydisperse random terpolymer, amphipol A8-35. Langmuir 22, 1281-1290.
Knowles, T. J., Finka, R., Smith, C., Lin, Y.-P., Dafforn, T. and Overduin, M.
(2009).
Membrane proteins solubilized intact in lipid containing nanoparticles bounded
by styrene
maleic acid copolymer. J. Am. Chem. Soc. 131, 7484-7485.
Laemmli, U. K. (1970) Cleavage of structural proteins during the assembly of
the head of
bacteriophage T4. Nature 227, 680-685.
Le Bon, C., Popot, J.-L. and Giusti, F. (2014). Labeling and functionalizing
amphipols for
biological applications. J. Membr. Biol. 247, 797-814.
Orwick-Rydmark, M., Lovett, J. E., Graziadei, A., Lindholm, L., Hicks, M. R.
and Watts, A.
(2012). Detergent-free incorporation of a seven-transmembrane receptor protein
into
nanosized bilayer Lipodisq particles for functional and biophysical studies.
Nano Lett. 12,
4687-4692.
Date Reçue/Date Received 2021-06-01
CA 03121693 2021-06-01
47
Oesterhelt & Stoeckenius (1971). Rhodopsin-like Protein from the Purple
Membrane of
Halobacterium halobium. Nat. New Biol. 233, 149-152.
Pierre Y, Breyton C, Kramer D, Popot JL. (1995). Purification and
characterization of the
cytochrome b6 f complex from Chlamydomonas reinhardtii. J Biol Chem.;270,
29342-9.
Sobel A, Weber M, Changeux JP. (1977) Large-scale purification of the
acetylcholine-
receptor protein in its membrane-bound and detergent-extracted forms from
Torpedo
marmorata electric organ. Eur. J. Biochem. 80, 215-224.
Zoonens M & Popot J-L. Amphipols for each season, J Membr Biol. 2014, 247:759-
96.
Date Reçue/Date Received 2021-06-01