Une partie des informations de ce site Web a été fournie par des sources externes. Le gouvernement du Canada n'assume aucune responsabilité concernant la précision, l'actualité ou la fiabilité des informations fournies par les sources externes. Les utilisateurs qui désirent employer cette information devraient consulter directement la source des informations. Le contenu fourni par les sources externes n'est pas assujetti aux exigences sur les langues officielles, la protection des renseignements personnels et l'accessibilité.
L'apparition de différences dans le texte et l'image des Revendications et de l'Abrégé dépend du moment auquel le document est publié. Les textes des Revendications et de l'Abrégé sont affichés :
| (12) Brevet: | (11) CA 2061196 |
|---|---|
| (54) Titre français: | L'ACETYLSALICYLOYL-L-CARNITINE ET PROCEDE POUR SA PREPARATION |
| (54) Titre anglais: | ACETYLSALICYLOYL L-CARNITINE AND PROCESS FOR ITS PREPARATION |
| Statut: | Périmé et au-delà du délai pour l’annulation |
| (51) Classification internationale des brevets (CIB): |
|
|---|---|
| (72) Inventeurs : |
|
| (73) Titulaires : |
|
| (71) Demandeurs : |
|
| (74) Agent: | G. RONALD BELL & ASSOCIATES |
| (74) Co-agent: | |
| (45) Délivré: | 2002-05-14 |
| (22) Date de dépôt: | 1992-02-13 |
| (41) Mise à la disponibilité du public: | 1993-08-14 |
| Requête d'examen: | 1998-09-04 |
| Licence disponible: | S.O. |
| Cédé au domaine public: | S.O. |
| (25) Langue des documents déposés: | Anglais |
| Traité de coopération en matière de brevets (PCT): | Non |
|---|
| (30) Données de priorité de la demande: | S.O. |
|---|
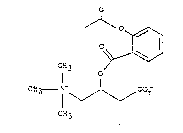
Novel 3-(2-acetoxybenzoyloxy)-4-
(trimethylammonio)-butyric acid betaine and its
pharmaceutically acceptable salts are disclosed. The
compounds are distinguished by high water solubility,
minimum toxicity and good gastric tolerance vis-a-vis
acetylsalicylic acid and can be prepared by acetylating the
corresponding salicylic acid ester of the carnitine.
Note : Les revendications sont présentées dans la langue officielle dans laquelle elles ont été soumises.
Note : Les descriptions sont présentées dans la langue officielle dans laquelle elles ont été soumises.
2024-08-01 : Dans le cadre de la transition vers les Brevets de nouvelle génération (BNG), la base de données sur les brevets canadiens (BDBC) contient désormais un Historique d'événement plus détaillé, qui reproduit le Journal des événements de notre nouvelle solution interne.
Veuillez noter que les événements débutant par « Inactive : » se réfèrent à des événements qui ne sont plus utilisés dans notre nouvelle solution interne.
Pour une meilleure compréhension de l'état de la demande ou brevet qui figure sur cette page, la rubrique Mise en garde , et les descriptions de Brevet , Historique d'événement , Taxes périodiques et Historique des paiements devraient être consultées.
| Description | Date |
|---|---|
| Le délai pour l'annulation est expiré | 2011-02-14 |
| Lettre envoyée | 2010-02-15 |
| Accordé par délivrance | 2002-05-14 |
| Inactive : Page couverture publiée | 2002-05-13 |
| Inactive : Taxe finale reçue | 2002-02-20 |
| Préoctroi | 2002-02-20 |
| Un avis d'acceptation est envoyé | 2001-08-27 |
| Lettre envoyée | 2001-08-27 |
| Un avis d'acceptation est envoyé | 2001-08-27 |
| Inactive : Approuvée aux fins d'acceptation (AFA) | 2001-08-09 |
| Modification reçue - modification volontaire | 2000-12-28 |
| Inactive : Dem. de l'examinateur par.30(2) Règles | 2000-09-05 |
| Modification reçue - modification volontaire | 1998-11-27 |
| Lettre envoyée | 1998-09-25 |
| Inactive : Dem. traitée sur TS dès date d'ent. journal | 1998-09-22 |
| Inactive : Renseign. sur l'état - Complets dès date d'ent. journ. | 1998-09-22 |
| Toutes les exigences pour l'examen - jugée conforme | 1998-09-04 |
| Exigences pour une requête d'examen - jugée conforme | 1998-09-04 |
| Demande publiée (accessible au public) | 1993-08-14 |
Il n'y a pas d'historique d'abandonnement
Le dernier paiement a été reçu le 2002-01-25
Avis : Si le paiement en totalité n'a pas été reçu au plus tard à la date indiquée, une taxe supplémentaire peut être imposée, soit une des taxes suivantes :
Les taxes sur les brevets sont ajustées au 1er janvier de chaque année. Les montants ci-dessus sont les montants actuels s'ils sont reçus au plus tard le 31 décembre de l'année en cours.
Veuillez vous référer à la page web des
taxes sur les brevets
de l'OPIC pour voir tous les montants actuels des taxes.
| Type de taxes | Anniversaire | Échéance | Date payée |
|---|---|---|---|
| TM (demande, 6e anniv.) - générale | 06 | 1998-02-13 | 1998-02-02 |
| Requête d'examen - générale | 1998-09-04 | ||
| TM (demande, 7e anniv.) - générale | 07 | 1999-02-15 | 1999-02-01 |
| TM (demande, 8e anniv.) - générale | 08 | 2000-02-14 | 2000-01-20 |
| TM (demande, 9e anniv.) - générale | 09 | 2001-02-13 | 2001-01-16 |
| TM (demande, 10e anniv.) - générale | 10 | 2002-02-13 | 2002-01-25 |
| Taxe finale - générale | 2002-02-20 | ||
| TM (brevet, 11e anniv.) - générale | 2003-02-13 | 2003-01-27 | |
| TM (brevet, 12e anniv.) - générale | 2004-02-13 | 2004-01-29 | |
| TM (brevet, 13e anniv.) - générale | 2005-02-14 | 2005-01-20 | |
| TM (brevet, 14e anniv.) - générale | 2006-02-13 | 2006-01-24 | |
| TM (brevet, 15e anniv.) - générale | 2007-02-13 | 2007-01-30 | |
| TM (brevet, 16e anniv.) - générale | 2008-02-13 | 2008-01-31 | |
| TM (brevet, 17e anniv.) - générale | 2009-02-13 | 2008-12-18 |
Les titulaires actuels et antérieures au dossier sont affichés en ordre alphabétique.
| Titulaires actuels au dossier |
|---|
| LONZA LTD. |
| Titulaires antérieures au dossier |
|---|
| THOMAS MEUL |