Note : Les descriptions sont présentées dans la langue officielle dans laquelle elles ont été soumises.
2096~88
La présente invention concerne un procédé de fabrication de `
chlorate de métal alcalin par électrolyse dans une cellule à membrane sans
adjonction de chrome.
La préparation de chlorate de métal alcalin par électrolyse dans
5 une cellule à membrane est décrite en particulier dans les demandes de
brevet FR-A-2 638 76~ et FR-A-2 655 061.
Les cellules à membrane sont généralement constituées de deux
compartiments, I'un anodique, I'autre cathodique, séparés par une
membrane qui permet le transfert sélectif d'ions d'un compartiment à un
10 autre, sous l'action d'un champ électrique.
Pour la préparation connue de chlorate de métal alcalin,
I'anolyte est constitué par une saumure de sel de chlorure dudit métal
alcalin, à laquelle peut être ajoutée, le cas échéant, une quantité
déterminée de chlorate du même métal alcalin, le catholyte étant pour sa
15 part constitué par une solution d'hydroxyde de métal alcalin.
Ce procédé de préparation de chlorate de métal alcalin
présente de nombreux avantages par rapport à la technique antérieure qui
nécessitait l'emploi d'additifs coûteux et dan~ereux pour l'environement, en
particulier du chrome hexavalant, chromate ou bichromate de sodium, pour
20 limiter l'influence néfaste de la réduction cathodique des ions hypochlorites et/ou chlorates.
Néanmoins, et malgré ce net progrès, les cellules à membranes
nécessitent l'emploi d'électrolytes particulièrement exempts d'impuretés.
En effet, la saumure de sel de chlorure de métal alcalin qui
25 alimente le compartiment anodique de la cellule, contient de faibles
quantités de sels métalliques, particulièrement de sels de métaux
alcalino-terreux, de métaux tels que l'aluminium, le cuivre, le manganèse
ou le zinc, ou d'impuretés telles que la silice, les sels de sulfate, le brome
ou l'iode qui risquent de détériorer ou de colmater la membrane lors de
30 I'électrolyse.
Il s'avère donc nécessaire de purifier la saumure avant son
introduction dans le compartiment anodique de la cellule, de manière à
abaisser les teneurs en impuretés à des niveaux acceptables.
':
6~8
Si les techniques usuelles de purification des saumures de sels
de chlorure, par précipitation et/ou absorption sur résine, permettent
d'abaisser les teneurs de certaines impuretés, notamment les sels de
calcium et de magnésium, il n'existe pas de procédé industriel permettant
5 de réduire la teneur d'éléments, tels que le silicium, I'aluminium ou
d'autres métaux à quelques ppm voire quelques ppb.
La présente invention concerne donc un procédé de préparation
de chlorate de métal alcalin par électrolyse dans une cellule à membrane,
d'un anolyte comprenant une solution de chlorure de métal alcalin et d'un
10 catholyte comprenant une solution d'hydroxyde de métal alcalin, la solution
de chlorure de métal alcalin étant obtenue à partir d'une saumure
préalablement purifiée de manière à éliminer la quasi totalité des
impuretés qui risqueraient de détériorer ou de colmater la membrane lors
de l'électrolyse.
Selon la présente invention, la purification de la saumure est
obtenue par la succession d'étapes suivantes:
- électrolyse dans une cellule de type "chlore-soude" d'une
saumure de chlorure de métal alcalin pour former d'une part du chlore
gazeux, et d'autre part une solution concentrée d'hydroxyde de métal
20 alcalin,
- transfert du chlore gazeux et de la solution d'hydroxyde de
métal alcalin produits, dans une colonne d'abattage, pour les faire réagir
l'un sur l'autre, et
- récupération de la solution saline ainsi obtenue, pour son
25 emploi comme anolyte dans la cellule à membrane.
La cellule de type "chlore-soude" employée dans le procédé
selon l'invention est de préférence une cellule à membrane. ;
- Ce type de cellule est bien connu dans l'art antérieur, puisque
décrit notamment dans le brevet US-A-I~ 285 795 ou dans "Ullmann's
30 Encyclopedia of Industrial Chemistry" (5eme édit., Vol. A6, p. 39g-481).
Les membranes sont des membranes synthétiques échangeuses
d'ions, préférentiellement en polymères fluorocarbonés susceptibles de
résister à des conditions opératoires drastiques, en particulier à des
solutions alcalines fortes, à de hautes températures.
,~' .
2~6~8~
A ces polymères flurocarbonés sont associés de fonctions acides
carboxyliques et/ou sulfoniques, préférentiellement sous la forme d'un sel
de métal alcalin. D'une manière préférentielle, les polymères fluoro-
carbonés sont des polytétrafluoroéthylènes (PTFE). Les membranes
employées sont obtenues par extrusion ou laminage du polymère, et
peuvent être renforcées par des pièces tissées de fibres de PTFE. -
Les membranes, développées depuis 1970, ont une sélectivité au
moins égale à celle des diaphragmes mais sont beaucoup plus sensibles aux
dégradations et aux colmatages dues aux impuretés présentes dans
1 0 l~électrolyte.
De manière à préserver la durée de vie des membranes, dans le
procédé selon l'invention, la saumure de chlorure de métal alcalin est
généralement prépurifiée par des méthodes classiques de précipitation
et/ou d'adsorption sur résines.
La saumure de métal alcalin employée comme anolyte dans la
cellule de type "chlore-soude" comprend de préférence en~re 170 et 315 g/l
de chlorure de métal alcalin, de préférence entre 290 et 310 g/l.
Par ailleurs, cette saumure est employée de préférence à un pH
compris entre 2 et 7, avantageusement entre 2,5 et 4,5.
La réaction globale effectuée dans la cellule électrolyse de
type "chlore-soude" peut se résumer par l'équation A suivante:
(A) 2 MeCI + 2 H2O ~ 2 MeOH + C12+H2
avec Me représentant un métal alcalin.
Cette réaction met en jeu le transfert de deux électrons pour
deux molécules de chlorures de métal alcalins impliquées.
Au cours de l'électrolyse, le chlore gazeux est produit dans le
compartiment anodique (2CI ~ C12+2e ), et l'hydrogène gazeux dans le
compartiment cathodique (2H2O+2e ~ 20H +H2).
Dans le même temps, sous l'action du champ électrique, les
deux ions de métal alcalin correspondant au chlore généré sont transférés
au travers de la membrane, du compartiment anodique vers le compartiment
~096~8~
cathodique de la cellule de type "chlore-soude" pour équilibrer la charge
électrique due à la production simultanée de deux anions hydroxyles.
La formation de chlore dans le compartiment anodique
s'accompagne donc d'une baisse de concentration en chlorure de métal
5 alcalin dans l'anolyte simultanément à un enrichissement en hydroxyde
métal alcalin du compartiment cathodique.
Après son électrolyse, la saumure appauvrie en chlorure de
métal alcalin est évacuée de la cellule de type "chlore-soude". On peut
donc envisager de recycler cette saumure appauvrie par l'ajout de chlorure
10 de métal alcalin.
Avantageusement, la solution d'hydroxyde de métal alcalin
obtenue par l'électrolyse a une concentration comprise entre 10 et 55% en
poids, de préférence entre 30 et 50% en poids.
Par le procédé selon l'invention, le chlore gazeux et la solution
5 d'hydroxyde produits sont exempts d'impureté détectable.
Ils sont alors transférés dans une colonne d'abattage pour les
faire réagir l'un sur l'autre.
La réaction dans la colonne d'abattage peut se résumer par
I'équation B suivante:
(B) 6 MeOH + 3C12 ~ 3 MeCI + 3 MeClO + 3 H2O,
Me étant défini précédemment.
L'hypoc:hlorite obtenu va alors se dismuter d'une part en
25 chlorure, et d'autre part en chlorate de métal alcalin selon l'équation C
cl-apres:
(C) 3 MeClO ~ 2 MeCI + MeClO3,
30 Me étant défini précédemment.
La solution saline obtenue en sortie de la colonne d'abattage ;
comprend entre 50 et 200 g/l de chlorure de métal alcalin et entre 30 et
700 g/l de chlorate de métal alcalin. Avantageusement, cette solution
:;' .
. .
2096~88
saline comprend entre 70 et 170 g/l de chlorure et entre 400 et 650 g/l de
chlorate de métal alcalin.
Afin de favoriser la dismutation de l'hypochlorite, la solution
saline avant son emploi comme anolyte dans la cellule à membrane peut
être avantageusement transférée dans un bac d'évolution pour un temps de
séjour prolongé, à un pH compris entre 6 et 8, de préférence entre 6,5 et 7.
Elle comprend alors moins de 5 g/l d'hypochlorite de métal
alcalin, de préférence moins d' 1 g/l.
Dans le procédé de préparation de chlorate selon la présente
0 invention, la solution saline obtenue par le procédé de purification décrit
précédemment, est alors employée comme anolyte dans la cellule à
membrane à un pH compris entre 1 et 8, préférentiellement entre 2 et 5, et
à une température comprise entre 50 et 100C, d'une manière avantageuse
entre 70 et 90C.
De manière préférée, après son électrolyse, une partie de
l'anolyte est recyclée dans la colonne d'abattage.
Avantageusement, la solution d'hydroxyde de métal alcalin,
obtenue par électrolyse dans la cellule à membrane, a une concentration
comprise entre 10 et 55% en poids et de préférence entre 30 et 50% en
poids. Elle est également transférée dans la colonne d'abattage.
Lors de l'électrolyse dans la cellule à membrane, du chlore
gazeux est également produit dans le compartiment anodique.
Ce chlore est alors tranféré dans la colonne d'abattage,
avantageusement en mélange avec le chlore gazeux produit lors de
I'électrolyse de type "chlore-soude".
On peut donc définir une boucle anodigue constituée par le
compartiment anodique de la cellue à membrane et la colonne d'abattage,
les produits en solution de l'électrolyse de la cellule à membrane étant
transférés dans la colonne d'abattage et inversement la solution obtenue en
sortie de la colonne d'abattage étant employée comme anolyte dans la
cellule à membrane.
Au cours du procédé selon la présente invention, on atteint
rapidement un état stationnaire où les différentes solutions, en sortie de
,
:
.
2~96~88
la colonne d'abattage ou en sortie du compartiment anodique de la cellule
à membrane ont une composition constante.
L'anolyte contient entre 50 et 200 ~/1 de chlorure de métal
alcalin et de préférence entre 70 et 170 g/l. Ia concentration en chlorate
5 sortie de la cellule à membrane nécessaire pour que celui-ci soit isolable
directement par cristallisation, est aisément déterminée à partir des
diagrammes de cristallisation connus des systèmes eau-chlorure-chlorate
(thèse de A. NALLET, faculté des Sciences de l'Université de Lyon, N
d'ordre 209, soutenue le 19 janvier 1955). Elle est par exemple comprise
10 entre 400 et 650 g/l d'anolyte.
Ainsi, selon la présente invention, une partie de l'anolyte après
son électrolyse est transférée dans un cristallisoir ou le chlorate est laissé
à cristalliser, les eaux mères étant récupérées et recyc~ées dans la boucle
anodique de la cellule à membrane. ~ -
15On peut également, d'une manière facultative, envoyer l'anolyte
dans un bac d'évolution avant son transfert vers le cristalliso;r.
Le métal alcalin employé dans le procédé selon l'invention, est
choisi parmi le lithium, le sodium et le potassium, de préférence le sodium.
La présente invention concerne également un dispositif pour la
20préparation d'un chlorate de métal alcalin, mettant en oeuvre le procédé
décrit précédemment, comprenant la combinaison d'une cellule de type
"chlore-soude" pour la préparation de chlore gazeux et d'hydroxyde de
métal alcalin, d'une colonne d'abattage du chlore par un hydroxyde de
métal alcalin, et une cellule à membrane pour l'électrolyse d'un anolyte
25comprenant une solution de chlorure de métal alcalin et d'un catholyte
comprenant une solution d'hydroxyde de métal alcalin.
D'autres caractéristiques du dispositif selon la présente
invention apparaîtront à la lecture de la description détaillée faite
ci-après, en référence aux dessins annexés dans lesquels: ~
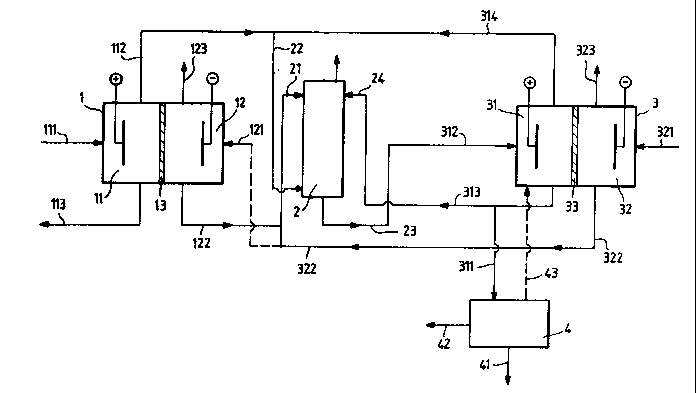
30_ la figure I représente un diagramme général de dispositif de - -
mise en oeuvre du procédé selon la présente invention,
- la figure 2 représente une réalisation préférentielle du
dispositif de purification de la saumure de sel de métal alcalin.
.. :'
' .'' ,: ,
.
. .
2096~g8
La figure 1 montre un dispositif, employé d'une manière
préférentielle, et dans lequel la cellule de type "chlore-soude" (1) est une
cellule à membrane, comprenant un ou plusieurs compartiments anodiques
(Il) séparés du ou des compartiments cathodiques (12) correspondant par
5 une membrane (13), le ou les compartiments anodiques comprenant chacun
un dispositif approprié d'admission (111) et de récupération (113) de
l'anolyte et un dispositif approprié de récupération du chlore gazeux (112), .
Ie ou les compartiments cathodiques (12) comprenant chacun un dispositif
approprié d'admission (121) et de récupération (122) du catolyte et un
10 dispositif approprié d'évacuation de l'hydrogène gazeux (123).
La colonne d'abattage (2) comprend au moins un dispositif
approprié d'admission d'une solution d'hydroxyde de métal alcalin (21) en
provenance de la cellule de type "chlore-soude", un dispositif approprié
d'admission du chlore gazeux (22) et de préférence un dispositif d'admission
15 (24) d'une solution saline pauvre en chlorure et un dispositif approprié (23) de récupération de la solution saline obtenue.
La cellule à membrane (3) comprend comme la cellule de type
"chlore-soude" (I) un ou plusieurs compartiments anodiques (31) séparés du
ou des compartiments cathodiques (32) correspondant par une membrane
20 (33), le ou les compartiments anodiques comprenant chacun un dispositif
approprié d'admission (312) de la solution saline, un dispositif approprié de
récupération du chlore gazeux (314) et un dispositif de récupération de la
solution saline après son électrolyse (311).
Le ou les compartiments cathodiques (32) de cette cellule à
25 membrane (3) comprennent quant à eux un dispositif approprié d'admission
(321) d'eau, un dispositif approprié de récupération (322) du catholyte après
son électrolyse et un dispositif approprié d'extraction de l'hydrogène (323).
- Selon l'invention, le dispositif approprié de récupération (313)
de l'anolyte de la cellule à membrane (3) est relié à un dispositif approprié
30 d'introduction de cet anolyte (24) dans la colonne d'abattage (2).
De mëme, le dispositif d'extraction (314) du chlore gazeux est
également relié à la colonne d'abattage par l'intermédiaire du dispositif
. approprié d'admission (22) du chlore gazeux.
:
~ .
~096~88
Enfin, le compartiment anodique (31) de la cellule à membrane
(3) est relié soit directement par un moyen approprié, soit par le dispositif
de récupération de la solution saline après son électrolyse (311) à un
cristallisoir (4).
D'une manière av~ntageuse, le cristallisoir comprend un
dispositif approprié de récupération des eaux mères (43) relié au
compartiment anodique (31 ) de la cellule à membrane (3). Dans une
variante du dispositif selon l'invention, les eaux mères peuvent être
renvoyées au niveau de la boucle anodique définie précédemment.
Lorsque l'on reprend le bilan global des réactions de la cellule
"chlore-soude" (A) et de la colonne d'abattage (B + C), on obtient l'équation
générale D suivante:
3xA6 MeCI + 6H20 ~6 MeOH + 3 Cl;~ + 3 H2
B6 MeOH + 3 C12 ~3 MeCI + 3 MeClO + 3 H2O
C3 MeClO ~2 MeCI + MeClO
6F
D 6 MeCI + 3 H2O ~ 5 MeCI + MeClO3 ~ 3 H2
Me étant défini précédemment, et F représentant un Faraday.
Le chlorate de métal alcalin obtenu entrant dans le bilan final
de la préparation de chlorate selon l'invention, on peut donc considérer
qu'il ne s'agit pas d'une impureté.
En conséquence, la combinaison d'une électrolyse de type
"chlore-soude" avec une colonne d'abattage du chlore par la soude peut
être considérée comme une étape de purification d'une saumure de métal
alcalin.~
De fait, la solution de chlorure obtenue est quasiment exempte
30 de toute impureté. Une telle combinaison électrolyse-colonne d'abattage
apparaît d'une manière inattendue comme le seul procédé industriel
permettant d'éviter l'ensemble des impuretés, néfastes au bon fonction-
nement des membranes, que sont le calcium, le magnésium, le strontium, le
, ,,~ . '
.
2096~88
baryum, I'iode, le brome, l'aluminium, la silice, le sulfate, le fer, le
manganèse, le cuivre, etc.
En conséquence, la présente invention concerne également un
dispositif de purification d'une saumure de chlorure de métal alcalin,
5 comprenant la combinaison d'une cellule à électrolyse de type "chlore-
soude" (1) et d'une colonne d'abattage (2) du chlore par la soude.
La figure 2 montre une cellule de type "chlore-soude" (1) à
membrane, constituée d'un ou plusieurs compartiments anodiques (I l)
séparés du ou des compartiments cathodiques (12) correspondant par une
10 membrane (13), le ou les compartiments anodiques comprenant chacun un
dispositif approprié d'admission (111) et de récupération (113) de l'anolyte
et un dispositif approprié de récupération du chlore gazeux (112), et le ou
les compartiments cathodiques (12) comprenant chacun un dispositif
approprié d'admission (121) et de récupération (122) du catholyte, et un
5 dispositif approprié d'évacuation de l'hydrogène gazeux (123). La colonne
d'abattage (2) comprend au moins un dispositif approprié d'admission d'une
solution d'hydroxyde de métal alcalin (21), un disposi~if approprié
d'admission (22) de chlore gazeux, et un dispositif approprié de récupéra-
tion ~23) d'une solution purifiée de chlorure de métal alcalin, les dispositifs
20 d'admission d'hydroxyde (21) et de chlore (22) étant respectivement reliés
directement aux dispositifs de récupération du catholyte (122) et de chlore
gazeux (112) de la cellule de type "chlore-soude" (1).
D'une manière avantageuse, on peut ajouter au dispositif de
purification selon l'invention, un bac d'évolution relié directement au5 dispositif de récupération (23) de la solution purifiée de métal alcalin.
Les exemples suivants permettront d'illustrer les différentes
étapes du procédé selon l'invention.
30 EXEMPLE 1: Purification de la saumure
Une cellule, "chlore-soude" (1) équipée d'une membrane (13) N
2096388
90209 (commercialisée sous la marque NAFION par la société DU PONT)
produit sous 30 A/dm~, 19 g/h de C12 et de la soude à 32%.
Pendant 4h le chlore est récupéré au pied d'une colonne
d'abattage (2) montée au-dessus d'un réservoir thermostaté à 50OC qui
contient 0,5 I d'eau. Une mesure de pH, permet de réguler l'addition de
soude à 32% pour abattre le chlore et maintenir le pH entre 6,5 et 7.
Environ 269 g de soude à 32% ont été nécessaire pour abattre
tout le chlore.
En final on récupère dans le réacteur une solution contenant
10 12,3% en poids de NaCI et 4,5% en poids de NaClO3 à 50C. La teneur des
différentes impuretés est en-dessous des limites de détection (Ca, Mg, Sr,
Ba, Si, Al, Mn, Fe, Cu, Zn, Pb~: 50 ppb et SO4~< 1 ppm)
EXEMPLE 2 : Influence du bac d'évolution
On reprend le dispositif opératoire décrit dans l'exemple 1,
associé à une cellule à membrane (3).
L'anolyte de l'électrolyseur à membrane (3) contient 120 à 150
20 g/l de NaCI et 450 à 500 g/l de NaClO3.
La soude du catholyte est à 32% en poids et la température à
90C. La tension aux bornes de l'électrolyseur est comprise entre 3,7 et 3,8 ~;
V à 30 A/dm .
Le chlore produit par la cellue à membrane (3) et la cellule
25 "chlore-soude" (1) est abattu dans la colonne (2). ;
La teneur en hypochlorite de sodium de la solution récupérée
en sortie de la colonne d'abattage (2) est de 7,5 à 8 g/l. Après son transfert ;
dans u~ bac d'évolution maintenu à 70C, la teneur en hypochlorite de : '
sodium est de I à 2 g/l. Le pH est régulé à 6,5 par addition de soude.
:
Le bilan réactionnel dans la cellule à membrane (3) peut se
résumer par l'équation générale E suivante: ;
5 MeCI + MeClO3 + 15H2O ~ 6 MeClO3 + 15H2
:
2096~88
Me étant définie précédemment et met en jeu le transfert de 30
électrons.
Le bilan global D+E du procédé de préparation du chlorate de
métal alcalin selon l'invention peut donc se résumer par l~équation F
5suivante:
6F
D 6 MeCI ~ 3H2O ~ 5 MeCI + MeClO3 + 3 H2
30F
E 5 MeCI + MeClO3 t 15 H2O t 6 MeClO3 + 15 H2
36F
F 6 MeCI + 18 H2O ~ 6 MeClO3 + 18 H2
Me et F etant défini précédemment.
On remarquera que seulement 1/6 du transfert électronique
total est effectué dans la cellule de type "chlore-soude" (1), alimentée en
saumure brute ou prépurifiée par des techniques usuelles, et 5/6 de ce
transfert dans la cellule à membrane (3).
Les produits (C12 et solution d'hydroxyde de métal alcalin)
passant de la cellule "chlore-soude" (I) à l'étape suivante sont très purs et
constituent ainsi en sortie de la colonne d'abattage (2) une saumure très
pure entrant dans la cellule à membrane (3). Cette cellule (3) et sa
membrane (33) vont donc fonctionner dans de très bonnes conditions qui
25 prolongeront la durée de vie (fortement influencée par la teneur en
impuretés de l'électrolyte) de la membrane. Ainsi 5/6 du chlorate produit
le sont dans de très bonnes conditions pour la durée de vie des membranes
dont le coût est élevé.
D'autre part, au point de vue bilan eau, le procédé habituel de
30 production de chlorate de sodium nécessite l'introduction de 1 563 kg d'eau
par tonne de NaClO3, associée au chlorure de sodium alimenté sous forme
de saumure contenant 26% en poids de NaCI.
Dans le procédé exposé, la cellule (3) est alimentée par un flux
.~ :
.:
,
20965~8 ::
issu de la réaction entre le chlore et la solution aqueuse à 33% en poids de
soude. Ceci n'induit globalement l'introduction que de 719 k~ d'eau par
tonne de NaClO3 produit. Il y a donc une économie de 844 kg d'eau qu'il
serait nécessaire d'évaporer dans une installation où le chlorate de sodium
5 sort à l'état solide, c'est-à-dire où toute quantité d'eau entrante doit être
evaporee.
.