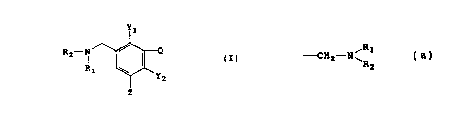Note : Les descriptions sont présentées dans la langue officielle dans laquelle elles ont été soumises.
CA 02297803 2000-O1-25
WO 99/05089 PCTIFR98101629
1
NOUVELLES N-ALiCYL-HYDROXYHENZYLAMINES,
LEUR PROCÉDÉ DE PRÉPARATION, LEURS APPLICATIONS
ET COMPOSITIONS LES CONTENANT
L'invention a pour objet de nouvelles N-alkyl-
hydroxybenzylamines.
Elle vise également un procédé de préparation de ces
N-alkyl-hydroxybenzylamines ainsi que leurs applications
dans les traitements des surfaces métalliques tant contre la
corrosion qu'en faveur d'une amélioration ultérieure
d'adhérence des peintures, et les compositions gui en
contiennent à titre de substance active.
On a déjà proposé d'utiliser dans la lutte contre la
corrosion des surfaces métalliques
- des polymères de structure polyvinylphénol
(document EP-0-091 166),
- des copolymères de condensation des
polyvinylphénols précédents avec des résines formol-phénol,
des tannins et des lignines (document EP-0 319 017 B1),
- des polyvinylphénols substitués (document US-A-
4 978 399),
- des poly-ortho-méthylène-phénols substitués
(document WO 95/28449),
- des poly-ortho-méthylène-bisphénols substitués
(documents WO 95/28509, WO 97/04244 et WO 97/04145 et
- des molécules monomères comportant un noyau
phénolique mono- et bis-amino substitué (respectivement
décrits dans les documents EP-0 276 072 B1 et EP-0 517 356
B1 ) .
Les structures connues tant polymères que monomères
ne sont pas entièrement satisfaisantes, notamment du point
de vue de l'obtention, après traitement, de surfaces offrant
simultanément d'excellentes propriétés sur le plan de la
résistance contre la corrosion que du point de vue de
l'adhérence des peintures qui y sont appliquées.
CA 02297803 2000-O1-25
WO 99/05089 PCT/FR98101629
2
L'invention a donc pour but, surtout, de remédier
aux insuffisances de l'art antérieur et de fournir des
N-alkyl-hydroxybenzylamines plus efficaces que les produits
polymères et monomères déjà connus.
Et la Société Demanderesse a eu le mérite de mettre
au point de nouvelles N-alkyl-hydroxybenzylamines permettant
d'atteindre ce but.
Les nouvelles N-alkyl-hydroxybenzylamines conformes
à l'invention sont caractérisêes par le fait qu'elles
IO présentent la formule générale
Y1
(I)
R i '\~~
Y2
Z
dans laquelle
- R1 et R2, gui sont identiques ou différents l'un
de l'autre, représentent un atome d'hydrogène ou un radical
alkyle en C1 à Cg mono- ou polyhydroxylé, R1 et R2 ne
pouvant représenter simultanément chacun un atome
d'hydrogëne,
- Q représente un radical -OH ou -NH2,
- Z représente un atome d'hydrogène ou le
groupement
R
-CH2-N
R2
dans lequel R1 et R2 ont les significations indiquées plus
haut et
- YI et Y2 représentent un atome d'hydrogène ou le
radical -OH, Y1 et Y2 ne pouvant représenter simultanément
chacun un atome d'hydrogène.
Les molécules de formule (I) présentent une très
CA 02297803 2000-O1-25
WO 99/05089 PCT/F'R98101629
3
forte affinité à l'égard des surfaces métalliques; cette
affinité est due à leur pouvoir chélatant; ces molécules
forment un réseau de recouvrement sur les surfaces
métalliques favorisant tout aussi bien l'adhérence d'un
revêtement que celle d'une peinture de protection; de plus
et c'est là leur fonction principale, elles évitent toute
corrosion par oxydation du support.
En d'autres termes, l'invention vise donc également
l'utilisation des N-alkyl-hydroxybenzylamines de formule (I)
dans le traitement des surfaces métalliques tant contre la
corrosion qu'en faveur d'une amélioration ultérieure
d'adhérence des peintures.
De par leur structure interne de forme ortho
phénolique, ces molécules sont à la fois réductrices et
chélatantes du fer; elles limitent donc l'oxydation
métallique du support et plus particulièrement l'oxydation
du Fe(0) en Fe (II) et Fe (III). Elles remplacent donc
avantageusement les structures polymères connues qui
présentent toujours l'inconvénient d'être mal définies.
De plus, ces molécules ne dégradent pas le support
métallique par attaque chimique; elles préservent donc
l'intégrité de la pièce comportant la surface traitée.
Enfin et surtout, elles permettent de rempïacer les
traitements de phosphatation chromiques actuellement
utilisés.
Le procédé conforme à l'invention pour la
préparation des composés de formule (I) est caractérisé par
le fait que l'on a recours à une condensation de Mannich en
présence de formol d'une amine de formule:
H-N-R1
(II)
R2
dans laquelle R1 et R2 ont les significations indiquées plus
haut, sur un phénol réducteur de formule:
CA 02297803 2000-O1-25
WO 99/05089 PCT/FR98101629
4
Y1
(III)
Y2
dans laquelle Q, Y1 et Y2 ont les significations indiquées
plus haut,
le schéma réactionnel étant
Yi Yi
¿
~~Q Rz-N~~Q
H-N-R1, + mCH20 + ~ I -~-
- m H20 R1
Rz !~m Y2 Y2
Z
IO (II) (III) (I)
dans lequel m est égal à 1 ou 2 et représente la
stoechiométrie de formaldéhyde soit pour une
monosubstitution, Z représentant alors H, soit pour une
disubstitution, Z représentant alors le groupement
IS
~ ~ uRz
R1
Les produits de départ de formules (II) et (III) se
20 trouvent dans le commerce ou sont facilement accessibles par
voie de synthèse par des techniques bien connues de l'homme
du métier.
La susdite réaction de condensation peut être
conduite en présence d'un solvant organique inerte.
25 Le solvant organique inerte peut être
avantageusement choisi parmi les essences aliphatiques du
groupe comprenant l'hexane, l'heptane, l'octane, le nonane
et le dodécane, parmi les dérivés chlorés du groupe
*rB
CA 02297803 2000-O1-25
WO 99105089 PCTIFR98101629
comprenant le dichlorométhane, le 1,2-dichloroéthane, le
chloroforme, le trichloréthylène et le tétrachloréthylène,
parmi les dialkyl-éthers du groupe comprenant les diéthyl-
et dipropyl-éthers ainsi que les dibutyl-éthers, parmi les
5 polyalcoxy-alcanes, les polyalcoxy-alcools et les alcools,
les solvants préférés étant le benzène, le toluène et le
xylène.
La quantité de solvant utilisé lors de la réaction
n'est pas critique.
IO De préférence, la réaction est conduite en présence
d'un solvant formant un hétéro-azéotrope avec L'eau au
reflux de cet azéotrope; ainsi, l'eau formée par la réaction
est soustraite du milieu réactionnel au fur et à mesure de
sa formation. Cette technique permet d'obtenir une
IS productivité et une conversion accrues.
La réaction est conduite à des températures de 50 à
200°C, de préférence de 50 à 150°C et plus préféren-
tiellement encore de 50 à 100°C.
Elle peut être mise en oeuvre sous pression
20 atmosphérique comme sous pression autogène de formaldéhyde;
toutefois, de préférence, elle est conduite à pression
atmosphérique sous reflux de formaldéhyde.
Les quantités molaires de formaldéhyde mises en
oeuvre par rapport à l'amine de formule (II) peuvent varier
25 dans les rapports de 0,1 à 5; on utilise de préférence une
quantité de formaldéhyde de 0,5 à 2,5 moI/mol d'amine de
formule (II) et, plus préférentiellement encore, de 1 à
2 mol/mol.
Les quantités molaires de phénol de formule (III)
30 mises en oeuvre par rapport à l'amine de formule (II)
peuvent varier dans les rapports de 0,1 à 2; on utilise de
préférence une quantité de phénol de 0,4 à 1,5 mol/mol
d'amine et, plus préférentiellement encore, de 0,5 à
1 mol/mol.
35 La réaction peut être conduite en l'absence de
CA 02297803 2000-O1-25
WO 99/05089 PCT/FR98I01629
6
catalyseur ou en présence de catalyseurs; de préférence, on
opère en présence d'un catalyseur basique pouvant être
choisi parmi les amines tertiaires aliphatiques telles que
la triméthylamine, la méthyldiéthylamine ou la
triéthylamine, les anilines tertiaires comme la
diméthylaniline, la diéthylaniline ou les amines cycliques
telles que la pyridine ou encore les imidazoles; il est
également possible d'utiliser les bases alcalines telles que
la soude, la potasse ou la chaux.
I0 La quantité de catalyseur mise en oeuvre par rapport
à l'amine de formule (II) est de 0,1~ à 5~-mol de catalyseur
par mol d'amine.
Les conditions réactionnelles sont maintenues
pendant ure âurée nécessaire et suffisante pour atteindre un
taux de conversion de l'amine supérieur à 95~.
Grâce à leurs propriétés particulièrement
intéressantes, les N-alkyl-hydroxybenzylamines conformes à
l'invention peuvent être mises en oeuvre sous la forme de
compositions de protection contre la corrosion dans des
procédés ne faisant pas appel à un traitement chromique.
I1 s'ensuit que la composition inhibitrice de
corrosion conforme à l'invention est caractérisée par le
fait qu'elle comprend une quantité efficace d'au moins une
N-alkyl-hydroxybenzylamine de formule (I) en solution ou
sous forme de dispersion dans l'eau ou dans un solvant en
présence éventuellement d'agents tensio-actifs, mouillants
et dispersants nécessaires à la formulation de la matière
active.
On désigne par ~~quantité efficace", la quantité de
matière active nécessaire et suffisante pour conférer à la
pièce traitée une protection contre la corrosion respectant
une tenue au test de brouillard salin telle que définie dans
la norme ISO 9227 d'au moins 100 heures.
Dans la pratique, la composition conforme à
l'invention contient de 0,01 à 400 g, de préférence de 0,2
CA 02297803 2000-O1-25
WO 99105089 PCT/FR98101629
7
à 100 g par litre de matière active.
La composition conforme à l'invention peut être
commercialisée sous forme de concentré.
La teneur en matière active du concentré est au
maximum celle de sa solubilité limite dans le solvant
utilisé.
Lorsque le solvant est l'eau, la teneur en question
peut atteindre 50~ en poids, c'est-à-dire 500 g/1 de solvant
ou eau.
Au moment de l'utilisation, le concentré est dilué
avec la quantité nécessaire de solvant ou d'eau.
L'eau est préférée en tant que solvant pour la
composition conforme à l'invention mais on peut également
utiliser les essences aliphatiques, les solvants aromatia_ues
tels que le benzène, le toluène, le xylène et 1.'alkyl-
naphtalène, les solvants halogénés, les alcools, les éthers,
Ies polyéthers, les cétones et les mélanges de ces solvants.
Comme indiqué plus haut, les formulations
exclusivement aqueuses sont préférées.
Le pH de la composition conforme à l'invention est
de 1 à 12, de préférence de 4 à 9, et plus préféren-
tiellement encore de 5 à 8.
Pour ajuster ce pH, on a recours à un acide
organique ou minéral et, de préférence, à un couple d'acides
dont l'un est organique et l'autre minéral; l'ajustement
précis du pH de la composition est effectué par l'addition
de petites quantités de bases minérales ou organiques.
Parmi les acides organiques utilisables, on peut
citer l'acide acétique, l'acide tartrique, l'acide oxalique,
l'acide citrique, l'acide adipique, les acides acryliques et
méthacryliques, l'acide succinique ainsi que les polyacides
carboxyliques du groupe comprenant les acides maléia_ue,
malonique, glutamique, aspartique, gluconique, lactique,
gallique, iminodiacétique, salicylique, sulfosalicylique,
glycollique.
CA 02297803 2000-O1-25
WO 99/05089 PCTIFR98/01629
ô
Parmi les acides minéraux, on peut citer l'acide
chlorhydrique, l'acide sulfurique, l'acide phosphoreux,
l'acide nitrique, sulfamique et l'acide phosphorique.
Les composants du couple "acide organique - acide
minéral" ainsi que le pH sont choisis de telle sorte qu'on
obtienne les performances optimales de protection contre 'la
corrosion.
La base mise en oeuvre pour ajuster le pH avec
précision est choisie préférentiellement parmi les
alkylamines du groupe comprenant la diéthylamine,
l'isopropylamine, l'éthylène-diamine, la diéthylènetriamine,
la triéthylène-tétramine, l'hexaméthylène-tétramine, les
amines à fonction OH du groupe comprenant l'hydroxylamine,
les mono- et poly-éthanolamines, les isopropanolamines, la
morpholine, le carbonate d'ammonium, l'ammoniaque, la soude
et la potasse.
I1 est possible d'ajuster le pH à l'aide d'un ou de
plusieurs de ces composés mis en oeuvre à raison de 0,1 à
100 g/1, de préférence de 0,5 à 30 g/1 au total.
La composition conforme à l'invention peut contenir
tout autre composé connu de l'homme du métier du groupe
comprenant d'autres inhibiteurs de corrosion, des promoteurs
d'adhérence, des dispersants, des mouillants, des
émulsifiants, des épaississants, des produits anti-mousse,
des plastifiants, des produits anti-gel, des produits
fongicides, des produits bactéricides, des résines solubles
ou insolubles, des polymères organiques, des pigments, des
colorants et des charges minérales.
Parmi les autres inhibiteurs de corrosion
utilisables, on peut citer ies phosphates de zinc et les
sulfonates alcalino-terreux mis en oeuvre à des
concentrations de 0,05 à 2~.
Parmi les promoteurs d'adhérence utilisables, on
peut citer les silanes, les organo-titanates, les complexes
zircoaluminates du type commercialisé sous la marque
CA 02297803 2000-O1-25
WO 99105089 PCTIFR98l01629
9
MANCHEM~.
Parmi les résines utilisables, on peut citer les
résines acryliques, les copolymères chlorés vinyl-acryliques
et les résines phénoliques modifiées par réaction de
Mannich.
Parmi les charges et pigments utilisables, on peut
citer les silices, les silicates, les silicoaluminates.
La composition conforme à l'invention peut être mise
en oeuvre dans le cadre d'un procédé comprenant
successivement:
- une étape de dégraissage de la surface de la
pièce à traiter à l'aide de toute composition ou technique
connue de l'homme du métier,
- une étape de rinçage de la pièce à traiter,
- une étape de traitement à l'aide de la
composition conforme à l'invention par immersion de la pièce
dans la composition, par aspersion de la composition sur la
surface de la pièce à traiter, ou par application au pinceau
ou au rouleau encreur, à une température de 15 à 60°C, de
préférence de 15 à 40°C,
- éventuellement une étape de rinçage à l'eau
éventuellement chaude,
- une étape de séchage à une température de 40 à
160°C.
On peut ensuite appliquer une peinture liquide ou en
poudre par toute technique d'application de peinture connue
de l'homme du métier.
Lorsque la composition est appliquée par immersion,
la durée d'immersion doit être suffisante pour conduire à un
dépôt uniforme de matière active, elle est généralement
inférieure à 15 minutes et souvent comprise entre 30 et 180
secondes; le dépôt ainsi obtenu correspond à un poids de
couche de l'ordre de 0,5 à 15 g/m2, soit en matière active
de 0,2 à 15 g m2 de surface traitée.
CA 02297803 2000-O1-25
WO 99105089 PCT/FR98l01629
EXEMPLE 1
Préparation des isomères N-méthyl-N-(1-déoxy-glucitol)3,4-
dihydroxyphénylméthylamine et N-méthyl-N-(1-déoxy-glucitol)
2,3-dihydroxyphénylméthyla~nine répondant aux formules:
S
HO OH
HO N ~~OH
~~
HO OH
~/~OH
10 et HO OH OH
HO
/~~N /~~OH
HO OH s
Dans un réacteur de 500 ml, équipé d'un agitateur,
d'un thermomètre, d'un condenseur à reflux, d'un "dean-
stark" (terme de métier pour désigner une garde de
distillation permettant de soutirer l'eau de réaction) et
d'une ampoule de coulée, on charge 70 g de toluène, 60 g de
n-butanol, 11 g (100 mmol) de pyrocatéchol, 23,4 g de
20. N-méthyl-glucamine (120 mmol) et 0,8 g (10 mmol) de soude à
50~.
On porte la température du mélange à 70°C, puis on
introduit en 15 minutes 12,5 g (154 mmol) de formaldéhyde â
36~.
On chauffe à reflux total pendant 1 heure, puis on
distille azéotropiquement, en 2 heures, une quantité de
9,5 g d'eau (soit 90~ de la quantité théorique).
On introduit alors par l'ampoule de coulée 100 g
d'eau distillée, puis on laisse décanter pendant 15 minutes
à 80°C.
On recueille la phase aqueuse qui est strippée
(terme de métier pour désigner l'entraînement des traces de
solvant par distillation) afin d'éliminer les traces
résiduelles de solvant.
On obtient ainsi 116 g d'une solution à 29~
CA 02297803 2000-O1-25
WO 99105089 PCTIFR98/01629
11
d'extrait sec du produit recherché constitué des deux
isomères monosubstitués:
N-méthyl-N-(1-déoxy-glucitol)3,4-dihydroxyphénylméthylamine,
N-méthyl-N-(1-déoxy-glucitol)2,3-dihydroxyphénylméthylamine,
S ce qui correspond à un rendement de 94~.
Les deux molécules étant efficaces, on ne cherche
pas à les séparer.
Cette solution de matière active est directement
utilisable pour la formulation d'une composition inhibitrice
de corrosion.
EXEMPLE 2
Prëparation de 2,4bis(N-méthyl-N-(1-déoxy-glucitol)amino-
méthyl)-6-hydroxyphénol et rëpondant à la formule:
HO OH OH
HO N ~~OH
HO OH ' ~//
OH OH
~. ~., oH
N .-
-'
OH OH
Dans un réacteur de 500 ml, équipé d'un agitateur,
d'un thermomètre, d'un condenseur à reflux, d'un "dean-
stark" et d'une ampoule de coulée, on charge 50 g de
toluène, 50 g de n-butanol, 5,5 g (50 mmol) de
pyrocatêchol, 21,5 g de N-méthyl-glucamine (110 mmol) et
0, 4 g (5 mmol) de soude à 50~.
On porte la température du mélange à 70°C, puis on
introduit en 15 minutes 11,7 g (140 mmol) de formaldéhyde à
36~.
On chauffe à reflux total pendant 1 heure, puis on
distille azéotropiquement, en 2 heures, une quantité de
10,2 g d'eau (soit 1005 de la quantité théorique).
CA 02297803 2000-O1-25
WO 99105089 PCTIFR98/01629
12
On introduit alors par l'ampoule de coulée 100 g
d'eau distillée, puis on laisse décanter pendant 15 minutes
à 70°C.
On recueille la phase aqueuse qui est strippée afin
d'éliminer les traces résiduelles de solvant.
On obtient ainsi 96 g d'une solution à 28~ d'extrait
sec du produit recherché, ce qui correspond à un rendement
de 95~.
Cette solution de matière active est directement
utilisable pour la formulation d'une composition inhibitrice
de corrosion.
EXEMPLE 3
Préparation des isomères 2,4bis(N-méthyl-N-(1-déoxy
glucitol)amino-méthyl)-6-amino-phénol et 3,5bis(N-méthyl-N
(I-déoxy-glucitol)amino-méthyl)-2-amino-phénol rëpondant aux
formules:
HO OH OH
NH
HO.~,-~.~y~~~wNy,' '-~~,, 2
HO OH ~wi
OH OH
N /W .~~./'~~/'OH
et
2S HO OH OH OH
HO ~.~~ N ~~~,\~/OH
HO OH ~~ ~~-~NH
2 OH OH
~OH
N, : I
oH ôH
Dans un réacteur de 500 ml, équipé d'un agitateur, d'un
thermomètre, d'un condenseur à reflux, d'un "dean-stark" et
d'une ampoule de coulée, on charge 50 g de toluène, 70 g de
n-butanol, 5,5 g (50 mmol) de 2-amino-phénol, 21,5 g de
CA 02297803 2000-O1-25
WO 99/05089 PCTlFR98/01629
13
N-méthyl-glucamine (210 mmol) et 0,4 g (5 mmol) de soude à
50$.
On porte la température du mélange à 70°C, puis on
introduit en 15 minutes 11,7 g (140 mmol) de formaldéhyde à
36$.
On chauffe à reflux total pendant 1 heure, puis on
distille azéotropiquement, en 2 heures, une quantité de
9,4 g d'eau (soit 98$ de la quantité théorique).
On introduit alors par l'ampoule de coulée 100 g
d'eau distillée, puis on laisse décanter pendant 15 minutes
à 80°C.
On recueille la phase aqueuse qui est strippée afin
d'éliminer les traces résiduelles de solvant.
On obtient ainsi 101 g d'une solution à 27$
d'extrait sec du produit recherché, ce qui correspond à un
rendement de 100.
Cette solution de matière active est directement
utilisable pour la formulation d'une composition inhibitrice
de corrosion.
EXEMPLE 4
Préparation de N-méthyl-N-(1-déoxy-glucitol)2,3,4-tri-
hydroxy phénylméthylamine répondant à la formule:
2S HO OH OH
HO N ~~OH
HO OH CH3
OH
Dans un réacteur de 1 1, équipé d'un agitateur, d'un
thermomètre, d'un condenseur à reflux, d'un "dean-stark" et
d'une ampoule de coulée, on charge 100 g de toluène, 200 g
de n-butanol, 25,2 g (200 mmol) de pyrogallol, 46,8 g de
N-méthyl-glucamine (240 mmol) et 1,6 g (20 mmol) de soude à
50$ .
CA 02297803 2000-O1-25
WO 99/05089 PCTIFR98I01629
14
On porte la température du mélange à 70°C, puis on
introduit en 15 minutes 25,0 g (300 mmol) de formaldéhyde à
36~.
On chauffe à reflux total pendant 1 heure, puis on
distille azéotropiquement, en 2 heures, une quantité de 22 g
d'eau.
On introduit alors par l'ampoule de coulée 250 g
d'eau distillée, puis on laisse décanter pendant 30 minutes
à 90°C.
On recueille la phase aqueuse qui est strippée afin
d'éliminer les traces résiduelles de solvant.
On obtient ainsi 242 g d'une solution à 31~
d'extrait sec du produit recherché, ce qui correspand à un
rendement de 99~.
IS Cette solution de matière active est directement
utilisable pour la formulation d'une composition inhibitrice
de corrosion.
EXEMPLE 5
Préparation des isomères N-méthyl-N-(2-hydroxyéthyl)3,4-
dihydroxyphénylméthylamine et N-méthyl-N-(2-hydroxyéthyl)
2,3-dihydroxyphénylméthylamine répondant aux formules:
OH CH3
OH
et OH
/~N ~ -,.~ /.~/OH
OH CH3
Dans un réacteur de 500 ml, équipé d'un agitateur,
d'un thermomètre, d'un condenseur à reflux, d'un "dean-
stark" et d'une ampoule de coulée, on charge 200 g de
toluène, 100 g de n-butanol, 22 g (200 mmo1) de
CA 02297803 2000-O1-25
WO 99/05089 PCT/FR98101629
pyrocatéchol, 18 g de 2-(méthylamino)-éthanol(240 mmol) et
1,6 g (20 mmol) de soude à 50~.
On porte la température du mélange à 70°C, puis on
introduit en 15 minutes 25 g (300 mmol) de formaldéhyde à
5 36~.
On chauffe à reflux total pendant 1 heure, puis on
distille azéotropiquement, en 2 heures, une quantité de
21,6 g d'eau.
On introduit alors par l'ampoule de coulée 200 g
10 d'eau distillée, puis on laisse décanter pendant 30 minutes
à 80°C.
On recueille la phase aqueuse qui est strippée afin
d'éliminer les traces résiduelles de solvant.
On obtient ainsi 146 g d'une solution à 18,5
15 d'extrait sec du produit recherché.
Cette solution de matière active est directement
utilisable pour la formulation d'une composition inhibitrice
de corrosion.
Dans les exemples qui suivent, on illustre
l'efficacité des N-alkyl-hydroxybenzylamines conformes à
l'invention pour l'inhibition de la corrosion des surfaces
métalliques.
A cet égard, les N-alkyl-hydroxybenzylamines
conformes à l'invention selon les exemples 1 à 3 et une
molécule de l'art antérieur sont mises en oeuvre dans un
procédé dont les étapes sont identifiées dans le tableau I
par indication des produits mis en oeuvre, de la durée, de
la température et du mode de réalisation.
Les compositions utilisées sont comme indiqué ci-
après:
CA 02297803 2000-O1-25
WO 99/05089 PCT/FR98101629
16
Composition A1 selon l'invention:
acide adipique 0,5 g/1
acide phosphorique 0,4 g/1
molécule de l'exemple 1 1 g/1
soude 0,15 g/1
triéthylène-tétramine qsp pH 6,0.
Composition A2 selon l'invention:
Identique à la composition A1, mais la molécule
testée est celle de l'exemple 2.
Composition A3 selon l'invention:
Identique à la composition A1, mais la molécule
testée est celle de l'exemple 3.
Composition C1 selon l'invention:
Identique à la composition A1, mais la molécule
testée est celle décrite dans le brevet EP N° 0 319 017-A2
(qui revendique la priorité de la demande US SN 128 673) et
ayant 1a formule
dans laquelle:
xl= H
OH HO
j
X1 OH X2 X2 /N~~ , ~OH
OH HO
CA 02297803 2000-O1-25
WO 99105089 PCTIFR98101629
17
TABLEAU I
Dure TempratureMode
Etape Produit mis en oeuvre
(min) ( de ralisation
C)
DgraissageRIDOLINE 417 CF 3% 5 60 immersion
v/v
RlDOSOL 161 CF 0,3%
v/v
Rinage eau permute 2 20 immersion
TraitementCompositions A1, A2, 1 20 aspersion
A3 et C1
de surface
Schage 10 100 tuve
Peinture PPG, rf. Y143W408 15 150 paisseur
35 Nm
par hand-coater
Les produits RIDOLINE 417 CF et RIDOSOL 161 CF sont
des compositions de dégraissage à base de dérivés alcalins
et de tensio-actifs commercialisées par Ia Société
Demanderesse.
Le procédé est appliqué à deux types d'éprouvettes,
les unes en acier doux laminé à froid d'épaisseur égale à
0,7 mm et de qualité ZES NFA 36.401 et les autres en acier
doux revêtu de zinc par voie électrolytique d'épaisseur
égale à 0,7 mm et de qualité NFA 36.260 noté EZ.
Ces ëprouvettes se présentent sous la forme de
panneaux dont les largeur et longueur sont respectivement de
10 et de 20 cm.
Egalement à titre comparatif, on a soumis les mêmes
éprouvettes à un traitement de phosphatation classique avec
post-rinçage chromique, les éprouvettes étant traitées selon
une gamme classique de phosphatation amorphe, les étapes
étant:
- dégraissage à l'aide de DURIDINE F 775 CF 1~ v/v +
RIDOSOL 162 CF 0,1~ v/v à une température de SO°C pendant
150 secondes,
- rinçage à la température ambiante pendant 60 secondes,
rinçage chromique à l'aide de DEOXYLYTE 41 0,1~ v/v à la
CA 02297803 2000-O1-25
WO 99105089 PCTIF'R98I01629
18
température ambiante pendant 40 secondes,
- rinçage en eau permutée à la température ambiante pendant
60 secondes,
- séchage à 80°C pendant 300 secondes.
Les produits DURIDINE F 775 CF et RIDOSOL 162 CF qui
sont respectivement des solutions aqueuses à base d'acide
phosphorique et de tensio-actifs, sont commercialisés par la
Société Demanderesse.
Après le traitement selon le tableau I et après le
traitement de phosphatation donné, on détermine, concernant
les surfaces traitées, la résistance à la corrosion et
l'adhérence d'une peinture appliquée.
La résistance à la corrosion est déterminée par le
test au brouillard salin selon la Norme ISO 9227.
Dans le cadre de ce test, on fait comporter aux
éprouvettes une blessure en forme de V inversé.
Après 100 heures d'exposition au brouillard salin,
on mesure l'épaisseur totale de la corrosion de part et
d'autre de la blessure.
Le résultat est considéré comme
- excellent et noté "++" pour une corrosion de 0 à 4 mm,
- moyen et noté "+" pour une corrosion supérieure à 4 mm
et jusqu'à 7 mm,
- mauvais et noté "-" pour une corrosion supérieure à
7 mm.
L'adhérence d'une peinture est déterminée par
l'évaluation de la résistance au quadrillage selon la Norme
NFT 30.038.
Les résultats sont notés de 0 à 5. La cotation 0
correspond à une excellente adhérence sans aucun décollement
et la cotation 5 à un décollement complet de la peinture.
Les résultats enregistrés sont réunis dans le
tableau II.
CA 02297803 2000-O1-25
WO 99105089 PCTlFR98101629
19
TABLEAU II
Composition Adhrence Rsistance
la corrosion
utilise Acier EZ Acier EZ
A1 0 0 ++ +
A2 0 0 ++ ++
A3 0 0 ++ ++
R1 0 0 + -
Phosphatation0 0 ++ ++
classique
I3 apparaît clairement à l'examen de ce tableau que
les compositions à base des molécules conformes à
l'invention donnent, d'une part, de meilleurs résultats que
les molécules de l'art antérieur comportant une molécule de
phénol dans leur structure et, d'autre part, des résultats
en tous points comparables aux techniques de phosphatation
classique sans présenter l'inconvénient de nécessiter un
post-rinçage chromique.
Par rapport à ces dernières techniques, elles
apportent également une réponse aux demandes d'économie
d'énergie car elles s'appliquent à température ambiante,
sont simples à mettre en oeuvre et ne nécessitent pas de
rinçage après traitement.