Note : Les descriptions sont présentées dans la langue officielle dans laquelle elles ont été soumises.
CA 02344255 2001-04-17
-1-
La présente invention concerne de nouveaux dérivés
d'hétérocycloalkylbenzocyclobutane et d'hétéroarylbenzocyclobutane, leur
procédé de
préparation et les compositions pharmaceutiques qui les contiennent.
Les composés de la présents: invention agissent comme de puissants inhibiteurs
de
recapture de la sérotonine et de la noradrénaline. A ce titre, ils sont
utiles, en tant que
médicament, pour le traitement de la dépression, des attaques de panique, des
troubles
obsessionnels compulsifs, des phobies, des troubles impulsifs, de l'abus de
drogue, de
l'anxiété, de l'obésité et de la boulimie.
En effet, les produits de la présente invention se sont montrés actifs d'une
part, in
1o vitro, sur le test de caractérisation de l'inhibition de la recapture de
sérotonine et de
noradrénaline, et d'autre part, in vivo. Ainsi, dans les expériences de
microdialyse,
réalisées dans le cortex frontal chez le rat, les composés de l'invention
entraînent dans
ce territoire une augmentation de la libération de sérotonine, de
noradrénaline et de
dopamine. Les composés revendiqués par la Demanderesse sont donc tout à fait
aptes
à être utilisés dans des pathologies qui sont liés à un défaut de transmission
de ces
deux neuromédiateurs. Cet effet particulièrement intéressant des composés de
l'invention est aussi démontré lors du test d'enfouissement des billes chez la
souris.
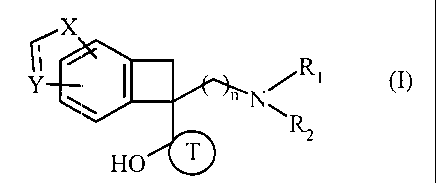
Plus particulièrement, la présente invention concerne les composés de formule
(I)
/X
Y / ' ( ~ /R' ~I)
N~R
a
HO
dans laquelle
---__ représente une liaison simple ou une liaison double,
n représente un entier compris entre 1 et 6 inclus,
Rl, R2, identiques ou différents, indépendamment l'un de l'autre représentent
un
groupement choisi parmi atome d'hydrogène, groupement alkyle C1-C6) linéaire
ou
CA 02344255 2001-04-17
-2-
ramifié, aryle, arylalkyle C1-C6) linéaire ou ramifié, cycloalkyle,
cycloalkylalkyle C1-
C6) linéaire ou ramifié, alkényle CZ-C6) linéaire ou ramifié, alkynyle C2-C6)
linéaire
ou ramifié, hétérocycloalkyle, hétérocycloalkylalkyle C~-C6) linéaire ou
ramifié,
hétéroaryle, et hétéroarylalkyle C1-C6) linéaire ou ramifié,
X représente un groupement choisi parmi -CH=CH-, atome d'oxygène, groupement
S(O)m dans lequel m est un f;ntier compris entre 0 et 2 inclus, et NR3 dans
lequel R3
représente un groupement choisi parmi atome d'hydrogène, groupement alkyle C i-
C6)
linéaire ou ramifié, aryle, arylalkyle Cl-C6) linéaire ou ramifié,
cycloalkyle,
cycloalkylalkyle C,-C6) linéaire ou ramifié, alkényle C2-C6) linéaire ou
ramifié, et
lo alkynyle (C2-C6) linéaire ou ramifié,
Y représente un groupement CH ou CHZ selon qw-w~ représente une liaison
simple ou une liaison double, ou peut prendre la définition supplémentaire
atome
d'oxygène quand X représente un atome d'oxygène,
T représente un groupement cycloalkyle (C3-C~2) monocyclique ou polycyclique,
dont
l'un des atomes de carbone d.u cycloalkyle peut éventuellement être remplacé
par un
groupement choisi parmi atome d'oxygène, atome de selenium, groupement de
formule S(O)P dans laquelle p représente un entier compris entre 0 et 2
inclus, NR3
dans laquelle R3 est tel que défini précédemment, et SiR4R5 dans laquelle R4
et R5,
identiques ou différents, représentent un groupement alkyle (Ci-C6) linéaire
ou
ramifié,
leurs isomères ainsi que leurs sels d'addition à un acide ou à une base
pharmaceutiquement acceptable.
Par groupement aryle, on comprend un groupement choisi parmi phényle,
biphényle,
naphtyle, dihydronaphtyle, tétrahydronaphtyle, indanyle, indényle, et
benzocyclobutyle, chacun de ces groupements pouvant être éventuellement
substitués
par un ou plusieurs groupements, identiques ou différents, choisis parmi
atomes
d'halogène, groupements alkyle (CI-C6) linéaire ou ramifié, hydroxy, alkoxy
(C1-C6)
CA 02344255 2001-04-17
-3-
linéaire ou ramifié, nitro, cyano, trihalogénoalkyle (C,-C6) linéaire ou
ramifié, amino,
monoalkylamino et dialkylamino (C,-C6) linéaire ou ramifié.
Par groupement hétéroaryle:, on comprend un groupement aryle tel que défini
précédemment, contenant au. sein du système cyclique de un à trois
hétéroatomes,
identiques ou différents, choisis parmi oxygène, azote et soufre, ledit
groupement
hétéroaryle étant éventuellement substitué par un ou plusieurs groupements,
identiques ou différents, choisis parmi les substituants définis précédemment
du
groupement aryle. Parmi les groupements hétéroaryles, on peut citer à titre
non
limitatif le groupement pyridyle, pyrimidinyle, indolyle, benzofuranyle,
1o benzothiényle, quinolylc;, isoquinolyle, benzo[1,4]dioxynyle, 2,3-
dihydrobenzo [ 1,4]dioxynyle, . . .
Par groupement cycloalkyle, on comprend un système mono ou polycyclique, de 3
à
12 chaînons, contenant éventuellement une ou plusieurs insaturations, celles-
ci ne
conférant pas de caractère aromatique audit système cyclique.
Par groupement hétérocycloalkyle, on comprend un groupement cycloalkyle tel
que
défini précédemment, contt~nant au sein du système cyclique de un à trois
hétéroatomes, identiques ou différents, choisis parmi oxygène, azote et
soufre.
Les composés préférés de l'invention sont les composés de formule (I) dans
laquelle n
prend la valeur 1.
2o Les substituants RI et R2 préférés, selon l'invention, sont l'atome
d'hydrogène, le
groupement alkyle (Ci-C6) linéaire ou ramifié, et le groupement 2,3-dihydro-
1,4-
benzodioxin-2-ylméthyle.
Le substituant T préféré selon l'invention est le groupement cycloalkyle
monocyclique
saturé (C3-C8).
CA 02344255 2001-04-17
-4-
D'une façon avantageuse, le substituant T préféré selon l'invention est le
groupement
cyclopentyle et cyclohexyle.
Selon une variante avantageuse de l'invention, les composés préférés de
l'invention
sont les composés de formule. (IfA)
Xlo ~/ ~Ri (I/A)
I n N
1'00 \
HO T RZ
dans laquelle n, Rl, RZ et T sont tels que définis dans la formule (I), Xlo
représente un
atome d'oxygène ou un atome de soufre, et Ylo représente un groupement CH.
Selon une autre variante avantageuse de l'invention, les composés préférés de
l'invention sont les composés de formule (IB)
Y \
I iRi (IB)
\ ~n'Nv
X R
z
HO T
lo
dans laquelle X, Y, n, Rl, R2, R3 et T sont tels que définis dans la formule
(I).
D'une façon intéressante, les composés préférés de l'invention sont les
composés de
formule (I/B) dans laquelle n est égal à 1, X représente un groupement NR3
dans
lequel R3 représente un atome d'hydrogène ou un groupement alkyle (C1-C6)
linéaire
ou ramifié.
Selon une troisième variante avantageuse de l'invention, les composés préférés
de
l'invention sont les composés de formule (I/C)
n N~RI (I/C)
~I
X \ I
~..Y ~oHO T Rz
dans laquelle n, Rl, R2, X et T sont tels que définis dans la formule (I), et
YZo
CA 02344255 2001-04-17
-5-
représente un groupement CI-I ou CHz.
Selon une quatrième variante avantageuse de l'invention, les composés préférés
de
l'invention sont les composés de formule (I/D)
~R~
(I/D)
dans laquelle n, Rl, Rz, X et T sont tels que définis dans la formule (I), et
Yzo
représente un groupement Cf~ ou CHz.
Selon une autre variante avantageuse de l'invention, les composés préférés de
l'invention sont les composés de formule (I/E)
n /: X
Y~ ~<
iRi
(I/E)
HO~T~ Rz
lo dans laquelle n, Rl, Rz, X et T sont tels que définis dans la formule (I),
et Yzo
représente un groupement CH ou CHz.
Enfin, selon une dernière variante intéressante de l'invention, les composés
préférés
de l'invention sont les composés de formule (I/F)
~R~
\ \ ~ n'N I/F
( )
Yzo , ~ T Rz
--X HO~
dans laquelle n, R~, Rz, X et T sont tels que définis dans la formule (I), et
Yzo
représente un groupement CH ou CHz.
Les composés préférés de l'invention sont le
CA 02344255 2001-04-17
-6-
~ 1-{6-[(diméthylamino)méthyl]-1-méthyl-2,3,5,6-tétrahydro-1H
cyclobuta[f]indol-
6-yl } cyclohexanol,
~ 1-{6-[(diméthylamino)mE'~,thyl]-2,3,5,6-tétrahydro-1H cyclobuta[f]indol-6-
yl}
cyclohexanol,
~ 1-{5-[(diméthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzofuran-5-yl}
cyclohexanol,
~ 1-{5-[(diméthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzothien-5-yl}
cyclohexanol,
~ 1-{6-[(diméthylamino)méthyl]-1-méthyl-5,6-dihydro-1H cyclobuta[f]indol-6-yl}
cyclohexanol,
~ 1-{7-[(diméthylamino)mf;thyl]-2,3,6,7-tétrahydro-1H cyclobuta[e]indol-7-yl}
cyclohexanol,
1-{5-[(méthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzothièn-5-yl}
cyclopentanol,
~ 1-{5-[(diméthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzothièn-5-yl}
cyclopentanol,
~ (+) 1-{5-[(diméthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzothièn-5-yl}
cyclopentanol,
~ (-) 1-{5-[(diméthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzothièn-5-yl}
2o cyclopentanol,
1-{6-[(diméthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzothièn-6-yl}
cyclopentanol,
~ 1-{5-[(diméthylamino)méthyl]-1-méthyl-5,6-dihydro-1H cyclobuta[f]indol-5-yl}
cyclopentanol,
~ 1-{7-[(diméthylamino)méthyl]-6,7-dihydrocyclobuta[g][1]benzofuran-7-yl}
cyclopentanol,
~ 1-{ 1-[(diméthylamino)méthyl]-1,2-dihydrocyclobuta[b]naphthalèn-1-
yl } cyclopentanol,
~ 1-{7-[(diméthylamino)mcahyl]-6,7-dihydro-3H cyclobuta[e]indol-7-
3o yl } cyclopentanol,
~ 1-{1-[(dimethylamino)methyl]-1,2-dihydrocyclobuta[a]naphthalèn-1-
yl } cyclopentanol.
CA 02344255 2001-04-17
7
Les isomères ainsi que les sels d'addition à un acide ou à une base
pharmaceutiquement acceptable des composés préférés font partie intégrante de
l'invention.
Par isomères, on comprend les isomères optiques tels que les diastéréoisomères
et les
énantiomères.
Parmi les acides pharmaceutiquement acceptables, on peut citer à titre non
limitatif
les acides chlorhydrique, bromhydrique, sulfurique, phosphonique, acétique,
trifluoroacétique, lactique, pyruvique, malonique, succinique, glutarique,
fumarique,
tartrique, maléïque, citrique, ascorbique, oxalique, méthane sulfonique,
camphorique,
etc...
Parmi les bases pharmaceutiquement acceptables, on peut citer à titre non
limitatif
l'hydroxyde de sodium, l'hydroxyde de potassium, la triéthylamine, la
tertbutylamine,
etc...
La présente invention concf;rne aussi le procédé de préparation des composés
de
formule (I), caractérisé en ce qu'on utilise comme produit de départ
a) soit un composé de formule (II)
H~-X
a
U (II)
CN
dans laquelle Xa représente un atome de soufre, d'oxygène, ou un groupement
NH,
2o composé de formule (II) que l'on fait réagir avec un composé de formule
(III)
Z - CH(OA)Z (III)
dans laquelle A représente un groupement alkyle (C1-C4) linéaire ou ramifié et
Z
représente un groupement formyle (dans le cas où Xa représente un groupement
NH),
ou un groupement -CHZHaI dans lequel Hal représente un atome de chlore, de
brome
ou d'iode,
CA 02344255 2001-04-17
g _
pour conduire aux composés de formule (IV)
X
a
AO~ \ ~ (IV)
OA CN
dans laquelle Xa et A sont teks que définis précédemment,
composés de formule (IV) qui sont soumis
~ soit dans le cas où X-a~rend la définition X~ représentant un atome
d'oxygène ou un
atome de soufre, à des conditions de cyclisation par action d'un acide tel que
l'acide
polyphosphorique ou un acide de Lewis, pour conduire aux composés de formule
(V/a)
~X1
(V/a)
CN
1o dans laquelle X1 représente un atome d'oxygène ou de soufre,
composés de formule (V/a) qui sont traités
* soit, en présence d'une base forte, par une cétone cyclique de formule (VI)
O~ (VI)
dans laquelle T a les mêmes significations que dans la formule (I),
pour conduire aux composés de formule (VII/a),
(VII/a)
CN
dans laquelle X~ et T sont tel~~ que définis précédemment,
composés de formule (VII/a) qui sont soumis à l'action d'un agent réducteur
selon des
conditions classiques de la synthèse organique, pour conduire aux composés de
2o formule (I/a), cas particulier des composés de formule (I)
CA 02344255 2001-04-17
- 9 -
Y
(I/a)
~2
dans laquelle X1 et T sont tels que définis précédemment,
composés de formule (I/a) pour lesquels
~ soit on substitue la fonction amine primaire selon des méthodes classiques
de la
synthèse organique, telle que; l'amination réductrice ou la substitution
nucléophile de
dérivé de formule (VIIIa)
R'1 - Z, (VIIIa)
dans laquelle R'1 a les mêmes définitions que R~ dans la formule (I) exceptées
la
valeur atome d'hydrogène, ca Z1 représente un groupe partant usuel de la
chimie
organique tel que atome d'halogène, groupement mésylate ou tosylate,
pour conduire aux composés de formule (I/bl), cas particulier des composés de
formule (I)
Y
(I/b~)
dans laquelle X~, T et R'1 sont tels que définis précédemment,
b soit selon une variante avantageuse du procédé, on traite par un dérivé de
formule
(VIIIb)
R" 1 - COZ2 (VIIIb)
dans laquelle R"1 représente un groupement hétérocycloalkylalkyle (C~-CS)
linéaire
ou ramifié, et Z2 représente un atome de chlore ou un groupement imidazolyle,
pour
conduire aux composés de formule (I/b2)
CA 02344255 2001-04-17
-10-
X~
O (I/b2)
\.
NH~R"
i
HO T
dans laquelle X1, T et R"1 sont tels que définis précédemment,
composés de formule (Ilb2) qui sont réduits par un agent réducteur
classiquement
utilisé en chimie organique, pour conduire aux composés de formule (I/b3)
_x
(I/b3)
NH~R"1
dans laquelle X1, R"1 et T sont tels que définis précédemment,
l'ensemble des composés de formule (I/b,) et (I/b3) forment les composés de
formule
(I~)~
~XI
.
NHR» (I/b)
HO~ ( T
dans laquelle X1 et T sont: tels que définis précédemment et R, l a les mêmes
définitions que R'1 et R"1 réunis.
composés de formule (I/b) qui sont traités selon les mêmes conditions que
décrites
précédemment par un composé de formule (VIIIc)
R'Z - Z1 (VIIIc)
dans laquelle Z1 est tel que défini précédemment et R'2 prend les mêmes
définitions
que RZ dans la formule (I) à l'exception de la valeur atome d'hydrogène,
pour conduire aux composés de formule (I/c), cas particulier des composés de
2o formule (I)
CA 02344255 2001-04-17
-11-
X
(I/c)
I N~R ~
1
~ R'
HO~
dans laquelle Xl, T, R'1 et R'2 sont tels que définis précédemment,
* soit, en présence d'une base forte, par une amine de formule (IX)
R
L -~ (CHZ)°1 - N~ 1 (IX)
Rz
dans laquelle R1 et R2 sont tels que définis dans la formule (I), nl est un
entier compris
entre 2 et 6 inclus, et L représente un groupe partant tel qu'un atome
d'halogène, un
groupement mésylate, tosylate ou trifluorométhanesulfonate, pour conduire aux
composés de formule (X)
X' R
w I (CHZ)ni N\ (X)
CN
lo dans laquelle Xi, nl, R1 et RZ sont tels que définis précédemment,
composés de formule (X) qui sont traités par de l'eau oxygéné en présence de
carbonate de sodium, pour conduire aux composés de formule (XI)
O
/Ri
(CHZ)° i N\ (XI)
R2
dans laquelle X1, nl, R, et RZ sont tels que définis précédemment,
composés de formule (XI) dui sont réduits par action de formiate d'ammonium en
présence de Pd/C à 10 %, pour conduire aux composés de formule (XII)
/Ri
'2)°i N\ (XII)
R2
CA 02344255 2001-04-17
-12-
dans laquelle Xl, nl, R1 et R2 sont tels que définis précédemment,
composés de formule (XII) qui sont soumis à l'action d'un composé de formule
(XIII)
(CH:3)2N - CH(OG)2 (XIII)
dans laquelle G représente un groupement alkyle (Cl-C6) linéaire ou ramifié,
benzyle
ou cyclohexyle,
pour conduire aux composés de formule (XIV)
X' R
/ i
(CHZ)~1 N~ (XIV)
R2
O O-G
dans laquelle X1, nl, R~ et RZ sont tels que définis précédemment,
lo composés de formule (XIV) qui sont traités par un dimagnésien de formule
(XV)
Hal - Mg~Mg - Hal (XV)
dans laquelle Hal représente; un atome d'halogène, et T est tel que défini
dans la
formule (I),
pour conduire aux composés de formule (I/d), cas particulier des composés de
formule (I)
/Ri
(CHZ)ni N~ (I/d)
R2
dans laquelle X1, n~, R~, R2 et T sont tels que définis précédemment,
l'ensemble des composés de i:ormule (I/a), (I/b), (I/c) et (I/d), dans le cas
particulier où
Xl représente un atome de soufre, forment les composés de formule (I/e)
G
/Ri
n N~ (I/e)
Rz
CA 02344255 2001-04-17
-13-
dans laquelle n, RI, RZ et T sont tels que définis dans la formule (I),
composés de formule (I/e) qui sont soumis à l'action d'un agent d'oxydation
selon des
conditions classiques de la synthèse organique, pour conduire aux composés de
formule (I/f), cas particulier des composés de formule (I)
I~I )p'
/R~
N\ (I/f7
R2
dans laquelle pl est un entier choisi parmi 1 et 2, et n, R~, R2 et T sont
tels que définis
précédemment,
l'ensemble des composés àle formule (I/a), (I/b), (I/c), (I/d) (dans lesquels
X~
représente un atome d'oxygène ou de soufre) et (I/f) forment les composés de
formule
(I/g)
v
/RI
N\ (I/g)
Ra
dans laquelle Xla représente un atome d'oxygène ou un groupement de formule
S(O)p
avec p tel que défini dans la formule (I), et n, R1, RZ et T sont tels que
définis dans la
formule (I),
composés de formule (I/g) qui sont soumis à l'action d'un agent réducteur
selon des
conditions classiques de la synthèse organique, pour conduire aux composés de
formule (I/h), cas particulier des composés de formule (I)
v
/R~
N\ (I/h)
dans laquelle Xla, n, RI, RZ et T sont tels que définis précédemment,
CA 02344255 2001-04-17
-14-
~ soit. dans le cas où X~~T2nd la définition X'Z représentant un groupement
NH, à
l'action d'un chlorure d'acide sulfonique de formule (XVI)
E -~S02C1 (XVI)
dans laquelle E représente un groupement alkyle (C,-C4) linéaire ou ramifié,
phényle
ou p-toluyle,
pour conduire aux composés de formule (XVII)
~ OZE
XZ _
(XVII)
AO~ OA\ CN
dans laquelle X2 représente un atome d'azote, E et A sont tels que définis
précédemment,
1o composés de formule (XVII) qui sont cyclisés par action d'un acide pour
conduire aux
composés de formule (V/b)
SOIE
Xz
(V/b)
CN
dans laquelle X2 et E sont tel; que définis précédemment,
composés de formule (V/b) dont on déprotège l'amine cyclique par action d'un
agent
basique, puis que l'on soum.èt à l'action d'un agent réducteur selon des
conditions
classiques de la synthèse org<~nique, pour conduire aux composés de formule
(V/c)
H
I
iX2
CN
dans laquelle XZ est tel que défini précédemment,
composés de formule (V/c) qui sont soumis à l'action d'un composé de formule
(VI)
2o tel que décrit précédemment pour conduire aux composés de formule (VII/b)
CA 02344255 2005-12-O1
-15-
(VIIIb)
dans laquelle XZ est tel que défini précédemment et T est tel que défini dans
la
formule (I),
composés de formule (VIi'/b) qui sont
~ soit traités selon les mêmes conditions que celles décrites pour les
composés de
formule (VII/a), pour conduire aux composés de formule (IJi), cas particulier
des
composés de formule (I)
H
I
(I/i)
dans laquelle X2 et T sont tels que définis précédemment,
lo composés de formule (I/i) qui peuvent être traités-successivement par un
composé de
formule (VIIIa) ou (VIIIb) suivi d'une réduction tels que définis
précédemment, puis
(VIIIc), tel que défini; précédemment, pour conduire respectivement aux
composés de
formule (I/j) et (I/k), cas particuliers des composés de formule (I)
ls
1 I
1
) ~)
CA 02344255 2005-12-O1
-16-
dans lesquelles X2, T, R'1 et R'2 sont tels que définis précédemment, et R'3 a
les
mêmes définitions et valeurs que R3 défini pnoédar, excepté lavaleur atome
d'hy~Ogàr.,
l'ensemble des composés de formules (I/i), (I/j), (I/k) forment les composés
de
formule (I/l)
~3
R (I/I) .
i
dans laquelle X2, R~, R2, R3 et T sont tels que définis dans la formule (I),
composés de formule (I/1) qui sont soumis à faction d'un agent oxydant tel que
le
dioxyde de manganése, pour conduire aux composés de formule (I/m), cas
particulier
des composés de formule (I)
(I/m)
lo
dans laquelle XZ, Ri, RZ, R3 et T sont tels que définis précédemment,
1 soit traités par un composé de formule (XVI) telle que définie précédemment,
pour
conduire aux composés de formule (XVIII)
~ 02E
(XVIII)
dans laquelle T, X2 et E sont tels que définis précédemment,
composés de formule (XVIII) qui sont réduits selon des conditions classiques
de la
synthèse organique, pour conduire aux composés de formule (XIX)
CA 02344255 2001-04-17
- 17 -
~ OZE
(XIX)
dans laquelle T, X2 et E sont tels que définis précédemment,
composés de formule (XIX) dont la fonction amine primaire peut être substituée
par
action d'un composé de fornmle (VIIIa) tel que défini précédemment, pour
conduire
aux composés de formule (XX)
~ OZE
'I (
dans laquelle T, X2, E et R'I ont les mêmes significations que celles décrites
précédemment,
composés de formule (XX) qui peuvent être transformés en amine tertiaire par
action
1o d'un composé de formule (VIIIb) telle que définie précédemment, pour
conduire aux
composés de formule (XXI)
~ OZE
R, (XXI)
I
dans laquelle T, XZ, E, R'I et R'2 sont tels que définis précédemment,
composés de formule (XX) ca (XXI) qui sont ensuite déprotégés par traitement
avec
du sodium dans l'ammoniaque liquide, pour conduire respectivement aux composés
de formules (I/n) et (I/o), cas particuliers des composés de formule (I)
CA 02344255 2001-04-17
-1g
H H
H
' ' R'
i
R' R~2
(I/n) (I/o)
dans laquelle T, X2, R'I et R'2 sont tels que définis précédemment,
b) sait un composé de formule (II/1)
O
;Kb / H
''., I (II/1)
~Yb \ Hal
dans laquelle Hal représente un atome d'halogène, et Xb représente un atome
d'oxygène quand Yb représente un atome d'oxygène et _____ représente une
liaison
simple,
ou Xb représente un groupement -CH=CH- quand Yb représente un groupement CH et
----- représente une liaison double,
lo composés de formule (II/1) qui est mis à réagir avec (Et0)2POCH2CN pour
conduire
aux composés de formule (II/2)
Xb / \ CN
v (II/2)
\ Hal
dans laquelle Hal, Xb et Yb sont tels que définis précédemment,
composés de formule (II/2) dui est d'abord soumis à l'action d'un réducteur
classique
de la chimie organique puis qui est mis à réagir avecNaNH2, pour conduire aux
composés de formule (II/3)
b /
'v ~ (II/3)
b CN
dans laquelle Xb et Yb sont tels que détïnis précédemment,
CA 02344255 2001-04-17
-19-
composés de formule (II/3) qui peuvent être traités dans les mêmes conditions
que les
composés de formule (V/a),
* sait par un composé de formule (VI), puis (VIIIa) ou (VIIIb), puis (VIIIc),
pour
conduire successivement aux composés de formules (I/3a), (I/3b) et (I/3~)
Xb / Xb /
~NH2 ~ ~ ~ ~ NHR' ~
Yb ~ Yb
HO T ,~ HO T
(I/3a) (I/3b)
Xb /
NR'iR'2
Yb u
HO T
(I/3~)
dans lesquelles Xb, Yb, T, R'1 et R'2 sont tels que définis précédemment,
* soit par un composé de formule (IX), le produit obtenu étant ensuite traité
comme
les composés de formule (X) et (XI), puis soumis à l'action successive d'un
composé
de formule (XIII) puis (XV), tels que décrits précédemment, pour conduire aux
composés de formule (I/3d)
b / /R1
v ~ I (CH2)m ' N ~ (I/3d)
Yb RZ
T
HO
dans laquelle Xb, Yb, n,, R1 et R2 sont tels que définis précédemment,
les composés (I/a) à (I/o) et (I/3a) à (I/3d) forment l'ensemble des composés
de
l'invention, que l'on purifie le cas échéant, selon une technique classique de
purification, qui peuvent, si on le désire, être séparés en leurs différents
isomères
selon une technique classique de séparation, et que l'on transforme, le cas
échéant, en
leurs sels d'addition à un acide ou à une base pharmaceutiquement acceptable.
CA 02344255 2001-04-17
-20-
Les composés de formule (II;1, (II/1), (III), (VI), (VIIIa), (VIIIb), (VIIIc),
(IX), (XIII),
(XV) et (XVI) sont soit des produits connus, soit des produits obtenus à
partir de
substances connues selon des procédés classiques de la chimie organique.
Les composés de la présente invention sont des inhibiteurs de la recapture de
la
sérotonine, de la noradrénaline et de la dopamine. Ils sont utiles, en tant
que
médicament, pour le traitement de la dépression, des attaques de panique, des
troubles
obsessionnels compulsifs, des phobies, des troubles impulsifs, de l'abus de
drogue, de
l'anxiété, de l'obésité et de la boulimie.
La présente invention a également pour objet les compositions pharmaceutiques
to contenant comme principe actif au moins un composé de formule (I), ses
isomères
optiques, ses sels d'addition à un acide ou à une base pharmaceutiquement
acceptable,
seul ou en combinaison avec un ou plusieurs excipients ou véhicules inertes,
non
toxiques, pharmaceutiquement acceptables.
Parmi les compositions pharmaceutiques selon l'invention, il sera cité plus
particulièrement celles qui conviennent pour l'administration orale,
parentérale
(intraveineuse, intramusculaire ou sous-cutanée), per ou transcutanée, nasale,
rectale,
perlinguale, oculaire ou respiratoire, et notamment les comprimés simples ou
dragéifiés, les comprimés sublinguaux, les gélules, les capsules, les
suppositoires, les
crèmes, les pommades, les gels dermiques, les préparations injectables ou
buvables,
les aérosols, les gouttes oculaires ou nasales, etc...
La posologie utile varie selon l'âge et le poids du patient, la voie
d'administration, la
nature et la sévérité de l'affection, et la prise de traitements éventuels
associés et
s'échelonne de 0,5 mg à 25 rng en une ou plusieurs prises par jour.
Les exemples suivants illustrent l'invention mais ne la limitent en aucune
façon. Les
produits de départ utilisés sont des produits connus ou préparés selon des
modes
opératoires connus. Les différentes préparations conduisent à des
intermédiaires de
CA 02344255 2001-04-17
-21 -
synthèse utiles pour la préparation des composés de l'invention.
Les structures des composés décrits dans les exemples ont été déterminées
selon les
techniques spectrophotométriques usuelles (infrarouge, résonance magnétique
nucléaire, spectrométrie de masse, . . . ).
Les points de fusion ont été déterminés soit à la platine chauffante de Kofler
(K.), soit
à la platine chauffante sous microscope (M.K.). Lorsque le composé existe sous
forme
de sel, le point de fusion donné correspond à celui du produit salifié.
A titre indicatif, la numérotation adoptée pour les différents systèmes
tricycliques est
la suivante
5
3Y / S 2~X / 6 4 / 6
I '
2 X ~ 6 ' 3Y ~ ; ' 3 ~ 7
4
z Y~
z 1
s ~Y ~X i
/ sX Y
4 I 6 ~ 7 3
/ 7
7 e
3Y 4 ~ 6 ~ 4 ~ I 6
5
z X1
pREFARATION 1
6-Cyano-1-méthylsulfonyl S,6-dibydrocyclobuta[f]indole
Stade 1 : 1-Gyana-S-f(2,2-diméthoxyéthyl)amino%ben2aeyclabutane
Sur une suspension de 13,5 g de 1-cyano-5-aminobenzocyclobutane dans 400 ml de
1,2-dichloroéthane sont ajoutés par un goutte à goutte rapide, 26,5 ml d'une
solution
de 2,2-diméthoxyacétaldéhyde à 45 % dans le terbutylméthyléther, puis 16 ml
d'acide
acétique et enfin, par fraction, 39,7 g de triacétoxyborohydrure de sodium.
Après
élévation de la température jusqu'à 29°C, on refroidit à température
ambiante puis
2o agite 1 h 15 et hydrolyse en versant sur S00 ml d'une solution aqueuse
saturée en
CA 02344255 2001-04-17
-22-
hydrogénocarbonate de sodium. La phase organique est séparée, lavée à l'eau et
concentrée sous pression réduite pour conduire, avec un rendement quantitatif,
au
produit désiré.
Stade 2 : 1-Cyano S-~(N (2,2-diméthoxyéthyl)N méthylsulfonylaminoJ
benzocyelobutane
Une solution préparée à partir de 21,6 g du produit obtenu au stade 1
précédent, 58 ml
de pyridine et 225 ml de diclalorométhane est refroidie à 0°C. 10,8 ml
de chlorure de
mésyle sont ajoutés au goutte à goutte pendant 20 minutes et on agite encore
pendant
40 minutes à 0°C puis 20 h.°ures à température ambiante. Le
milieu réactionnel est
1o ensuite versé sur 40 ml d'une solution aqueuse saturée en
hydrogénocarbonate de
sodium. Après décantation, la phase aqueuse est extraite par 2 fois 150 ml de
chlorure
de méthylène. Les phases organiques jointes sont lavées à l'acide
chlorhydrique 1N,
séchées et concentrées pour conduire au produit attendu avec un rendement
quantitatif.
t5 Stade 3 : 6-Cyano-1-méthylscclfonyl-S,6-dihydrocyclobutaffJindole
Sur 2,1 1 de toluène à reflux sont coulés simultanément en 1 h 15, une
solution de 10,9
ml de chlorure de titane dans 450 ml de toluène et une solution de 27,9 g du
produit
obtenu au stade 2 dilué dans 450 ml de toluène. A la fin de l'addition, on
laisse
redescendre la température jusqu'à 40°C, puis verse sur 1,8 1 d'une
solution aqueuse
2o saturée en hydrogénocarbon,~te de sodium. Après décantation, la phase
aqueuse est
extraite au toluène, les phases organiques sont réunies, lavées, séchées,
concentrées.
Le résidu est purifif; par chromatographie sur gel de silice
(dichlorométhane/cyclohexane : 75/25) pour conduire au produit attendu et à
son
régioisomère.
25 Point de fusion : I42-144°C (MK)
PREPARA~~I[Q
6-Cyano-5,6-dihydrocyclobuta[f]indole
2,6 g du produit de la préparation 1 sont introduits dans une solution de 7,7
g de
CA 02344255 2001-04-17
- 23 -
potasse dans 190 ml de méthanol. Après 12 heures à reflux, le méthanol est
évaporé et
le résidu repris par de l'éther. Après lavage, la phase organique est séchée
et
concentrée pour conduire au produit attendu.
Point de fusïon : 126-128°C (MK)
PRFPARA_TIQN 3
6-Cyano-2,3,5,6-tétrahydrocyclobuta [ f ]indole
3,43 g du produit obtenu à. la préparation 2 sont solubilisés dans 55 ml
d'acide
acétique. Dans le milieu réacaionnel refroidi à 13°C, sont ajoutés, par
portions, en 5
minutes, 3,84 g de cyanoborohydrure de sodium. Après retour à température
lo ambiante, l'agitation est maintenue pendant 2 heures, puis le milieu
réactionnel est
refroidi à 0°C et amené à
pH = 11 par addition d'une solution de soude (45 g dans 250 ml d'eau). La
solution
laiteuse obtenue est extraite à l'éther. Les phases organiques sont lavées,
séchées et
concentrées pour conduire au. produit attendu sous forme de solide blanc.
Point de fusion : 85-87°C (MK)
~R,EPARAT10N 4
4-Cyano-1-méthylsulfonyl-4,5-dihydrocyclobuta [e] indole
Le régioisomère obtenu au stade 3 de la préparation 1 correspond au produit
attendu.
Point de fusion : 118-120°C (MK)
2o PRÉPARATION 5 :
4-Cyano-4,5-dihydrocyclobuta[eJindole
Le produit est obtenu selon le procédé de la préparation 2, en utilisant comme
substrat
le produit de la préparation 4.
Point de fusion : 132-134°C (MK)
CA 02344255 2001-04-17
-24-
P$~~'~,~,ATIUN 6
4-Cyano-2,3,4,5-tétrahydrocyclobuta[e]indole
Le produit est obtenu selon le; procédé de la préparation 3, en utilisant
comme substrat
le produit de la préparation 5.
PAR ,',PARATION 7
5-Cyano-5,6-dïhydrocyclobuta(f]benzothiophène
Stade 1: I-Cyano-4-thiométhyibenzocyclobutane
Dans 3,5 1 d'ammoniac liquide à reflux contenant des quantités catalytiques de
ferrocyanure de potassium et de trinitrate de fer monohydrate, sont introduits
en 2
to heures 50,8 g de sodium, puis en 5 minutes, 153 g de 3-(2-chloro-S-
thiométhylphényl)
propionitrile. On laisse réagir 1 heure à -33°C puis on introduit 118,2
g de chlorure
d'ammonium solide. Après ;,vaporation de l'ammoniac, le résidu est repris par
de
l'éther, les sels sont filtrés et le filtrat est évaporé à sec permettant de
conduire au
produit attendu.
t s Stade 2 : 1-Cyano-4-méthylsulfinylbenzocyclabutane
11 g de produit du stade 1 précédent sont dissous dans 70 ml de
dichlorométhane. Sur
la solution refroidie à -5"C est coulée une solution de 15,8 g d'acide m-
chloroperbenzoïque dans 80 ml de dichlorométhane. Après 10 minutes
d'agitation, le
milieu réactionnel est versé sur 100 ml d'eau et 100 ml de soude 1N. On
décante,
2o extrait à nouveau la phase aqueuse au dichlorométhane. Les phases
organiques
réunies sont lavées à l'hydrog;énosulfate de sodium, puis à la soude 1N, au
bicarbonate
de sodium et enfin à l'eau jusqu'à neutralité. La phase organique est séchée
et
concentrée pour conduire au produit attendu.
Stade 3 : 1-Cyano-4-mercaptobenzocyclobutane
CA 02344255 2001-04-17
- 25 -
Sur une solution de 11 g de produit obtenu au stade précédent dans 100 ml de
dichlorométhane sont ajoutés 9,76 ml d'acide trifluoroacétique dissous dans 20
ml de
dichlorométhane. L'addition dure 45 minutes durant laquelle la température est
maintenue à 25°C. Le milieu. réactionnel est encore agité 1 h 30 à
cette température,
puis évaporé à sec. Le résidu est repris 10 minutes sous agitation en présence
d'un
mélange 50/50 de triéthylamine et de méthanol. Après évaporation, on dilue au
dichlorométhane, lave par une solution saturée de chlorure d'ammonium puis à
l'eau,
sèche et concentre pour obtenir le produit attendu sous forme d'une huile.
Stade 4 : 1-Gyano-4-(2,2-diëthoxyéthylsulfanyl)benzocyclobutane
lo Sur une solution de 9,1 g du produit obtenu au stade 3 précédent dans 20 ml
de
tétrahydrofurane et 140 ml d'éthanol sont additionnés, à 20°C et par
portions 3,65 g de
borohydrure de sodium. Après 1 heure à 50°C, 2,14 g de borohydrure de
sodium
solide sont à nouveau ajoutés. Le milieu réactionnel est ensuite porté à
80°C et à cette
température on coule en 1 heure, 39 ml de diéthylacétal du bromoacétaldéhyde.
Le
chauffage est encore maintenu pendant 12 heures, puis le milieu réactionnel
refroidi
est versé sur 1 litre d'eau glacée. Le mélange obtenu est extrait à l'éther et
la phase
organique est lavée avec une solution de bicarbonate de sodium à 10 % puis à
l'eau.
La phase étherée est séchée et concentrée sous vide pour conduire au produit
attendu
sous forme d'huile.
2o Stade S : S-~yano-5,6-dihydrocyclabuta(fJbenzothiophène
10 g d'acide polyphosphorique, 8,5 g du produit obtenu au stade 4 précédent
dans 500
ml de chlorobenzène sont portés à 130°C pendant 4 heures. Après
refroidissement, le
surnageant est soutiré et le résidu est rincé au dichlorométhane. Le
surnageant et la
phase dichlorométhane sont réunies et neutralisées en ajoutant du bicarbonate
de
sodium en poudre. Après 15 minutes d'agitation, on filtre et évapore à sec. Le
résidu
est purifié par chromatographie sur gel de silice (cyclohexane/dichlorométhane
50/50) permettant d'obtenir lc produit attendu ainsi qu'un produit secondaire.
CA 02344255 2001-04-17
-26-
Point de fusion : 1(l2-103°C (MK)
PRFPARA_TI(?~8_
6-Cyano-5,6-dihydrocyclo>?uta[f ] benzothiophène
Le produit est obtenu selon le procédé de la préparation 7 des stades 1 à S
mais en
utilisant au stade 1 le 3-(3-bromo-4-thiométhylphényl)propionitrile à la place
du 3-(2-
chloro-5-thiométhylphényl)propionitrile.
PREPARA'~~[f)]~9
5-Cyano-5,6-dihydrocyclobuta[f]benzofurane
Stade 1: T-Cyana-4-(2,2-diéthoxyéthoxy)benzocyclobutane
lo Une solution de 16,5 g de 1-cyano-4-hydroxybenzocyclobutane dans 205 ml de
diméthylformamide est coulée sur une suspension de 67,8 mmol d'hydrure de
sodium
dans 160 ml de diméthylforrnamide. Le milieu réactionnel est agité 30 minutes
puis
une solution de 10,2 ml de 1-bromo-2,2-diéthoxyéthane dans 40 ml est
additionnée en
minutes et la température. est ensuite portée à 60°C pendant 6 heures.
On laisse
15 encore 12 heures sous agitation, évapore le diméthylformamide, reprend à
l'eau,
extrait au dichlorométhane, sèche et concentre sous vide. Le résidu est
chromatographié sur gel d.e silice (CHZCl2/AcOEt : 95/5) permettant d'isoler
le
produit attendu.
Stade 2 : S ~'yana-5,6-dihydrocyclabr~ta~fJbenzafurane
2o Le produit est obtenu comme au stade 3 de la préparation 1 mais en
utilisant le produit
du stade 1 précédent. Au cours d'une chromatographie sur gel de silice
(CHZC12/cyclohexane : 80/:?0), on isole le produit attendu ainsi qu'un produit
secondaire.
CA 02344255 2004-12-07
-27-
~-Cynno-5,6-dihydrocyclobuts~[/jbenzafnrane
Le produit est obtenu comme le produit de la préparation 9 mais en utilisant
au stade 1
le 1-cyano-5-hydroxybenzocyclobutane et au stade 2 comme éluant dans la
séparation
s des régioisomères le mélange CH2C12/cyclohexane : 75/25. Le produit attendu
est
isolé sous forme d'une huile.
5-Cyano-4,5-dihydrocyclobutx[e]benzothiapAène
Le produit secondaire obtenu au stade 5 de la préparation 7 correspond au
produit
1 o attendu.
,,
4-Cyano-4"â-dihydrocyclobuta[e]benzothiaphène
Le produit est obtenu au cours du stade S de la préparation 8.
is 5-Cys~no-4,5-dihydrncycMbuta[e]benzofu~ne
Le produit secondaire obtenu au stade 2 de la préparation 9 correspond au
produit
attendu.
4-Cynno-4,5-dihydrocyclobutn[e]benzofurnne
2o Le produit secondaire isolé lors de la chromatographie de la préparation 10
correspond au produit attendu.
CA 02344255 2001-04-17
-28-
~,6-Dihydrocyclobuta[f ] [1,3] benzodiaxole-5-carbonitrïle
46 g de 3-(6-bromo-1,3-benzodioxol-5-yl)propanenitrile sont introduits par
portions
dans 1,4 1 d'ammoniac liquide dans lequel est dissous de l'amidure de sodium
préalablement préparé par introduction de 16,7 g de sodium dans l'ammoniac
liquide.
Après 30 minutes de contact, le milieu réactionnel est traité par 38,7 g de
chlorure
d'ammonium puis l'ammoniac est distillé à température ambiante. Le résidu est
repris
par l'éther et filtré ; le précipité est lavé à l'éther. Les phases éthérées
réunies sont
évaporées et le résidu obtenu est recristallisé de l'alcool isopropylique
permettant
1o d'isoler le produit attendu.
Point de fusion : 91°C (M.K.)
6,?-DihydrocycIobuta[g] [1]benzofuran-7-carbonitrile
Stade 1 : 1-Cyano-6-(2,2-diéthoxyéthoxy) benzocyclobutane
Le produit est obtenu selon le procédé du stade 1 de la préparation 9 en
utilisant
comme substrat le 1-cyano-6-hydroxybenzocyclobutane.
Stade 2 b,? Dihydroçyclobuta~gJ(lJbenzofuran-1 carbonitrzle
Le produit est obtenu selon le procédé du stade 3 de la préparation 1 en
utilisant
comme substrat le produit obtenu au stade 1 précédent.
2o PREP~?,~1TION 1?
1,2-Dihydrocyclobuta[b]na~hthalène-1-carbonitrile
Le produit est obtenu selon le procédé de la préparation 15 en utilisant comme
substrat le 3-(3-iodo-2-naphthyl)propionitrile.
Point de fusion : 98-1Q2°C (M.K.}
CA 02344255 2001-04-17
-29-
]PREPA I_tATION 18
1,2-Dihydrocyclohuta[a]naphthalène-1-carbonitrile
Stade l : l,l Diéthaxy-1,2-dihydracyclobuta~aJnaphthalène
9,4 g d'amidure de sodium sont introduits dans 350 ml de tétrahydrofurane. Sur
ce
mélange sont coulés successivement 25,9 g de 1-bromonaphtalène et 28 g de 1,1-
diéthoxyethylène fraîchement préparé. Le milieu réactionnel est porté à reflux
pendant 16 heures puis repris à l'eau et l'éther. Après lavage à pH neutre de
la phase
organique et séchage de celle-ci, le produit attendu est isolé et
chromatographié sur
gel de silice (dichlorométhane/cyclohexane : 1/1).
1o Stade 2 : ~'yclobutafaJuaphtlralèn-1(2H)-one
lOg du produit obtenu au stade 1 sont traités à température ambiante par 42 ml
d'acide chlorhydrique 1N dissous dans 170 ml de tétrahydrofurane. Après 1h30
de
contact, le solvant est concentré et le résidu est versé sur 170 ml d'eau. 6,9
g d'un
solide correspondant au produit attendu sont alors isolé.
Pont de fusion : 92-94°C (M.K)
Stade 3 : 1,.~-Iaihydrocyclaf~uta~aJuaphthalèn-1-al
1,4 g de borohydrure de sodium sont ajoutés à une suspension, à 0-5°C,
de 5,2 g de
produit obtenu au stade 2 dans 150 ml de méthanol. Après 15 minutes à cette
température puis 1 heure à température ambiante, le milieu réactionnel est
coulé sur
300 g de glace et extrait au dichlorométhane. Après traitement usuel, 5,2 g du
produit
attendu sont isolés.
Point de fusion : 9G-100°C (M.K.)
Stade 4 : 1,2-Dihydraçyclobuta(aJnaphthalène-1-carbonitrile
CA 02344255 2001-04-17
-30-
5,1 g du produit obtenu au stade 3, 14,2 g de triphénylphosphine, 12 g de
tétrabromure de carbone dans 150 ml d'éther sont portés 2 heures à reflux.
Après
refroidissement, le milieu réactionnel est filtré, concentré, repris par 50 ml
d'éther,
filtré et évaporé. Les 7,85 g du résidu obtenu sont traités par 10,5 g de
tétrabutylammonium cyanure, dans 150 ml de tétrahydrofurane. Après 64 heures
de
contact à température ambiante, on concentre le milieu réactionnel et on le
reprend
par de la glace et de l'éther. Après décantation, une huile est isolée qui est
purifiée par
chromatographie sur gel de silice (dichlorométhane) permettant d'isoler le
produit
attendu.
to Point de fusion : ?8-84°C
PREPARA~~~,1~T 19 :
1-(Méthylsulfonyl)-5,6-dihydro-lhl cyclobuta[fjindole-5-carbonitrile
Le produit est obtenu selon lc~ procédé de la préparation 1 des stades 1 à 3
en utilisant
au stade 1 le 4-amino-1-cyanobenzocyclobutane.
I s Point de fusion : 164-168°C (M.K.)
~REPA ATION 20
5,6-Dihydro-1H eyclobuta[~]indole-5-carbonitrile
Le produit est obtenu selon le procédé de la préparation 2 mais en utilisant
comme
substrat le produit de la préparation 19.
2o Point de fusion : 109-113°C (M.K.)
PREPARATIQN 21 :
2,3,5,6-Tetrahydro-1H cyclobuta[~indole-5-carbonitrile
Le produit est obtenu selon le procédé de la préparation 3 mais en utilisant
comme
substrat le produit de la préparation 20.
25 Point de fusion : 100-105°C (M.K.)
CA 02344255 2001-04-17
-31 -
I-[6-(Aminométhyl)-2,3,5,6-tétrahydro-1H cyclobuta[f]indol-6-yl]cyclohexanol
Stade A : 6-(1-Hydro~eycyclohexyl)-2,3,5,6-tétrahydro-IH cyelobuta~fJindole-
6-
earbor~itrile
4,1 g du produit obtenu à la préparation 3 sont dissous dans 215 ml de
tétrahydrofurane. Le milieu réactionnel est refroidi à -80°C et 19,25
ml d'une solution
2,5 M de n-butyllithium dans l'hexane sont additionnés. A la fin de
l'addition,
l'agitation est maintenue 20 minutes puis 6,2 ml de cyclohexanone sont coulés
en 3
1o minutes. Après 2 heures de contact à 80°C, on laisse revenir à
température ambiante
et introduit 23 ml d'une solution aqueuse saturée de chlorure d'ammonium, puis
135
ml d'eau. Après décantation, la phase organique est lavée par une solution
saturée de
chlorure de sodium, séchée, concentrée. Le résidu obtenu est concrétisé de
l'éther
isopropylique, filtré pour obtenir le produit désiré et le filtrat est purifié
par
chromatographie sur gel de silice (CHZC12/AcOEt : 90/10) pour isoler une
quantité
supplémentaire de produit attendu.
Point de fusion : I68-170°C
Stade B : 1 ~G-(Aminorraëthyl)-2,3,5,6-tétrahydro-1H cyclobuta(fJindol 6 ylj
cyclohexar~ol
4 g du produit obtenu au stade A précédent sont dissous dans 200 ml d'une
solution
3,6 N de méthanol ammoniacal contenant 2 ml de nickel de Raney. Le mélange
réactionnel est hydrogéné sous une pression de 30 bars à 60°C pendant
24 heures.
Après filtration et évaporation du solvant, le résidu est repris par du
dichlorométhane,
lavé à l'eau jusqu'à neutralitc:, séché et concentré pour isoler le produit
attendu sous
forme d'une huile.
~,~:
I-{6-[(Diméthylamino)méthyl]-1-mëthyl-2,3,5,6-tétrahydro-1H
CA 02344255 2001-04-17
-32-
cyclobuta[f]indol-6-yl}cyclohexanol
659 mg du produit de l'exemple 1 sont dissous dans 20 ml d'acétonitrile. Dans
la
solution refroidie à 0°C, 608 mg de cyanoborohydrure de sodium et 1,5
ml d'une
solution de formaldéhyde ~i 37 % dans l'eau sont introduits en maintenant la
température à 0°C. Après 20 heures à température ambiante, on hydrolyse
par 33 ml
d'acide chlorhydrique 1 N, et: agité pendant 3 heures. Le mélange réactionnel
est lavé
avec 30 ml d'éther puis basifié par de la soude à 20 %. La phase aqueuse est
extraite
au dichlorométhane. Après séchage et évaporation, le résidu est purifié par
chromatographie sur gel de silice (CHZCIz/EtOH : 95/5) pour conduire au
produit
1 o attendu.
Point de fusïon : 121-124°C (MIS)
1~.XL1V11~'L~. 3
1-~6-[(Diméthylamino)méthyl]-2,3,5,6-tétrahydro-1H cyclobuta[f]indol-6-yl}
cyclohexanol
t5 Stade.A : b-(1-FiydroxJacyclahexyl~-1-(méthylsulfvnyl)-2,3,5,6-tétrahydro-
ll
cyclvbuta%fji'ndale-6-curbonitrile
On procède comme au stade 2 de la préparation 1 mais en utilisant le produit
du stade
A de l'exemple 1. Le produit attendu est concrétisé dans l'éther sous forme
d'un solide
violet.
2o Point de fusïon : 1?4-176°C
Stade B : l-~6-(Aminamëthyl)-1-(méthylsulfonyl)-2,3;5,6-tétrahydro-1H
cyclobuta~fJi'ndol 6 ylJcyclohexanol
On procède comme au stade B de l'exemple 1 mais en utilisant le produit du
stade A
ci-dessus. On obtient le produit attendu sous forme d'une meringue jaune.
25 Stade ~ : I-,(6-~(Dimétitylamino)rnéthylj I-(méthytsutfonyl)-2,3,5,~-
CA 02344255 2001-04-17
-33-
tétrahydro-Ihl-
cyclobuta(fJindol-6 ylJcyclohexanol
On procède dans l'exemple 2 mais en utilisant le produit du stade B ci-dessus.
Le
produit attendu est obtenu sous forme d'un solide jaune.
Point de fusion : 156-158°C (MK)
Stade D : 1-(6 ~(Diméthylamino)méthylJ 2,3,5,6-tétrahydra-IH
cyclobuta(fjindol
6 yl,~cyclohexanol
40 ml d'ammoniac liquide sont introduits dans un tricol puis 380 mg du produit
obtenu au stade C dissout dans 10 ml de tétrahydrofurane. On refroidit à -
50°C et
introduit dans le milieu réactionnel 100 mg de sodium en plusieurs fois. Après
15
minutes de contact, on introduit par fractions 430 mg de chlorure d'ammonium
en
poudre. On laisse ensuite remonter à température ambiante. Après évaporation
de tout
l'ammoniac, on reprend à l'eau, extrait à l'éther, sèche et concentre, pour
obtenir le
produit attendu.
Point de fusion : 159-161°C (MK)
1-[5-(Amïnom~thyl)-5,6-dihydrocyclobuta [ f ] [1] benzofuran-5-yl]
cyclohexanol
StadeA : S-(I-Hydroxycyclohexyl)-5,6-dihydrocyclobuta%fJ~IJbenzafuran-5:-
carbonitrile
On procède comme au stade A de l'exemple 1 mais en utilisant le produit de la
préparation 9 et en effectuant l'hydrolyse du milieu réactionnel à -
75°C. On isole le
produit attendu sous forme d'un solide.
Point de fusion : 154-158°G (MK)
CA 02344255 2001-04-17
-34-
Stade B : 1-~S (Aminométhyl)-5,6-dihydrocyelobuta(fJ(IJbenzofuran-5 ylj
eyclohexan o l
Une solution de 520 mg du produit obtenu au stade A précédent dans 10 ml de
tétrahydrofurane est additionnée goutte à goutte à 0°C, sous courant
d'azote, à une
suspension de 177 mg d'aluminohydrure de sodium dans 10 ml d'éther. Le milieu
réactionnel est agité une heure à température ambiante puis hydrolysé par 0,26
ml
d'eau, 0,79 ml de soude à 20 % et 1,05 ml d'eau. Après 15 minutes d'agitation
à
température ambiante, on filtre et évapore à sec. Le produit attendu est
obtenu sous
forme d'une meringue collante.
1 o EXEAMPLE 5 :
1-(5-[(Dim~thylamino)méthyl]-5,6-dihydrocyclobuta[f] [1]benzofuran-5-yl}
cyclohexanol
400 mg du produit de l'exemple 4 sont solubilisés dans 12 ml d'acétonitrile.
Après
refroidissement à 0°C sont successivement ajoutés 0,55 ml d'une
solution de
formaldéhyde à 37 % dans l'eau et 185 mg de cyanoborohydrure de sodium . Après
1
heure à 0°C et 2 heures ,~ température ambiante, 0,55 ml de la solution
de
formaldéhyde à 37 % dans :l'eau et 185 mg de cyanoborohydrure de sodium sont à
nouveau ajoutés et l'agitation. est encore maintenue 12 heures à 20°C.
On hydrolyse à
température ambiante par 22.,3 ml d'acide chlorhydrique (1N) et agite 1 heure,
basifie
2o à 0°C par de la soude à 20 %, extrait au dichlorométhane, lave à
l'eau, sèche et
concentre. Une chromatographie sur gel de silice (CHZC12/EtOH : 90/10) permet
d'isoler le produit attendu sous forme de cristaux blancs.
Point de fusion : 127-136°C (M.K)
ALE 6
1-[5-(Aminomëthyl)-5,6-dihydrocyclobuta[f] [1]benzothien-5-yl]cyclohexanol
On procède comme dans l'exemple 4, des stades A à B, en utilisant au stade A
le
CA 02344255 2004-12-07
- 35 -
produit de la préparation 7.
FXF~IP~L~F ?
1-{5-[~im~thylamina)méthyl]-â,&-dihydracyclabuta[,/'j [1]ben~athïen-â-yl}
cycloheaanol
s On procède comme dans l'exemple 5 en utilisant comme substrat le produit de
l'exemple 6.
Foïnt de fusion : 151-155°C (MK)
F1~FMPt.F 8
1-{6-[(Diméthylamino)m~thyl]-1-m~thyl-5,6-dihydro-1H-cyclabuta [f ] indal-6-
yl}
io cyclohexanol
0,44 g du produit de l'exemple 2 et 1,23 g de dioxyde de manganèse sont
introduits
dans 15 ml de toluène. Le milieu réactionnel est agité 24 heures à température
ambiante puis 0,6 g de dioxyde de manganèse sont à nouveau introduits,
l'agitation
étant poursuivie 24 heures supplémentaires. Après filtration sur CéliteTM et
1 s évaporation du solvant, le résidu est purifié par chromatographie rapide
sur gel de
silice (CHZCI2/NieOH/NH40H : 98/20/0,2 %) pour conduire au produit attendu.
Païnt de fusïon :148-150°'C (MK)
F~E~L~.g
1-{?-[(Dim~thylamina)méthyl]-2,3,6,?-têtrahydro-1H-cyclobu~[e]indol-?-yl}
2o cyclahexnnol
Stu~A : 7-(1 Hydraxyc~clotee~xyl)-2,~,~,~-tël~ahydn~-ll~-cycl~butofeJind~le~-
?-carbonitrile
Le produit est obtenu comme au stade A de l'exemple 1 mais en utilisant le
produit de
la préparation 6 au lieu du produit de la préparation 3.
CA 02344255 2001-04-17
-36-
Stade B : 1-~7 ~(Dimétliylamino~méthylJ-2,3,6,7 tétrahydro-1H-
eyclobc~ta~eJindol-
7 ylJcyclohexanol
On procède comme à l'exemple 3 des stades A à D mais en utilisant au stade A
de cet
exemple le produit du stade A ci-dessus.
1-[6-(Aminométhyl)-5,6-dihydrocyclobuta [ f ] [1 ] benzothien-6-
yl]cyclohexanol
Le produit est obtenu selon l.e procédé de l'exemple 4 des stades A à B, en
utilisant
comme substrat au stade A le composé de la préparation 8.
to
~X~PLE I1
1-[6-(Aminoraéthyl)-5,6-dihydrocyclobuta[~j [1]benzofuran-6-yl]cyclohexanol
Le produit est obtenu selon ie procédé de l'exemple 4 des stades A à B, en
utilisant
comme substrat au stade A le composé de la préparationl0.
FXF~LV~P~~~E I2
1-{6-[(Diméthylamino)méthyl]-S,fi-dihydrocyclobuta[f j [1]benzofuran-6-yl}
cyclohexanol
Le produit est obtenu selon le procédé de l'exemple 5, en utilisant comme
substrat le
composé de l'exemple 11.
E~EMFLE 13
1-[6-(Aminométhyl)-6,7-dihydrocyclobuta[e][1]benzothien-6-yl]cyclohexanol
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, en
utilisant
comme substrat au stade A le composé de la préparation 11.
CA 02344255 2001-04-17
-37-
1-[7-(Aminomëthyl)-6,7-dihydrocyclobuta[e] [1]benzothien-?-yljcyclohexanol
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, en
utilisant
comme substrat au stade A le composé de la préparation 12.
EXEMPLE 15 :
1-[6-(Aminométhyl)-6,7-dihydrocyclobuta[e] [1]benzofuran-6-yl]cyclohexanol
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, en
utilisant
comme substrat au stade A le composé de la préparation 13.
1-[7-(Aminomëthyl)-6,7-dihydrocyclobuta[e] [1]benzofuran-7-yl]cyclohexanol
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, en
utilisant
comme substrat au stade A le composé de la préparation 14.
1-{6-[(Dimëthylamino)mëthyl]-5,6-dihydrocyclobuta[f J [1]benzothièn-6-yl}
ts cycIohexanol
Le produit est obtenu selon le procédé de l'exemple 2, en utilisant comme
substrat le
composé de l'exemple 10.
Point de fusion : 161-166°C (M.K.)
1-{5-[(I?imëthylamino)mëthyl]-5,6-dihydrocyclobuta(f] [1,3]benzodioxol-5-
yl}cyclohexanol
CA 02344255 2001-04-17
-38-
Le produit est obtenu selon le procédé de l'exemple 1 des stades A à B, puis
selon le
procédé de l'exemple 2, en utilisant comme substrat au stade A de l'exemple 1
le
produit de la préparation 15 à la place de celui de la préparation 3.
Point de fusion : 94-96°C (M.K.)
~ E~MFLE 19 :
1-~5-[(Diméthylamino)méthyl]-5,6-dihydrocyclobuta(fj [1]benzofuran-5-
yl]cyclopentanol et son chlorhydrate
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, puis
selon le
procédé de l'exemple 5, en utilisant comme substrat au stade A la
cyclopentanone à la
1o place de la cyclohexanonè. La base libre est transformée en son
chlorhydrate par
action de l'éther chlorhydrique.
Point de fusion : 258-262°C (M.K.)
~,xLmrL~ ~u :
1-(S-[(~iméthylamino)méthyl]-5,6-dihydrocyclobuta[f] [1,3]benzodioxol-5-yl}
cyclopentanol
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, puis
selon le
procédé de l'exemple 5, en utilisant comme substrat au stade A la
cyclopentanone à la
place de la cyclohexanone e1; le produit de la préparation 15 à la place de
celui de la
préparation 9.
2o Point de fusion : ?1-?4°C (lWI.K.)
~EMP ':
1-[5-(Aminométhyl)-5,6-dihydrocyclobuta[f] [1]benzothièn-5-yl]cyclopentanol
CA 02344255 2001-04-17
-39-
Le produit est obtenu selon :le procédé de l'exemple 4 des stades A à B en
utilisant
comme substrat au stade A la cyclopentanone à la place de la cyclohexanone et
le
produit de la préparation 7 à la place de celui de la préparation 9.
Point de fusion : 14~-153°C (M.K.)
EKEMPLE 22
1-{5-[(Mëthylamino)méthyl]-5,6-dihydrocyclobuta [f] [ 1] benzothièn-5-
yl}cyclopentanol
Sur un mélange de 1 g du produit de l'exemple 21, 1,2 ml de triéthylamine et
60 ml
de dichlorométhane est introduite, à 0°C, une solution de 0,29 ml de
chloroformiate
1o d'éthyle dans 40 ml de dichlorométhane. Après retour à température
ambiante, le
milieu réactionnel est lavé par de l'acide chlorhydrique 0,1 N puis par une
solution
saturée de bicarbonate de sodium, séché puis évaporé. Le résidu obtenu est
dissout
dans 20 ml de tétrahydrofurane. La solution est ajoutée à un mélange de 1,3 g
de
AlLiH4 dans 60 ml de tétrahydrofurane. Le milieu réactionnel est porté au
reflux
pendant 3 heures puis hydrolysé par 0,65 ml d'eau, 0,45 ml de soude à 20% et
2,1 ml
d'eau. Après filtration et concentration, le résidu est purifié par
chromatographie sur
gel de silice (dichlorométhane/éthanol/NH40H : 95/5/0,5) et recristallisé de
l'éther
isopropylique pour conduire au produit attendu.
Point de fusion : 166-169°C (M.K.)
2o EXEMPLE 23 :
1-{5-[(Diméthylamino)méth.yl]-5,6-dihydrocyclobuta [f] [ 1 ] benzothièn-5-yl}
cyclopentanol
Le produit est obtenu selon le procédé de l'exemple 5 en utilisant le produit
de
l'exemple 21 à la place de celui de l'exemple 4.
Point de fusion : 93-98°C (M.K.)
E~T~~L.E.~4
(+) 1-{5-[(Diméthylamino)méthyl]-5,6-dihydrocyclobuta[f][1]benzothièn-5-yl}
cyclopentanol
CA 02344255 2001-04-17
-40-
Le produit de l'exemple 23 est injectée sur une colonne chirale avec une phase
mobile
composé de méthanol/diéthylamine : 1000/1. Le premier produit élué correspond
à
l'isomère (+).
Point de fusion : 122-126°C (M.K.)
s F-X~Mp~,E 2S
(-) 1-{5-[(Dimëthylamino)mëthyl]-5,6-dihydrocyclobuta(f][1]benzothièn-5-yl}
cyclopentanol
Le produit de l'exemple 23 est injectée sur une colonne chirale avec une phase
mobile
composé de méthanol/diéthylamine : 1000/1. Le deuxième produit élué correspond
à
lo l'isomère (-).
Point de fusion : 123-127°C (M.K.)
EXEI\%I~~'t
1-[6-(Aminomëthyl)-5,6-dihydrocyclobuta[f] [1]benzothièn-6-yl]cyclopentanol
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B en
utilisant
15 comme substrat au stade A la cyclopentanone à la place de la cyclohexanone
et le
produit de la préparation 8 à la place de celui de la préparation 9.
Point de fusion : 141-143°C (M.K.)
EXEMPLI~;, 27 :
1-{6-[(Mëthylamino)mëthyl]-5,6-dihydrocyclobuta[fJ[1]benzothièn-6-
20 yl}cyclopentanol
Le produit est obtenu selon le procédé de l'exemple 22 en utilisant le produit
de
l'exemple 26 à la place de celui de l'exemple 21.
Point de fusion : 11?-12Q°C (M.K.)
~XEMPhE 28
25 1-{6-[(Dimëthylamïno)mëthyl]-S,6-dihydrocyclobuta[f j [1]benzothïèn-6-
yl}cyclopentanol
CA 02344255 2001-04-17
-41 -
Le produit est obtenu selon le procédé de l'exemple 5 en utilisant le produit
de
l'exemple 26 à la place de celui de l'exemple 4.
Point de fusion : 94-96°C (M.K.)
~XEI~IE~
1-}6-[(~iméthylamïno)méthyl]-1-méthyl-5,6-dihydro-1H cyclobuta[f]indol-6-yl}
cyclopentanol
Le produit est obtenu successivement selon le procédé des exemples 1, 2 et 8,
en
utilisant au stade A de l'exemple 1 la cyclopentanone à la place de la
cyclohexanone.
Foint de fusion : 108-111°C (M.K.)
i o ~:~E. 30
1-{S-[(diméthylamino)méthyl]-1-méthyl-5,6-dihydro-1H cyclobuta[JJindol-5-yl}
cyclopentanol
Le produit est obtenu successivement selon le procédé des exemples 1, 2 et 8,
en
utilisant au stade A de l'exemple 1 la cyclopentanone à la place de la
cyclohexanone
et le produit de la préparation 21 à la place de celui de la préparation 3.
Point de fusion : 100-104°C (M.K.)
~'~~:EMPLE 31
1-{7-[(Diméthylamino)méthyl]-6,7-dihydrocyclobuta[g] [1]benzofuran-7-yl}
cyclopentanol
2o Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B,
puis selon le
procédé de l'exemple 5, en utilisant comme substrat au stade A la
cyclopentanone à la
place de la cyclohexanone et le produit de la préparation 16 à la place de
celui de la
préparation 9.
Point de fusion : 135-137°C (M.K.)
CA 02344255 2001-04-17
-42-
~YE~P~L~E 32
I- f 6-[(Dimëthylamino)méthyl]-5,6-dihydrocyclobuta[f] [1]benzofuran-6-yl}
cyclopentanol et son chlorhydrate
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, puis
selon le
s procédé de l'exemple 5, en utilisant comme substrat au stade A la
cyclopentanone à la
place de la cyclohexanone et le produit de la préparation 10 à la place de
celui de la
préparation 9.Le chlorhydrate est préparé par action de l'éther chlorhydrique.
Point de fusion (chlorhydrate) : 225-235°C (M.K.)
F~~EMPLE 33 :
l0 1-~6-[(Dimëthylamino)méth.yl]-2,3,5,6-tétrahydro-IH cyclobuta[f]indol-6-yl)
cyclopentanol
Le produit est obtenu selon le procédé de l'exemple 3 des stades A à B en
utilisant au
stade A le produit préparé au stade A de l'exemplel à partir de la
cyclopentanone et
non pas de la cyclohexanone.
ts Point de fusïon : 1(15-I08°C; (M.K.)
~~IEMPLE 34
1-(6-[(Diméthylamino)méthyl]-5,6-dihydro-1H cyclobuta[f]indol-6-
yl)cyclopentanol
Le produit est obtenu selon le procédé de l'exemple 8 en utilisant comme
substrat le
2o produit de l'exemple 33.
Point de fusion : 180-I84°C,' (M.K.)
~~XEM~1~E 35 :
I-{1-[(I~imëthylamino)méthyl]-1,2-dihydrocyclobuta[b]naphthalèn-1-
yl)cyclopentanol
CA 02344255 2001-04-17
- 43 -
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, puis
selon le
procédé de l'exemple 5, en utilisant comme substrat au stade A la
cyclopentanone à la
place de la cyclohexanone et le produit de la préparation 17 à la place de
celui de la
préparation 9.
s Point de fusion : I33-I35°Cò (M.K.)
1-(7-[(Diméthylamino)méthyl]-6,7-dihydro-3H cyclobuta[e]indol-7-
yl}cyclopentanol
Le produit est obtenu selon le procédé de l'exemple 3 des stades A à D, puis
de
to l'exemple 8 en utilisant au stade A de l'exemple 3 le produit préparé au
stade A de
l'exemple 1 mais en utilisant d'une part le produit de la préparation 9 et
d'autre part la
cyclopentanone.
Point de fusion : 200-204°C,' (M.K.)
15 1-{1-[(Dimcthylamino)methyi]-I,2-dihydrocyclobuta[a]naphthalèn-1-
yl}cyclopentanol et son chlarhydrate
Le produit est obtenu selon le procédé de l'exemple 4 des stades A à B, puis
selon le
procédé de l'exemple 5, en utilisant comme substrat au stade A la
cyclopentanone à la
place de la cyclohexanone et: le produit de la préparation 18 à la place de
celui de la
2o préparation 9. Le chlorhydrate est préparé à partir de l'éther
chlorhydrique.
Point de fusion (chlorhydrate) : 258-262°C (M.K.)
I-(?-}[((2S) 2,3-Dihydro-I,4-benzodioxin-2-ylméthyl)amïno]méthyl}-6,7-
dihydrocyclo-buta[g][I]benzofuran-7-yl)cyclopentanol et son chlorhydrate
CA 02344255 2001-04-17
-44-
StadeA : 1 ~7 (Amïnomëthyl)-6,7 dihydrocyclobuta~gJ~IJbenzofuran-7 ylj
cyclapentanol
Le produit est obtenu selon l.e procédé de l'exemple 4 des stades A à B en
utilisant
comme substrat au stade A la cyclopentanone à la place de la cyclohexanone et
le
produit de la préparation 16 à la place de celui de la préparation 9.
Stade B : (~R) N-~f7 (1-Hydroxycyclopentyl)-6,7 dihydrocyclo-
butafgj~IJbenzofuran-7 ylJmethylf-2,3-dihydro-1,4-benzodioxëne-2-
earboxamide
Sur 900 mg du composé obtebu au stade A dans 30 ml de dichlorométhane et 1,2
ml
1o de düsopropyléthylamine, à 0°C, est ajoutée une solution de 762 mg
de chlorure de
l'acide (2R) 2,3-dihydrobenzo[1,4]dioxin-2-yl carboxylique. Après 48 heures à
température ambiante, le milieu réactionnel est dilué à l'eau, extrait au
dichlorométhane. Un traitement classique des phases organiques permet après
évaporation sous pression réduite d'isoler le produit attendu sous forme de
meringue.
Stade E'' : 1-(7 ~~((2S) 2,3 Dihydro-1,4-benzodioxin-2-
ylméthyl)aminoJméthyl)-6, 7
dïhydrocyclobuta~gJ~IJbenzofuran-7 yl)cyclopentanol et son
chlorhydrate
500 mg d'hydrure de lithium aluminium dans 20 ml de tétrahydrofurane sont
portés à
2o reflux, puis 1,1 g du produit obtenu au stade B dissout dans 20 ml de
tétrahydrofurane
sont ajoutés. Après 3h30 de relux, le milieu réactionnel est hydrolysé par
addition de
0,45 ml d'eau, 0,31 ml de soude à 20% et 1,67 ml d'eau. Après filtration et
évaporation, une chromatographie sur gel de silice du résidu
(dichlorométhane/éthanol : 98/2) permet d'isoler le produit attendu qui est
transformé
en son chlorhydrate par action de l'éther chlorhydrique.
Point de fusion (chlorhydrate) : 213-235°C
CA 02344255 2001-04-17
- 45 -
IF~~F
1-(5-{[((2R) 2,3-Dihydro-1,4-benzodioxin-2-ylméthyl)amino]méthyl}-~,6-
dïhydro-
cyclobuta[j][1,3]benzadioxol-5-yl)cyclopentanol et son chlorhydrate
Le produit est obtenu selon le procédé de l'exemple 3$ des stades A à C, en
utilisant
au stade A le produit de la préparation 15 et au stade B le chlorure de
l'acide (2S)-2,3-
dihydrobenzo[1,4]dioxin-2-yl carboxylique.
Point de fusion (chlorhydrate) : 109-119°C (M.K.)
1 o EXh,MPLE 4Q
1-(1-f [[2-(5-Fluoro-1H indol-3-yl)éthyl](méthyl)amino]méthyl}-1,2-
dihydrocyclobuta[b]naphthalén-1-yl)cyclopentanol
Stade A : 1-~~(Méthyl)aminoJméthylJ-1,2-dihydrocyclohuta,(bJnaphthalèn-1-
yl)
t 5 cyclopentanal
Le produit est obtenu selon le: procédé de l'exemple 22 en utilisant comme
substrat le
1-[1-(aminométhyl)-1,2-dihydrocyclobuta[b]naphthalèn-1-yl]cyclopentanol qui
est
obtenu à partir de la préparation 17
Stade B : 2-(S Fluoro-IH indot 3 yl)N-~~l-(1-hydroxycyclopentyl)-1,2-
2o dihydrocyclohuta(bJnaphthalèn-I ylJméthylJ N-mëthylacétamide
0,652 g d'acide (5-fluoro-indol-3-yl)acétique dissous dans 30 ml de
dichlorométhane
sont traités par 0,61 g de carbonyldümidazole, à température ambiante pendant
30
minutes. Une solution de 0,95 g du produit obtenu au stade A dissous dans 5 ml
de
dichlorométhane sont coulés sur la solution. En fin de réaction, le milieu
réactionnel
25 est repris par de l'eau, décanté, séché, évaporé, pour conduire au produit
attendu.
Stade ~' : I-(I-~(~2-(S-fluoro-IH indal 3 yl)éthylJ(méthyl)aminoJméthylJ-1,2-
CA 02344255 2001-04-17
-46-
dihydrocyelobuta~bJnaphthalèn-I yl)cyclopentanol
Le produit est obtenu selon le; procédé de l'exemple 39 en utilisant comme
substrat le
produit obtenu au stade B précédent.
ÉTUDE PHAI~MACOLOGIpUE DES COMPOSES DE L'INTENTION
A. Études in vitro
Détermination de l'affïnité pour les sites de recapture de la sërotonine
L'affinité a été déterminée par des expériences de compétition avec la [3H]-
paroxetine
(NEN, Les Ulis, France). Le:. membranes sont préparées à partir de cortex
frontal de
1o rat et incubées en triple avec 1,0 nM de [3H]-paroxetine et le ligand froid
dans un
volume final de 0,4 ml, pendant 2 heures à 25° C. Le tampon
d'incubation contient 50
nM de TRIS-HCl (pH 7,4), 120 mM de NaCI et 5 mM de KCI. La fixation non-
spécifique est déterminée avec 10 ~M de citalopram. A la fin de l'incubation,
le
milieu d'incubation est filtre et lavé trois fois avec 5 ml de tampon
refroidi. La
radioactivité retenue sur les filtres est déterminée par comptage du liquide
de
scintillation. Les isothermes de binding sont analysées par régression non-
linéaire
pour déterminer les valeurs d'ICso. Elles sont converties en constante de
dissociation
(K;) par l'intermédiaire de l'équation de Cheng-Prusoff
K;=ICSa/(1 +L/Kd)
2o dans laquelle L est la concentration de [3H]-paroxetine et Kd est la
constante de
dissociation de [3H]-paroxetine pour le site de recapture de la sérotonine
(0,13 nM).
Les résultats sont exprimés en pK; (- log K;).
Les composés de la présente invention montrent une très bonne affinité pour
les sites
de recapture de la sérotonine, leur pK; est >_ 7.
CA 02344255 2001-04-17
-47-
EXEMPLE 42
Déterminatia~n de l'afîinité pour les sites de recapture de la noradrénaline
L'affinité a été déterminée par des expériences de compétition avec la [3H]-
nisoxétine
(Amersham, les Ulis, France). Les membranes sont préparées à partir de cortex
frontal
de rat et incubées en triple avec 2 nM de [3H]-nisoxétine et le ligand froid
dans un
volume final de 0,5 ml, pendant 4 heures à 4° C. Le tampon d'incubation
contient 50
mM de TRIS-HCl (pH 7,4), 300 mM de NaCI et 5 mM de KCI. La fixation non-
spécifique est déterminée avec 10 pM de desipramine. A la fin de l'incubation,
le
milieu d'incubation est filtra; et lavé trois fois avec 5 ml de tampon de
filtration
1o refroidi (50 mM de TRIS-HCI, pH 7,4, 300 mM de NaCI et 5 mM de KCl). La
radioactivité retenue sur les filtres est déterminée par comptage du liquide
de
scintillation. Les isothermes de binding sont analysées par régression non-
linéaire
pour déterminer les valeurs d'ICSO. Elles sont converties en constante de
dissociation
(K;) par l'intermédiaire de l'équation de Cheng-Prusoff
K;=ICSO/(1+L/Kd)
dans laquelle L est la concentration de [3H]-nisoxetine et Kd est la constante
de
dissociation de [3H]-nisoxetine pour le site de recapture de la noradrénaline
(1,23
nM). Les résultats sont exprimés en pKi (-log Ki).
Le pKi des composés de l'invention est >_ 6.
2o B. Études in vivo
EXEIVIFLE 43
Expérience de la microdialyse chez le rat
Les rats sont anesthésiés au pentobarbital (60 mg/kg i.p.). Ils sont placés
dans un
appareil stéréotaxique de Kopf et le guide de la canule est implanté dans le
cortex
frontal cingulé suivant les coordonnées décrites comme suit dans l'atlas de
Paxinos et
Watson (1982) : AP = + 2,2 ; L = ~ 0,6 ; DV = - 0,2. Les rats sont mis en cage
séparément et ne sont utilisés en dialyse que 5 jours plus tard. Le jour de la
dialyse la
CA 02344255 2001-04-17
-48-
sonde est descendue lentement et maintenue dans sa position. La sonde est
perfusée à
un débit de 1 ~1/mn avec u.ne solution de 147,2 mM de NaCI, 4 mM de KCl et
2,3 mM de CaCl2 amené à pH 7,3 avec un tampon phosphate (0,1 M). Deux heures
après l'implantation, les échantillons sont collectés toutes les 20 minutes
pendant
4 heures. Trois échantillons de base sont collectés avant l'administration des
produits
à tester. Les rats sont laissés dans leur cage individuelle pendant toute
l'expérience. A
la fin de l'expérience, les rats sont décapités et le cerveau prélevé est
congelé dans
fisopentane. Des sections d'une épaisseur de 100 qm sont coupées et colorées
avec du
cresyl violet, ce qui permet la vérification de l'emplacement des sondes.
lo La quantification simultanée de dopamine, norépinéphrine et sérotonine est
effectuée
de la façon suivante : 20 ~l d'échantillon de dialyse sont dilués avec 20 ~1
de phase
mobile (NaH2PO4 : 75 mM, EDTA : 20 ~M, sodium 1-decanesulfonate : 1 mM,
méthanol : 17,5 %, triethylamine : 0,01 %, pH : 5,70) et 33 ~l d'échantillons
sont
analysés par HPLC avec une colonne en phase inverse thermostatée à 45°
C et
quantifiés par l'intermédiaire d'un détecteur coulométrique. Le potentiel de
la
première électrode du détecteur est fixée à
- 90 mV (réduction) et la seconde à + 280 mV (oxydation). La phase mobile est
injectée avec une pompe à un débit de 2 ml/mn. Les limites de sensibilité pour
la
dopamine, la norépinéphrine et la sérotonine sont de 0,55 fmole par
échantillon. Tous
les produits de l'invention sont injectés par voie sous-cutanée dans un volume
de
1,0 ml/kg. Les produits sont dissous dans de l'eau distillée additionnée de
quelques
gouttes d'acide lactique si nécessaire.
Résultats
A titre d'exemple et pour illustrer l'activité des produits de l'invention, le
composé de
l'exemple 5, administré à la dose de 10 mg/kg, par voie sous-cutanée, augmente
le
niveau de sérotonine de : 250 ~ 15 %, celui de la noradrénaline de 500 ~ 13 %
et celui
de la dopamine 400 ~ 50 % (% maximal de l'effet par rapport au niveau basal
défini
comme le 0 %).
CA 02344255 2004-12-07
-49-
' '
Test d'enfouissement des billes chez la souris
Ce test permet d'évaluer la capacité d'agents pharmacologiques à inhiber le
comportement spontané d'enfouissement de billes chez la souris, cette
inhibition étant
s prédictive d'action antidépressive et/ou anti-impulsive. Des souris mâles de
souche
NMRI (Iffa-Credo, fArbresle, France), pesant 20-25 g le jour de l'expérience,
sont
placées individuellement dans des boîtes en Macrolon~ (30 x 18 x 19 cm)
contenant 5
cm de sciure et recouvertes par une plaque en PlexiglassTM perforée. Vingt-
quatre
billes en verre "oeil-de-chat" sont réparties régulièrement sur la sciure à la
périphérie
1o de la boîte. Au terme de 30 minutes d'exploration libre, les animaux sont
retirés de la
boîte et le nombre de billes enfouies est comptabilisé.
R~str&t~
A titre d'exemple, le tableau montre (effet d'un produit de (invention, en
comparaison
avec celui de la fluoxétine, un antidépresseur de référence.
Exemple Enfoui,~se~tt des illes chez
la sorarts DIS~
Fluoxtine 8,03
5 0,6
1 s DIso ose inhibitriceso
= d
Les doses
sont exprimes
en mg/kg
s.c.
Composition pharmaceutique : comprimés
Formule de préparation pour 1000 comprimés dosés à 5 mg
2o Composé de I exemple 5
...............................................................................
... 5 g
Hydroxypropylméthylcellulose
....................................................................... 5 g
Amidon de
blé............................................................................
.................... 10 g
Lactose
.....................................................................:.........
.......................... 100 g
Stéarate de
Magnésium......................................................................
.............. 2 g