Note : Les descriptions sont présentées dans la langue officielle dans laquelle elles ont été soumises.
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
1
Pièce composite pour implantation endo-osseuse et procédé de
fabrication d'une telle pièce
L'invention concerne une pièce destinée à être implantée dans un
tissu osseux tel qu'un implant dentaire, une prothèse ou un comblement
osseux à des fins médicales ou vétérinaires, ladite pièce étant constituée
d'un matériau qui, combiné à un procédé d'obtention particulier, permet
d'accélérer son ostéo-intégration dans le tissu receveur.
On connaît de l'art antérieur, différents implants constitués d'un
polymère biocompatible dont le procédé d'obtention permet la création d'une
texture de surface constituée de micropores favorisant la colonisation
cellulaire par le tissu receveur et accélérant ainsi l'ostéo-intégration dudit
implant.
Ces implants de l'art antérieur procurent des résultats très
satisfaisants, cependant, l'épaisseur de la couche d'ostéo-intégration
obtenue par ce mécanisme, qui correspond à la profondeur des micropores
de surface est de l'ordre de 1000 nanomètres (1 pm). Or, il est généralement
admis qu'une épaisseur d'interpénétration du tissu et de l'implant plus
importante, au moins comprise entre 1 pm et 10 pm, est préférable et ceci
sera d'autant plus vrai que les caractéristiques d'élasticité entre l'implant
et le
tissu receveur seront différentes. Une telle interpénétration accrue sera donc
particulièrement recherchée lorsque l'implant est renforcé, notamment par
des fibres et plus particulièrement au début du processus d'ostéo-intégration
lorsque la corticale en formation ne présente pas encore un module
d'élasticité comparable à celui de l'implant.
Par ailleurs, de telles textures microporeuses de surface sont
difficiles, voire impossibles à obtenir par des procédés économiques de
fabrication de l'implant tel que le moulage par injection.
L'invention a pour objet de résoudre ces insuffisances de l'art
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
2
antérieur en proposant un implant et un procédé d'obtention économique de
celui-ci permettant d'augmenter la profondeur d'interpénétration entre
l'implant et le tissu osseux receveur.
A cette fin l'invention propose une pièce adaptée à une implantation
endo-osseuse in vivo constituée d'un matériau comprenant :
- un liant organique thermoplastique ; et
- une charge fibreuse,
dont les fibres sont majoritairement délaminées du liant sur une
partie de leur longueur dans une couche surfacique de ladite pièce.
On entend par fibres des microfibres, des nanofibres ou des
nanotubes dont le ratio longueur sur épaisseur est supérieur à 10. Les
microfibres sont des fibres dont l'épaisseur est de l'ordre du micromètre ou
micron, c'est-à-dire dont l'épaisseur est sensiblement comprise entre 10-6 et
10-5 mètres. Les nanofibres et les nanotubes sont des fibres dont l'épaisseur
est de l'ordre du nanomètre, c'est-à-dire sensiblement comprise entre 10-9 et
10-8 mètres.
Le délaminage des fibres dans la couche surfacique permet de créer
des interstices qui agissent comme des conduits et par capillarité dans
l'épaisseur de cette couche pour y transporter les fluides organiques
accélérant ainsi la colonisation cellulaire de celle-ci. La nature des fibres
permet également de favoriser et d'accélérer, par absorption, le transport de
ces fluides organiques.
L'invention peut être mise en oeuvre selon des modes de réalisation
avantageux décrits ci-après lesquels peuvent considérés individuellement ou
Avantageusement le liant thermoplastique est constitué de
polyétheréthercétone (PEEK) dont les propriétés de biocompatibilité sont
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
3
connues.
Avantageusement également, la charge fibreuse comprend des
fibres constituées d'un polymère de la famille des polyamides aromatiques
qui présentent également d'excellentes propriétés de biocompatibilité alliées
à des caractéristiques mécaniques élevées. Plus particulièrement des fibres
poly(amide-imide) dont la température de transition vitreuse est proche de la
température de moulage par injection du PEEK permettent par leur facilité de
déformation en cours d'injection une répartition homogène des fibres dans
l'implant même lorsque celles-ci sont relativement longues.
L'effet de conduction des fibres délaminées dans la couche
surfacique permet d'obtenir une épaisseur de ladite couche d'au moins 2 pm,
c'est-à-dire nettement supérieure à ce qu'il est possible d'obtenir avec des
implants obtenus par injection plastique comportant des micropores en
surface sans effet de délaminage.
Avantageusement le matériau constituant l'implant comprend, en
plus des fibres, une charge de composants à base de calcium et de
phosphore. Ces composés résorbables favorisent l'ostéo-intégration et la
cicatrisation.
Avantageusement la charge de composant à base de calcium est
constituée de phosphate tricalcique Ca3(PO4)2 de structure 13 hexagonale.
Ces composés de phosphate tricalcique sont transformés lors de l'opération
de moulage par injection en cristaux d'apatite de calcium non
stoechiométrique, résorbable.
Avantageusement matériau constituant la pièce implantable peut
également contenir une charge de zéolites. Ceux-ci favorisent les liaisons
électrostatiques avec le milieu d'implantation et un accrochage ionique avec
celui-ci. Cette charge contribue en outre à la radio-opacité du matériau.
Avantageusement la charge fibreuse comprend des fibres
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
4
constituées de silicates de calcium (Ca2SiO4). La présence de ces fibres en
surface de la pièce accélère l'absorption des fluides interstitiels dans le
milieu d'implantation et par suite la colonisation cellulaire de la surface de
la
pièce.
L'invention concerne également un procédé pour la fabrication d'un
tel implant ledit procédé comprenant des étapes consistant à:
a) mélanger par extrusion et granulation un polymère thermoplastique
et une charge de fibres ;
b) mouler la pièce par injection dans un moule comprenant une
empreinte de forme appropriée à partir du granulat obtenu à l'étape
a) ;
c) soumettre l'ébauche obtenue à l'étape b) à des bains de décapage
sous ultrasons durant un temps approprié pour produire un
délaminage des fibres dans une couche surfacique.
Le procédé d'injection plastique permet de produire de manière
économique ce type d'implant en cote finie dès l'opération de moulage et en
quantité importante. Il permet en outre d'orienter les fibres par le flux de
matière pénétrant dans le moule et ainsi d'obtenir un effet de renforcement
optimal même pour les implants de forme complexe. Le traitement physico-
chimique combinant l'effet chimique des bains et mécanique des ultrasons
permet à la fois de décaper / dérocher la surface de l'implant, afin d'en
éliminer toute pollution relative au procédé de moulage par injection, et de
produire, dans une couche surfacique, les délaminages des fibres aptes à
produire l'effet de conduction recherché.
Afin d'obtenir une pièce comprenant, en plus des fibres, des
composés à base de calcium et de phosphates, l'invention concerne
également un procédé d'obtention d'un granulat, ou compound, comprenant
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
les étapes consistant à:
- fabriquer un premier granulat, ou compound, en mélangeant, par
extrusion et granulation, le liant polymère avec des composés introduits
sous forme de poudres ; et
5 - mélanger ce premier granulat avec des fibres au cours d'une seconde
opération d'extrusion granulation de sorte à former le granulat utilisé pour
l'opération de moulage par injection.
Avantageusement la charge de zéolites peut également être introduite
lors de la fabrication du premier granulat.
La charge de fibres est avantageusement comprise en 5 % et 15 %
en masse du mélange. Cette proportion offre à la fois un effet de
renforcement important de la pièce finale tout en permettant son obtention
par le procédé d'injection et en permettant le mélange des fibres au liant
polymère par extrusion granulation ou compounding , que celui-ci ait ou
non été préalablement chargé par des composés contenant du calcium et/ou
des zéolites.
L'invention concerne également un granulat, ou compound, pour la
fabrication par injection plastique d'un implant renforcé par des fibres
lequel
granulat comprenant :
- un liant polymère de polyétheréthercétone (PEEK) ;
- une charge de 10 % à 20 % en masse de composés contenant du
calcium et des zéolites ;
- une charge de 5 % à 15 % de fibres.
Ce type de granulat peut être utilisé directement pour la fabrication
par injection plastique, selon l'étape b) du procédé objet de l'invention.
Selon un premier mode de réalisation du granulat objet de
l'invention, la charge fibreuse comprend des fibres constituées d'un
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
6
poly(amide-imide), dont la température de transition vitreuse et égale ou
inférieure à la température d'injection du PEEK.
Selon un deuxième mode de réalisation du granulat objet de
l'invention la charge fibreuse comprend des fibres constituées de silicate de
calcium (Ca25iO4).
Après moulage, la pièce subi un décapage dans une succession de
bains soumis aux ultrasons, dans le but de la rendre apte à une implantation
in vivo et pour y créer avantageusement une couche surfacique favorisant
l'ostéo-intégration dans le milieu receveur.
Avantageusement le décapage est réalisé dans une succession de
bains comprenant, dans l'ordre :
- un passage dans un bain soumis aux ultrasons apte à réduire les
particules contenant du fer;
- un passage dans un solvant du liant soumis aux ultrasons, inerte vis-
à-vis des fibres.
Le premier bain permet d'éliminer la pollution surfacique par les
particules métalliques issues de la presse d'injection et du moule. Le
deuxième bain, en ne dissolvant que le liant, permet, avec l'action conjuguée
des ultrasons, de créer les décohésions ou délaminages entre les fibres et la
matrice dans une couche surfacique. L'ordre des bains est important dans la
mesure où l'acide peut également avoir une action réductrice vis-à-vis des
fibres et / ou vis-à-vis de la charge de composés contenant du calcium ou
des zéolites présents en surface. En réalisant l'attaque acide en premier,
l'action suivante du solvant a pour effet de refaire apparaître ces composés
en surface.
Selon un mode de réalisation avantageux, plus particulièrement
adapté au mode de réalisation pour lequel le matériau constituant l'implant
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
7
comprend des fibres et une charge de zéolites et de composés contenant du
calcium dans une matrice PEEK, l'opération de décapage comprend le
passage dans les bains suivants :
- Acide chlorhydrique
-Acétone
- Eau oxygénée
Séparés par des rinçages dans un bain d'eau également soumis aux
ultrasons. Le dernier bain d'eau oxygénée permet notamment lorsque la
pièce implantable objet de l'invention contient des fibres de silicates de
calcium de créer à la surface de ces fibres émergentes en surface de la
pièce, une couche de silice (5i02). Cette couche de silice en absorbant
l'humidité favorise la conduction des fluides organique dans la couche
superficielle de l'implant.
L'invention sera maintenant plus précisément décrite dans le cadre
de modes de réalisation préférés, nullement limitatifs, représentés sur les
figures 1 à 4, dans lesquelles :
- la figure 1 représente de face un implant dentaire endo-osseux
selon un exemple de réalisation de l'invention ;
- la figure 2 montre un détail Y défini figure 1 selon une coupe AA
définie également figure 1 ;
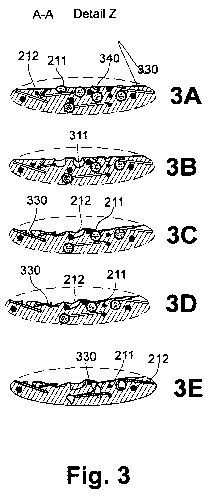
- la figure 3 représente selon un détail Z, défini figure 2 en coupe
selon A A de la surface d'un implant selon un exemple de réalisation
de l'invention au cours des phases de réalisation et d'implantation
intra-osseuse dudit implant, figures 3A à 3E;
- et la figure 4 est un synoptique des différentes phases de
réalisation et de mise en oeuvre d'un implant selon l'invention.
Figure 1, un exemple d'implant (100) présentant une forme
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
8
complexe peut être obtenu de manière économique par un procédé de
moulage par injection plastique. Cet exemple de réalisation, nullement
limitatif, représente une application de l'invention à la réalisation d'un
implant
dentaire. Ledit implant dentaire comprend une partie supérieure (101)
destinée à recevoir des superstructures telles qu'un faux moignon, et une
partie dite inférieure (110) destinée à être implantée dans un tissu osseux.
La
partie inférieure (110) peut optionnellement comprendre des reliefs tels que
des stries aptes à favoriser son accrochage mécanique primaire dans un
logement tel qu'un alésage pratiqué dans le tissu osseux receveur. Ces
stries ou reliefs d'accrochage primaire ont une dimension de l'ordre du
millimètre. Ledit implant est constitué majoritairement d'un polymère
thermoplastique présentant de bonnes caractéristiques de biocompatibilité et
apte à être mis en oeuvre par des techniques de moulage par injection. A titre
d'exemple non limitatif ledit polymère peut être constitué de
polyétheréthercétone ou PEEK tel que distribué commercialement par la
société VICTREX sous la dénomination VICTREX PEEK 150G .
Avantageusement le liant peut être constitué d'un matériau comprenant à la
fois du PEEK, des charges de composés contenant du calcium et des
zéolites telles que le matériau décrit dans le brevet français FR2722694 ou le
brevet américain US5872159.
Figure 2, selon une première vue de détail, en coupe, matériau
constituant l'implant comprend une matrice (210), ou liant, de PEEK, des
particules (230) de composés contenant du calcium, d'un diamètre de l'ordre
de 1 pm (10-6 mètre) et des fibres (220) de renfort. Selon cet exemple de
réalisation, les fibres (220) de renfort sont constituées d'un poly(amide-
imide), telles que des fibres disponibles commercialement sous la
dénomination KERMEL TECH auprès de la société KERMEL , 20 rue
Ampère, F-68027 Colmar. Selon un exemple de réalisation à base de
microfibres, celles-ci ont un diamètre d'environ 7 pm pour une longueur
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
9
d'environ 700 pm (0,7 mm). L'implant étant obtenu par un procédé d'injection
plastique, la température d'injection du PEEK est égale ou supérieure à la
température de transition vitreuse de ce polymère de sorte que ces fibres
sont facilement déformables à la température d'injection et qu'elles suivent
sensiblement le flux de matière.
La charge fibreuse peut, selon un mode de réalisation avantageux,
contenir également, ou exclusivement, des fibres de silicate de calcium
(Ca2Si0.4) (non représentées figure 2). Ce matériau est rigide à la
température d'injection et n'est donc pas déformé à cette température. Aussi,
les fibres de silicate de calcium seront de préférence de plus petite
dimension, de l'ordre de 1 pm de diamètre pour 10 pm à 50 pm en longueur.
Pour éviter tout phénomène de bourrage lors de l'injection, la fraction totale
de fibres, tous types de fibres confondus, ne doit pas excéder 15 % en
masse.
Avantageusement la charge de composés (230) comprenant du
calcium est constituée de phosphate tricalcique Ca3(PO4)2 en phase 13. La
phase 13 du phosphate tricalcique est la phase cristalline de structure
hexagonale stable à basse température.
Ce composé subit, par combinaison avec l'humidité contenue dans
les poudres de calcium tricalcique, de PEEK et éventuellement de zéolites,
une transformation lors de l'opération de moulage par injection selon la
réaction suivante :
4Ca3(PO4)2+ 4(H20) => 3((Ca3(PO4)2)(0F1)2Ca + 2F1PO4 + % 02
3((Ca3(P0.4)2)0H2)Ca correspond à l'hydroxyapatite. Cette apatite
est totalement non stoechiométrique, donc résorbable, ce qui confère au
matériau de la pièce implantable selon l'invention des propriétés
d'intégration, à la manière d'une greffe, dans un tissu osseux.
A cette fin les poudres mises en oeuvre lors de l'injection ne sont pas
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
déshydratées. Elles peuvent avantageusement être réhydratées ou faire
l'objet d'un ajout d'acide orthophosphorique (H3PO4) pour favoriser cette
réaction.
Figure 3, l'observation de la surface à une échelle encore plus fine
5 permet
d'analyser la morphologie de cette surface en fonction des étapes de
mise en oeuvre du procédé et de la pièce implantables de l'invention, les
étapes du procédé étant reprise figure 4.
Selon un exemple de réalisation, l'implant est obtenu par une
première étape visant à l'obtention d'un granulat mélangeant :
10 - 80 % en poids de PEEK
10 % en poids de phosphate tricalcique (Ca3PO4 )
10 % en poids de dioxyde de titane (Ti02)
L'ensemble étant mélangé par extrusion à une température
comprise entre 340 C et 400 C.
Par granulation de cette extrusion on obtient un premier granulat,
lequel est mélangé avec 10 % en masse de fibres Poly(amide-imide) de type
KERMEL TECH et de fibres de silicate de calcium selon le même procédé
d'extrusion granulation.
Le second granulat ainsi obtenu est utilisé pour le moulage (410) par
injection plastique de l'implant. Le moulage se déroule à une température
comprise entre 340 C et 400 C sous une pression comprise entre 70 et
140 MPa, le moule étant chauffé à une température supérieure à la
température de transition vitreuse du PEEK soit une température de
préchauffage du moule d'environ 160 C.
La température de transition vitreuse des fibres de type KERMEL
étant de 340 C celles-ci sont déformables à la température d'injection ce qui
leur permet de suivre le flux d'écoulement de la matière et de se répartir de
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
11
manière homogène, dans le granulat lors de l'opération d'extrusion
granulation et dans la pièce lors de l'opération de moulage par injection.
A l'issue de l'opération de moulage (410), figure 3A, la surface de
l'implant est sensiblement lisse et comprend quelques particules (211) de
composés comprenant du calcium et zéolites (212) légèrement émergentes.
Des fibres (330), ici de silicate de calcium sont également présentes au
voisinage de la surface et éventuellement légèrement émergentes de ladite
surface. La surface de l'implant comprend également des inclusions (340)
métalliques issues du contact avec le moule et avec la vis de la presse
d'injection.
A l'issue de l'opération de moulage, l'implant est soumis à une série
de bain d'attaque chimique / décapage soumis aux ultrasons. A titre
d'exemple le protocole suivant, procure de bons résultats pratiques, les
ultrasons étant appliqués avec une fréquence de 42 kHz:
- HCI 30 %: 35 minutes
H20: 10 minutes (ou rinçage)
C3H60 (acétone) : 35 minutes à température d'ébullition de l'acétone
Séchage de l'implant par évaporation de l'acétone
H202 30 %: 35 minutes
- NaCIO : 35 minutes
H20: 10 minutes (ou rinçage)
L'implant est ensuite plongé, toujours sous ultrasons dans des produits
stérilisants :
GIGASEPT 12 %: 35 minutes
- H20 ppi : 35 minutes
Le bain dans la solution GIGASEPT étant facultatif.
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
12
Selon une première étape (420) l'implant est soumis à une attaque
acide dans l'acide chlorhydrique. Cette attaque a pour but essentiel de
supprimer les inclusions métalliques. A l'issue de cette attaque, la surface
de
l'implant, figure 3B, les inclusions métalliques sont éliminées, mais
également les particules comprenant du calcium qui étaient émergentes,
laissant la place à des cavités (311) correspondantes.
Après rinçage, l'étape suivante (430) consiste à plonger l'implant
dans un bain d'acétone également soumis aux ultrasons. Figure 3C, à l'issue
de cette étape (430), une épaisseur de PEEK est dissoute, laissant
apparaître les particules (211, 212) de composés comprenant du calcium et
de zéolites initialement sous-jacentes. L'action des ultrasons tend également
à produire des délaminages entre les fibres (330) émergeant en surface et
leur implantation dans la matrice.
Après un rinçage, l'étape (440) suivante consiste à soumettre
l'implant à un bain d'eau oxygénée également soumis aux ultrasons. Ce bain
ne modifie pas fondamentalement, figure 3D, la morphologie de la surface.
En revanche, il a une action sur la surface des fibres de silicate de calcium
où il tend à former par oxydation de la silice (5i02) à la surface de celles-
ci.
Avantageusement, l'implant est ensuite inséré dans une gaine de
stérilisation pour son passage en autoclave. Il subit alors un cycle de
stérilisation à une température de l'ordre de 135 C pendant 10 minutes,
sous une pression de l'ordre de 2150 hPa. Cette opération de stérilisation
par autoclave contribue à la fonction de décapage surfacique ; elle peut être
associée à un traitement par oxyde d'éthylène ou par rayons gamma. En
outre, elle favorise la cristallisation des particules de composés de calcium
en surface. A l'issue de cette stérilisation l'implant est conditionné dans un
emballage stérile est se trouve prêt à être implanté dans un tissu osseux.
Lors de l'implantation (450) dudit implant dans le tissu, les fluides
CA 02841336 2014-01-09
WO 2012/007535
PCT/EP2011/062011
13
organiques, tels que le sang, vont suivre par capillarité les délaminages
entre
les fibres et la matrice, qu'il s'agisse des fibres de KERMEL ou des fibres de
silicate de calcium, figure 3E. Dans le cas des fibres de silicate de calcium
la
silice présente en surface de ces fibres, absorbe ces fluides et favorise
ainsi
la conduction sous la surface. En surface, et par conduction par les fibres,
sous cette surface les composés à base de calcium (211) se trouvent en
contact avec ces fluides organiques. La nature résorbable de ces composés
favorise ainsi la colonisation cellulaire conduisant à une greffe de la
surface
de l'implant dans le tissu osseux.
L'application de ce traitement surfacique à un implant, de l'art
antérieur, ne contenant que des composés de phosphate de calcium et du
dioxyde de titane dans une matrice en PEEK permet d'obtenir une épaisseur
de couche surfacique active d'environ 1 pm. Le même traitement appliqué à
un implant de forme identique mais constitué d'un matériau comprenant en
plus 10 % de fibres de poly(amide-imide) ou de fibre de silicate de calcium
permet d'obtenir une épaisseur de couche surfacique active de 3,6 pm.
La description ci-avant illustre clairement que par ses différentes
caractéristiques et leurs avantages, la présente invention atteint les
objectifs
qu'elle s'était fixés. En particulier, elle permet d'obtenir un implant moulé
par
injection et renforcé, comprenant une couche surfacique d'ostéo-intégration
d'épaisseur au moins trois fois supérieure à ce qu'il est possible d'obtenir
sans renforcement.