Note : Les descriptions sont présentées dans la langue officielle dans laquelle elles ont été soumises.
~3~}S~C.~Z
La presente invention concerne de nouveaux dérivés
tertiobutyles du benzylidène camphre, leur procédé de
préparation et leurs utilisations en tant qu'agents
anti-oxydants ainsi que dans des compositions cosmétiques
à usage quotidien ou anti-solaire et dans des compositions
pharmaceutiques pour le traitement preventif des
inflammations et allergies cutanees ou de certaines formes
de cancer.
Il est bien connu que la peau est sensible aux
radiations solaires qui peuvent provoquer un banal coup de
soleil ou erythème mais aussi des brûlures plus ou moins
accentuées.
Cependant les radiations solaires ont également
d'autres effets nefastes tels qu'une perte d'élasticité de
la peau et l'apparition de rides conduisant à un
vieillissement premature. On peut même aussi observer
parfois des dermatoses. Le cas extrême est la survenance
chez certains sujets, de cancers cutanes.
Il est egalement souhaitable d'assurer aux cheveux
une bonne protection contre la dégradation photochimique
afin d'eviter un changement de nuance, une décoloration ou
une dégradation des propriétés mécaniques.
On sait par ailleurs que les constituants entrant
dans les preparations cosmétiques ne possèdent pas
toujours une stabili-te suffisante à la lumiere et se
degradent sous l'ac-tion des radiations lumineuses.
Il est bien connu que la partie la plus dangeureu-
se du rayonnement solaire est constituee par les
radiations ultraviolettes de longueurs d'onde inferieures
à 400 nm. On sait aussi que, de par l'existence de la
couche d'ozone de l'atmosphère terrestre qui absorbe une
- 1 - ~
l~a~s~2
par-tie du rayonnement solaire, la limite inférieure du
rayonnement ultraviolet atteignant la surfac'e' de la terre
se situe aux environ de 280 nm.
Par consequent, il parait souhaitable de disposer
de composes susceptibles d'absorber les radiations
ultraviolettes dans une large bande de longueurs d'onde
allant de 280 à 400 nm, c'est-à-dire aussi bien les rayons
UV-B de longueurs d'onde comprises entre 280 et 320 nm
jouant un rôle preponderant dans la production de
l'erythème solaire, que les rayons ~V-A de longueurs
d'onde comprises entre 320 et 400 nm provoquant le
brunissement de la peau, mais aussi son vieillissement et
favorisant le declenchement de la réaction érythémateuse
ou amplifiant cette réaction chez certains sujets ou
pouvant même être à l'origine de reactions phototoxiques
ou photoallergiques.
Au cours de ses recherches, la Demanderesse vient
de découvrir les nouveaux derives du benzylidène camphre
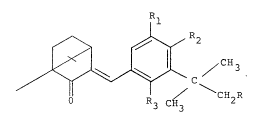
ayant la formule suivante:
/ (I)
I R3 CH3 C 2
dans laquelle:
R represente un atome d'hydrogène ou un reste
tert.-butyle,
Pl represente un reste alkyle lineaire ou ramifie
en Cl-C8 ou un reste alcoxy lineaire ou ramifie en Cl-C8,
-- 2
~3~5~2
R2 et R3 représentent un atome d'hydrogène ou un
radical hydroxyle, sous réserve que l'un au moins des
radicaux R2 et R3 représente un radical hydroxyle.
Outre leurs bonnes proprietes filtrantes dans la
gamme de ]ongueurs d'onde allant de 280 à 380 nm, les
composés ci-dessus présentent simultanement, de manière
inattendue, d'excellentes proprietes anti-oxydantes
vis-à-vis de la peroxydation des lipides polyinsatures et
egalement vis-à-vis des substances susceptibles de subir
des reactions d'oxydation thermo- ou photoinduites (telle$
que des proteines, des polymères...).
Or, on sait que la peroxydation des lipides
implique la formation de radicaux libres intermediaires
qui endommagent les membranes cellulaires se composant,
entre autres, de phospholipides et sont responsables
notamment des phonomènes de vieillissement de la peau (A.L
TAPPEL dans "Federation Proceedings" Vol. 32, No. 8, Août
1973).
Il est extrêmement interessant de disposer de
composés presentant à la fois des proprietes filtrantes
dans une large bande et des proprietes anti-oxydantes
potentialisant l'effet filtre. De tels composes peuvent
permettre par exemple de mieux lutter contre le vieillis-
sement premature de la peau dû à la peroxydation des
lipides cutanes.
Ils peuvent aussi permettre d'assurer une
meilleure conservation des compositions cosmetiques
comportant une phase grasse en evitant le rancissement des
lipides insatures qui y sont contenus et qui peuvent être
d'origine animale comme la lanoline, la cetine (blanc de
baleine), la cire d'abeille, le perhydrosqualène, l'huile
~3~PS4~Z
de tortue, ou végétale comme l'huile d'olive, l'huile de
ricin, l'huile de mals, l'huile d'amande douce, l'huile
d'avocat, l'huile de karité, l'huile de tournesol, l'huile
de soja, l'huile d'arachide, les huiles de coprah ou de
palmiste hydrogénées, des acides gras essentiels comme la
vitamine F et certaines huiles essentielles présentes dans
les parfums comme l'huile de citron ou de lavande.
La Demanderesse a également découvert de manière
extrêmement surprenante que les composés de formule (I)
ci-dessus pouvaient être utilisés pour le traitement
préventif des inflammations et allergies cutanées et
également dans la prévention de certains cancers.
Outre leurs bonnes propriétés filtrantes et
anti-oxydantes, les composés selon l'invention présentent
un excellent caractère liposoluble ainsi qu'une très bonne
stabilité thermique et photochimique.
Ces composés présentent également l'avantage de ne
pas être toxiques ou irritants et d'avoir une parfaite
innocuité vis-à-vis de la peau.
Ils se répartissent uniformément dans des supports
cosmétiques classiques aptes à former un film continu et
notamment dans les supports gras et peuvent ainsi être
appliqués sur la peau pour constituer un film protecteur
efficace.
La présente invention a donc pour objet les
nouveaux composés de formule (I) ci-dessus.
Dans cette formule, Rl peut désigner par exemple
un radical méthyle, éthyle, n-propyle, isopropyle,
n-butyle, isobutyle, tertiobutyle ou l,1,3,3-tétraméthyl-
butyle ou bien un reste méthoxy, éthoxy, propoxy, butox~y,
pentyloxy, hexylo~y, heptyloxy ou octyloxy.
~3~'54~2
Parmi les composés preferes de formule generale
(I), on peut citer: ~
- le 3'-tert.-butyl-2'-hydroxy-5'-methoxy-3-benzylidène-
d,1-camphre,
- le 3'-tert.-butyl-2'-hydroxy-5'-methyl-3-benzylidène-
d,l-camphre,
- le 3',5'-ditert.-butyl-4'-hydroxy-3-benzy~dène-d-
camphre,
- le 3',5'-ditert.-butyl-4'-hydroxy-3-benzylidène-d,l-
camphre,
- le 3',5'-ditert.-butyl-2'-hydroxy-3-benzylidène-d,l-
camphre,
- le 3'-tert.-octyl-2'-hydroxy-S'-methyl-3-benzylidène-
d,l-camphre.
La présente invention a egalement pour objet le
procede de préparation des-nouveaux composes de formule
(I) ci-dessus.
Le procede selon l'invention consiste essentielle-
ment à condenser un aldehyde aromatique de formule:
~C R3
CH/ ~ CH0 (III)
Rl
dans laquelle R, Rl, R2 et R3 ont les signification
precitees, sur le camphre synthetique (d,l-camphre) ou le
camphre naturel (d-camphre).
Les aldehydes de formule (III) sont prepares se~on
des methodes connues
~34~ 5~
La condensation de l'aldéhyde de formule (III) sur
le camphre peut etre effectuée selon lrun des deux
procedes suivants:
ler Procede
La condensation est effectuée en présence d'un
alcoolate de metal alcalin tel que le méthylate de sodium
ou le tertiobutylate de potassium, dans un solvant tel que
le -toluene, a la temperature de reflux du solvant. La
condensation peut egalement être effectuée en présence
d'une base minerale telle qu'un amidure ou un hydrure de
metal alcalin, en présence d'un solvant tel que le
diméthoxyéthane, à une température de reflux du solvant.
2ème Procédé
La condensation de l'aldéhyde de formule (III)
sur le camphre est effectuée en présence d'un borane de
formule (IV) suivante: -
R4
\ B - 0 - C - R (IV)
dans laquelle R4 représente un reste alkyle en Cl-C6 et R5
represente un reste alkyle en Cl-C4. Ce composé est
obtenu selon le mode opératoire décrit par L.H. TOPORCER
et al, J. Am. Chem. Soc. 87, 1236 (1965). Son isolement
et sa purification ne sont pas nécessaires pour réaliser
la condensation de l'aldéhyde de formule (III) sur le
camphre.
La reaction de condensation est effectuée à une
temperature de 140-160 C sans solvant.
~3rJs~ 5~Z
L'invention vise également une composition
cosmétique comprenant, dans un support cbsmétiquement
acceptable contenant au moins une phase grasse, une
quantité efficace d'au moins un dérivé de benzylidène
camphre de formule (I) ci-dessus.
La composition cosmétique de l'invention peut etre
utilisée comme composition protectrice de l'épiderme
humain ou des cheveux ou comme composition anti-solaire.
La présente invention a également pour objet un
procédé de protection de la peau et des cheveux naturels
ou sensibilisés vis-à-vis du rayonnement solaire,
consistant a appliquer sur la peau ou les cheveux une
quantité efficace d'une composition cosmétique telle que
définie ci-dessus.
On entend par "cheveux sensibilisés" des cheveux
ayant subi un traitement de permanente, de coloration ou
de décolora-tion.
L'invention a également pour objet une composition
cosmétique coloree ou non colorée, stabilisée a la lumière
et/ou à l'oxydation, comprenant une quantité efficace d'au
moins un dérivé de benzylidène camphre de formule (I)
ci-dessus.
Iorsqu'elle est utilisée comme composition
destinée à protéger l'épiderme humain contre les rayons
ultraviolets, la composition cosmétique selon l'invention
peut se présenter sous les formes les plus diverses
habituellemen-t utilisées pour ce type de composition.
Elle peu-t notamment se présenter sous forme de lotions
huileuses ou oléoalcooliques, d'émulsions telles qu'une
13~g~Z
crème ou un lait, de gel oléoalcooliques, alcooliques ou
hydroalcooliques, de bâtonnets solides ou etre condition-
nee en aerosol.
Elle peut contenir les adjuvants cosmétiques
habituellement utilisés dans ce type de composition tels
que des épaississants, des adoucissants, des humectants,
des tensio-actifs, des conservateurs, des anti-mousses,
des parfums, des huiles, des cires, de la lanoline, des
propulseurs, des colorants et/ou pigments ayant pour
fonction de colorer la composition elle-même ou la peau ou
tout autre ingrédient habituellement utilisé en cosméti-
que.
Le composé de formule (I) est présent dans des
proportions comprises de préférence entre 0,1 et 2~ en
poids, par rapport au poids total de la composition
cosmétique protectrice de l'épiderme humain.
Comme solvant de solubilisation, on peut utiliser
une huile, une cire et de façon générale tout corps gras,
un monoalcool ou un polyol inférieur ou leurs mélanges.
Les monoalcools ou polyols plus particulièrement préférés
sont l'éthanol, l'isopropanol, le propylèneglycol, la
glycérine et le sorbitol.
Une forme de réalisation de l'invention est une
émulsion sous forme de crème ou de lait protecteurs
comprenant en plus du composé de formule (I), des alcools
gras, des esters d'acides gras et notamment des triglycé-
rides d'acides gras, des acides gras, de la lanoline, des
huiles ou cires naturelles ou synthétiques et des
émulsionnants, en présence d'eau.
~ 3~S ~
Une autre forme de réalisation est constituée par
des lotions huileuses à base d'huiles et cires naturelles
ou synthétiques, de lanoline, et d'esters d'acides gras,
notamment de trigycerides d'acides gras, ou par des
lotions oléoalcooliques à base d'un alcool inférieur tel
que l'éthanol ou d'un glycol tel que le propyleneglycol
et/ou d'un polyol tel que la glycérine et d'huiles, de
cires et d'esters d'acides gras tels que les triglycérides
d'acides gras.
La composition cosmétique de l'invention peut
également etre un gel alcoollque comprenant un ou
plusieurs alcools ou polyols inférieurs tels que
l'éthanol, le propylèneglycol ou la glycérine et un
épaississant tel que la silice. Les gels oléolacooliques
contiennent en ou-tre une huile ou une cire naturelle ou
synthétique.
Les batonnets solides sont constitués de cires et
d'huiles naturelles ou synthétiques, d'alcools gras,
d'esters d'acides gras, de lanoline et autres corps gras.
La presente invention vise également les
compositions cosmetiques anti-solaires contenant au moins
un compose de formule (I) et pouvant contenir d'autres
filtres UV-B et/ou UV-A.
Dans ce cas, la quantité de filtre de formule (I)
est comprise de préference entre 0,2 et 15% en poids, la
quantite totale de filtres présents dans la composition
anti-solaire, c'est-à-dire le composé de formule (I) et
éventuellement les autres filtres, étant comprise entre
0,5 et 15% en poids par rapport au poids total de la
cornposition anti-solaire.
g
13~5~
Dans le cas d'une composition conditionnée en
aérosol, on u-tilise les propulseurs classiques tels que
les alcanes, les fluoroalcanes et les chlorofluoroalcanes.
Lorsque la composition cosmétique selon l'inven-
tion est destinee à protéger des rayons UV les cheveux
naturels ou sensibilisés, cette composition peut se
présenter sous forme de shampooing, de lotion, gel ou
émulsion à rincer, à appliquer avant ou après le
shampooing, avant ou après coloration ou décoloration,
avant ou après permanente, de lotion ou gel coiffants ou -
traitants, de lotion ou gel pour le brushing ou la mise en
plis, de laque pour cheveux, de composition de permanente,
de coloration ou déco~oration des cheveux. Cette
composition peut contenir, outre le composé de l'inven-
tion, divers adjuvants utilisés dans ce type de composi-
tion, tels que des agents--tensio-actifs, des épaissis-
sants, des polymeres, des adoucissants, des conservateurs,
des stabilisateurs de mousses, des électrolytes, des
solvants organiques, des dérivés silicones, des huiles,
des cires, des agents anti-gras, des colorants et/ou
pigments ayant pour fonction de colorer la composition
elle-même ou la chevelure ou tout autre ingrédient
habituellement utilisé dans le domaine capillaire. Elle
contient de preference 0,25 a 2% en poids de composé de
formule (I).
La presente invention vise également les
composi-tions cosmetiques contenant au moins un composé de
formule (I) ci ti-tre d'agent de protection contre les
rayons ul-traviolets et agent anti-oxydant, constituees par
39 des compositions capillaires telles que les laques pour
cheveux, les lotions de mise en plis eventuellement
- 10 -
~3~154~92
traitantes ou démêlantes, les shampoolngs, les shampooings
colorants, les compositions tinctoriales pour~cheveux, par
des produits de maquillage tels que les vernis à ongles,
les crèmes et huiles de traitement pour l'épiderme, les
fonds de teint, les bâtons de rouge à lèvre, les
compositions pour les soins de la peau telles que des
huiles ou crèmes pour le bain, ainsi que toute autre
composition cosmé-tique pouvant présenter du fait de ses
constituants, des problèmes de stabilité à la lumière
et/ou à lloxydation au cours du stockage.
De telles compositions contiennent de préférence
0,1 à 2% en poids de compose de formule (I).
L'invention vise également un procedé de
protection des compositions cosmétiques contre les rayons
ultraviolets et l'oxydation, consistant à incorporer à ces
compositions une quantité efficace d'au moins un composé
de formule (I).
L'invention a également pour objet l'utilisation
des composés de formule (I) en tant qu'agents anti-oxy-
dants ainsi que leur utilisation en tant que filtressolaires à large bande absorbant dans la gamme de
longueurs d'onde allant de 280 à 380 nm.
L'invention vise également l'application à titre
de produits cosmétiques des composés de formule (I).
Comme on l'a indiqué ci-dessus, la Demanderesse a
en outre decouvert au cours de ses recherches, que les
composes de formule (I) presentaient une activité
pharmacologique interessante dans le domaine du traitement
preventif des inflammations et allergies cutanees et
pouvaient être egalement utilises dans la prevention de
certains cancers.
13~5~
L'invention a donc pour objet l'utilisation des
composés de formule (I) comme médicaments.
L'invention a également pour objet une composition
pharmaceutique contenant uen quantité efficace d'au moins
un composé de formule (I) à titre d'ingrédient actif, dans
un support ou un excipient non toxique.
La composition pharmaceutique conforme à
l'invention peut etre administrée par voie orale ou par
voie topique.
10Pour la voie orale, la composition pharmaceutique
peut se présenter sous forme de comprimés, de gélules, de
dragées, de sirop, de suspensions, de solutions,
d'émulsions etc. Pour la voie topique, la composition
pharmaceutique selon l'invention se présente sous forme
d'onguent, de crème, de pommade, de solution, de lotion,
de gel, spray, suspension, etc.
Cette composition médicamenteuse peut contenir des
additifs inertes ou pharmacodynamiquement actifs et
notamment: des agents hydratants, des antibiotiques, des
agents anti-inflammatoires stéroldiens ou non stéroldiens,
des caroténoldes, des agents anti-psoriasiques.
Cette composition peut également contenir des
agents d'amélioration de la saveur, des agents conserva-
teurs, des agents stabilisants, des agents régulateurs
d'humidité, des agents régulateurs de pH, des agents
modificateurs de la pression osmotique, des agents
émulsionnants, des anesthésiques locaux, des tampons etc.
Elle peut aussi etre conditionnée sous des formes
retard ou a libération progressive connues en elles-memes.
- 12 -
13~5~
Le composé de formule (I) conforme à l'invention
est présent dans les compositions pharmaceutiques dans des
proportions comprises de preference entre 0,01 et 80% en
poids, et en particulier entre 0,1 et 20% en poids, par
rapport au poids total de la composition.
Dans l'application therapeutique, le traitement
est determine par le medecin et peut varier selon l'âge,
le poids et la réponse du patient ainsi que la gravité des
symptômes.
Lorsque les composes de formule (I) sont
administres par voi orale, le dosage est generalement
compris entre 0,1 et 50 mg/kg/jour et de preference entre
0,2 et 20 mg/kg/jour. La duree du traitement est varia~le
suivant la gravite des symptômes et peut s'etaler entre 1
et 25 semaines, de facon continue ou discontinue.
Les compositions par voie topique contiennent de
preference de 0,25% a 4% en poids de compose de formule
(I).
Comme support ou excipient de la composition
pharmaceutique de l'invention, on peut utiliser tous
supports ou excipients conventionnels non toxiques.
Les exemples suivants sont destines a illustrer
l'invention sans pour autant presenter un caractere
limitatif.
- 13 -
13~54~;~
EXEMPLES DE PREPARATION
EXEMPLE 1 ~-
Préparation du 3'-tert.-butyl-2'-hydroxy-5'-méthoxy-3-
benzylidène-d,l-camphre de formule:
oc~3
OH C~3 3
On dissout 21 g (0,138 mole) de d,l-camphre dans
10 cm3 de diméthoxyethane seche sur tamis moléculaire de 4
A. On ajoute 6,35 g (0,276 mole) d'hydrure de sodium et
on chauffe au reflux pendant une heure.
On ajoute goutte a goutte 24 G (0,115 mole) de
3-tert.-butyl-2-hydroxy-5-methoxy-benzaldehyde dissous
dans 80 cm3 de 1,2-dimethoxyethane. On chauffe au reflux
pendant 3 heures. Apres refroidissement, le melange
reactionnel est verse dans l'eau. On acidifie par
addition d'acide chlorhydrique ~ 10~. Le precipite forme
est filt,e, lave à l'eau et recristallisé dans l'éthanol
absolu.
On obtient 12,35 g (31~) de produit attendu
possedant les caracteristiques suivantes:
- aspect : cristaux jaunes
- point de fusion : 223C
- analyse elementaire : C22H3003
C~ H~ 0
Calcule 77,15 8,83 14,01
13C~5a~2
Trouvé 76,87 8,83 13,88
- Spectre UV (methanol) : -
maxl = 297 nm C = 15700
~ max2 = 365 nm ~ = 10460
- Spectre de RMN H(80 MHz) (CDC13 + DMSO d6) :
conforme à la structure attendue.
EXEMPLE 2
Preparation du 3'-ter-t.-butyl-2'-hydroxy-5'-méthyl-3-
benzylidène-d,l-camphre
CH3
~ 3
Ce compose est obtenu selon le mode operatoire
decrit à l'exemple 1 dans lequel le 3-tert.-butyl-2-hy-
droxy-5-me-thoxybenzaldéhyde est remplacé par le 3-tert.-
butyl-2-hydroxy-5-méthylbenzaldéhyde.
Le produit obtenu possède les caractéristiques
suivantes:
- aspec-t : cristaux jaunes
- point de fusion : 213&
- analyse elementaire C22H3002
C~ H~ 0~
Calcule 81,18 8,98 9,83
Trouv~ 81,39 9,04 9,92
- Soectre UV (methanol)
~ maxl = 295 nm ~ = 14600
~ max2 = 335 nm ~ = 8470
13~e;4~Z
- Spectre RMN H (80 MHz) (CDC13 + D~ISO d6) :
conforme à la structure attendue~.
E`'EMPLE 3
Préparation du 3',5'-ditert.-butyl-4'-hydroxy-3-benzyli-
dènecamphre
CIH3
CH3 - C - CH3
C\c~ -
CH3 3
a) lère méthode de synthèse : (derive du camphre
naturel)
On dissout 50 g (0,32-8 mole) de d-ca~.phre dans 400
cm3 de 1,2-dimethoxy-ethane. On ajoute 17,5 g d'hydrure
de sodium (0,73 mole) et on porte au reflux pendant une
heure. On ajoute 70 g (0,3 mole) de 3,5-ditert.-butyl-4-
hydroxybenzaldehyde et on chauffe au reflux pendant 10
heures. Après refroidissement, le milieu réactionnel est
dilue progressivement par 100 cm d'ethanol, puis par 100
cm3 d'eau. On acidifie par addition d'acide chlorhydrique
à 10~. Le précipité formé est filtre, lavé à l'eau et
seché. Après recristallisation dans l'ether isopropylique
puis dans l'ethanol, on obtient 54,5 g (rendement 49~) de
produit attendu possedant les caracteristiques suivantes :
- aspect : cristaux blancs
- point de fusion : 186C
- analyse elémentaire C25H362
- 16 -
~3~,54~
C~ H~ 0~
Calculé 81,47 9,84 8,68
Trouvé 81,40 9,87 8,79
- Spectre UV (chloroforme)
~ max : 325 nm ~ = 23000
- Spectre RMN H (80 MHz) (CDC13 ~ DMSO d6) :
conforme à la structure attendue.
b) 2ème méthode de synthèse : (dérivé du camphre
synthétique)
A 500 cm3 de solution lM de triethylborane dans
l'hexane, on ajoute à 0C, 41 g (0,4 mole) d'acide
pivalique. Après 15 nm d'agitation à 0 C, on laisse
revenir à temperature ambiante puis on ajoute 28 g (0,19
mole) de d,l-camphre et 44,5 g (0,19 mole) de 3,5-
ditert.-butyl-4-hydroxybenzaldehyde.
L'hexane est distillé et on chauffe à 150-160C
pendant 3 heures. On distille les produits volatils sous
pression réduite (1995 Pa.s puis 13 Pa.s).
Le mélange réactionnel est dilué par 200 cm
d'acétate d'éthyle. La phase organique est lavée à l'eau,
puis séchée. Le solvant est distillé sous pression
réduite. Après recristallisation dans l'éther isopropyli-
que, on obtient 50,1 g (rendement 72~) de produit attendu
possédant les caractéristiques suivantes :
- aspect : cristaux blancs
- poin-t de fusion : 158C
- analyse élémentaire : C25H3602
C~ H~ 0~
Calculé 81,47 9,84 8,68
Trouvé 81,37 9,84 8,78 !~
- Spec-tre UV (chloroforme)
13~5~caz
~ max = 323 nm ~ = 24200
- Spectre RMN H (80 MHz) (CDC13 + DMSO d6) :
conforme a la structure attendue.
~XEMPL~ 4
Préparation du 3',5'-ditert.-butyl-2'-hydroxy-3-benzylidè-
ne-d,l-camphre de formule:
tert.-butyle
tert.-butyle
0 OH
Ce compose est obtenu selon le mode opératoire
decrit a l'exemple 1 dans lequel le 3-tert.-butyl-2-hy-
droxy-5-methoxy-benzaldéhyde est remplace par le
3,5-ditert.-butyl-2-hydroxybenzaldéhyde.
Le produit obtenu possède les caractéristiques
suivantes:
- Point de fusion : 220C
- Analyse elementaire ; C25H3602
C~ H~ 0~
Calcule 81,47 9,85 8,68
Trouvé 81,29 9,79 8,89
- Spectre UV (dichlorométhane)
maxl : 292 nm
1 : 13000
~ max2 : 330 nm
2 : 7500
- 18 -
13~5~
- Spectre RMN H (80 MHz) (CDC13 + DMSO d6)
conforme à la structure attendue.
EXEMPLE 5
Préparation du 3'-tert.-octyl-2'-hydroxy-5'-méthyl-3-
benzylidène-d,l-camphre de formule:
] ~ tert.-octyle
O OH
Ce composé est obtenu selon le mode opératoire
décrit à l'exemple 1 dans lequel le 3-tert.-butyl-2-hy-
droxy-5-mé~hoxy-benzaldéhyde est remplacé par le
3-tert.-octyl-2-hydroxy-5-méthyle-benzaldéhyde.
Le produit obtenu possède les caractéristiques
suivantes:
- Point de fusion : 176C
- Analyse elémentaire : C26H3802
C~ H~ 0~
Calculé 81,62 10,01 8,36
Trouvé 81,84 9,95 8,51
- Spectre ~V (dichloromethane)
maxl : 293 nm
~1 : 12000
~max2 : 335 nm
~2 : 6~60
- Spectre RMN H (80 MHz) (CDC13 ~ DMSO d6) :
conforme à la structure attendue.
-- 19 --
~3(}54~
EXEMPLES D'APPLICATION
Exemple 1 - Huile an-ti-solaire -
On melange les ingrédients suivants en chauffant
eventuellement à 40-45C pour homogénéiser:
- Compose de l'exemple 3 . 0,6 g
- Benzoate d'alcools en C12-C15 vendu sous la
marque de commerce FINSOLV TN par FINETEX 30,0 g
- Huile de Tournesol 20,0 g
- Parfum 1,0 g
10- Dimethyl polysiloxane cyclique vendu sous
la marque de commerce VOLATILE SILICONE 7207
par ~NION CARBIDE qsp 100 g
On peut remplacer le compose de l'exemple 3 par
celui de l'exemple 4.
Exemple 2 - Gel protecteur de la peau
On prepare le gel suivant:
- Compose de l'exemple 3 0,12 g
- Acide polyacrylique réticulé par un
agent polyfonctionnel vendu sous la
marque de commerce CARBOPOL 934 par la
Societe GOODRICH 0,8 g
- Glycerine 12,0 g
- Ethanol 15,0 g
- Conservateur 0,2 g
- Parfum 0,2 g
- Triethanolamine qs pH 5,3
- Eau demineralisee qsp 100 g
On dissout le filtre dans le melange ethanol-gly-
cerine; on ajoute l'eau, les conservateur et parfum. Dans
cette phase aqueuse, on disperse le Carbopol de faSon
homogène et on ajoute le pH a 5,3 par la triéthanolamine.
- 20 -
~3(I549z
Exemple 3 - Stick anti-solaire
On prépare le bâtonnet solide suivant
- Composé de l'exemple 3 1,0 g
- Ozokérite vendu sous la marque de
commerce SP 1020 par STRAHL
& PITSCH 20,0 g
- Cire d'abeilles 7,0 g
- Alcool oléique 12,0 g
- Lanoline hydrogénée vendue sous la
marque de commerce HYDROLAN H par ONYX
CHEMICAL 8,0 g
- Huile de lanoline vendue sous la
marque de comrnerce ARGONOL 60 par
WESTBROOK LANOLIN 8,0 g
- Cire de carnauba 1,0 g
- Benzoate d'alcools en C12-C15 vendu sous
la marque de commerce FINSOLV TN par
FINETEX 17,0 g
- Octaméthylcyclotétrasiloxane vendu sous
la marque de commerce ABIL K4 par
GOLDSCHMIDT 3,0 g
- Huile de vaseline qsp 100 g
On fond les différents composés vers 70-75 C de
façon à obtenir une phase liquide dans laquelle on dissout
le fil-tre. On coule cette solution dans des moules et on
laisse refroidir.
Exemple 4 - Lait anti-solaire
- Cornposé de l'exemple 3 0,25 g
- Benzylidene camphre 2,0 g
- Melange d'esters d'acides gras, d'esters
polyglyceroles et de tensio-actifs
- 21 -
~3~;4~2
silicones vendu sous la marque de
commerce ABIL WS08 par GOLDSCHMIDT ~ 5,0 g
- Vaseline blanche 2,0 g
- Cire d'abeilles 2,5 g
- Benzoate d'alcools en C12-C15 vendu sous
la marque de commerce FINSOLV TN par
FINETEX 19,0 g
- Glyce~rine 5,0 g
- Chlorure de sodium 2,0 g
- Parfum 0,4 g
- Conservateur 0,2 g
- Eau déminéralisee qsp 100 g
Il s'agit d'une émulsion eau-dans-l'huile. On
dissout les filtres dans les corps gras et l'émulsionnant
et on chauffe à 70-30C; on chauffe à la même température
la phase aqueuse constituée- par l'eau, le chlorure de
sodium et la glycerine; on ajoute sous vive agitation la
phase aqueuse à la phase grasse, puis on laisse refroidir
sous agitation modérée et vers 40C, on ajoute parfum et
conservateur.
Exemple 5 - Lait anti-solaire
- Compose de l'exemple 3 1,5 g
- p-méthoxycinnamate de 2-éthylhexyle
vendu sous la marque de commerce PARSOL
~ICX par GIVAUDAN 3,5 g
- 2-hydroxy-4-methoxybenzophénone
(UVINUL M40; marque de commerce) 1,0 g
- Alcool cétylique 1,0 g
- Ælcool oléoce~ylique a 30 moles d'oxyde
d'éthylène vendu sous la marque de
commerce MERGITAL OC 30 par HENKEL 5,0 g
13~54~2
- Alcool stéarylique 4,0 g
- Huile de synthèse de formule: ~
15 3lcoocH2-clH-cH2ocH2-cH-c4H9 2,0 g
OH C2H5
- Melange 90/10 de 2-ethyl-hexanoate de
cetostearyle et de myristate d'isopropyle
(CERAMOLL (Creations Aromatiques); marque
de commerce) 2,0 g
- Huile de vaseline 8,0 g
- Propylene glycol 4,0 g
- Conservateur 0,2 g
- Parfum 0,4 g
- Eau déminéralisée qsp 100 g
Il s'agit d'une émulsion huile-dans-l'eau. On
dissout les filtres dans les corps gras vers 70-80C; on
chauffe à la même temperatuEe la phase aqueuse constituée
par l'eau, le propylène glycol et l'émulsionnant et on
ajoute sous vive agitation la phase grasse à la phase
aqueuse puis on laisse refroidir sous agitation modérée et
on ajoute conservateur et parfum vers 40C.
Exemple 6 - Crème anti-solaire
On prépare de la même façon que dans l'exemple 5
la crème suivante constituant une émulsion huile-dans-
l'eau dont la phase aqueuse est constituée d'eau, de
sorbitol, de lactate de sodium et de l'émulsionnant et
dans laquelle on dissout le méthylsulfate de 4-[(2-oxo-3-
bornylidène)mé-thyl] phényl triméthylammonium:
- Compose de l'exemple 3 0,5 g
- Methylsulfate de 4-[(2-oxo-3-bornylidène)-
methyl] phenyl trimethylammonium 4,0 ~ g
- Lactate de sorlium à 60~ 1,0 g
13(~'S9~Z
~ Mélange d'alcool cétylstearylique et
d'alcool cetylstearylique oxyethylene à
33 moles d'oxyde d'ethylène vendu sous la
marque de commerce SINNOWAX AO par HENKEL 7,5 g
- Alcool cetylique 1,0 g
- Alcool myristique vendu sous la marque
de commerce SIPOL C14 par KENKEL 0,6 g
- Sorbitol à 70?~ 3,0 g
- Palmitate d'isopropyle 10,0 g
- Huile de vaseline 7,0 g
- Conservateur 0,2 g
- parfum 0,6 g
- ~au demineralisee qsp 100 g
Exemple 7 - Huile anti-solaire
On melange les ingredients suivants en chauffant
eventuellement à 40-45C pour homogéneiser:
- Compose de l'exemple 2 0,2 g
- p-methyl-benzylidène camphre 2 g
- parfum qs
- ~yristate d'isopropyle qsp 100 g
On peut remplacer le compose de l'exemple 2 par
celui de l'exemple 5.
Dans les exemples 8 et 9 ci-après, les composes de
l'invention sont utilises comme anti-oxydants pour eviter
le rancissement des compositions.
Exemple 8 - Crème de soin
On prepare de la même façon que dans l'exemple 4
la crème suivante constituant une emulsion eau-dans-
l'huile dont la phase aqueuse comprend l'eau, l'acide
ascorbique, l'EDTA, le glutathion et l'acide citrique:
- Lanolate de magnesium 14,4 g
- 24 -
13~54~2
- Alcool de lanoline 3,6 g
- Huile de tournesol -40,0 g
- Myristate d'isopropyle 8,0 g
- Ozokérite 4,0 g
- Vitamine F 2,0 g
- Acide ascorbique 0,5 g
- Lécithine de soja 5 g
- Composé de l'exemple 3 0,25 g
- Palmitate d'ascorbyle 1,0 g
- Glu.athion 0,1 g
- N-acétyl-cystéine 0,05 g
- Acide citrique 0,05 g
- Acide éthylenediamine tétracétique (EDTA) 0,15 g
- Parfum 0,8 g
- Parahydroxybenzoate de méthyle0,3 g
- Eau - qsp 100 g
Exemple 9 - Huile pour le visage et le corps
On mélange les ingrédients suivants en chauffant
éventuellement a 40-45C pour homogénéiser:
- Huile de karité 2,0 g
- Huile de tournesol 31,8 g
- Vitamine F 2,0 g
- Huile de soja 32,0 g
- Composé de l'exemple 1 0,1 g
- Acide citrique 0,05 g
- Palmitate d'ascorbyle 1,0 g
- N-acétyl cystéine 0,1 g
- Acide éthylenediamine ~étracétique (EDTA) 0,15 g
- Lécithine de soja 0,1 g
- Huile d'arachide qsp 100 ! g
- 25 -
~3~ 32
Compositions pharmaceutiques utilisees par voie topique:
Exemple 10 - Onguent apaisant
(A appliquer su une peau irritee pour calmer)
- Composé de l'exemple 3 2,00 g
- Huile de vaseline fluide9,10 g
- Silice vendue par la société DEGUSSA sous
la marque de commerce AEROSIL 200 9,20 g
- Myristate d'isopropyle qsp100 g
Exemple 11 - Crème (huile-dans-l'eau) anti-inflammatoire
10 - Composé de l'exemple 4 3,00 g
- Dodecyl sulfate de sodium0,80 g
- Glycerol 2,00 g
- Alcool stéarylique 20,00 g
- Triglycerides d'acides caprique/caprylique
vendus sous la marque de commerce MIGLYOL ~12
par la Societé DYNAMIT NOBEL20,00 g
- Conservateurs qs
- Eau demineralisee qsp 100 g
Exemple 12 - Gel apaisant
20 - Compose de l'exemple 5 1,00 g
- Hydroxypropyl cellulose vendue sous la
marque de commerce KLUCEL HF par la
Societe HERCULES 2,00 g
- Ethanol 70,00 g
- Eau qsp 100 g
- 26 -